Содержание
- 4. Предельные углеводороды “Алканы”
- 6. 1. 1 Общая формула, название класса Алканы (предельные углеводороды, парафины) Алканы – алифатические (ациклические) предельные углеводороды,
- 7. Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода. Число
- 8. 1.2 Виды изомерии. Изомерия – явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но
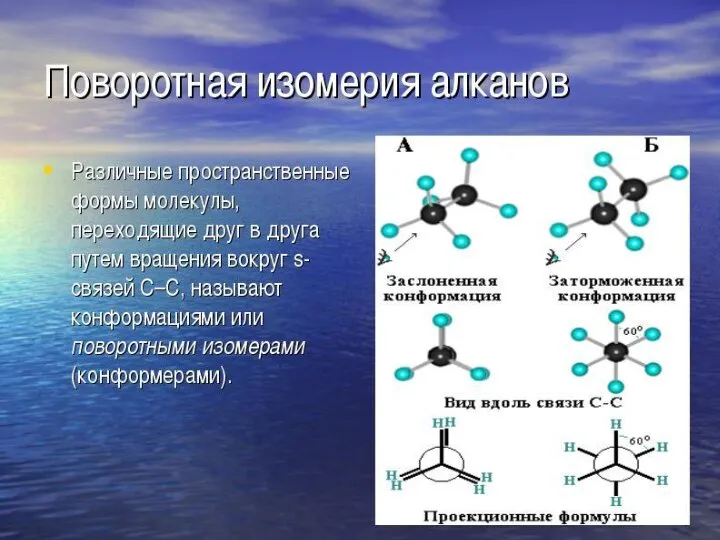
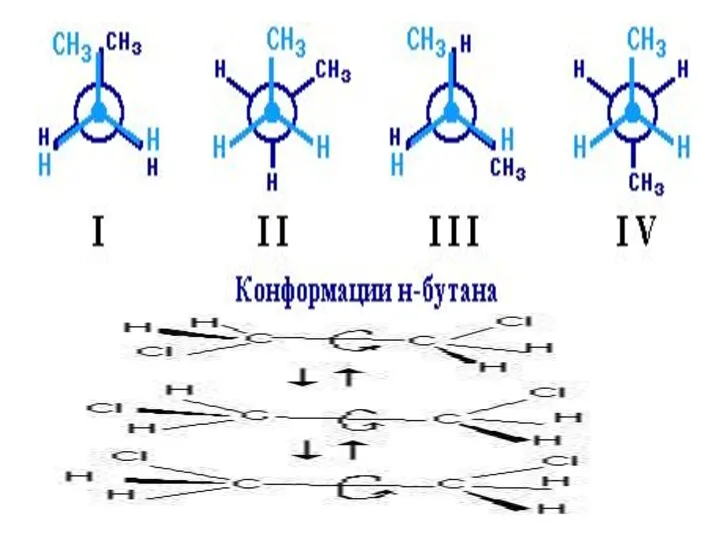
- 9. Если в молекулах одинакового состава и одинакового химического строения возможно различное взаимное расположение атомов в пространстве,
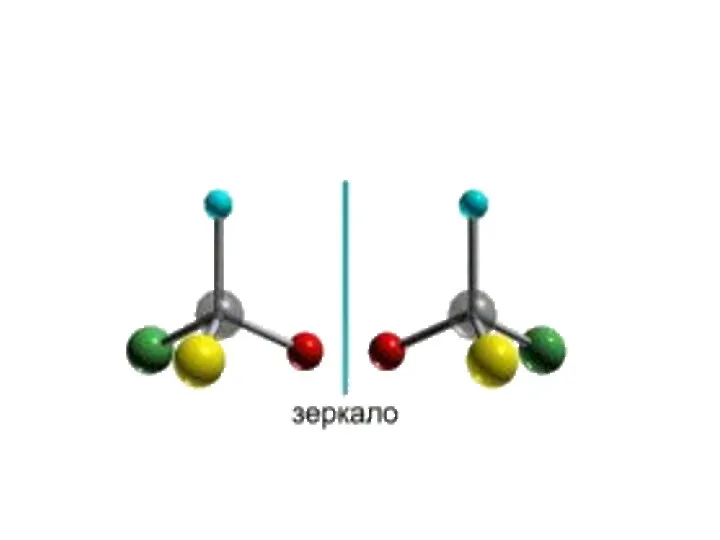
- 12. Кроме того, при наличии в молекуле атома углерода, связанного с 4-мя различными заместителями, возможен еще один
- 14. 1.4 Номенклатура. Номенклатура органических соединений – система правил, позволяющих дать однозначное название каждому индивидуальному веществу. Это
- 15. 1.3 Особенности электронного и пространственного строения. Химическое строение (порядок соединения атомов в молекулах) простейших алканов –
- 16. Электронные и структурные формулы отражают химическое строение, но не дают представления о пространственном строении молекул, которое
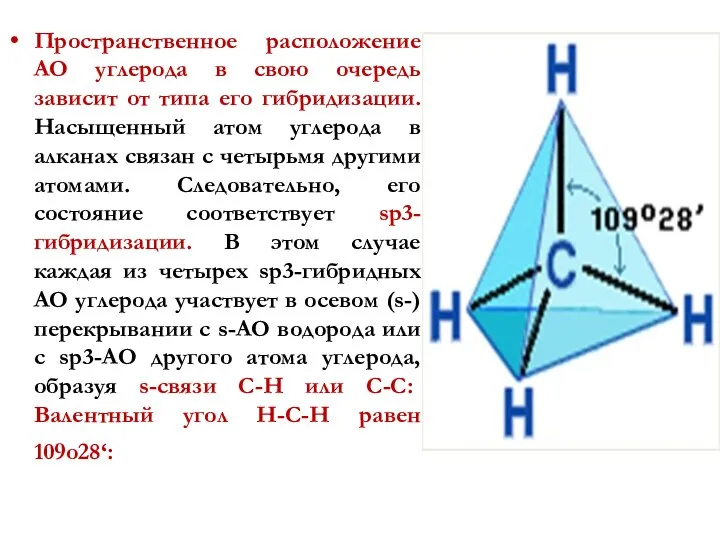
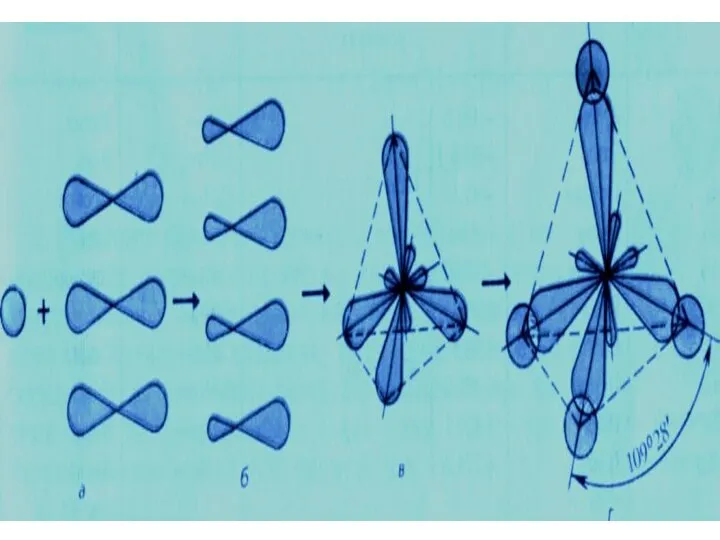
- 17. Пространственное расположение АО углерода в свою очередь зависит от типа его гибридизации. Насыщенный атом углерода в
- 19. Химические свойства любого соединения определяются его строением, т.е. природой входящих в его состав атомов и характером
- 20. Во-первых, предельная насыщенность алканов не допускает реакций присоединения, но не препятствует реакциям разложения, изомеризации и замещения.
- 21. Поскольку гетеролитический разрыв связей С–С и С–Н в обычных условиях не происходит, то в ионные реакции
- 23. 1.6 Физические свойства. Физические свойства. Алканы - бесцветные вещества, нерастворимые в воде. В обычных условиях они
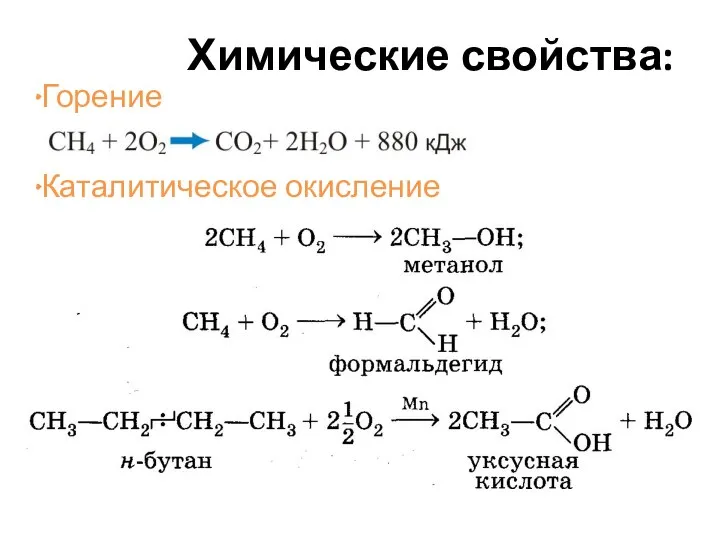
- 24. Химические свойства: Горение Каталитическое окисление
- 25. 1.7 Химические свойства. Тип Замещение Галогенирование. Для алканов характерны реакции замещения с галогенами, причем с фтором
- 26. Реакции замещения (по свободнорадикальному механизму) разрыв связей C – H и замещение атомов водорода Галогенирование Алканы
- 27. Механизм радикального замещенияSR Радикальные реакции имеют цепной механизм, включающий стадии: зарождение, развитие и обрыв цепи. Зарождение
- 28. SR Предельные углеводороды вступают в реакции нитрования, сульфирования, сульфохлорирования и сульфоокисления углеводородов: RH + НО-NO2 =
- 29. Химические свойства: Нитрование (Реакция Коновалова) В первую очередь замещаются атомы водорода у III > II >
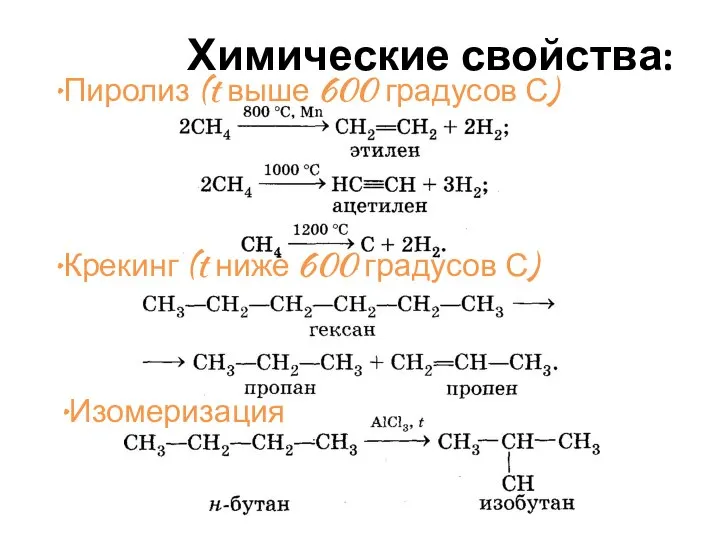
- 30. Химические свойства: Пиролиз (t выше 600 градусов С) Крекинг (t ниже 600 градусов С) Изомеризация
- 31. 1.5 Способы получения. Алканы выделяют из природных источников (природный и попутный газы, нефть, каменный уголь). Используются
- 32. 2. Синтез более сложных алканов из галогенопpоизводных с меньшим числом атомов углеpода: 3.Из солей карбоновых кислот:
- 33. 1.5 Способы получения. 5. Гидрирование непредельных углеводородов: 6. Газификация твердого топлива (при повышенной температуре и давлении,
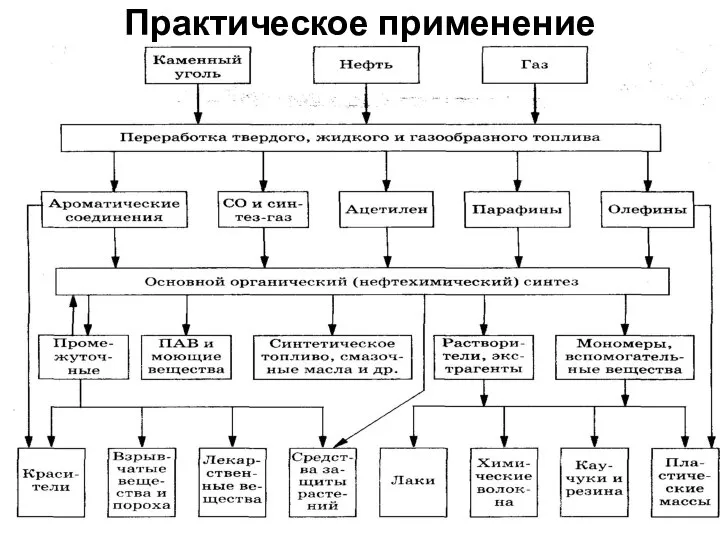
- 34. Практическое применение
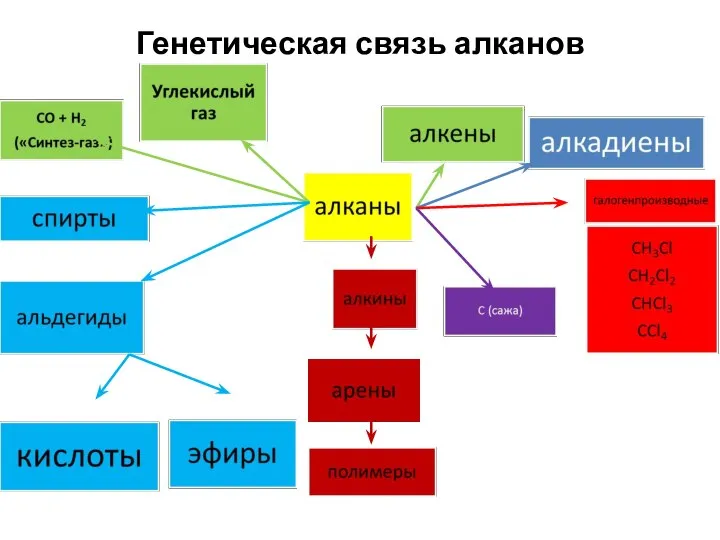
- 35. Генетическая связь алканов
- 36. Генетическая связь алканов Решить превращение 38(ЕГЭ)
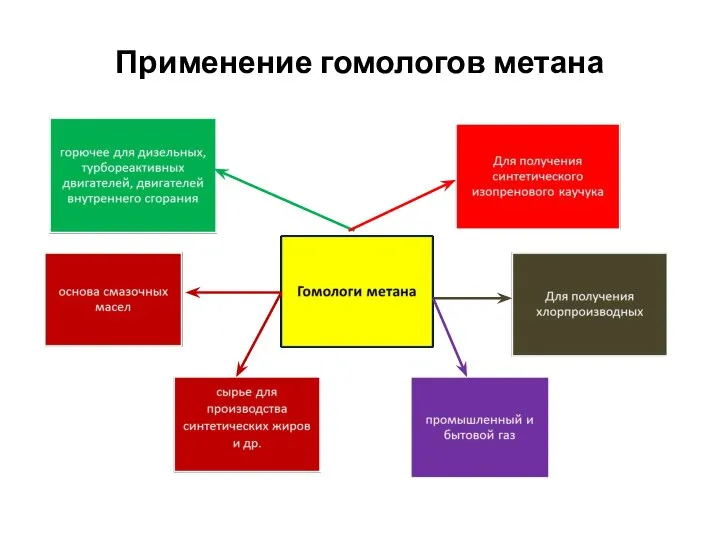
- 37. Применение гомологов метана
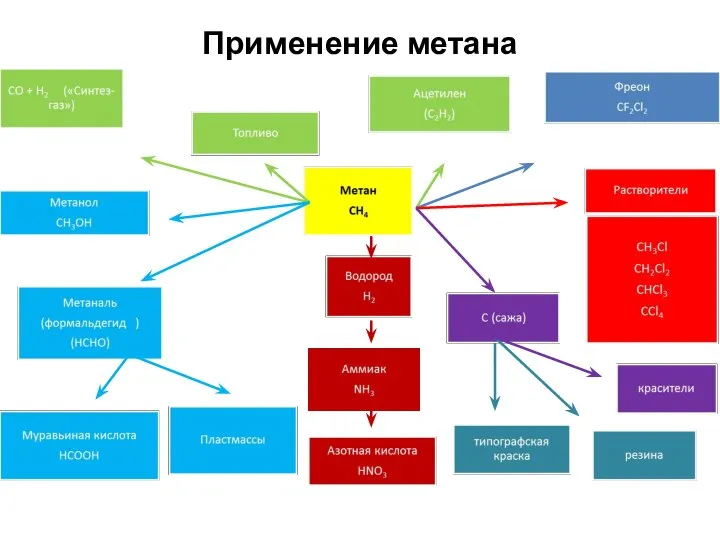
- 38. Применение метана
- 40. Скачать презентацию


























 Презентація по хімії на тему:БУДІВЕЛЬНІ МАТЕРІАЛИ
Презентація по хімії на тему:БУДІВЕЛЬНІ МАТЕРІАЛИ  Основные разделы химии
Основные разделы химии Защита металлов от коррозии
Защита металлов от коррозии Рубидий, цезий, франций
Рубидий, цезий, франций Каталитикалық риформинг
Каталитикалық риформинг Скорость химических реакций
Скорость химических реакций Естественная и техногенная радиоактивность ос. Радиохимические методы исследования радионуклидного состава
Естественная и техногенная радиоактивность ос. Радиохимические методы исследования радионуклидного состава Химические и физические явления
Химические и физические явления Неорганическая химия (все для повторения)
Неорганическая химия (все для повторения) Трансформация соединений азота
Трансформация соединений азота Презентация Белки
Презентация Белки Карбонильные производные (кислоты, альдегиды, кетоны, сложные эфиры)
Карбонильные производные (кислоты, альдегиды, кетоны, сложные эфиры) Нефть как дисперсная система
Нефть как дисперсная система Графит. Химические свойства
Графит. Химические свойства Окислы. Лекция 14
Окислы. Лекция 14 Растворы
Растворы Кислоты, соли
Кислоты, соли Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Клеящие материалы. Классификация и ассортимент клея
Клеящие материалы. Классификация и ассортимент клея Введение. Тренажер
Введение. Тренажер Ароматические углеводороды
Ароматические углеводороды Химическая связь и ее типы
Химическая связь и ее типы Аминспирттер және олардың биологиялық ролі.Элементорганикалық қосылыстар және олардың қасиеті
Аминспирттер және олардың биологиялық ролі.Элементорганикалық қосылыстар және олардың қасиеті Каучуки. Гума
Каучуки. Гума Радиоактивный распад. Чернобыль
Радиоактивный распад. Чернобыль Химико – математические проценты
Химико – математические проценты Кислоты. Классификация кислот
Кислоты. Классификация кислот Термодинамическая теория растворов электролитов. Электропроводность растворов электролитов
Термодинамическая теория растворов электролитов. Электропроводность растворов электролитов