Содержание
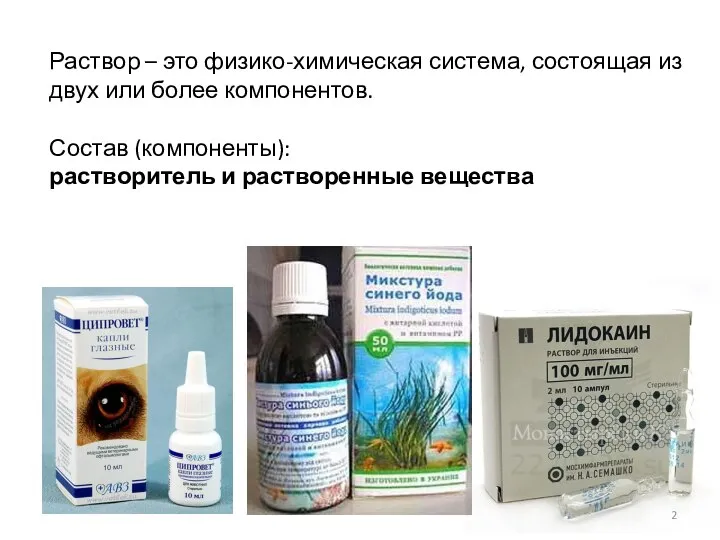
- 2. Раствор – это физико-химическая система, состоящая из двух или более компонентов. Состав (компоненты): растворитель и растворенные
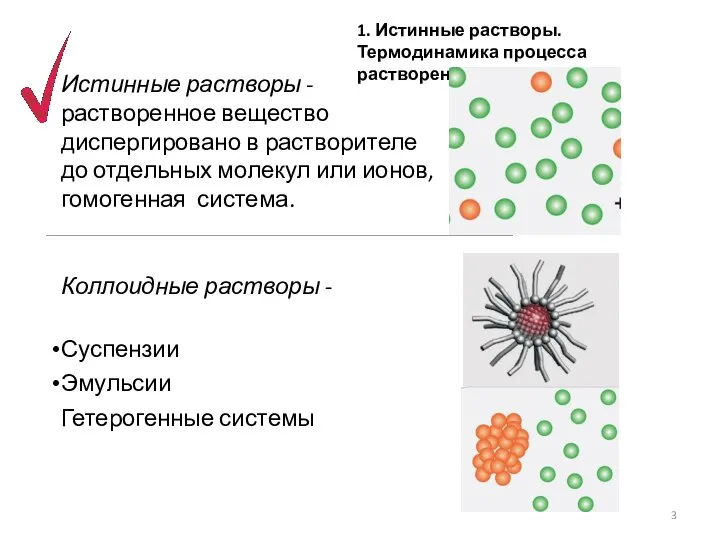
- 3. Истинные растворы - растворенное вещество диспергировано в растворителе до отдельных молекул или ионов, гомогенная система. Коллоидные
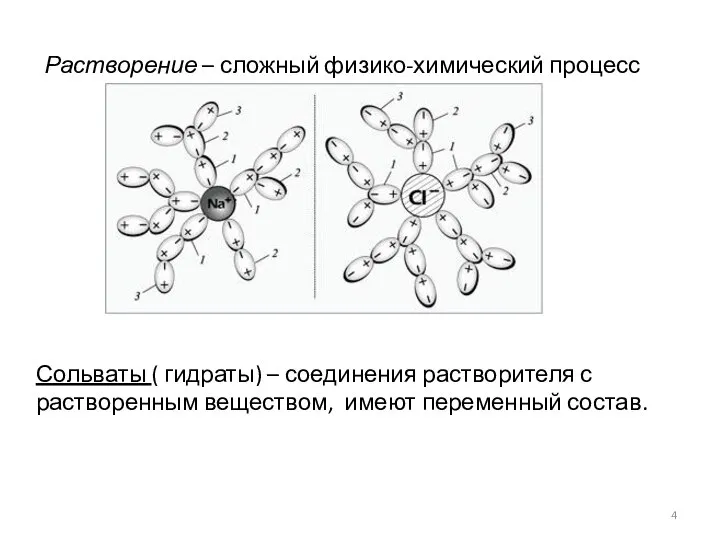
- 4. Сольваты ( гидраты) – соединения растворителя с растворенным веществом, имеют переменный состав. Растворение – сложный физико-химический
- 5. В ряде случаев гидратная вода удерживается твердой фазой кристаллогидраты CuSO4 ⋅ 5H2O CuSO4 ⋅ 3H2O гипс
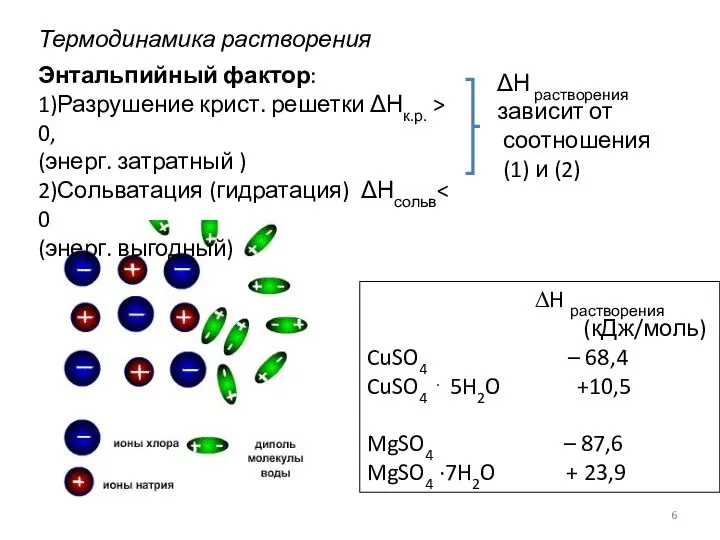
- 6. Термодинамика растворения Энтальпийный фактор: 1)Разрушение крист. решетки ΔНк.р. > 0, (энерг. затратный ) 2)Сольватация (гидратация) ΔНсольв
- 7. Растворение твердого вещества - ∆H раств 0 (от соотношения 1 и 2) Растворение жидкости или газа
- 8. Самопроизвольное растворение: ΔG Энтропийный фактор: При растворении тв. в-ва и жидк. ΔS > 0 При растворении
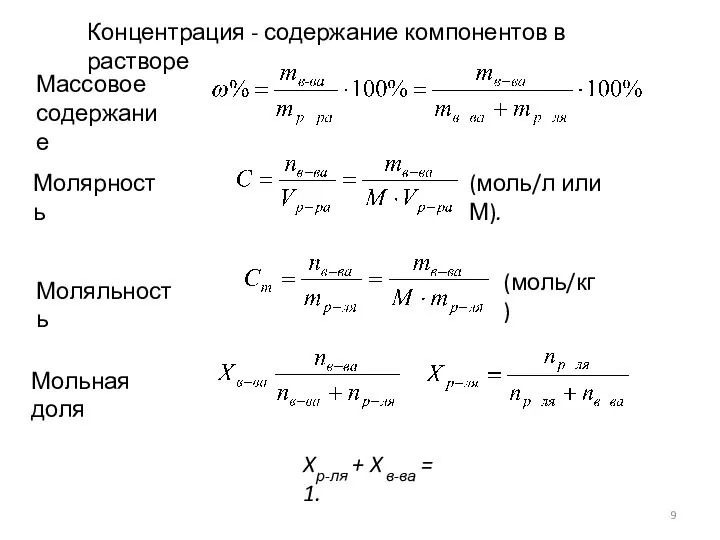
- 9. (моль/л или М). (моль/кг) Xр-ля + X в-ва = 1. Мольная доля Массовое содержание Молярность Моляльность
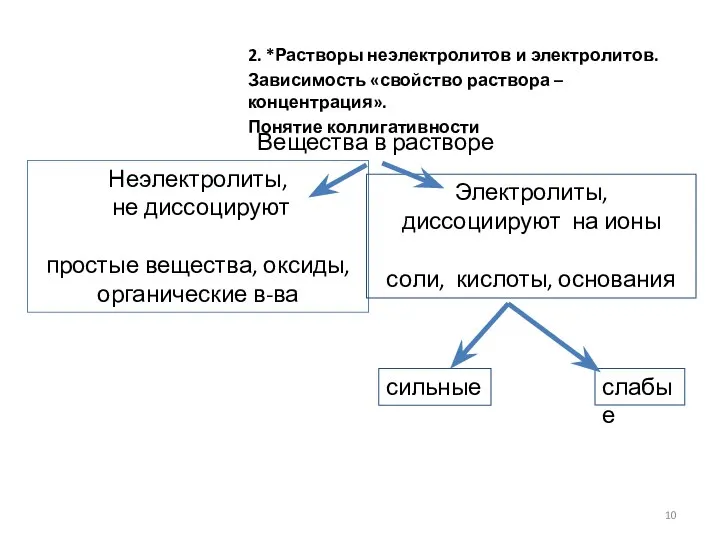
- 10. Неэлектролиты, не диссоцируют простые вещества, оксиды, органические в-ва Электролиты, диссоциируют на ионы соли, кислоты, основания сильные
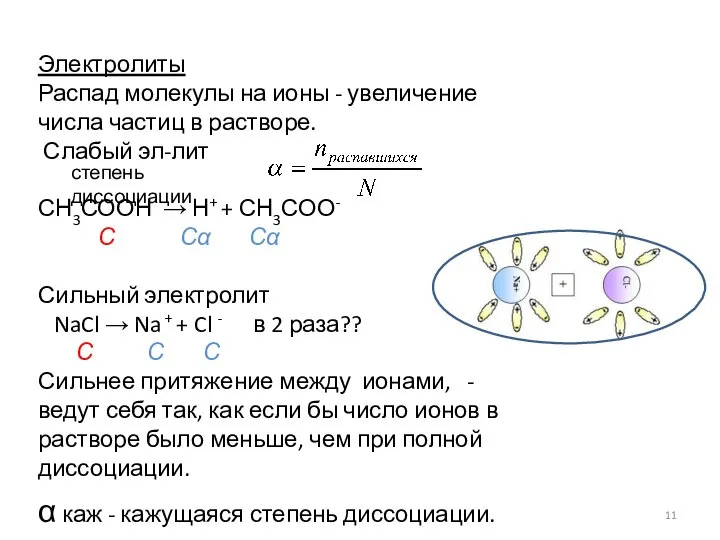
- 11. Электролиты Распад молекулы на ионы - увеличение числа частиц в растворе. Слабый эл-лит СН3СООН → Н+
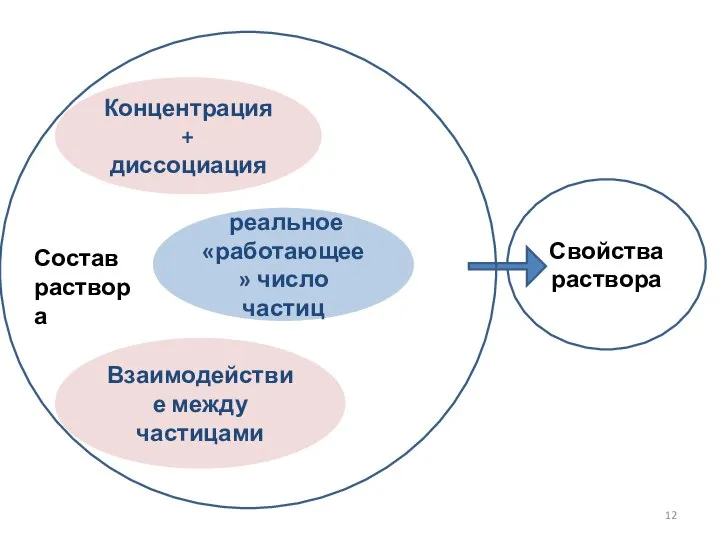
- 12. Свойства раствора Концентрация + диссоциация реальное «работающее» число частиц Взаимодействие между частицами Состав раствора
- 13. Коллигативные свойства (от лат. colligatus — обобщать) – зависят не от природы растворителя и растворенного вещества,
- 14. 3.* Осмос и осмотическое давление. Закон Вант-Гоффа. Изотонический коэффициент. Осмоляльность и осмолярность. Плазмолиз, гемолиз, тургор. Гипо-,
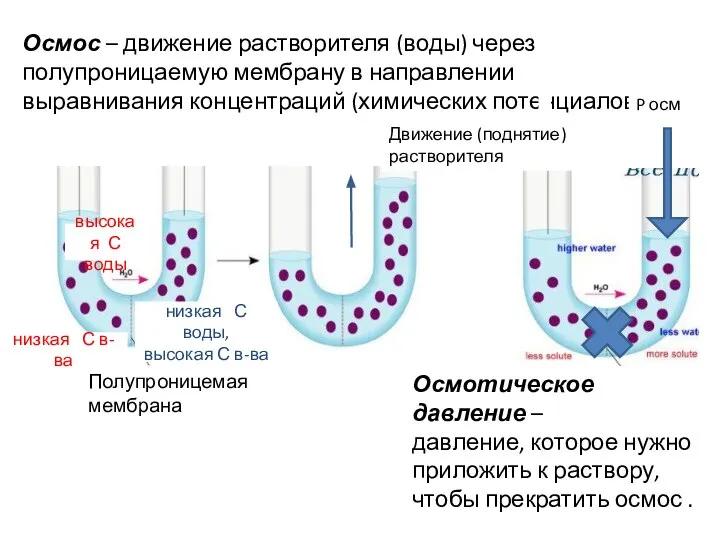
- 15. Осмос – движение растворителя (воды) через полупроницаемую мембрану в направлении выравнивания концентраций (химических потенциалов) P осм
- 16. Доп. материал: Если P > P осм – обратный осмос Нужно приложить внешнее давление, превосходящее Pосм,
- 17. Pосм = RTС (идеальные растворы) CИ: Pосм [ Па = Н/м2], C [ моль/м3], R =
- 18. Если молекула распадается на n ионов (NaCl – 2, ZnCl2 – 3), количество исходных молекул N,
- 19. *Метод определения степени диссоциации α. пример 0,05 М раствор NaCl при 25°С , Pосм = 235256,1
- 20. 0,05 М раствор NaCl i = 1,9 (вместо 2,0 ) 0,05 М раствор MgSO4 i =1,3
- 21. Осмотическое давление биологических жидкостей создается ионами (Na+ К+, Сl-, НСО3- и др.), молекулами неэлектролитов (мочевина, глюкоза
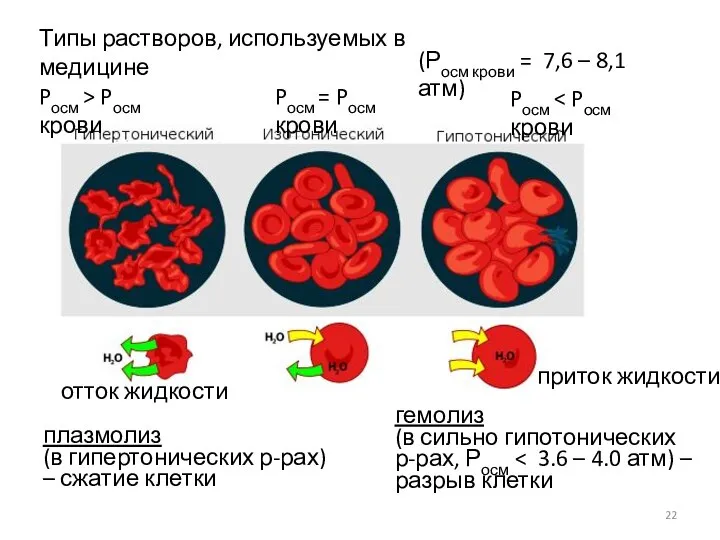
- 22. Типы растворов, используемых в медицине Pосм > Pосм крови Pосм = Pосм крови Pосм отток жидкости
- 23. Онкотическое давление – осмотическое давление, обусловленное белками крови Ронк = 0,03 – 0,04 атм Ронк крови
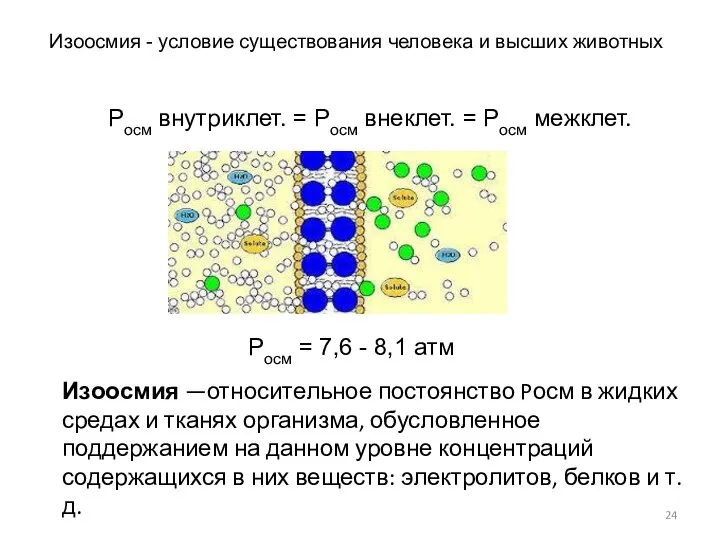
- 24. Изоосмия - условие существования человека и высших животных Росм = 7,6 - 8,1 атм Изоосмия —относительное
- 25. Изотонические растворы, используемые в медицине Росм = СRT = С . 0,082 . 310 = 7,62
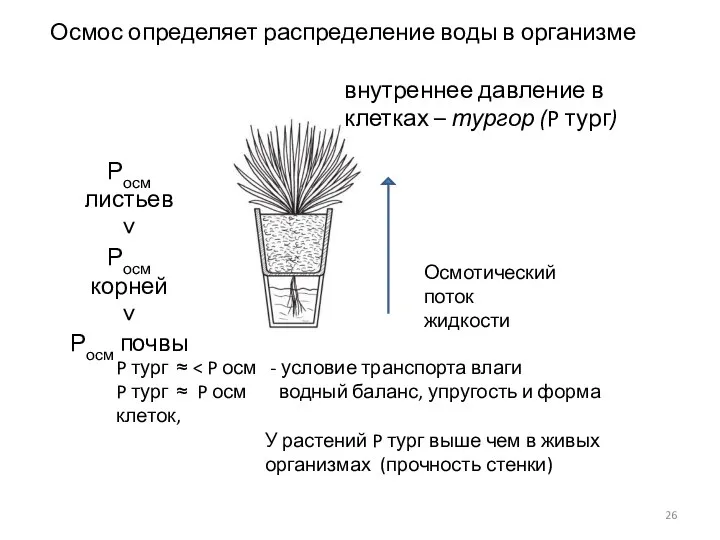
- 26. Осмос определяет распределение воды в организме Росм листьев ˅ Росм корней ˅ Росм почвы внутреннее давление
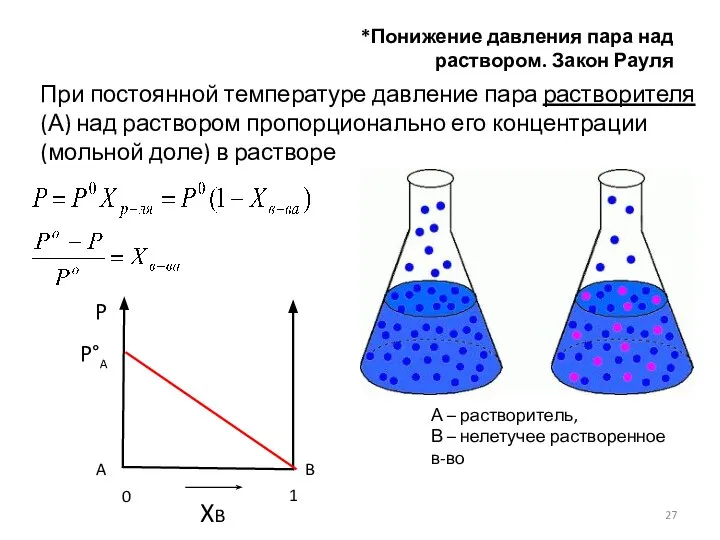
- 27. *Понижение давления пара над раствором. Закон Рауля При постоянной температуре давление пара растворителя (А) над раствором
- 28. Для разбавленных водных растворов на 1000 г воды : Неэлектролиты Электролиты
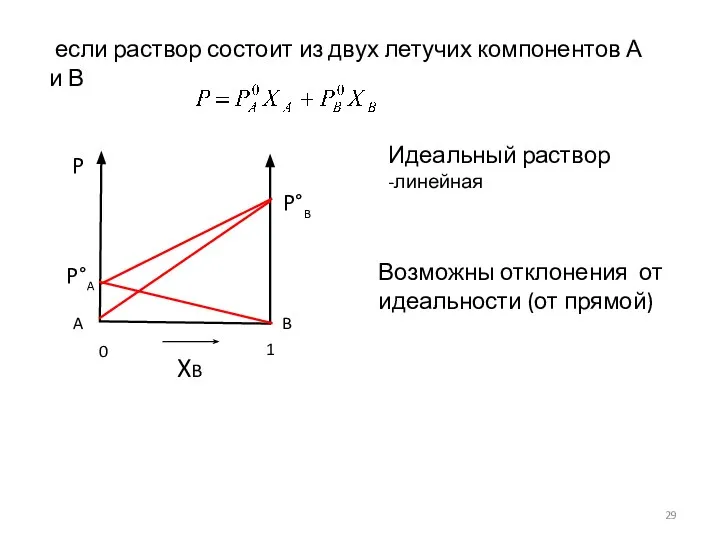
- 29. если раствор состоит из двух летучих компонентов А и В Возможны отклонения от идеальности (от прямой)
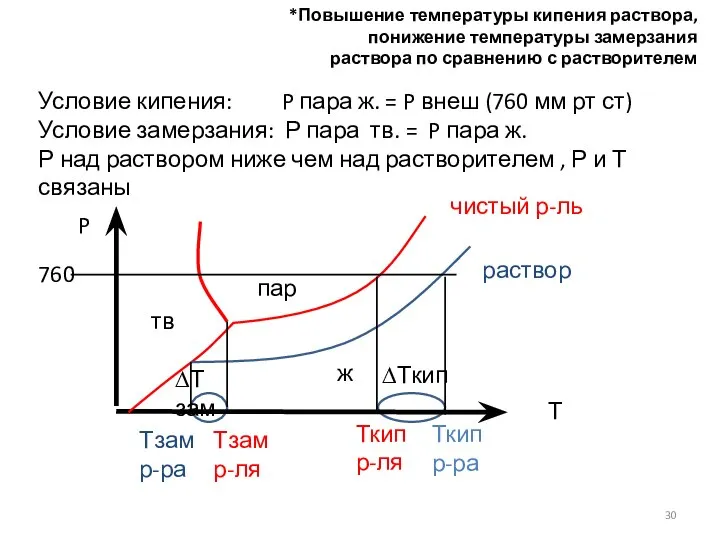
- 30. *Повышение температуры кипения раствора, понижение температуры замерзания раствора по сравнению с растворителем Условие кипения: P пара
- 32. Скачать презентацию






![Pосм = RTС (идеальные растворы) CИ: Pосм [ Па = Н/м2],](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1398019/slide-16.jpg)







 Аминокислоты
Аминокислоты Введение в биохимию. Значение биохимии для врача. Химия белка
Введение в биохимию. Значение биохимии для врача. Химия белка Кинетика ферментативного катализа. Регуляция активности ферментов. (Лекция 6)
Кинетика ферментативного катализа. Регуляция активности ферментов. (Лекция 6) Презентація на тему: Каучук. Історія його відкриття
Презентація на тему: Каучук. Історія його відкриття  Марки бензина
Марки бензина Естественные семейства элементов
Естественные семейства элементов Хроматографические методы анализа
Хроматографические методы анализа Аналитическая химия стойких органических загрязнителей
Аналитическая химия стойких органических загрязнителей Кинетические методы анализа
Кинетические методы анализа Презентация по Химии "Химические тайны запаха" - скачать смотреть
Презентация по Химии "Химические тайны запаха" - скачать смотреть  Свойства атомов
Свойства атомов Макро, микро и ультрамикроэлементы. Их роль
Макро, микро и ультрамикроэлементы. Их роль Объединение по интересам “тайны вещества”
Объединение по интересам “тайны вещества” Химические реакции Выполнила Болгова ЕД преподаватель химии ГБОУ ГАК с Московское
Химические реакции Выполнила Болгова ЕД преподаватель химии ГБОУ ГАК с Московское Механизм действия гидрофильных и липофильных гормонов. (Лекция 11)
Механизм действия гидрофильных и липофильных гормонов. (Лекция 11) Повторяем: все о спиртах! Красный цвет -1балл; синий цвет -2 балла; зеленый цвет – 3 балла.
Повторяем: все о спиртах! Красный цвет -1балл; синий цвет -2 балла; зеленый цвет – 3 балла. Растворы электролитов
Растворы электролитов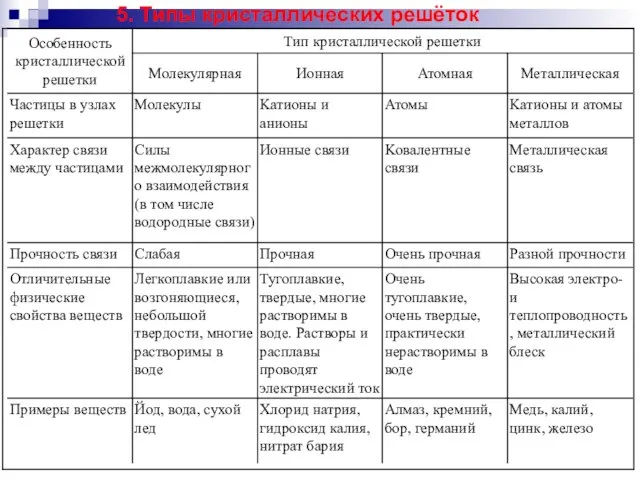 Типы кристаллических решёток. (Лекция 3)
Типы кристаллических решёток. (Лекция 3) Основные вулканические породы. Основные плутонические породы
Основные вулканические породы. Основные плутонические породы Презентация Вещества и их свойства
Презентация Вещества и их свойства Азотсодержащие и гетероциклические соединения. Низкомолекулярные биологическиактивные соединения
Азотсодержащие и гетероциклические соединения. Низкомолекулярные биологическиактивные соединения Личная жизнь и научная деятельность Михаила Васильевича Ломоносова Работу выполнил: ученик 8-го «А» класса лицея № 1571 г.Москвы Ани
Личная жизнь и научная деятельность Михаила Васильевича Ломоносова Работу выполнил: ученик 8-го «А» класса лицея № 1571 г.Москвы Ани Многоатомные спирты. Вопросы для повторения
Многоатомные спирты. Вопросы для повторения Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно
Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно Этот удивительный песок
Этот удивительный песок Основания. Физические и химические свойства оснований
Основания. Физические и химические свойства оснований Второй закон термодинамики. Биоэнергетика
Второй закон термодинамики. Биоэнергетика Оксосинтез. Процессы оксосинтеза
Оксосинтез. Процессы оксосинтеза