Содержание
- 2. УМК «ХИМИЯ» Тема лекции: Комплексные соединения Лектор – Иванов М.Г.
- 3. СОДЕРЖАНИЕ Основные понятия Классификация Номенклатура Изомерия Геометрическая Оптическая Связевые изомеры Гидратные и ионизационные изомеры Конформационные изомеры
- 6. Классификация Координационные ацидосоединения, во внутренней сфере которых содержатся только кислотные остатки; Молекулярные координационные соединения, во внутренней
- 9. Изомерия Геометрические изомеры содержание Транс-изомер Цис-изомер
- 14. Изомерия Конформационные изомеры содержание
- 15. Лиганды Типы: содержание нейтральные: H2O, NH3, CO, Н2N-CH2-CH2-NH2 анионы: Cl-, OH-, CN-, F-, оксалат-ион- С2O42- Дентатность:
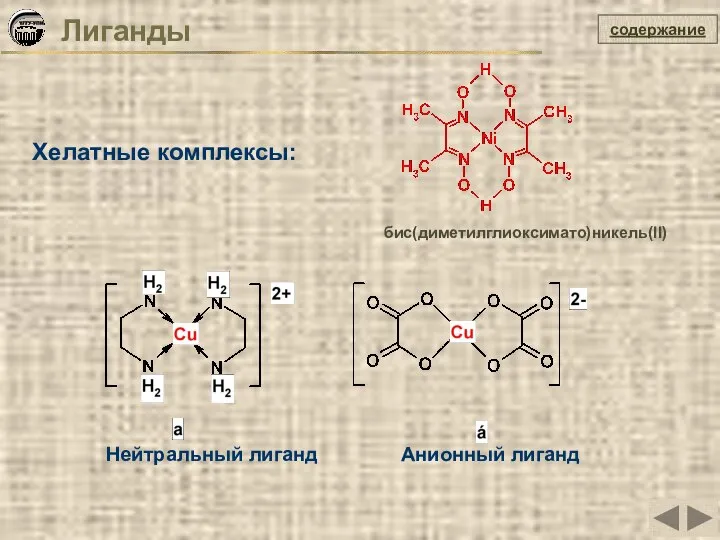
- 16. Хелатные комплексы: Лиганды содержание Нейтральный лиганд Анионный лиганд бис(диметилглиоксимато)никель(II)
- 17. Лиганды Макроциклический содержание [Ni(H2O)6]2+ + n L [Ni(L)n(H2O)2]2+ + 4H2O
- 18. Лиганды содержание Макроциклические 12-краун-4 15-краун-5 18-краун-6
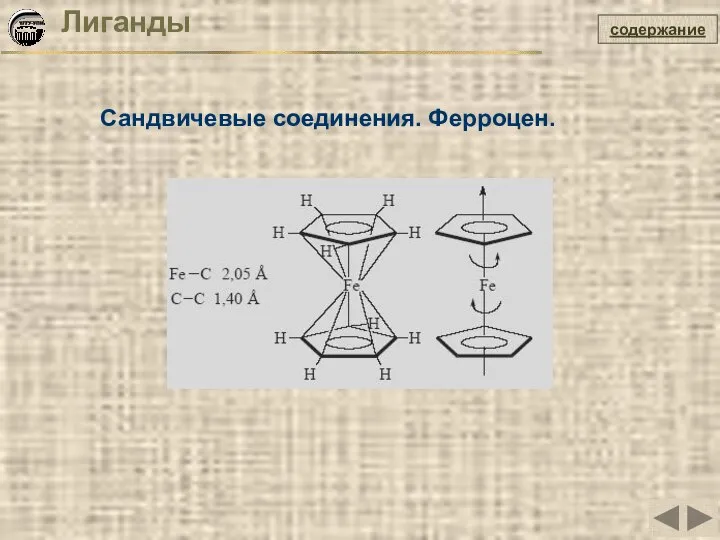
- 19. Лиганды Сандвичевые соединения. Ферроцен. содержание
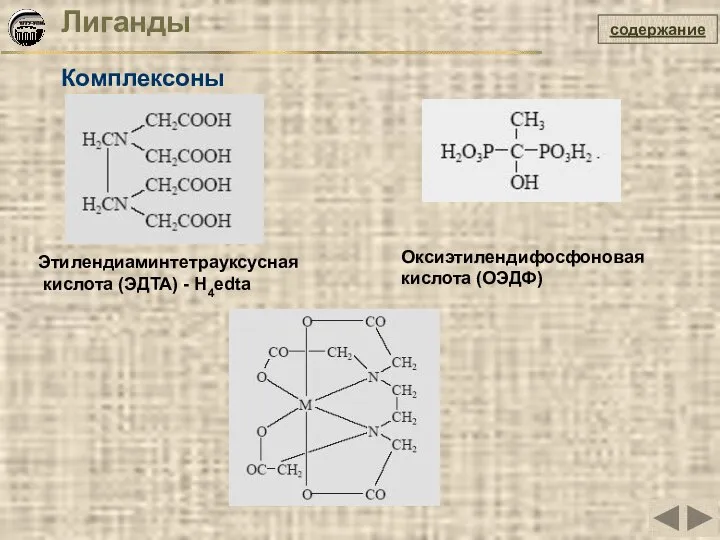
- 20. Лиганды Комплексоны содержание Этилендиаминтетрауксусная кислота (ЭДТА) - H4edta Оксиэтилендифосфоновая кислота (ОЭДФ)
- 21. Многоядерные комплексы Многоядерный комплекс относят к кластерному типу, когда атомы комплексообразователя непосредственно связаны между собой: ион
- 22. Многоядерные комплексы Карбонильные кластеры: содержание Os3(CO)12 CO (окись углерода), имеет свободные π* орбиты, является важнейшим из
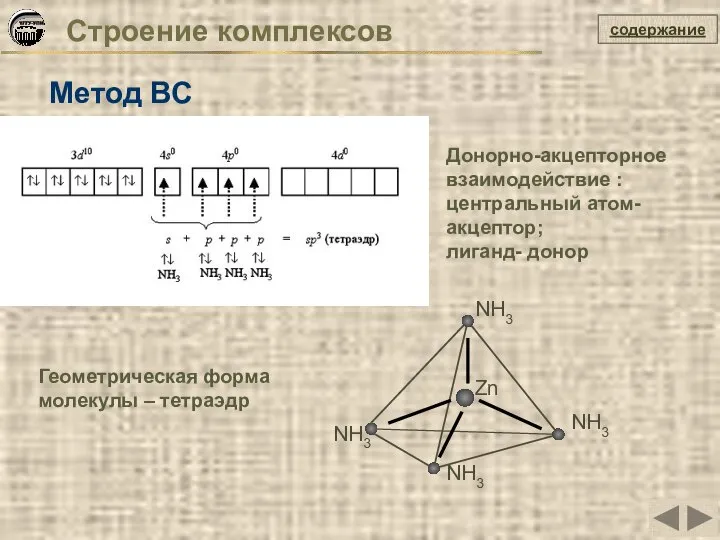
- 23. Строение комплексов Метод ВС Zn NH3 NH3 NH3 NH3 Геометрическая форма молекулы – тетраэдр содержание Донорно-акцепторное
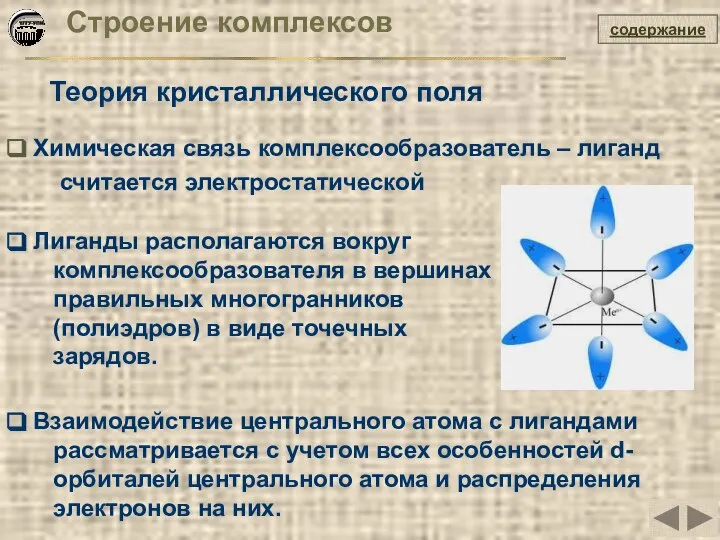
- 26. Строение комплексов Теория кристаллического поля Химическая связь комплексообразователь – лиганд считается электростатической Лиганды располагаются вокруг комплексообразователя
- 28. Строение комплексов Расщепление d-орбиталей содержание Орбитали dх2-у2 (а) и dxz (б) в октаэдрическом поле лигандов (а)
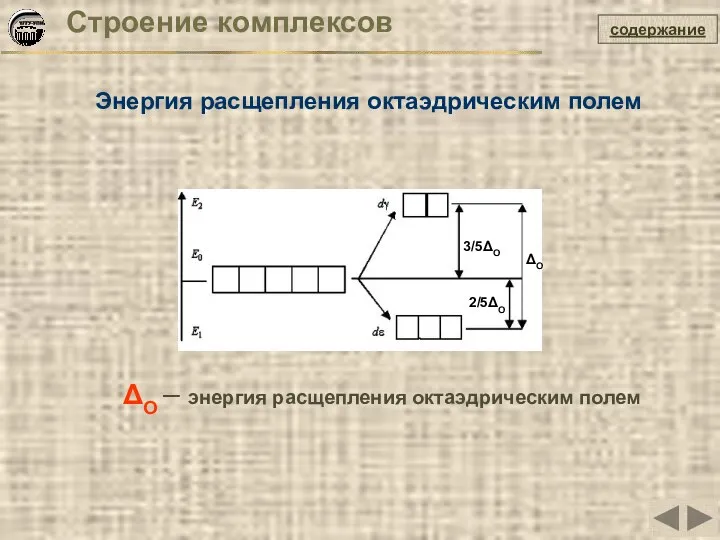
- 29. Строение комплексов Энергия расщепления октаэдрическим полем содержание ΔO – энергия расщепления октаэдрическим полем ΔO 2/5ΔO 3/5ΔO
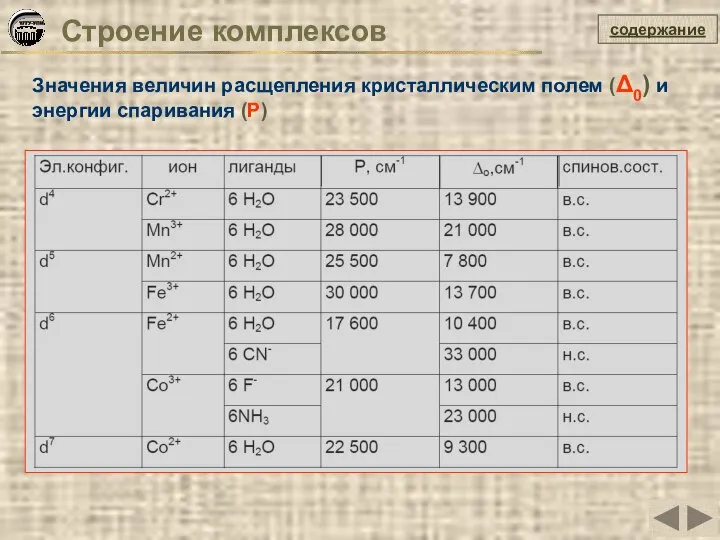
- 30. Строение комплексов Значения величин расщепления кристаллическим полем (Δ0) и энергии спаривания (P) содержание
- 31. Строение комплексов содержание Сильное и слабое поле ΔO > P (энергии спаривания электронов) – комплекс низкоспиновый
- 32. Строение комплексов содержание Сильное и слабое поле ΔO комплекс высокоспиновый (слабое поле) [Fe(H2O)6]2+ 3d6 ΔO =
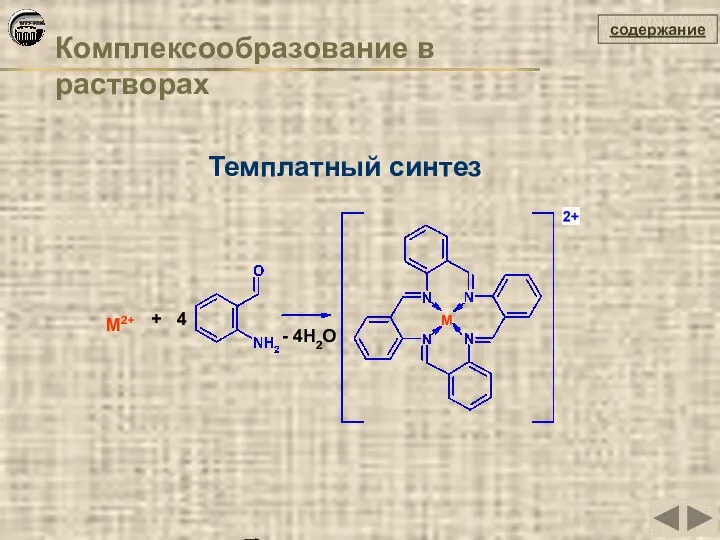
- 36. Комплексообразование в растворах содержание Темплатный синтез M2+ M + 4 - 4H2O
- 38. Устойчивость комплексов содержание [М(H2O)6]n+ + m L [M(L)m(H2O)k]n+ + (6-k)H2O Куст = [M(L)m n+] [L]m [Mn+]
- 39. Устойчивость комплексов содержание [М]n+ + L [ML]n+ ; К1 = [MLn+] [L] [Mn+] К2 = ΔG0
- 40. Разрушение комплексов содержание
- 41. Устойчивость комплексов содержание Константы нестойкости некоторых комплексов
- 43. Химия комплексных соединений важнейшей является частью неорганической химии. Знание о природе взаимодействия атомов металла и лигандов
- 45. Скачать презентацию














![Лиганды Макроциклический содержание [Ni(H2O)6]2+ + n L [Ni(L)n(H2O)2]2+ + 4H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395273/slide-16.jpg)













![Устойчивость комплексов содержание [М(H2O)6]n+ + m L [M(L)m(H2O)k]n+ + (6-k)H2O Куст](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395273/slide-37.jpg)
![Устойчивость комплексов содержание [М]n+ + L [ML]n+ ; К1 = [MLn+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395273/slide-38.jpg)




 Вирощування кристалів в додомашніх умовах
Вирощування кристалів в додомашніх умовах Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине
Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине Определение валентности элементов
Определение валентности элементов V група періодичної системи Менделєєва
V група періодичної системи Менделєєва Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады) Альдегидтер және кетондар
Альдегидтер және кетондар Кристаллические решетки
Кристаллические решетки Получение и установление состава кристаллогидрата фосфата цинка
Получение и установление состава кристаллогидрата фосфата цинка Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Теоретические основы органической химии
Теоретические основы органической химии Железо и его соединения.
Железо и его соединения. Beryllium. The physical properties of beryllium
Beryllium. The physical properties of beryllium Физический процесс и химическая реакция.
Физический процесс и химическая реакция. Общая и неорганическая химия
Общая и неорганическая химия Химические свойства алканов
Химические свойства алканов Расчёт равновесного состава
Расчёт равновесного состава Викторина. Дмитрий Иванович Менделеев
Викторина. Дмитрий Иванович Менделеев Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары
Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары Уран. Получение урана
Уран. Получение урана Значение основных химических элементов в жизни человека
Значение основных химических элементов в жизни человека Сведения о воде
Сведения о воде Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs
Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs Буровые технологические жидкости для бурения и крепления горизонтальных скважин
Буровые технологические жидкости для бурения и крепления горизонтальных скважин Имеет ли вода форму
Имеет ли вода форму Методы хроматографии. Ионообменная хроматография
Методы хроматографии. Ионообменная хроматография Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Кислород. Получение кислорода и его физические свойства
Кислород. Получение кислорода и его физические свойства