Содержание
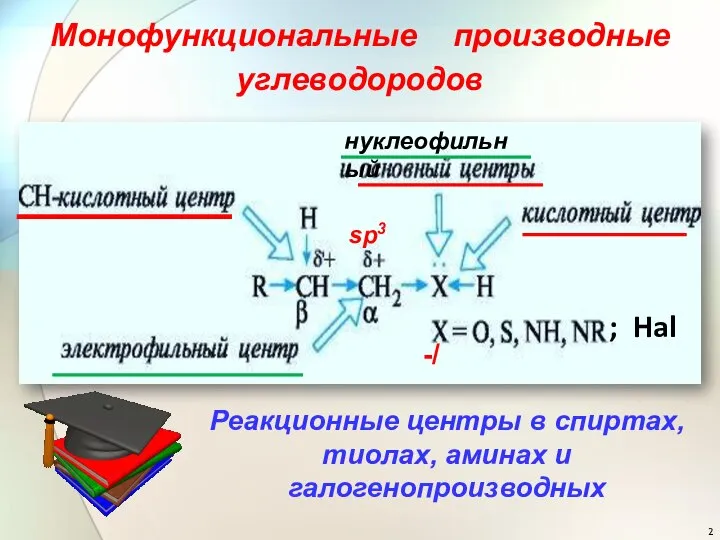
- 2. Реакционные центры в спиртах, тиолах, аминах и галогенопроизводных sp3 ; Hal -/ нуклеофильный Монофункциональные производные углеводородов
- 3. Нуклеофильное замещение у насыщенного атома углерода Нуклеофильность - способность к взаимодействию с атомом С, несущим частичный
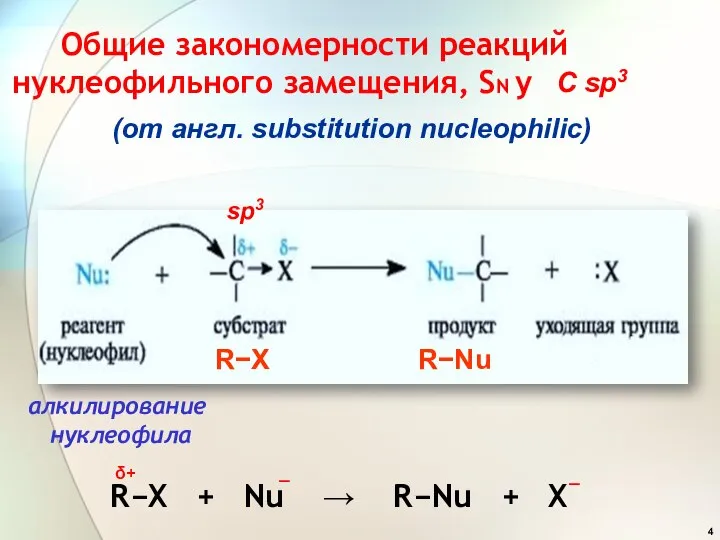
- 4. Общие закономерности реакций нуклеофильного замещения, SN у С sp3 (от англ. substitution nucleophilic) sp3 R−X R−Nu
- 5. 1. Связь в молекуле R− Х (субстрат) должна быть достаточно поляризована в сторону Х. Реакционная способность
- 6. 2. Оценочные критерии нуклеофильности: • нуклеофильность заряженного нуклеофила выше, чем соответствующей нейтральной молекулы: HO- > H2O;
- 7. 3. Замещаемый Х по нуклеофильности должен уступать атакующему Nu чем больше размер атома, тем выше нуклеофильность
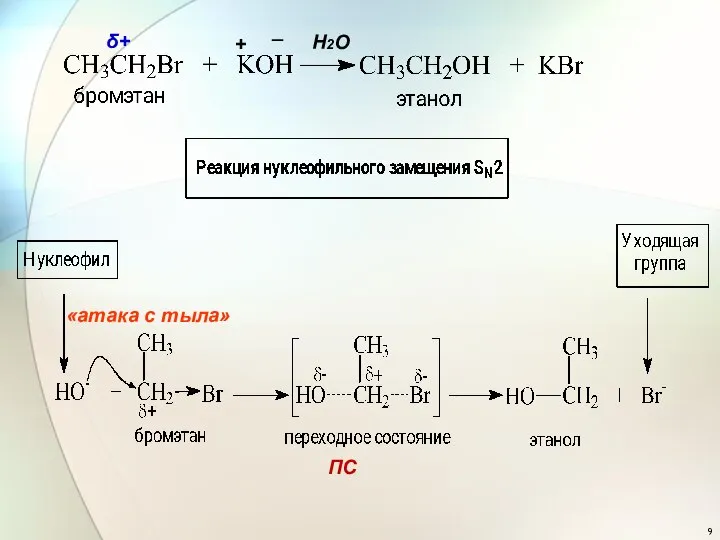
- 8. Бимолекулярное нуклеофильное замещение, SN2 : v = k ⋅ [ RX ] ⋅ [ Nu ]
- 9. «атака с тыла» ПС δ+ + _ Н2О
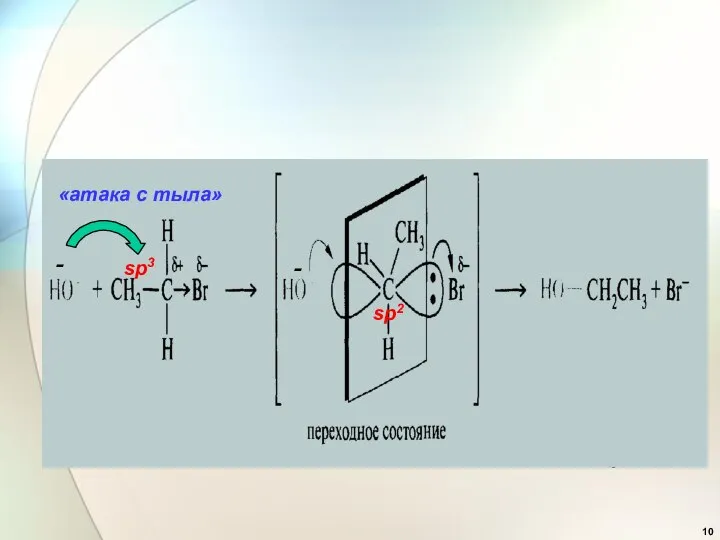
- 10. - - sp2 «атака с тыла» sp3
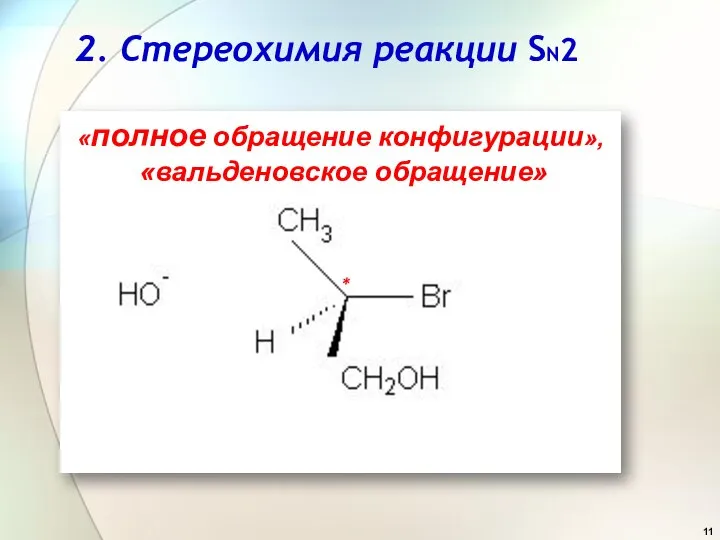
- 11. «полное обращение конфигурации», «вальденовское обращение» 2. Стереохимия реакции SN2 *
- 12. Вальден Павел Иванович – известный русский, латышский, немецкий химик, ординарный академик Императорской Академии Наук. 1863-1957 1895
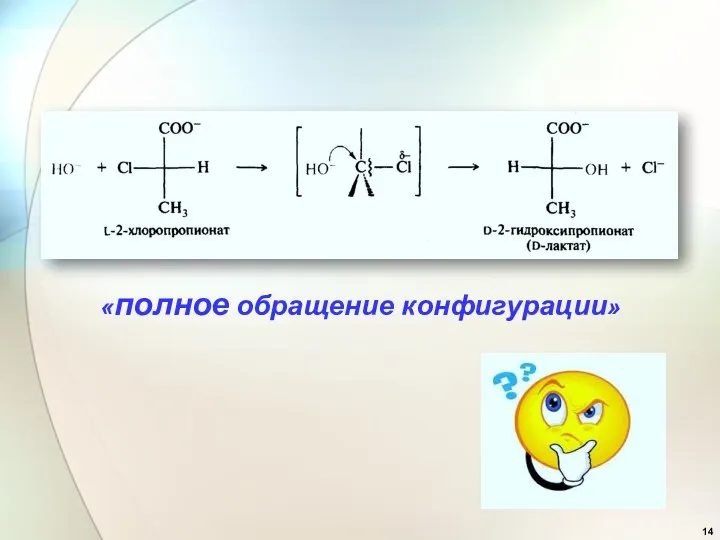
- 14. «полное обращение конфигурации»
- 15. 3. Влияние степени замещения реакционного центра Относительные скорости реакции SN2: втор. трет. CH3Br > CH3CH2Br >
- 16. трет. галогеналкан
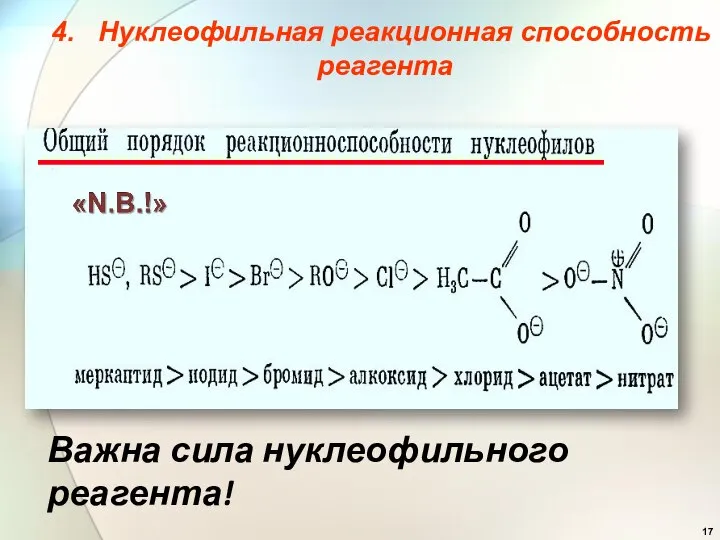
- 17. 4. Нуклеофильная реакционная способность реагента Важна сила нуклеофильного реагента!
- 18. 5. Влияние растворителя. Чем полярнее растворитель, тем менее вероятно протекание реакции по механизму SN2 Нужен неполярный
- 19. Замещаемый Х по нуклеофильности должен уступать атакующему Nu чем больше размер атома, тем выше нуклеофильность его
- 20. ХУГ- наиболее слабые основания ( галогенид-ионы); ПУГ – сильные основания ( ОН-, RO-, NH2- )
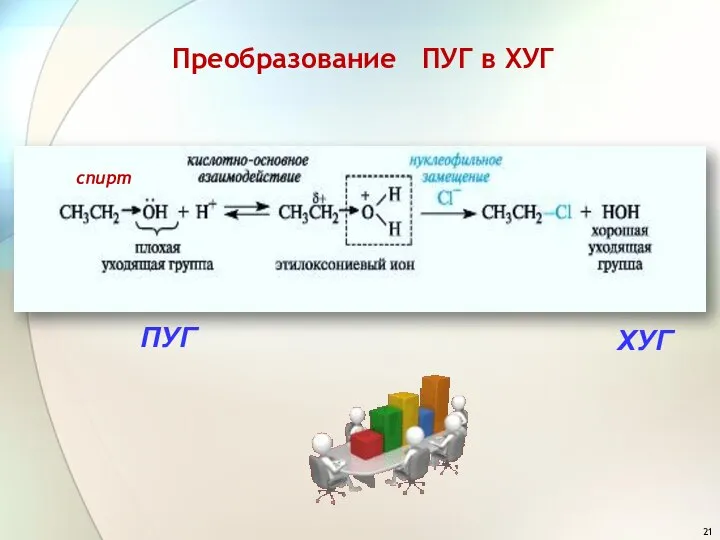
- 21. ХУГ ПУГ спирт Преобразование ПУГ в ХУГ
- 22. Реакции элиминирования – конкурирующая реакция CH- кислотный центр нуклеоф. св-ва α β α основные св-ва -I
- 23. Реакции элиминирования α β β1 КОН/спирт наиболее замещенный алкен
- 24. Мономолекулярное нуклеофильное замещение, SN1 (асинхронный механизм, диссоциативный)а v = k ⋅ [ RX ], R−X +
- 25. Реакции трет.алкилгалогенидов 1 стадия 2 стадия SN1 самопроизвольная диссоциация медленная стадия трет.
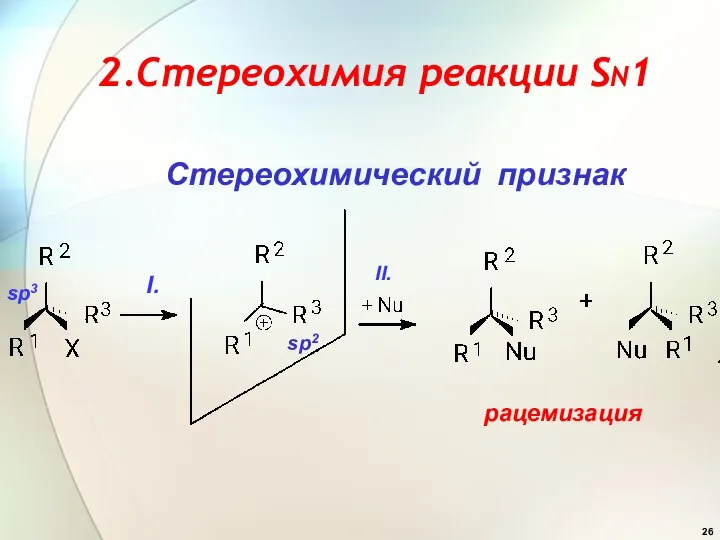
- 26. 2.Cтереохимия реакции SN1 Cтереохимический признак sp2 рацемизация I. II. sp3
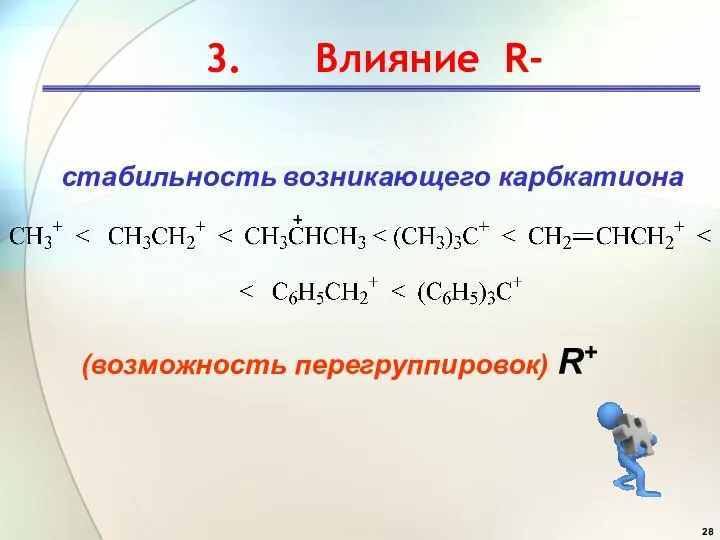
- 28. 3. Влияние R- стабильность возникающего карбкатиона (возможность перегруппировок) R+
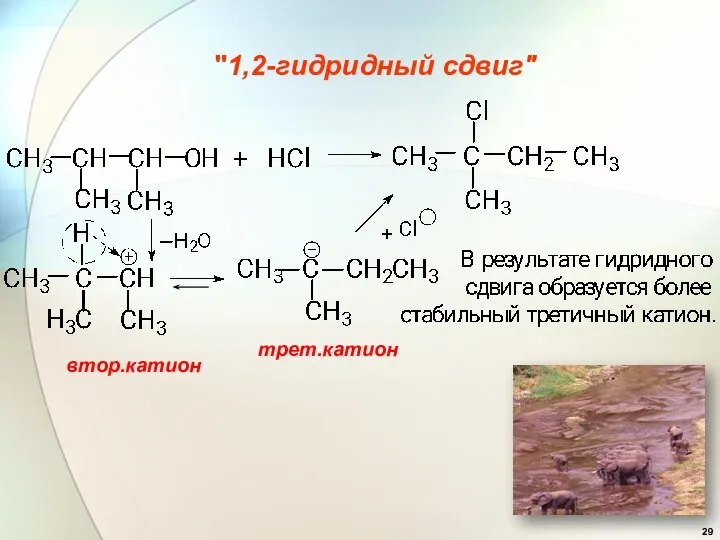
- 29. "1,2-гидридный сдвиг" втор.катион трет.катион
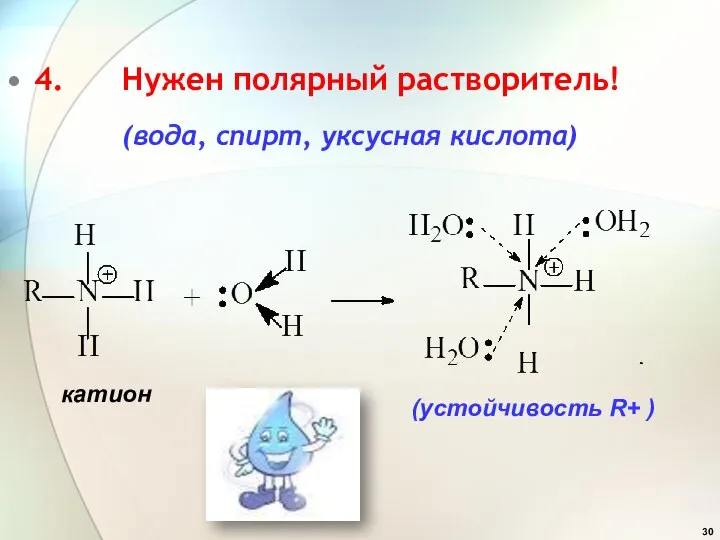
- 30. 4. Нужен полярный растворитель! (вода, спирт, уксусная кислота) (устойчивость R+ ) катион
- 31. 5. Сила нуклеофила – не влияет ( нейтральные реагенты C2H5OH ) 6. Уходящая группа ( ряд
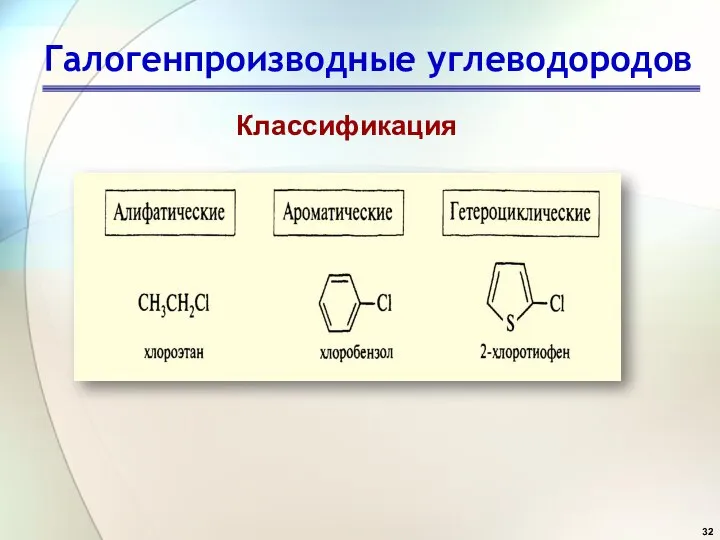
- 32. Галогенпроизводные углеводородов Классификация
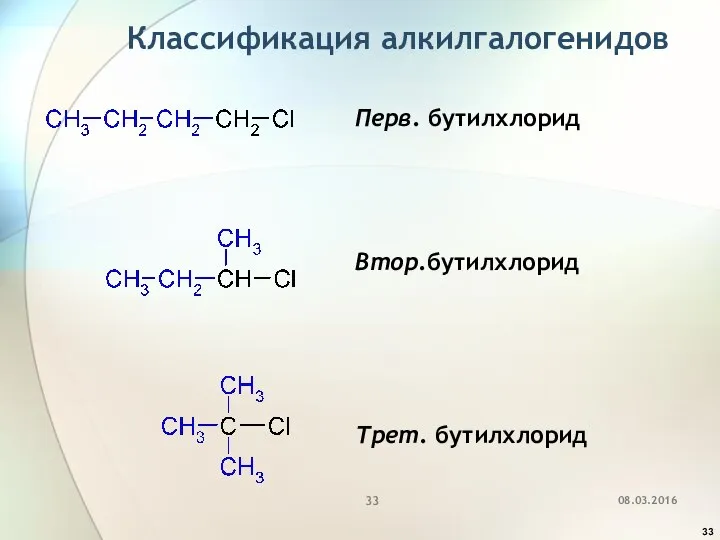
- 33. Классификация алкилгалогенидов Перв. бутилхлорид Втор.бутилхлорид Трет. бутилхлорид 08.03.2016
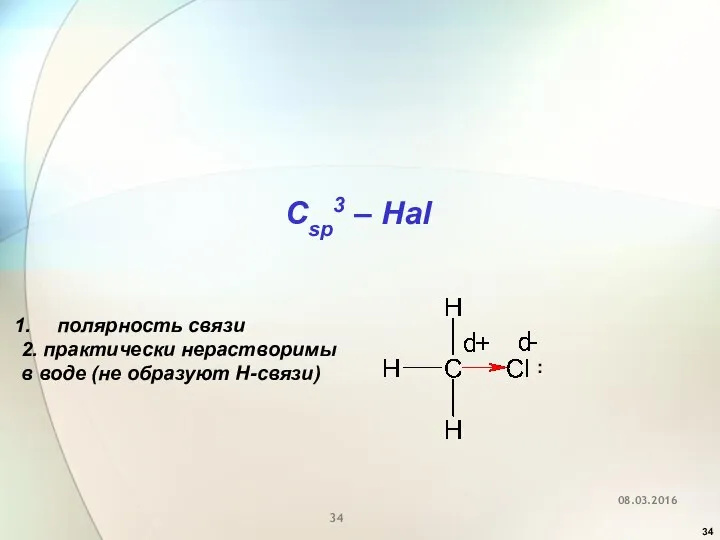
- 34. 08.03.2016 Csp3 – Hal полярность связи 2. практически нерастворимы в воде (не образуют Н-связи) :
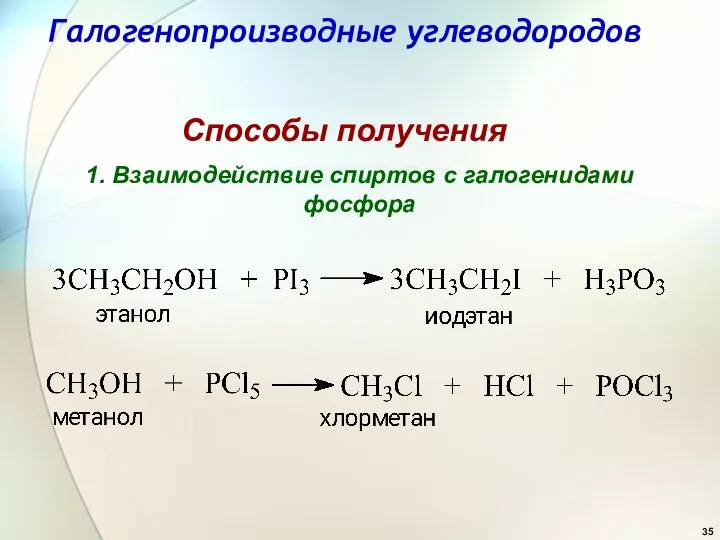
- 35. Способы получения 1. Взаимодействие спиртов с галогенидами фосфора Галогенопроизводные углеводородов
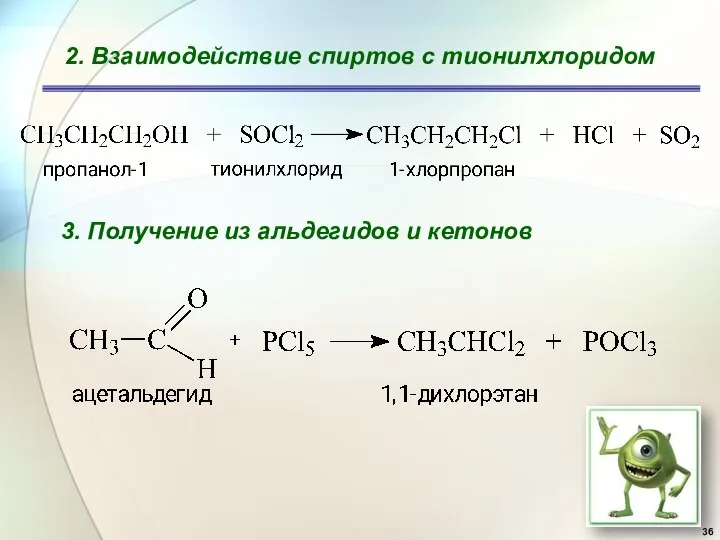
- 36. 2. Взаимодействие спиртов с тионилхлоридом 3. Получение из альдегидов и кетонов
- 37. 1. Получение простых эфиров [ + El ] Алкоголиз галогенопроизводных: перв алкоголят фенолят Получение простых эфиров
- 38. Алкилирование аминов (реакция Гофмана, 1850) 19.02.1660 - 12.11.1742 Галле Гофман Фридрих 2. Аминолиз галогенопроизводных
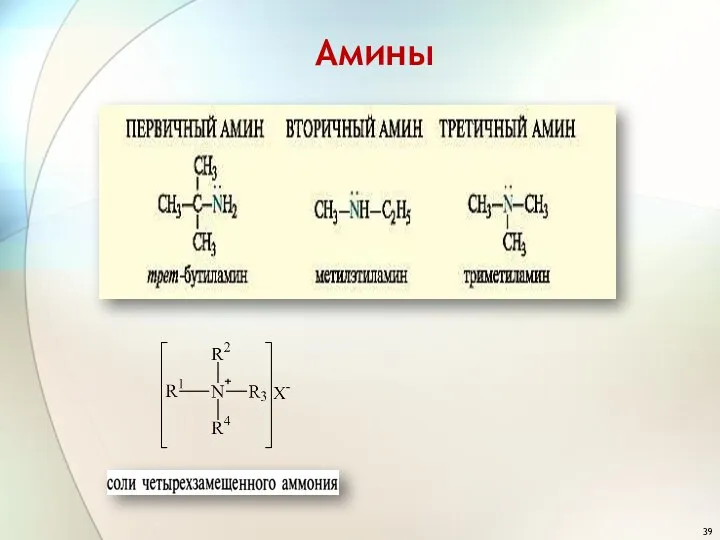
- 39. Амины
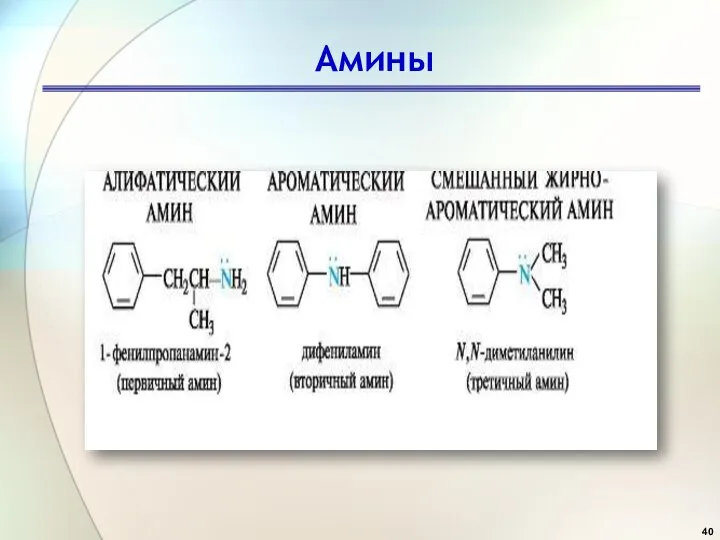
- 40. Амины
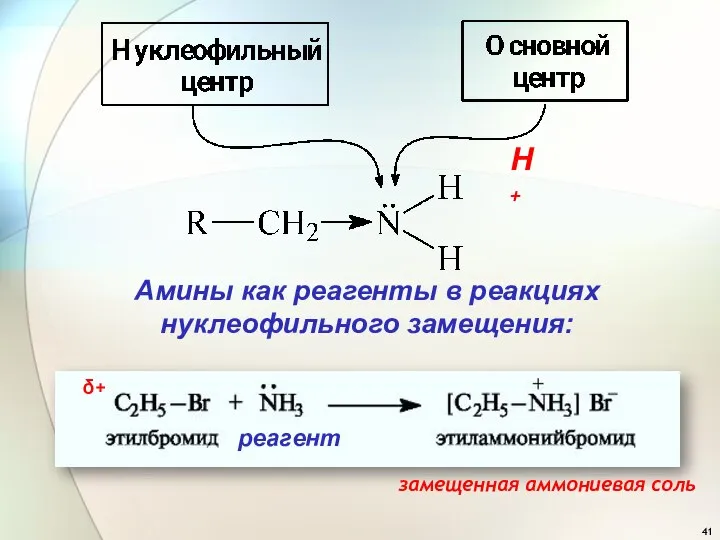
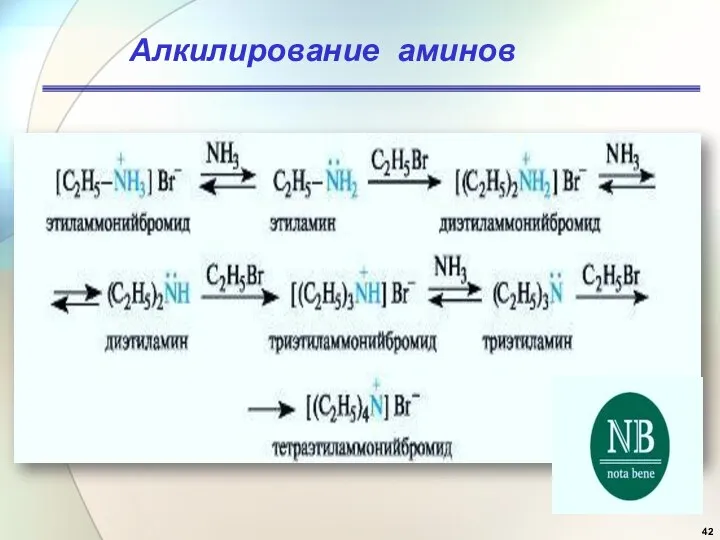
- 41. Амины как реагенты в реакциях нуклеофильного замещения: реагент Н+ δ+ замещенная аммониевая соль
- 42. Алкилирование аминов
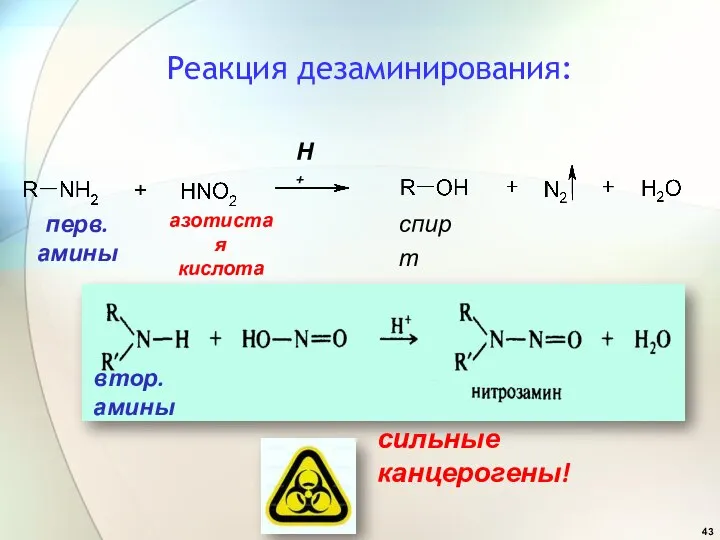
- 43. Реакция дезаминирования: перв. амины втор.амины сильные канцерогены! Н+ азотистая кислота спирт
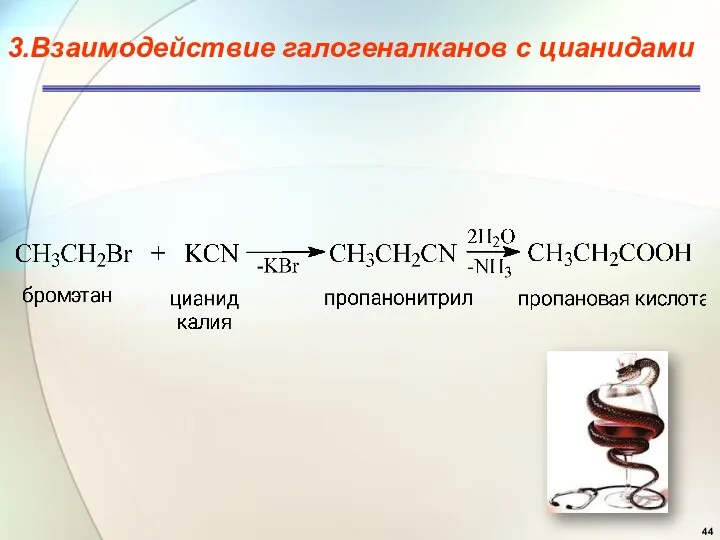
- 44. 3.Взаимодействие галогеналканов с цианидами
- 45. 4. Гидролиз галогенопроизводных (получение спиртов): RCl +H2O + KOH → ROH + KCl + H2O для
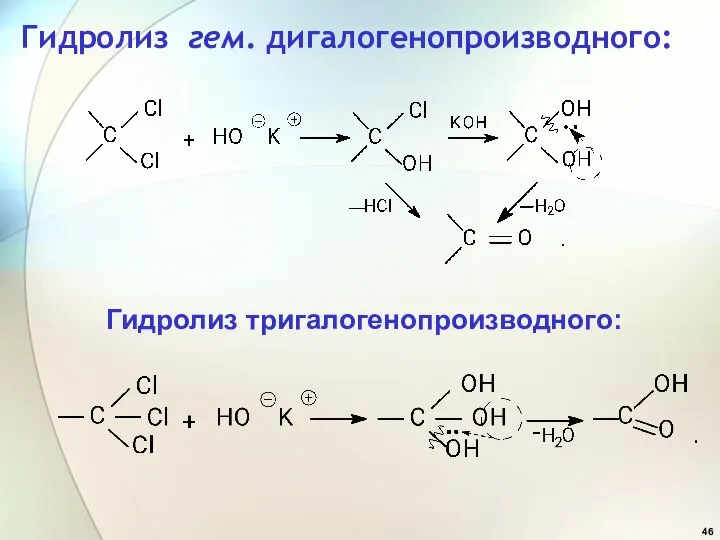
- 46. Гидролиз гем. дигалогенопроизводного: Гидролиз тригалогенопроизводного:
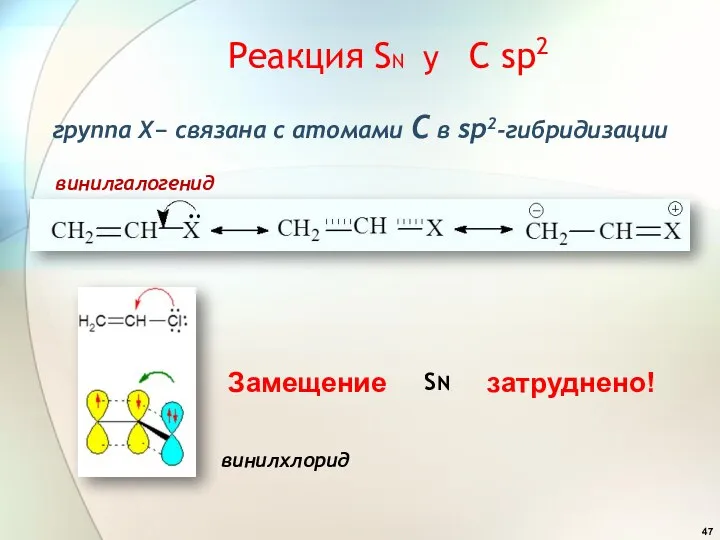
- 47. SN Реакция SN у C sp2 группа Х− связана с атомами С в sp2-гибридизации винилхлорид Замещение
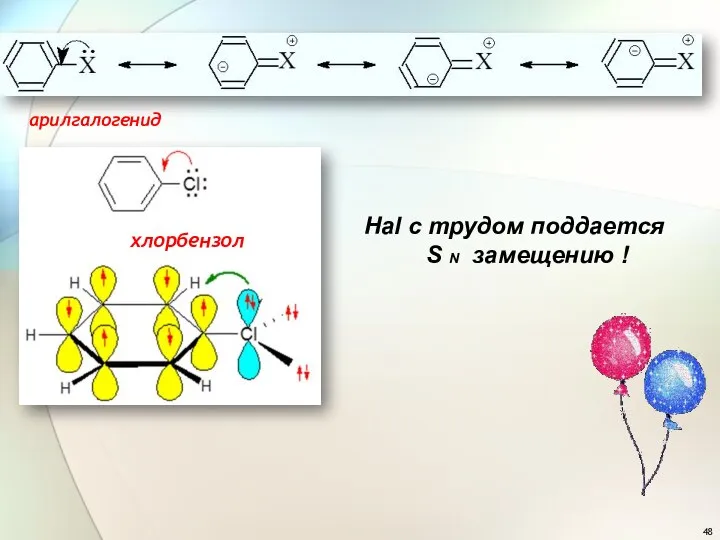
- 48. хлорбензол арилгалогенид Hal с трудом поддается S N замещению !
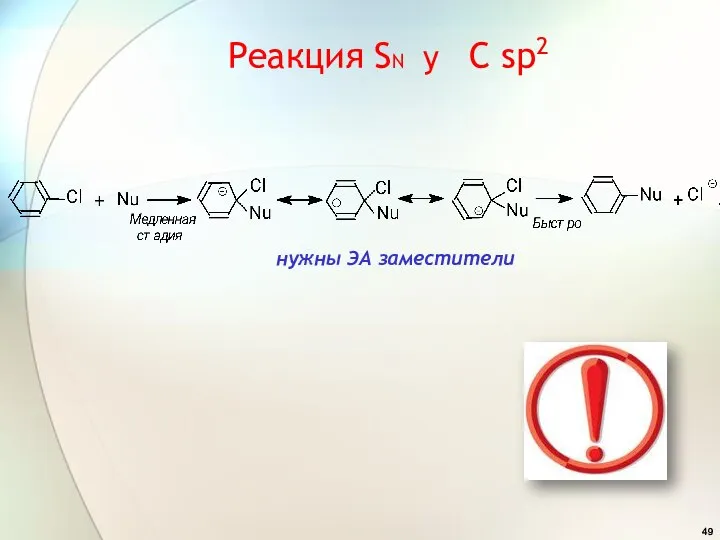
- 49. нужны ЭА заместители Реакция SN у C sp2
- 50. 6. Замещение на карбоксилат-анион (получение сложных эфиров): R- Hal + R'COO−Na+ → R−OCOR' + NaHal
- 51. 7. Замещение на нуклеофильную серу: а) получение тиолов: ОН - RHal + H2S → RSH +
- 52. 8. Замещение одного галогена на другой, более нуклеофильный ацетон RBr (или RCl) + NaJ → RJ
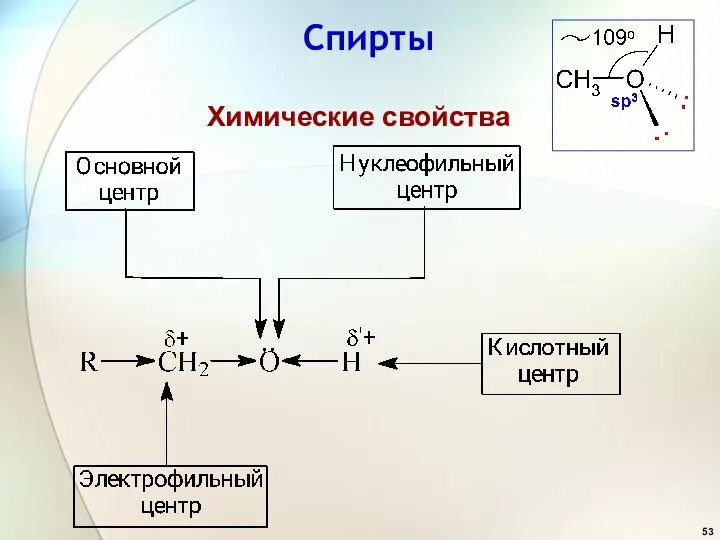
- 53. Спирты Химические свойства
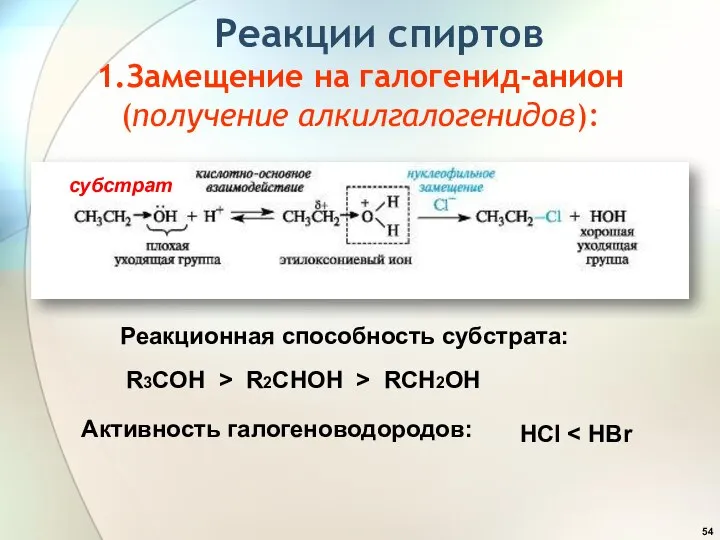
- 54. Реакции спиртов 1.Замещение на галогенид-анион (получение алкилгалогенидов): Реакционная способность субстрата: R3COH > R2CHOH > RCH2OH Активность
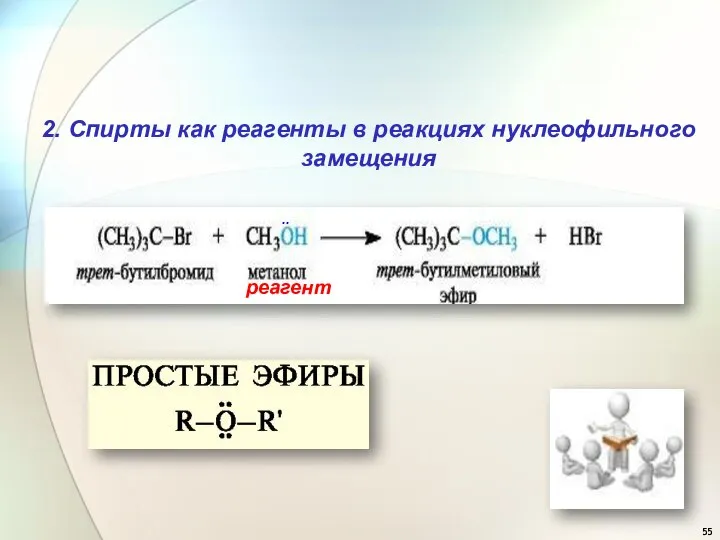
- 55. 2. Спирты как реагенты в реакциях нуклеофильного замещения реагент ∙∙
- 56. 08.03.2016 ВИНИЛИН - «бальзам Щостаковского» поливинилбутиловый эфир Обладает противомикробным действием, способствует очищению ран, регенерации тканей и
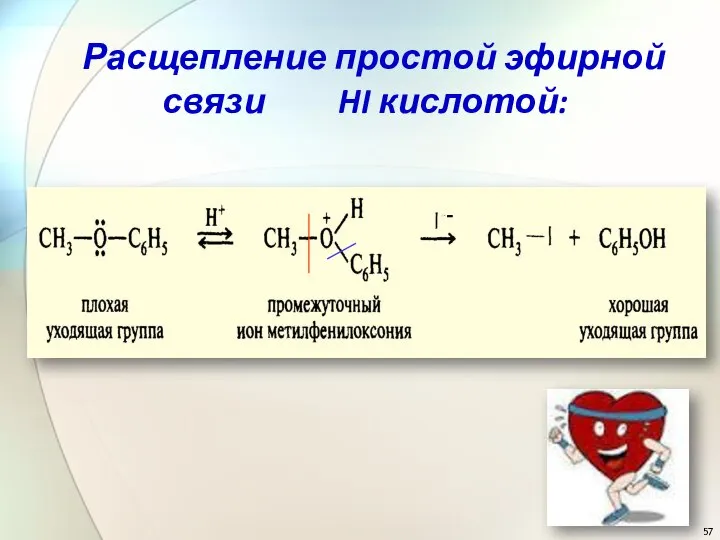
- 57. - Расщепление простой эфирной связи HI кислотой:
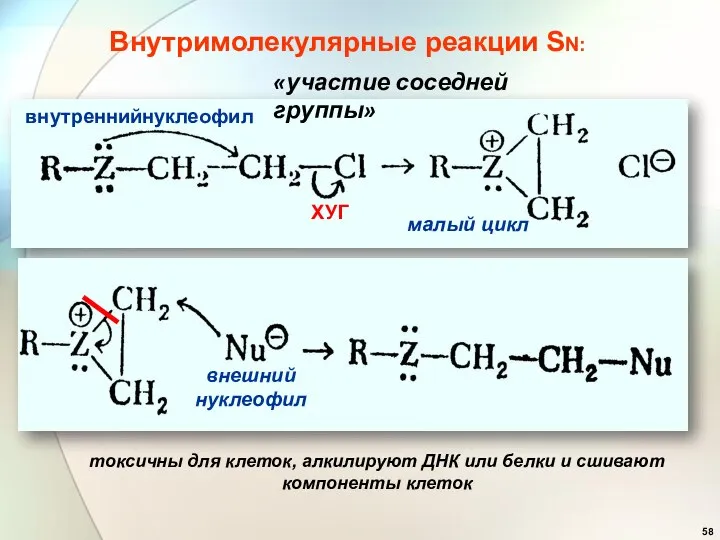
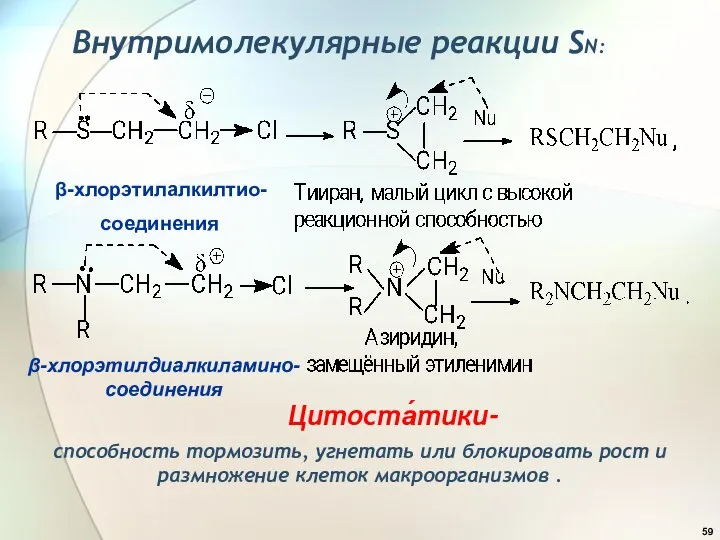
- 58. Внутримолекулярные реакции SN: малый цикл нуклеофил внутренний ХУГ внешний нуклеофил «участие соседней группы» токсичны для клеток,
- 59. Внутримолекулярные реакции SN: β-хлорэтилалкилтио- β-хлорэтилдиалкиламино- соединения соединения Цитоста́тики- способность тормозить, угнетать или блокировать рост и размножение
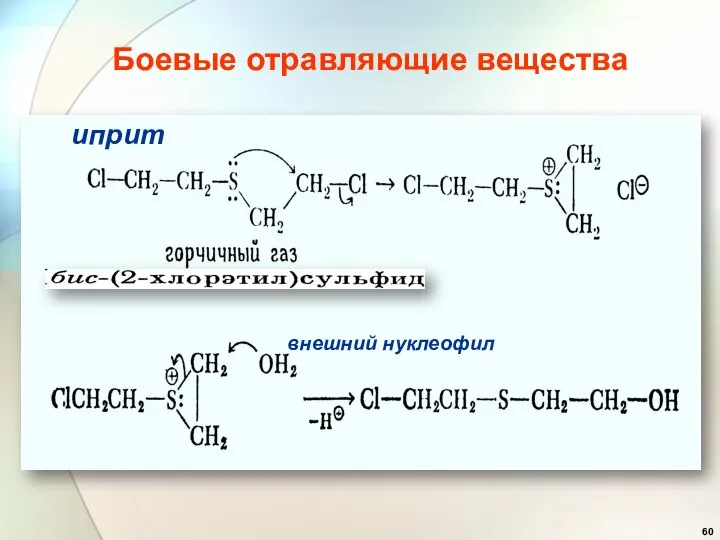
- 60. Боевые отравляющие вещества иприт внешний нуклеофил
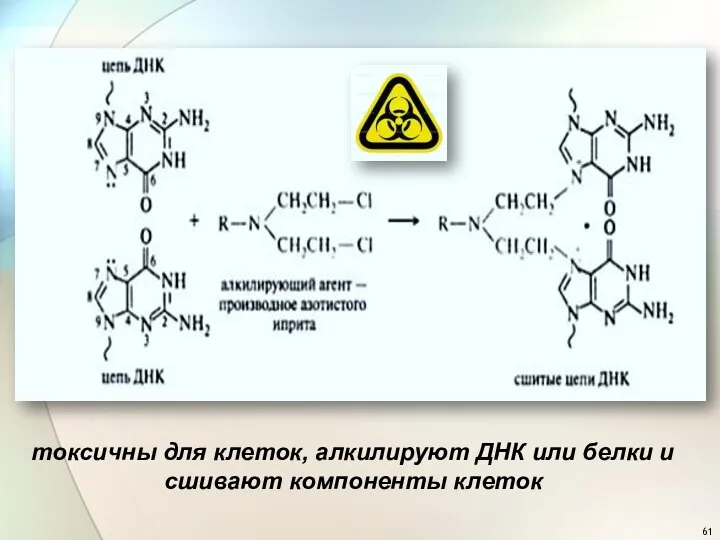
- 61. токсичны для клеток, алкилируют ДНК или белки и сшивают компоненты клеток
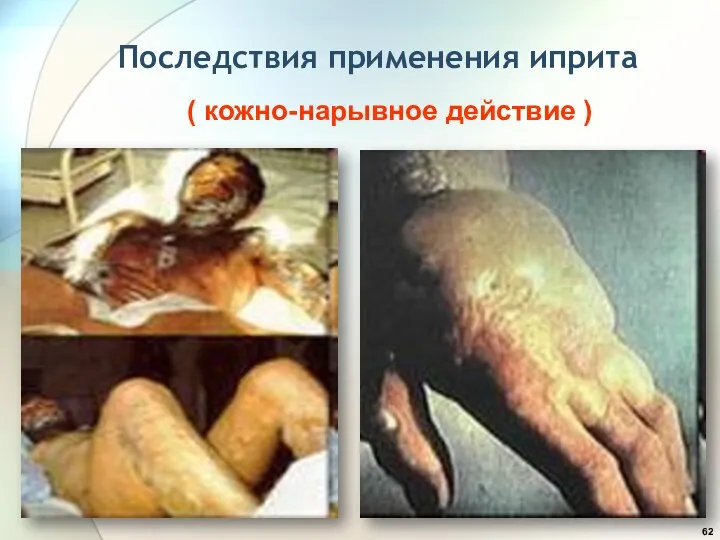
- 62. Последствия применения иприта ( кожно-нарывное действие )
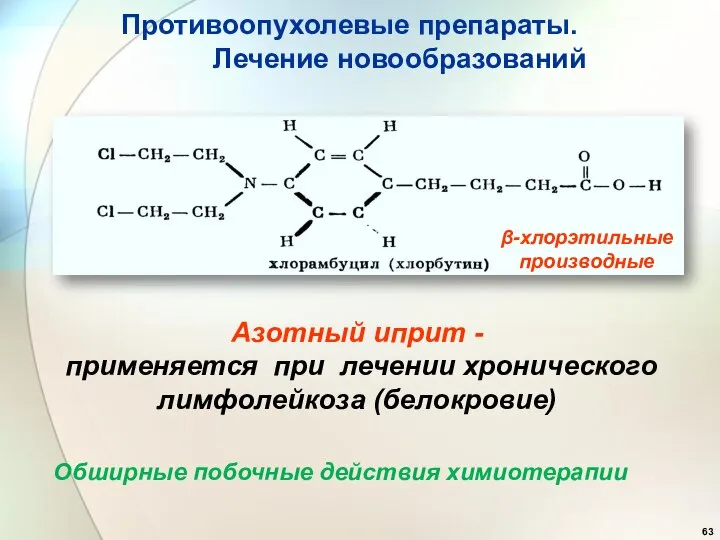
- 63. β-хлорэтильные производные Азотный иприт - применяется при лечении хронического лимфолейкоза (белокровие) Противоопухолевые препараты. Лечение новообразований Обширные
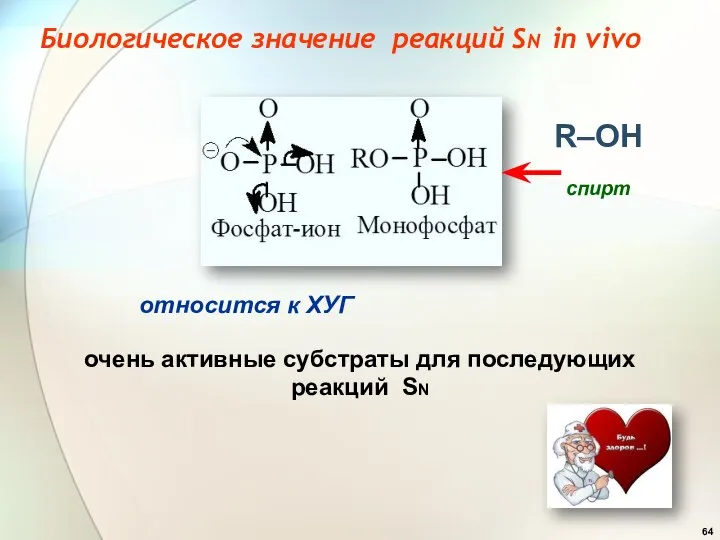
- 64. Биологическое значение реакций SN in vivo R–OH относится к ХУГ очень активные субстраты для последующих реакций
- 65. спасибо за внимание!
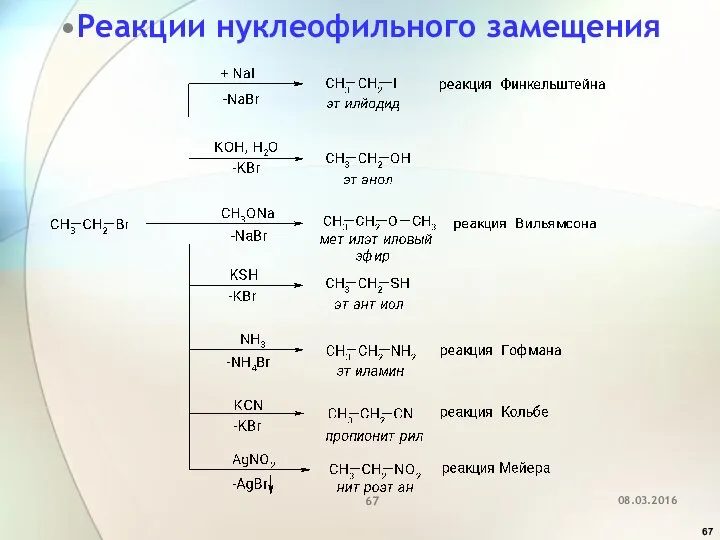
- 67. Реакции нуклеофильного замещения 08.03.2016
- 69. Скачать презентацию


















![1. Получение простых эфиров [ + El ] Алкоголиз галогенопроизводных: перв](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1392611/slide-36.jpg)








 углерод и его свойства
углерод и его свойства Адские задания. ЕГЭ по химии
Адские задания. ЕГЭ по химии Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Физико-химические методы исследования биополимеров: Структурная формула соединения
Физико-химические методы исследования биополимеров: Структурная формула соединения Высoкомолекулярные соединения (ВМС). Основные понятия. Химическое строение
Высoкомолекулярные соединения (ВМС). Основные понятия. Химическое строение Термодинамика и теплопередача. Реальные газы
Термодинамика и теплопередача. Реальные газы Структура и функции биомакромолекул. Лекция 1
Структура и функции биомакромолекул. Лекция 1 Растворы неэлектролитов и электролитов
Растворы неэлектролитов и электролитов «Химия позволяет раскрыть тайны мироздания»
«Химия позволяет раскрыть тайны мироздания» Горение. Подводный факел
Горение. Подводный факел Эндогенная серия. Карбонатитовая группа
Эндогенная серия. Карбонатитовая группа Углерод и кремний
Углерод и кремний Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Презентация по Химии "НИТРАТЫ. ИХ ВЛИЯНИЕ НА ЗДОРОВЬЕ ЛЮДЕЙ" - скачать смотреть бесплатно
Презентация по Химии "НИТРАТЫ. ИХ ВЛИЯНИЕ НА ЗДОРОВЬЕ ЛЮДЕЙ" - скачать смотреть бесплатно Электроотрицательность (ЭО). Ковалентная связь
Электроотрицательность (ЭО). Ковалентная связь Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп
Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп Просто знать еще не все, знания необходимо еще использовать
Просто знать еще не все, знания необходимо еще использовать Мухит пен өзен суларының қаттылық қасиеттерін анықтау
Мухит пен өзен суларының қаттылық қасиеттерін анықтау Нефть и способы её переработки
Нефть и способы её переработки Мыло. Синтетические моющие средства
Мыло. Синтетические моющие средства Презентация по Химии "Презентация Медь" - скачать смотреть
Презентация по Химии "Презентация Медь" - скачать смотреть  Пластмассы. Компоненты
Пластмассы. Компоненты Карбоновые кислоты
Карбоновые кислоты Продукты - рекордсмены по содержанию различных минеральных компонентов
Продукты - рекордсмены по содержанию различных минеральных компонентов Весы. Камни Весов
Весы. Камни Весов Качественное и количественное определение содержания аскорбиновой кислоты в продуктах питания
Качественное и количественное определение содержания аскорбиновой кислоты в продуктах питания Нанотехнологии в быту
Нанотехнологии в быту Установление структуры биополимеров
Установление структуры биополимеров