Содержание
- 2. План лекции 1. Агрегатные состояния вещества. 2. Свойства разбавленных растворов. Осмос. Кипение и замерзание растворов. 3.Теория
- 3. 1.Агрегатные состояния вещества. плавление кристаллизация испарение конденсация возгонка сублимация
- 4. 2.Осмос. Осмос – это односторонняя диффузия молекул растворителя через полупроницаемую мембрану из растворителя в раствор или
- 5. Кипение и замерзание растворов неэлектролитов Δ t кип. - повышение температуры кипения раствора Δ t кип.
- 6. Свойства растворов электролитов. i- изотонический коэффициент показывает меру отклонения поведения растворов электролитов от неэлектролитов. ( i
- 7. 3.Теория электролитической диссоциации Аррениуса (ТЭД) Электролиты- это вещества, растворы или расплавы которых проводят электрический ток. Неэлектролиты
- 8. 4. Сильные и слабые электролиты. α- степень диссоциации электролита: α= n/N·100% n –число молекул, распавшихся на
- 9. Константа диссоциации слабых электролитов Слабые электролиты диссоциируют обратимо и ступенчато. В их растворах устанавливается динамическое равновесие.
- 10. 5.Равновесие в растворах слабых электролитов. Влияние одноименного иона на диссоциацию слабого электролита. Пример. Что произойдет с
- 11. Влияние связывающего иона на диссоциацию слабого электролита. Пример. Что произойдет с диссоциацией HF при добавлении КОН?
- 12. Способы выражения концентрации растворов 1. Массовая доля, С, % - показывает сколько граммов растворенного вещества содержится
- 13. 3. Моляльная концентрация, , моль/кг растворителя. - показывает сколько моль растворенного вещества содержится в 1 кг
- 14. 5. Титр, Т, г/мл – показывает сколько граммов растворенного вещества содержится в 1 мл раствора 6.
- 15. Значение растворов электролитов для живых организмов 1. Электролиты – это составная часть жидкостей и плотных тканей
- 17. Скачать презентацию














 Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1)
Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1) Штучні і синтетичні волокна
Штучні і синтетичні волокна  Химиялық реакция белгілерін атаңыз
Химиялық реакция белгілерін атаңыз Металлы и сплавы с высокой удельной прочностью
Металлы и сплавы с высокой удельной прочностью Физические и химические явления
Физические и химические явления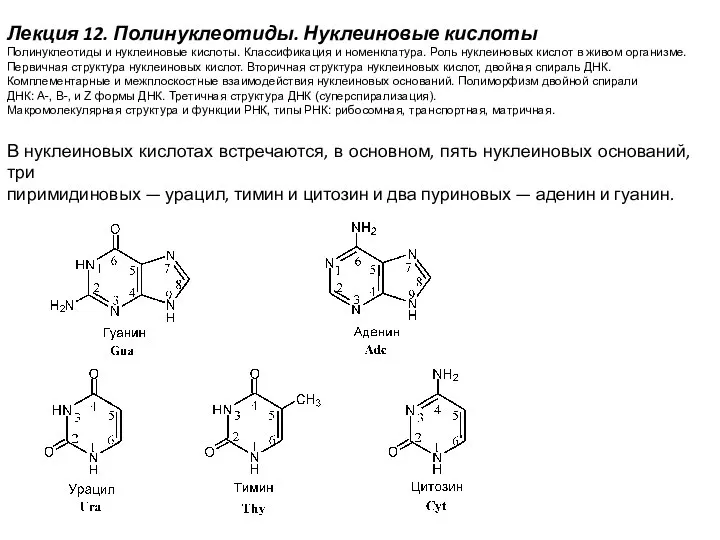 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты Выдающиеся ученые - химики и их заслуги
Выдающиеся ученые - химики и их заслуги Классификация моющих средств
Классификация моющих средств Узинская ООШ исслед.работа Лобановой Елизаветы
Узинская ООШ исслед.работа Лобановой Елизаветы Молярный объём газообразного вещества
Молярный объём газообразного вещества Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов Тыңайтқыштар
Тыңайтқыштар Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат
Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат Неидеальные растворы
Неидеальные растворы Introduction to metabolism
Introduction to metabolism Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов.
Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов. Алкены
Алкены Презентация Лекарства дома
Презентация Лекарства дома Химия (Органическая химия)
Химия (Органическая химия) Цикли трикарбонових кислот
Цикли трикарбонових кислот Алкадиены
Алкадиены Оксиды азота.
Оксиды азота. Общая химия, понятия
Общая химия, понятия Р-элементы IV группы: C, Si, Ge, Sn, Pb
Р-элементы IV группы: C, Si, Ge, Sn, Pb Основні класи неорганічних сполук
Основні класи неорганічних сполук Общая и неорганическая химия
Общая и неорганическая химия Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще
Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии
Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии