Содержание
- 2. Главные научные открытия в области обмена белков принадлежат Российским ученым
- 3. Академик Опарин Александр Иванович (Лауреат Ленинской премии 1974 г.; Премии им. А.Н. Баха, Награжден Золотой медалью
- 4. Академик Баев Александр Александрович. (Лауреат Государственной премии 1969 г)
- 5. Академик Спирин Александр Сергеевич (лауреат Ленинской премии 1976 г. Награжден медалью им. Ганса Кребса федерации Европейского
- 6. Роль белков в организме Структурная Каталитическая Транспортная Регуляторная Защитная Гомеостатическая Депонирующая Функциональная
- 7. Динамика обновления белков За сутки распадается белков ~ 400 г Из них распадается полностью до СО2;
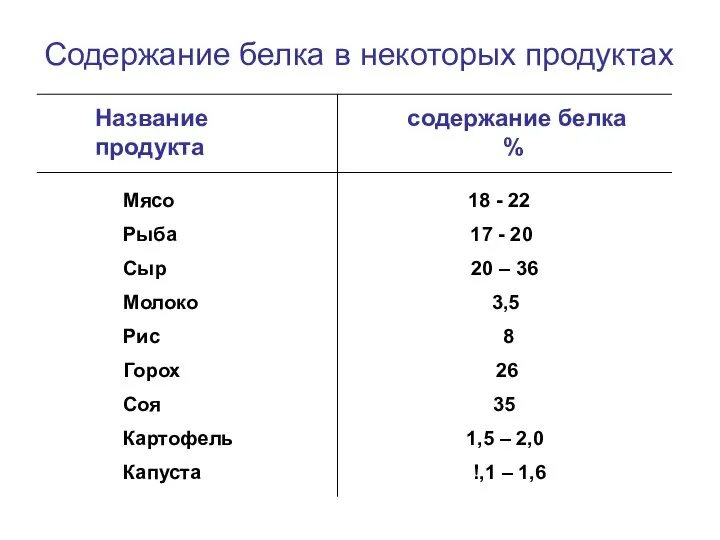
- 8. Содержание белка в некоторых продуктах Название содержание белка продукта % Мясо 18 - 22 Рыба 17
- 9. Биологическая ценность аминокислот заменимые пируват ----------------------→ аланин глицерин- ---------------------→ серин серин -------------------------→ глицин аланин-----------------------→ цистеин щук
- 10. примеры продуктов, содержащие неполноценные белки название продукта 1. белки растительных несбалансированный продуктов аминокислотный состав 2. белки
- 11. Переваривание белков в желудочно-кишечном тракте
- 12. Слизистая оболочка желудка
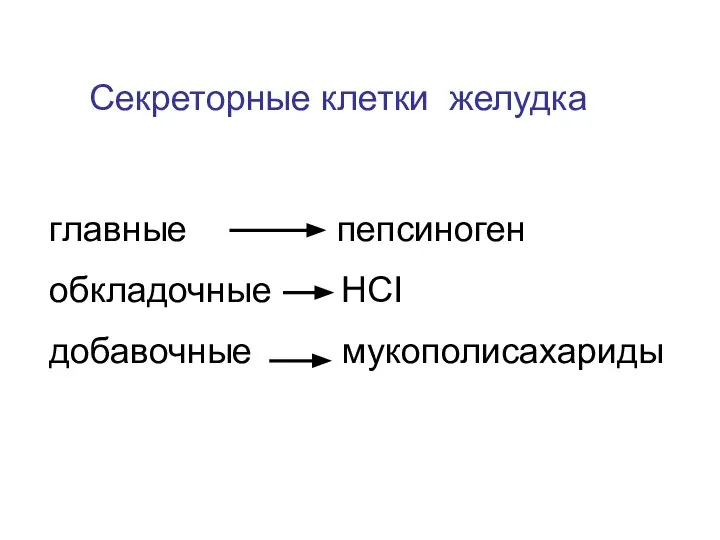
- 13. Секреторные клетки желудка главные пепсиноген обкладочные НCI добавочные мукополисахариды
- 14. Состав желудочного сока Вода 99% НСI 0,5-0,6% Соли 0,1% Пепсин 2 г/сут Гастриксин Реннин (у детей)
- 15. Роль НСI в переваривании белков Создает оптимум рН для активности пепсина; 2. Обладает бактерицидным действием; Разрушая
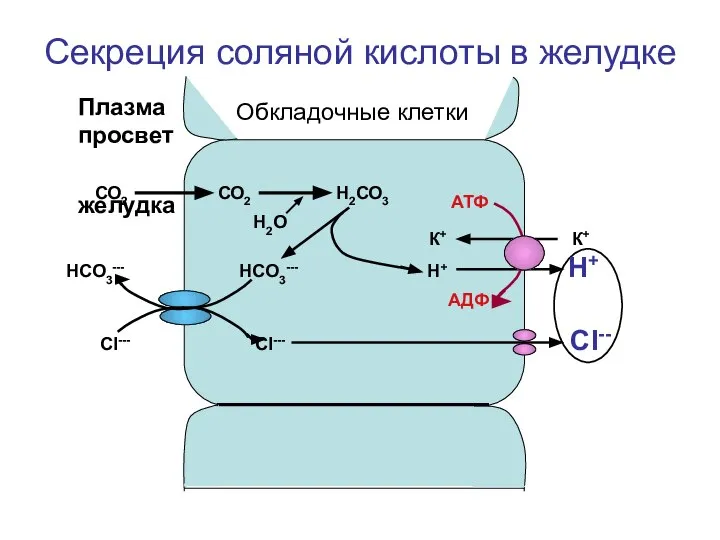
- 16. Секреция соляной кислоты в желудке Обкладочные клетки СО2 СО2 Н2СО3 К+ К+ НСО3--- НСО3--- Н+ Н+
- 17. Медицинские названия нарушений кислотности желудочного сока Повышенная кислотность гиперхлоргидрия Пониженная кислотность гипохлоргидрия Прекращение образования соляной кислоты
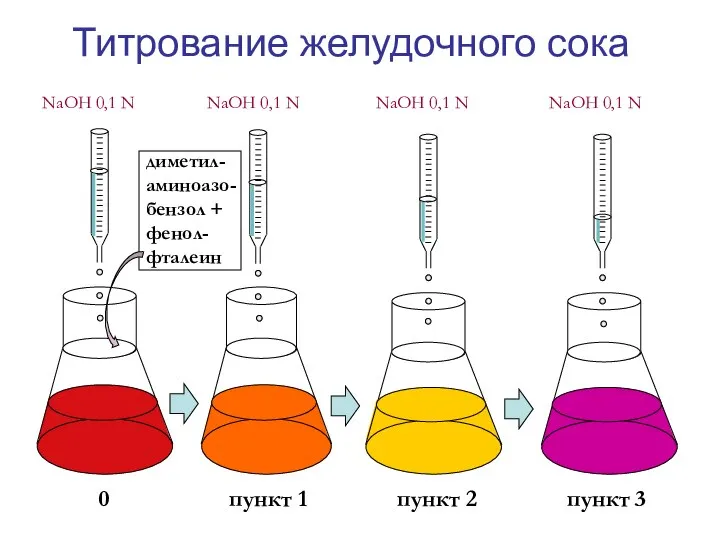
- 18. Титрование желудочного сока NaOH 0,1 N NaOH 0,1 N NaOH 0,1 N NaOH 0,1 N диметил-аминоазо-бензол
- 19. Расчет результатов титрования Пункт 1. нейтрализация свободной НСI. (мл х 10 = Т.Е.) Пункт 3. нейтрализация
- 20. Показатели кислотности желудочного сока в норме (после стимуляции секреции отваром капусты) Общая кислотность - 40 -
- 21. Показатели кислотности желудочного сока в норме (после стимуляции секреции гистамином) Общая кислотность - 100 - 120
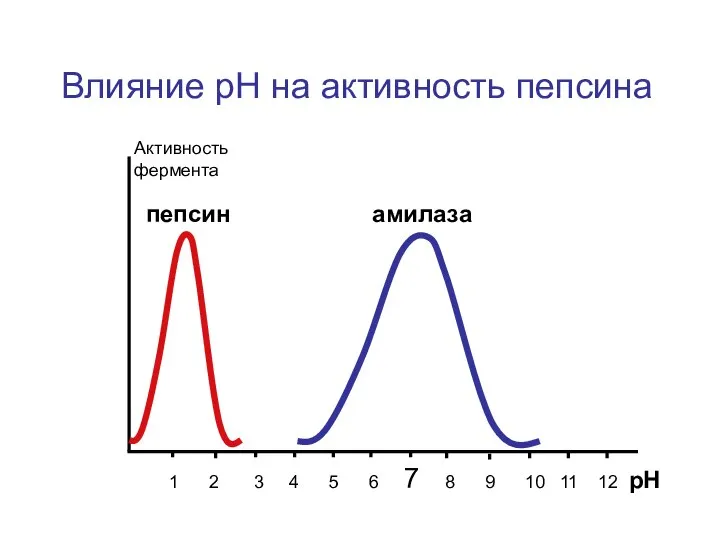
- 22. 1 2 3 4 5 6 7 8 9 10 11 12 рН Активность фермента Влияние
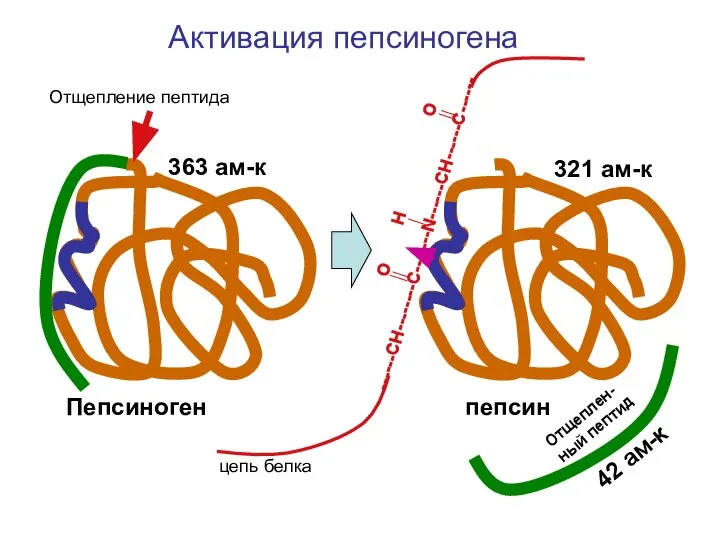
- 23. O H O ------CH--------С-------N------CH------C------ цепь белка Пепсиноген пепсин Отщепление пептида Отщеплен-ный пептид Активация пепсиногена 363 ам-к
- 24. Защита эпителиальных клеток полисахаридным слоем Слизистая оболочка стенки желудка
- 25. Дефект слизистой оболочки при язвенной болезни желудка
- 26. Протеолитические проферменты и ферменты, образующиеся в поджелудочной железе и механизм их активации трипсиноген трипсин химотрипсиноген химотрипсин
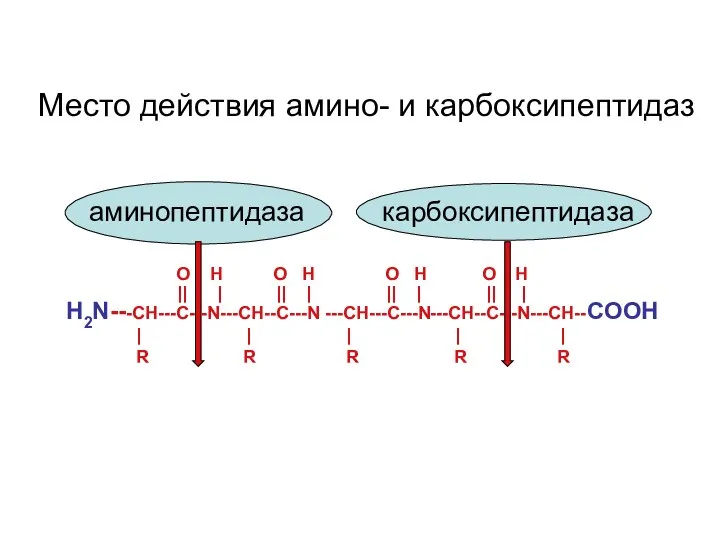
- 27. O H O H O H O H Н2N---CH---С---N---CH--C---N ---CH---С---N---CH--C---N---CH--COOH || | || | || |
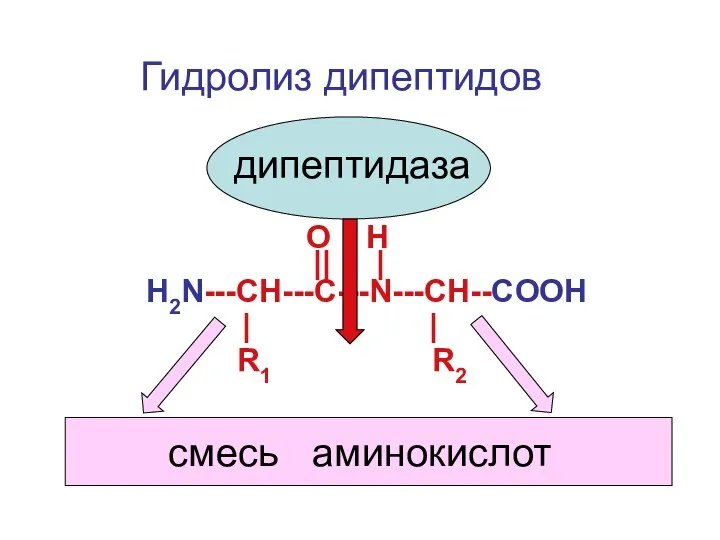
- 28. O H Н2N---CH---С---N---CH--COOH || | R1 R2 | | дипептидаза Гидролиз дипептидов смесь аминокислот
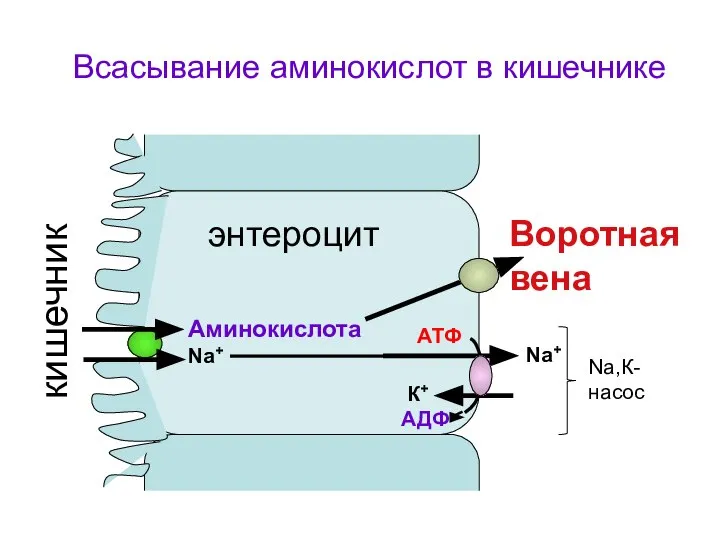
- 29. Аминокислота Na+ Nа+ К+ АТФ АДФ Воротная вена кишечник Всасывание аминокислот в кишечнике Na,К-насос энтероцит
- 30. Образование токсичных веществ из аминокислот в кишечнике под влиянием бактерий
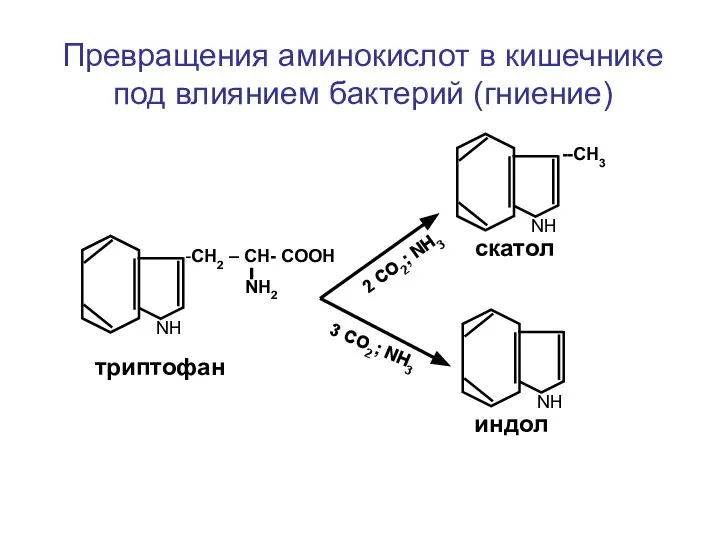
- 31. Превращения аминокислот в кишечнике под влиянием бактерий (гниение) -СН2 – СН- СООН NН2 NН NН NН
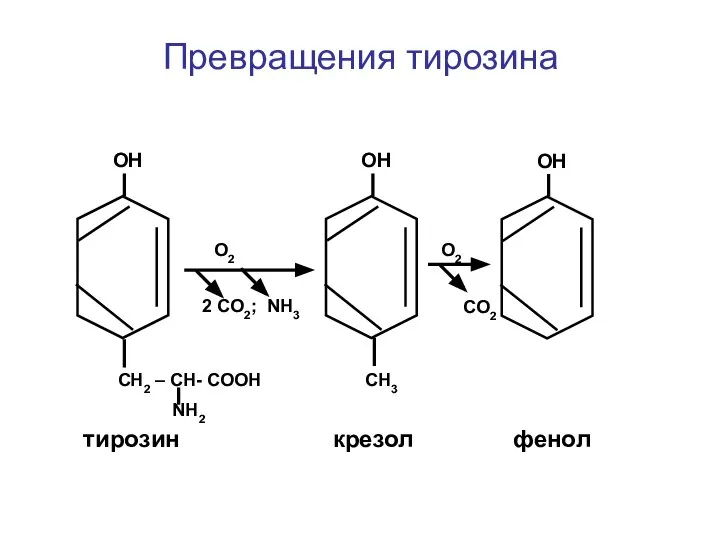
- 32. Превращения тирозина ОН СН2 – СН- СООН NН2 ОН СН3 ОН 2 СО2; NH3 CO2 O2
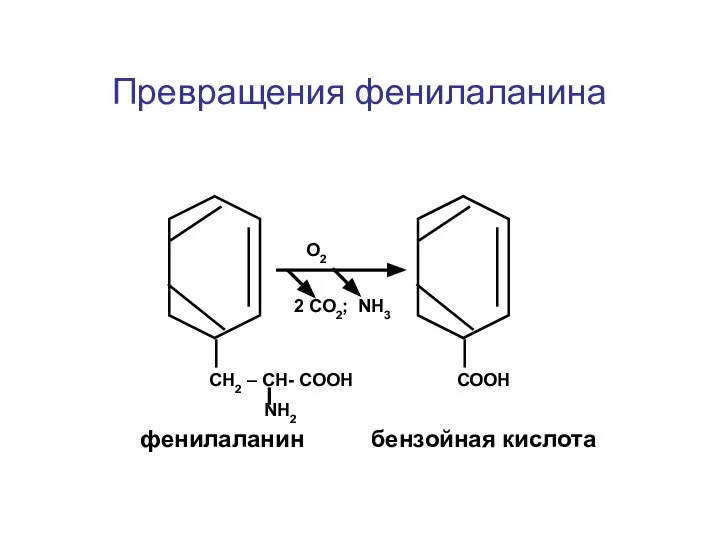
- 33. Превращения фенилаланина СН2 – СН- СООН NН2 СООН 2 СО2; NH3 O2 фенилаланин бензойная кислота
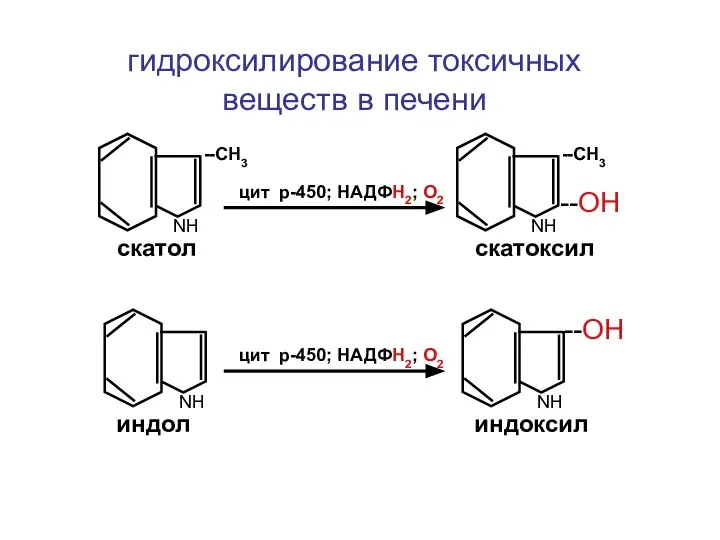
- 34. NН NН --СН3 скатол индол NН NН --СН3 скатоксил индоксил --ОН --ОН цит р-450; НАДФН2; О2
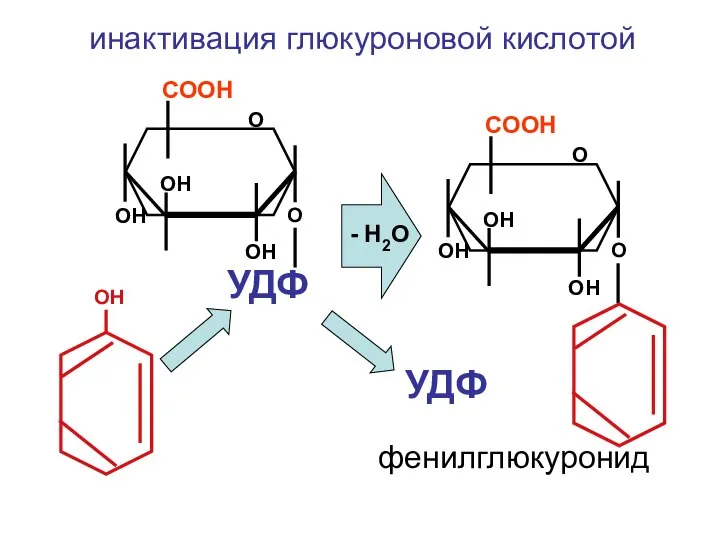
- 35. О СООН ОН ОН ОН УДФ О ОН О СООН ОН ОН ОН О инактивация глюкуроновой
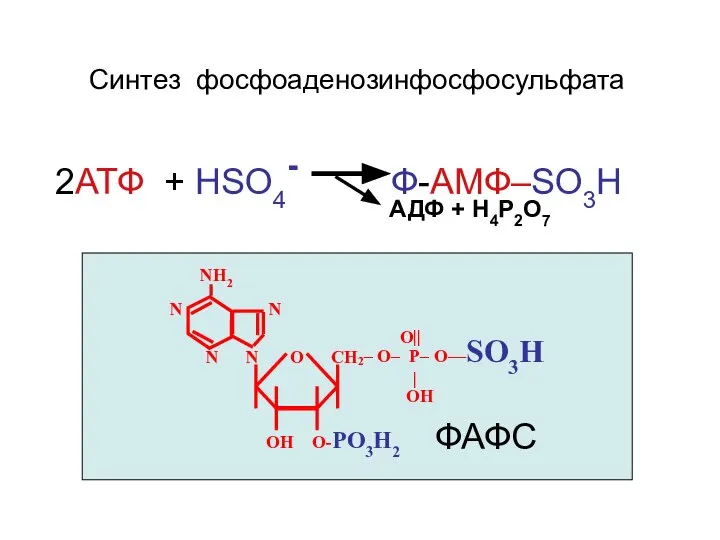
- 36. Синтез фосфоаденозинфосфосульфата 2АТФ + НSO4- Ф-АМФ–SO3H АДФ + Н4Р2О7 NH2 N N О || N N
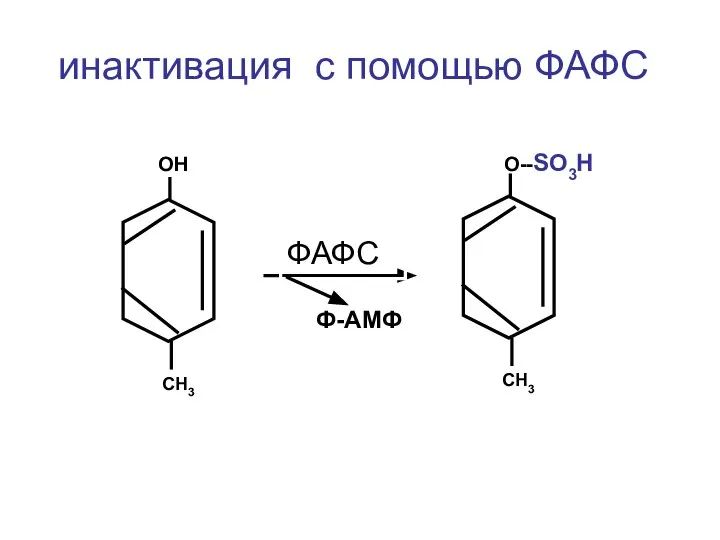
- 37. инактивация с помощью ФАФС ОН СН3 О--SO3H СН3 ФАФС Ф-АМФ
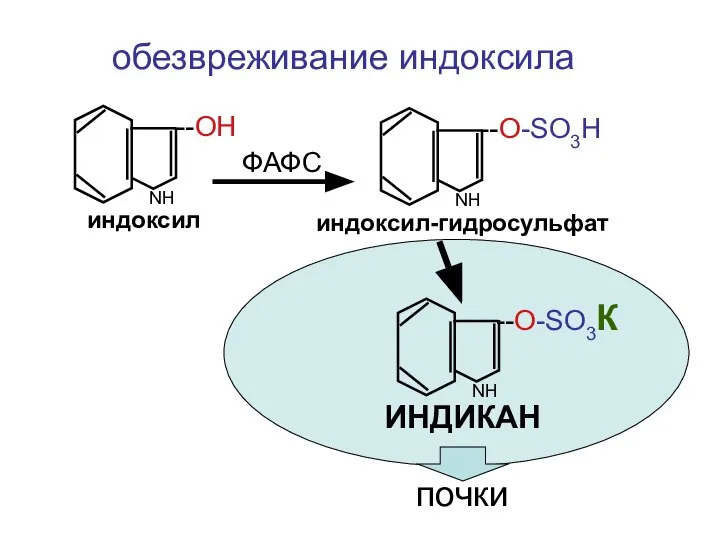
- 38. NН индоксил --ОН NН индоксил-гидросульфат --О-SO3H ФАФС NН --О-SO3К ИНДИКАН обезвреживание индоксила почки
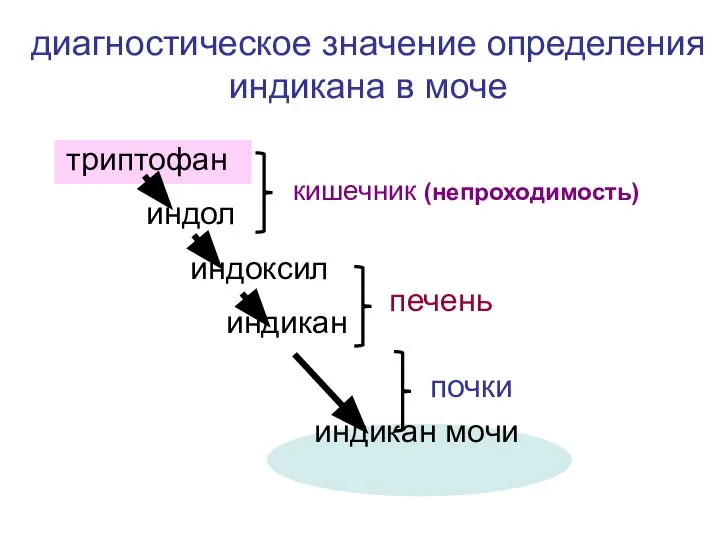
- 39. триптофан индол индоксил индикан индикан мочи кишечник (непроходимость) печень почки диагностическое значение определения индикана в моче
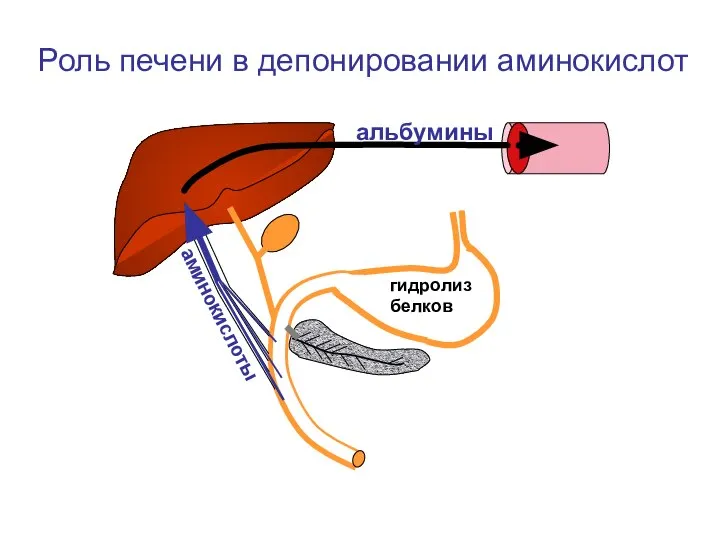
- 40. аминокислоты альбумины Роль печени в депонировании аминокислот гидролиз белков
- 41. Роль альбумина Запасной источник аминокислот Компонент буферной системы Осмотически активный белок Переносчик жирных кислот Переносчик жирорастворимых
- 42. Какому больному можно сделать операцию? Больной № 1 Общий белок – 65 г/л Альбумины - 40
- 43. В аппарат Гольджи Многие белки требуют достраивания.
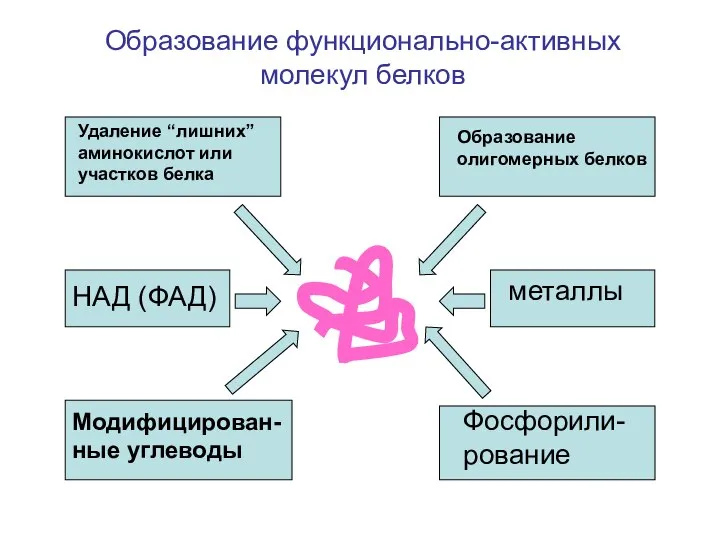
- 44. НАД (ФАД) Модифицирован-ные углеводы металлы Фосфорили-рование Удаление “лишних” аминокислот или участков белка Образование олигомерных белков Образование
- 45. Присоединение к растущей белковой молекуле углеводных структур
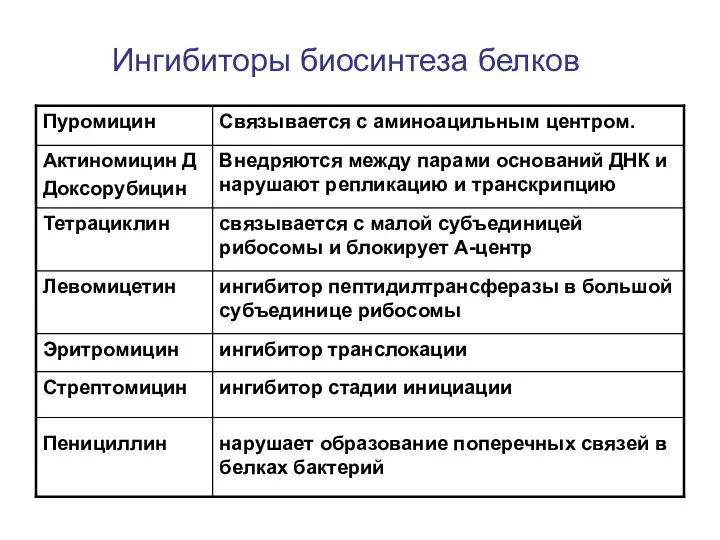
- 46. Ингибиторы биосинтеза белков
- 47. Пути превращений аминокислот в клетке Реакции поликонденсации Реакции трансаминирования Реакции декарбоксилирования Реакции окислительного дезаминирования
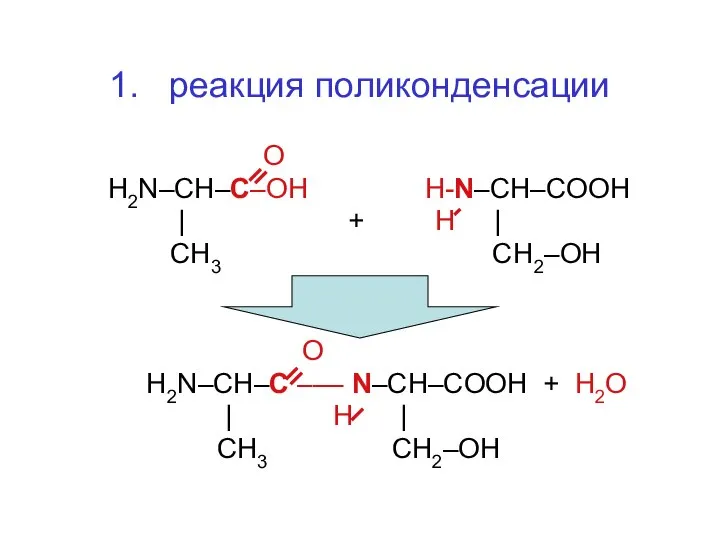
- 48. 1. реакция поликонденсации О H2N–CH–C–OH H-N–CH–CООH | + H | СН3 СН2–ОН О H2N–CH–C ––– N–CH–CОOH
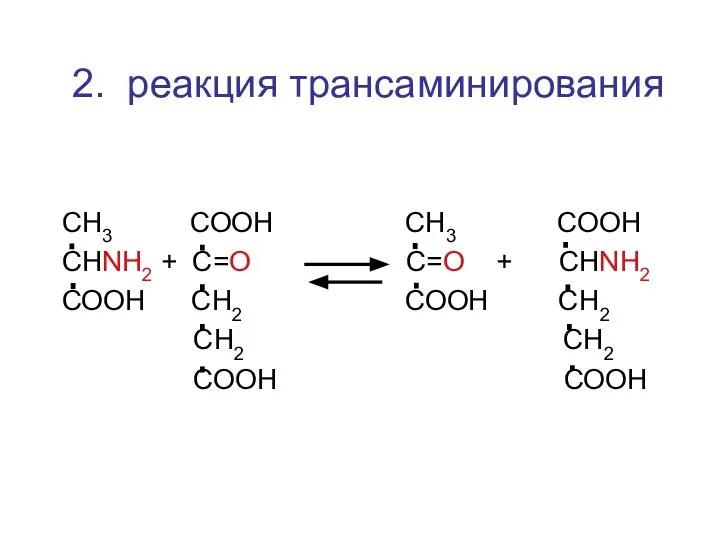
- 49. СН3 СООН СН3 СООН СНNH2 + C=О С=О + СНNH2 СООН СН2 СООН СН2 СН2 СН2
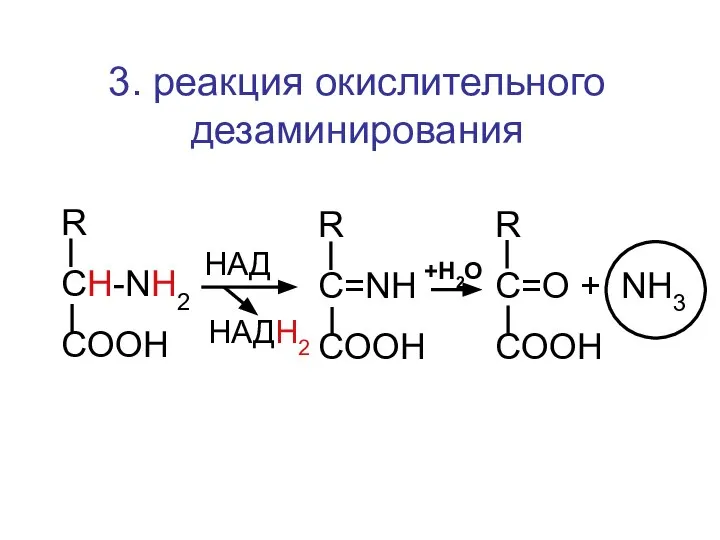
- 50. 3. реакция окислительного дезаминирования R CH-NH2 COOH R C=NH COOH R C=O + NH3 COOH HАД
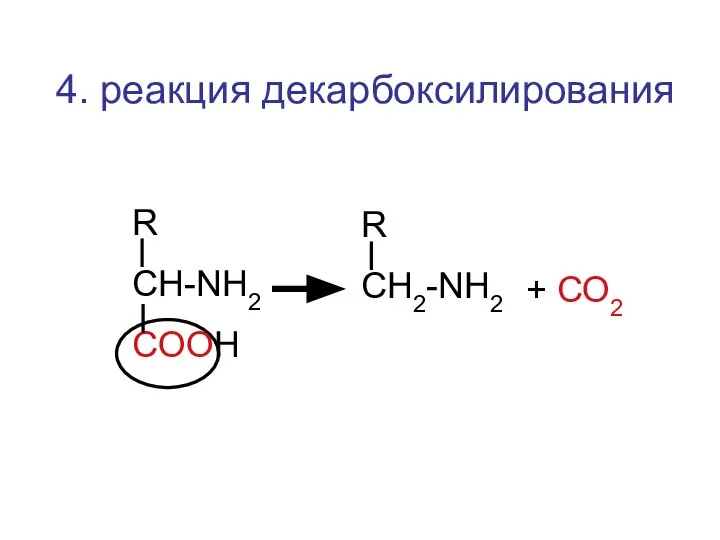
- 51. 4. реакция декарбоксилирования R CH-NH2 COOH R CН2-NH2 + СО2
- 52. Биосинтез белка в клетке
- 53. Перечень веществ, необходимых для синтеза белка и-РНК (зрелая) т-РНК ( 61) 20 аминокислот АТФ, ГТФ Ферменты
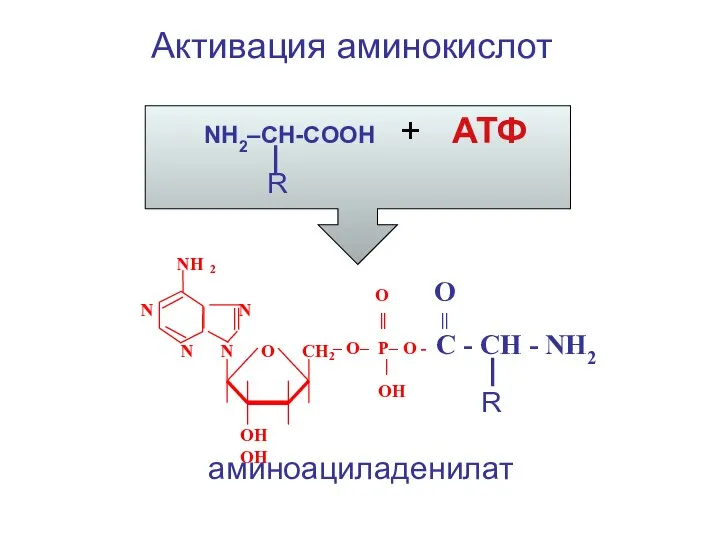
- 54. Активация аминокислот NH2–CH-COOH + АТФ R NH 2 N N O O || || N N
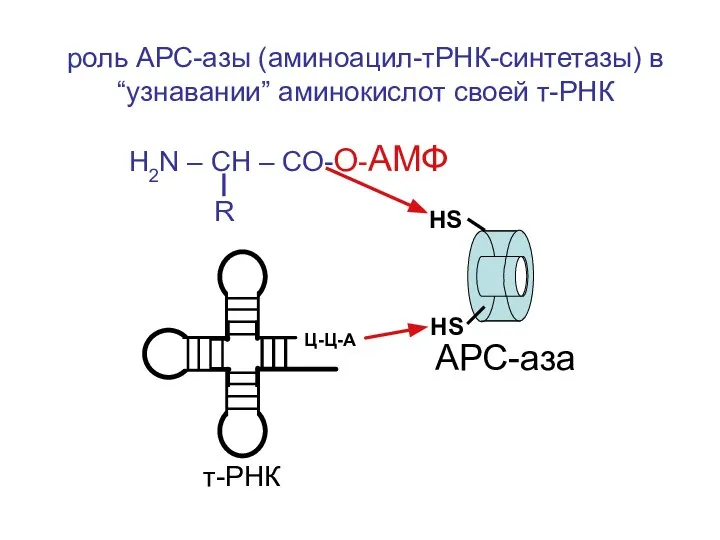
- 55. роль АРС-азы (аминоацил-тРНК-синтетазы) в “узнавании” аминокислот своей т-РНК H2N – CH – CO-O-АМФ R НS HS
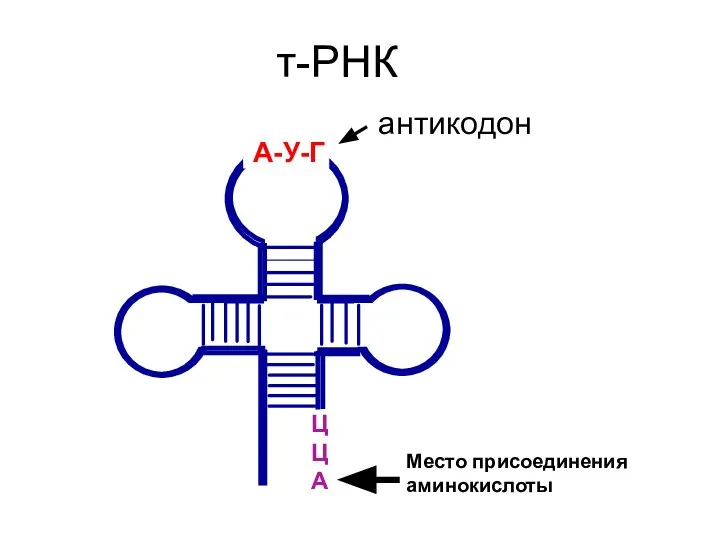
- 56. Ц ЦА т-РНК А-У-Г антикодон Место присоединения аминокислоты
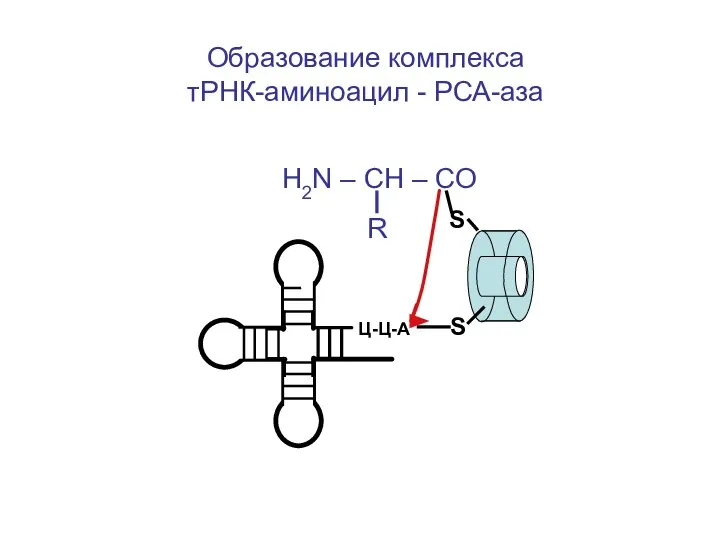
- 57. Образование комплекса тРНК-аминоацил - РСА-аза H2N – CH – CO R S S Ц-Ц-А
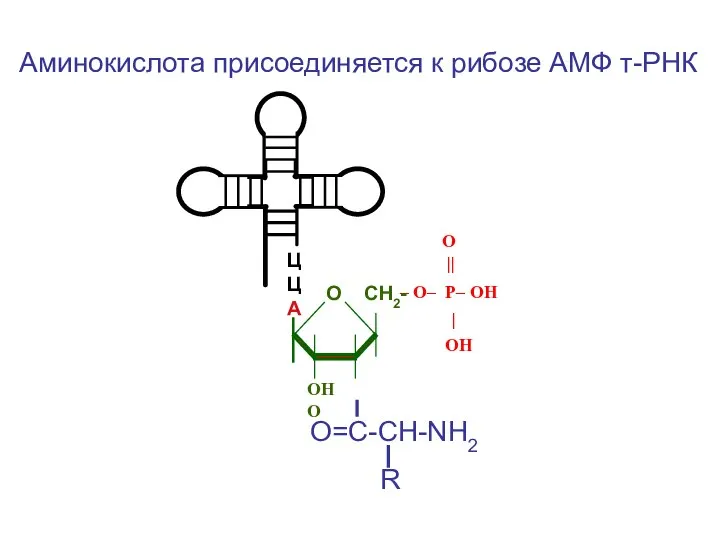
- 58. ЦЦА O || – O– P– OН | ОН ОН О О СН2- О=С-СН-NH2 R Аминокислота
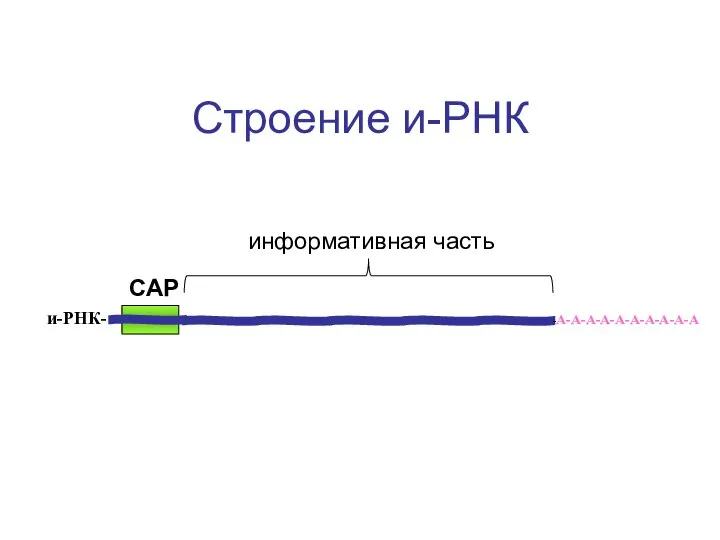
- 59. Строение и-РНК -А-А-А-А-А-А-А-А-А-А и-РНК- САР информативная часть
- 60. Стадии синтеза белка образование инициирующего комплекса; элонгация (удлинение полипептидной цепи); терминация (завершение синтеза); процессинг (окончательное достраивание
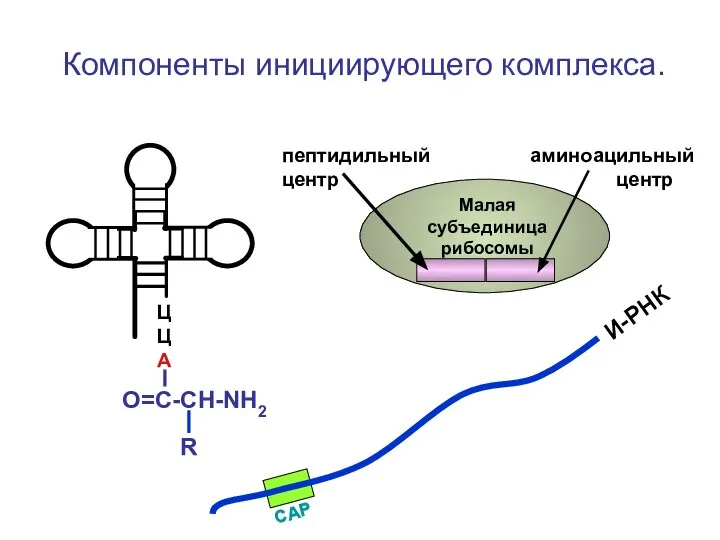
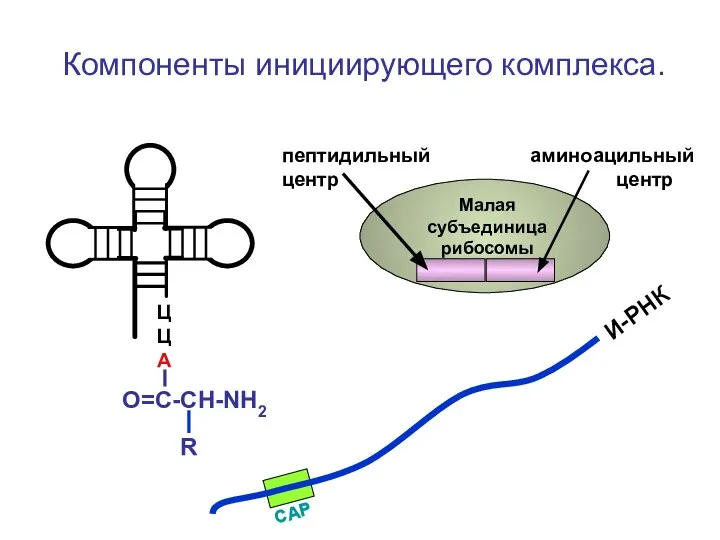
- 61. Компоненты инициирующего комплекса. ЦЦА О=С-СН-NH2 И-РНК Малая субъединица рибосомы пептидильный аминоацильный центр центр R
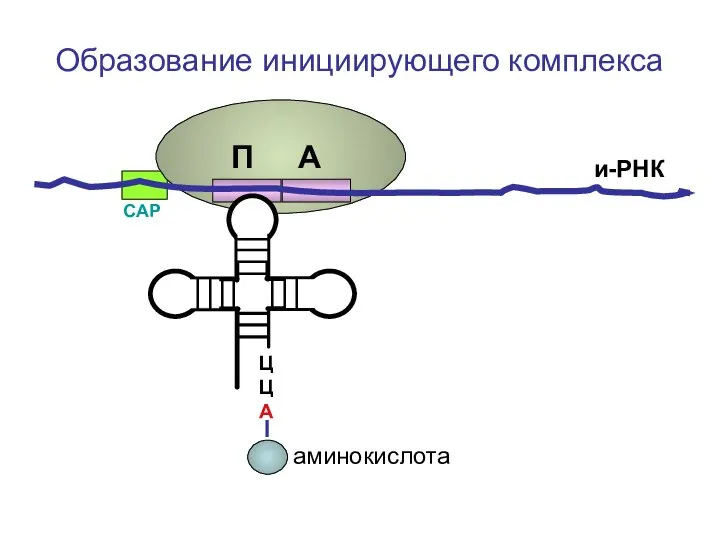
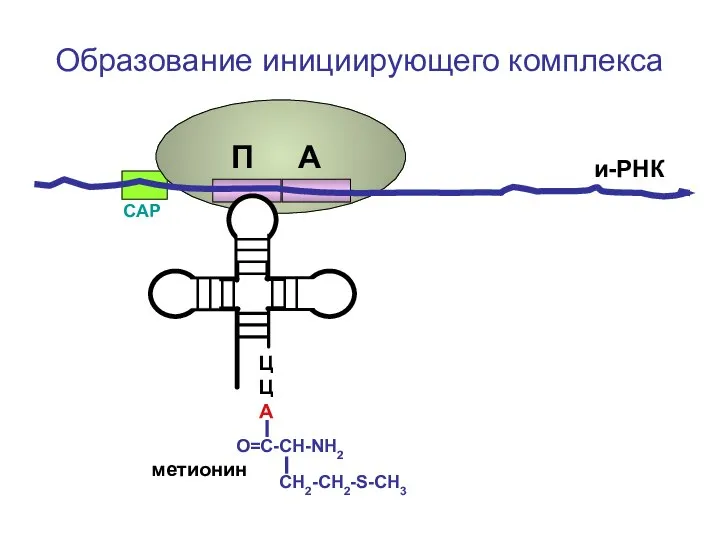
- 62. ЦЦА О=С-СН-NH2 СН2-СН2-S-CH3 Образование инициирующего комплекса метионин и-РНК СAP П А
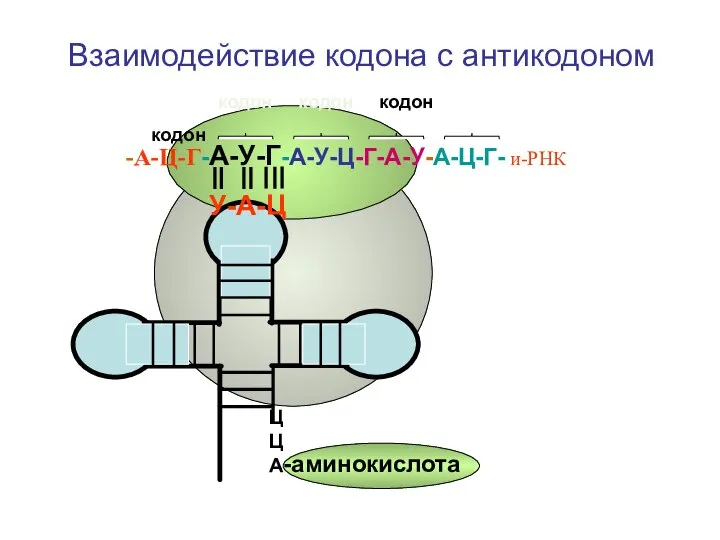
- 63. Взаимодействие кодона с антикодоном кодон кодон кодон кодон -А-Ц-Г-А-У-Г-А-У-Ц-Г-А-У-А-Ц-Г- и-РНК У-А-Ц ЦЦА -аминокислота
- 64. Биосинтез белка
- 65. ЦЦА Образование инициирующего комплекса и-РНК СAP П А аминокислота
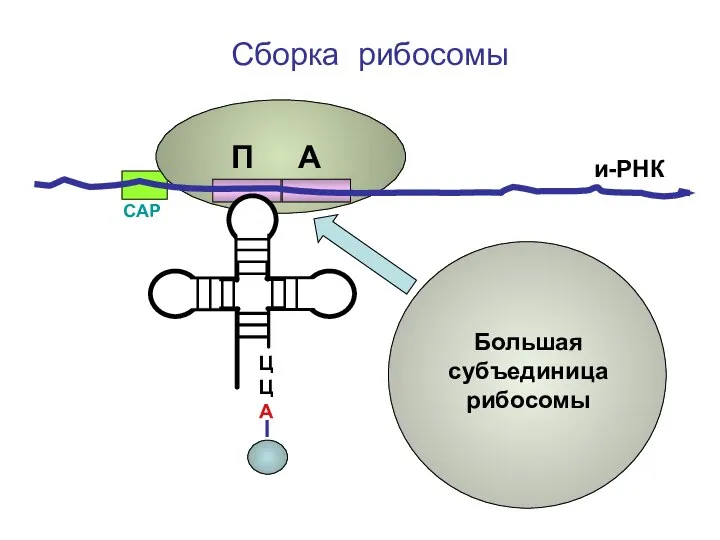
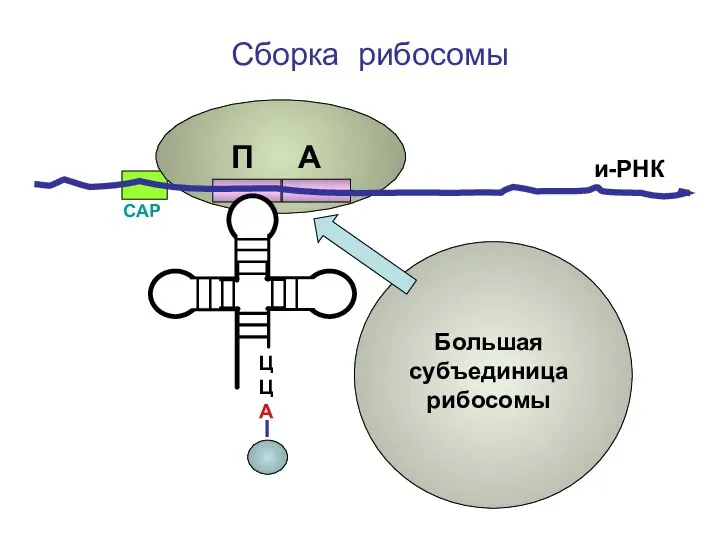
- 66. ЦЦА Сборка рибосомы и-РНК СAP Большая субъединица рибосомы П А
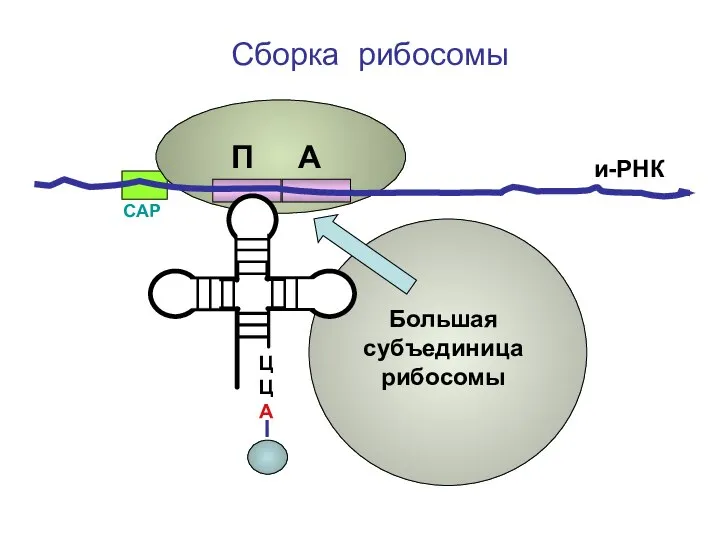
- 67. ЦЦА Сборка рибосомы и-РНК СAP П А
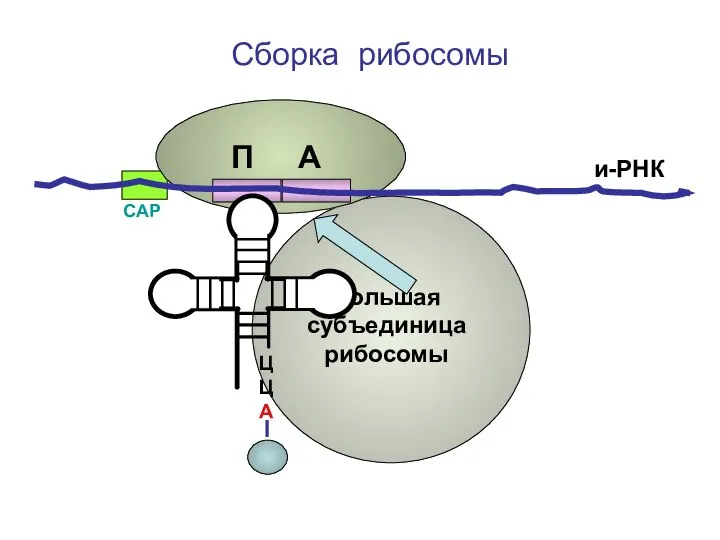
- 68. ЦЦА Сборка рибосомы и-РНК СAP П А
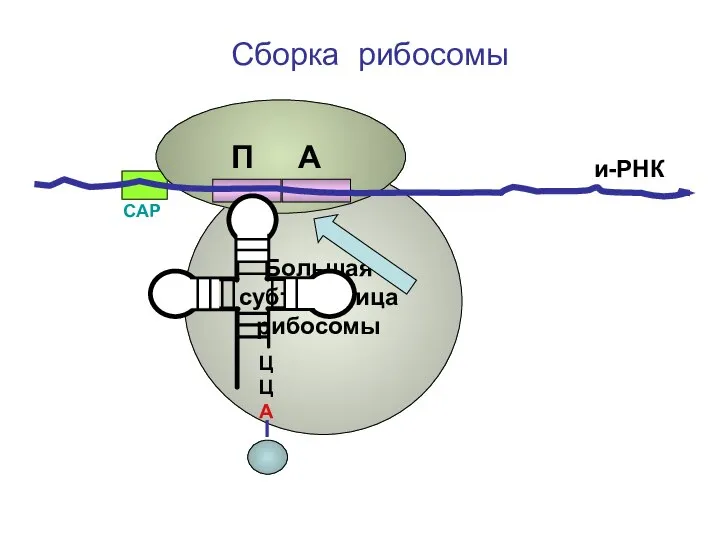
- 69. ЦЦА Сборка рибосомы и-РНК СAP П А
- 70. ЦЦА Сборка рибосомы и-РНК СAP П А
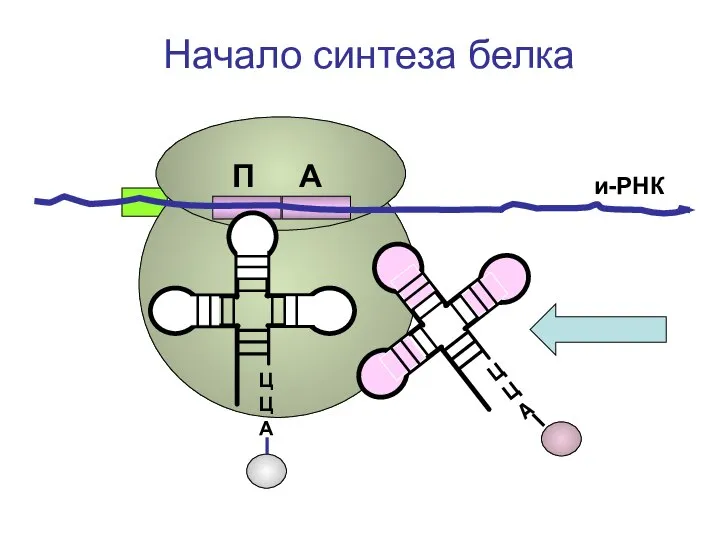
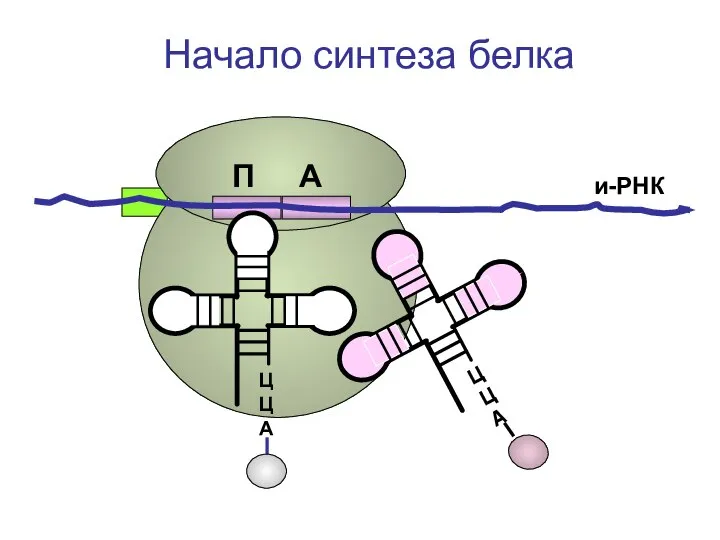
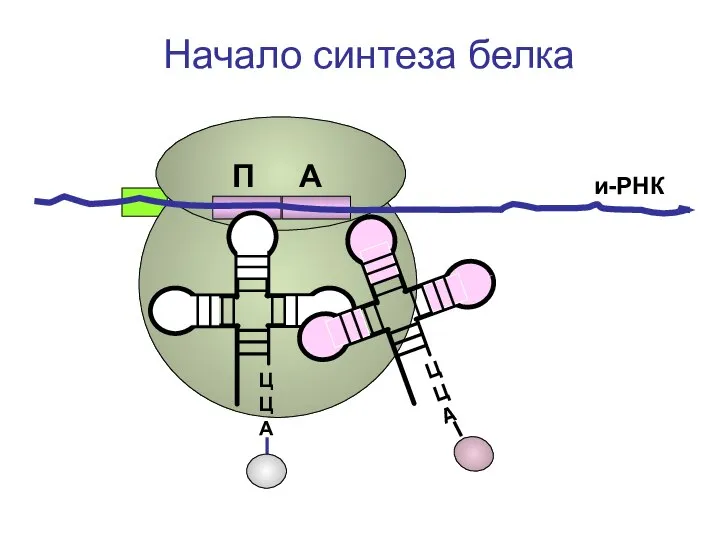
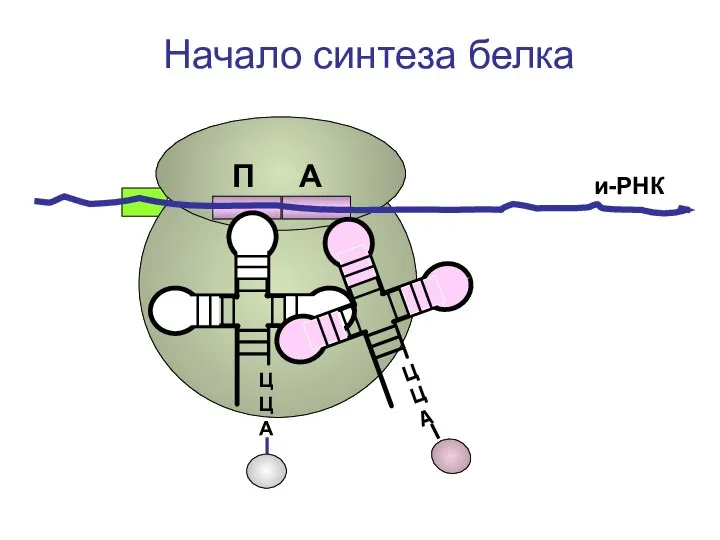
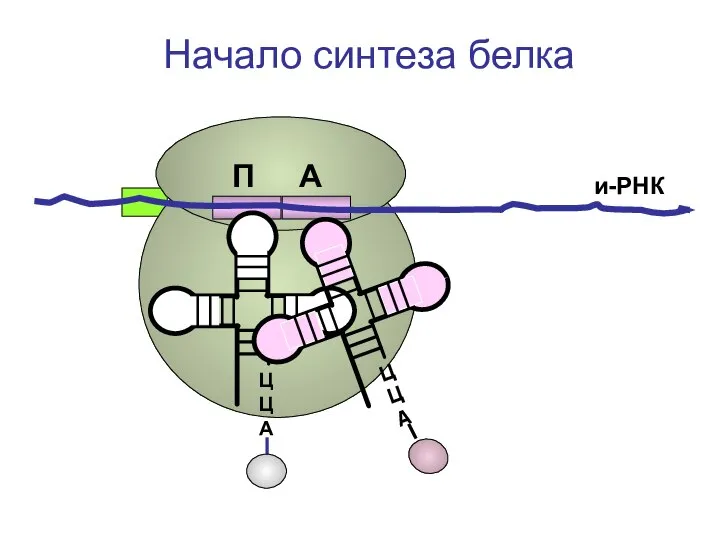
- 71. ЦЦА ЦЦА и-РНК Начало синтеза белка П А
- 72. ЦЦА и-РНК Начало синтеза белка П А
- 73. ЦЦА и-РНК Начало синтеза белка П А
- 74. ЦЦА и-РНК Начало синтеза белка П А
- 75. ЦЦА и-РНК Начало синтеза белка П А
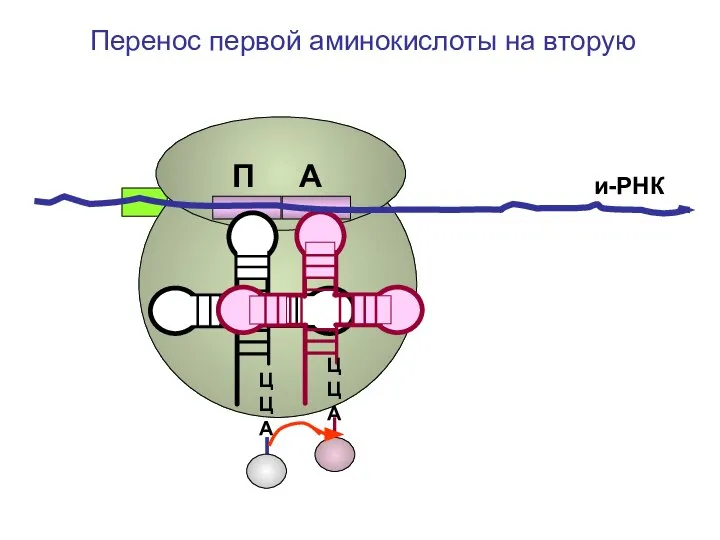
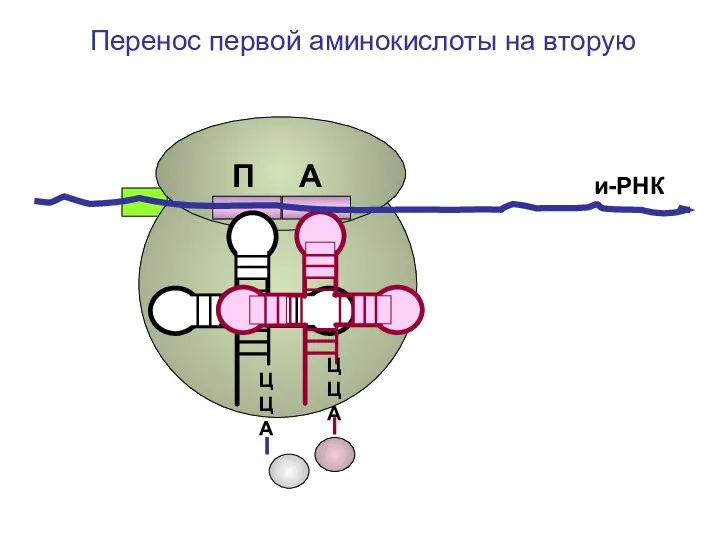
- 76. ЦЦА ЦЦА и-РНК Перенос первой аминокислоты на вторую П А
- 77. ЦЦА ЦЦА и-РНК Перенос первой аминокислоты на вторую П А
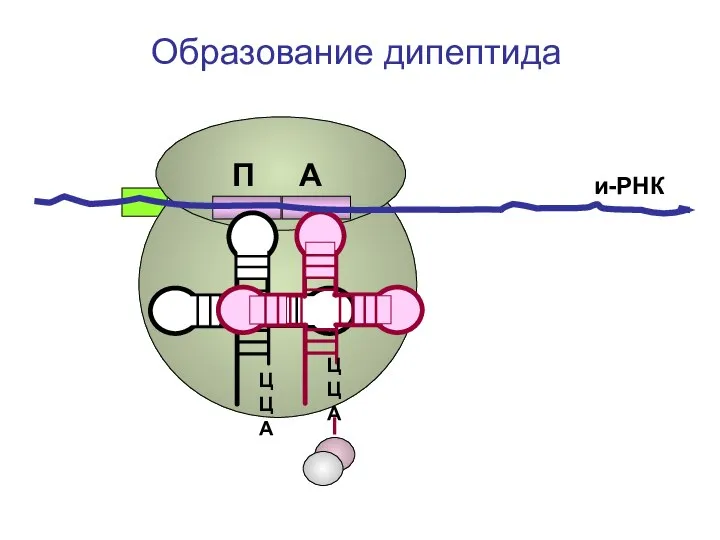
- 78. ЦЦА ЦЦА и-РНК Образование дипептида П А
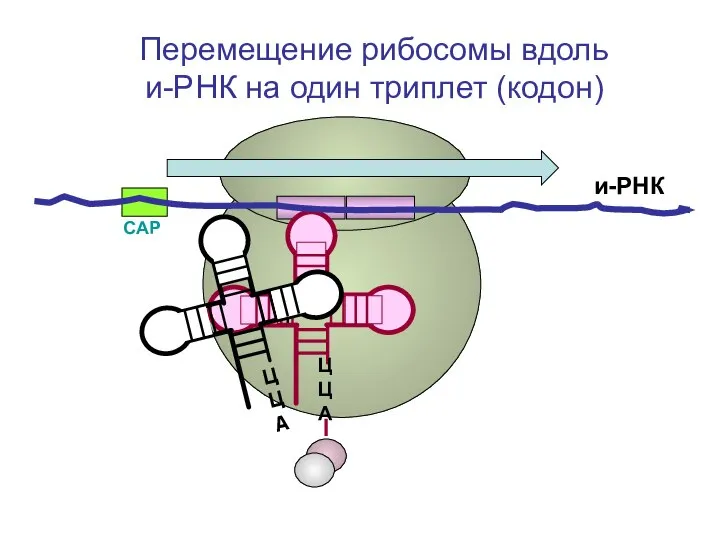
- 79. СAP и-РНК ЦЦА Перемещение рибосомы вдоль и-РНК на один триплет (кодон)
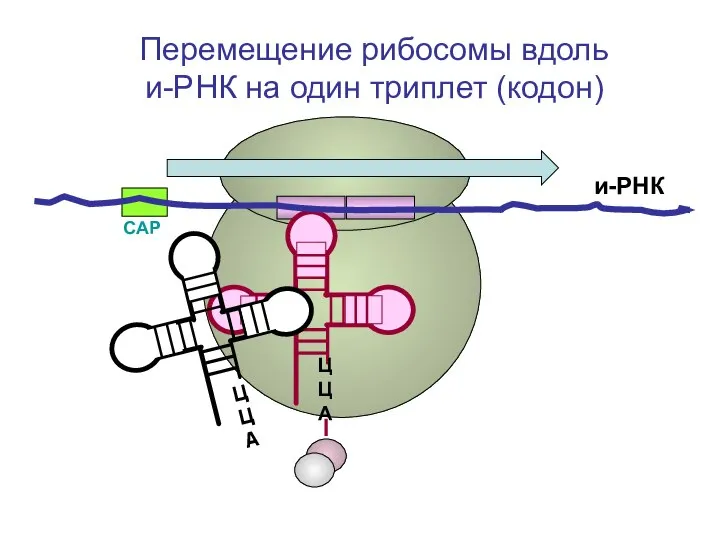
- 80. СAP и-РНК ЦЦА Перемещение рибосомы вдоль и-РНК на один триплет (кодон)
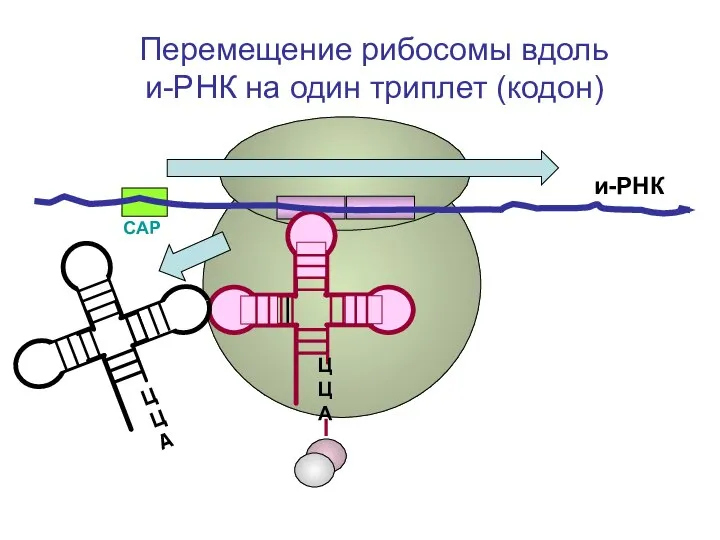
- 81. СAP и-РНК ЦЦА Перемещение рибосомы вдоль и-РНК на один триплет (кодон) ЦЦА
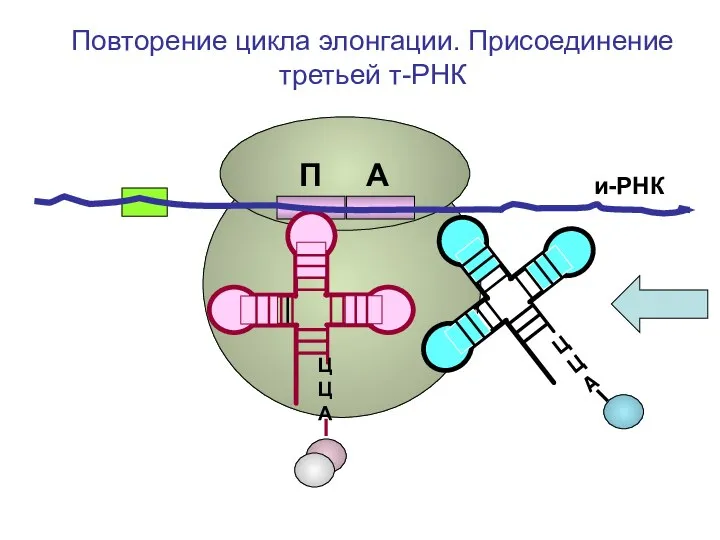
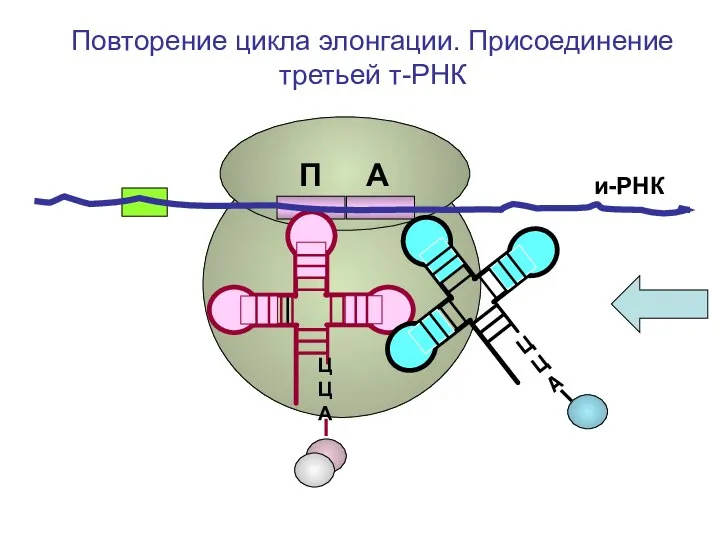
- 82. и-РНК ЦЦА ЦЦА Повторение цикла элонгации. Присоединение третьей т-РНК П А
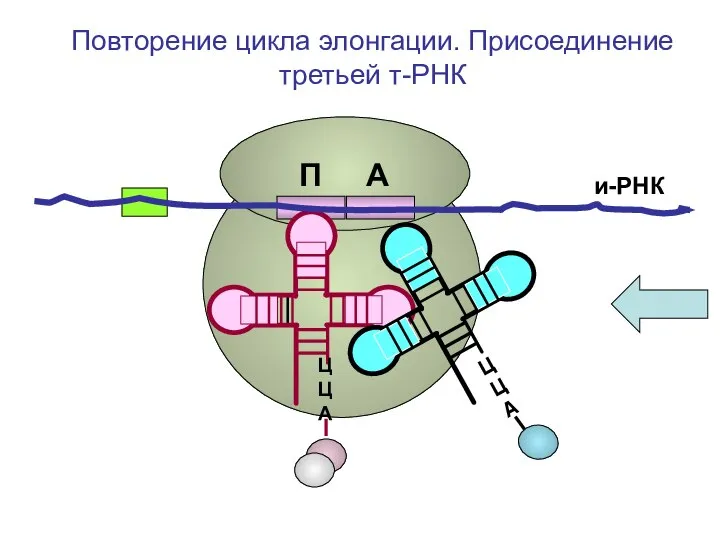
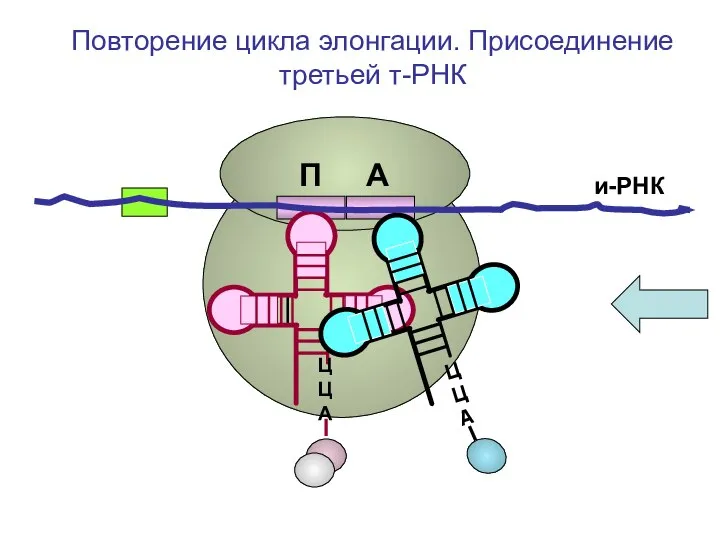
- 83. и-РНК ЦЦА Повторение цикла элонгации. Присоединение третьей т-РНК П А
- 84. и-РНК ЦЦА Повторение цикла элонгации. Присоединение третьей т-РНК П А
- 85. и-РНК ЦЦА Повторение цикла элонгации. Присоединение третьей т-РНК П А
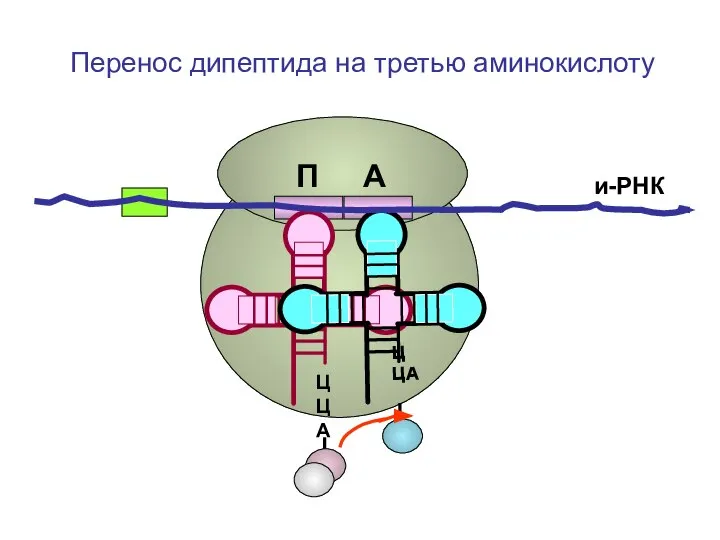
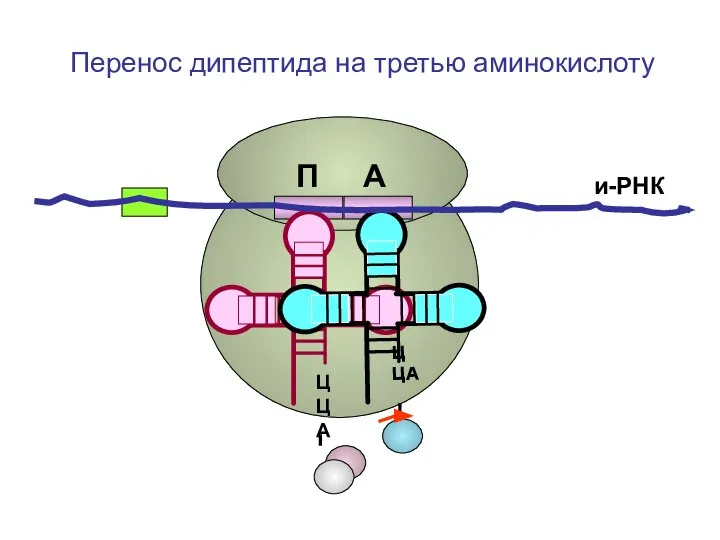
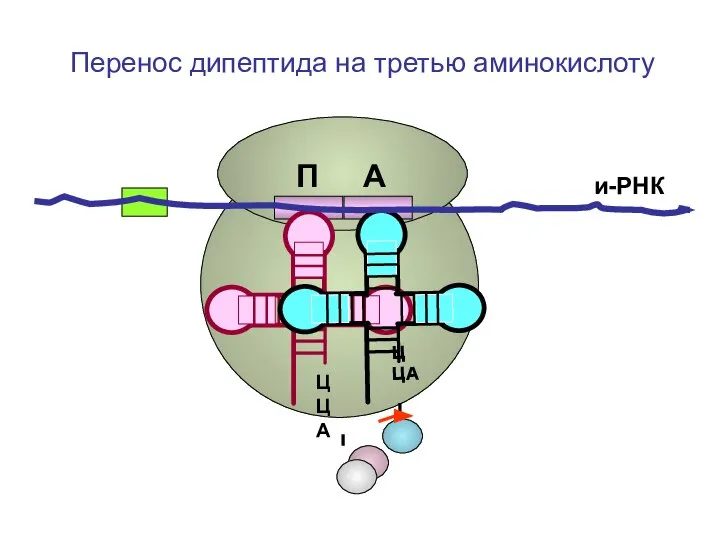
- 86. ЦЦА ЦЦА и-РНК П А Перенос дипептида на третью аминокислоту
- 87. ЦЦА ЦЦА и-РНК П А Перенос дипептида на третью аминокислоту
- 88. ЦЦА ЦЦА и-РНК П А Перенос дипептида на третью аминокислоту
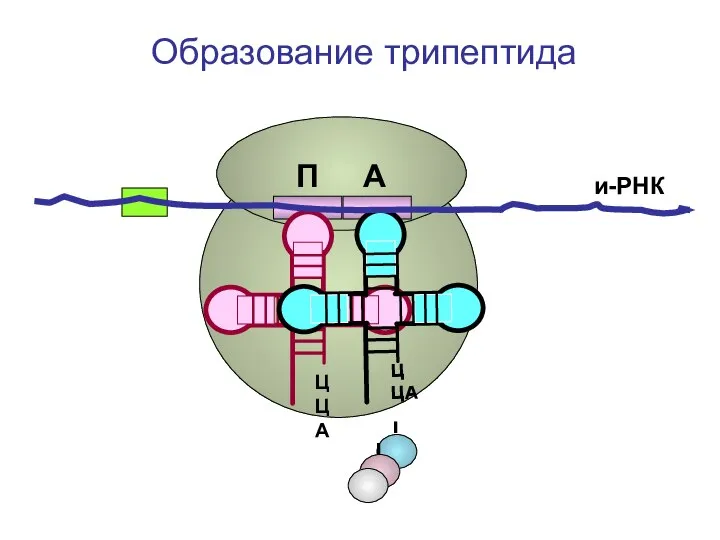
- 89. ЦЦА ЦЦА и-РНК П А Образование трипептида
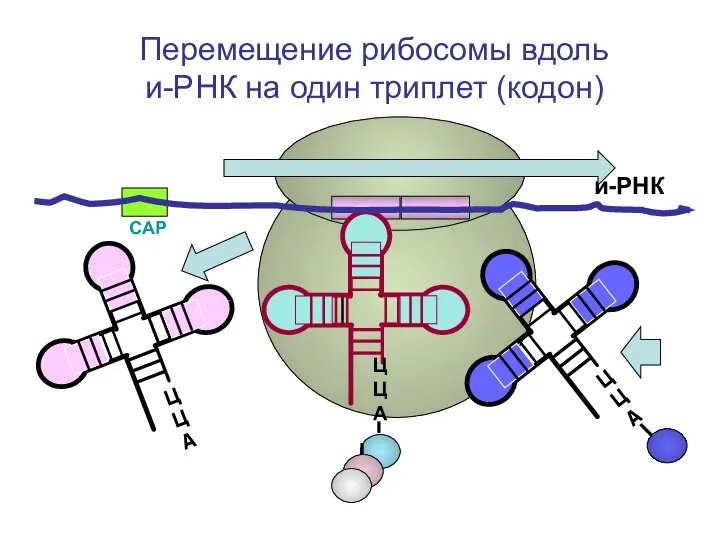
- 90. СAP и-РНК ЦЦА Перемещение рибосомы вдоль и-РНК на один триплет (кодон) ЦЦА ЦЦА
- 91. Многократное повторение циклов элонгации, до полного построения белковой молекулы
- 92. Компоненты инициирующего комплекса. ЦЦА О=С-СН-NH2 И-РНК Малая субъединица рибосомы пептидильный аминоацильный центр центр R
- 93. ЦЦА О=С-СН-NH2 СН2-СН2-S-CH3 Образование инициирующего комплекса метионин и-РНК СAP П А
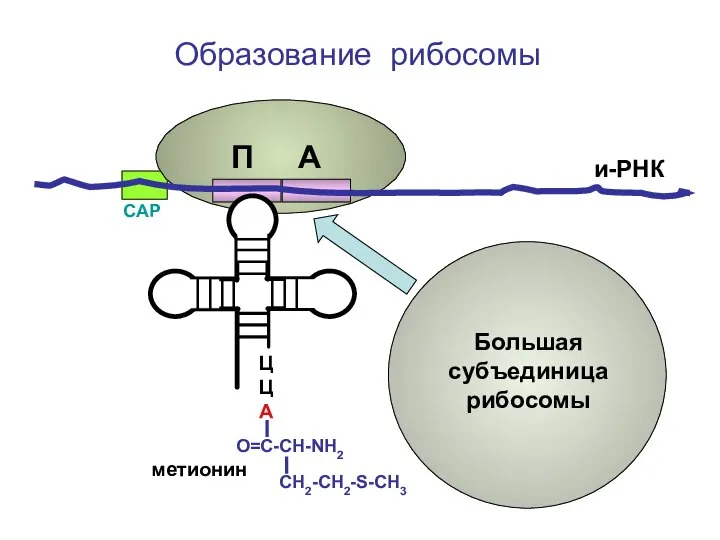
- 94. ЦЦА О=С-СН-NH2 СН2-СН2-S-CH3 Образование рибосомы метионин и-РНК СAP Большая субъединица рибосомы П А
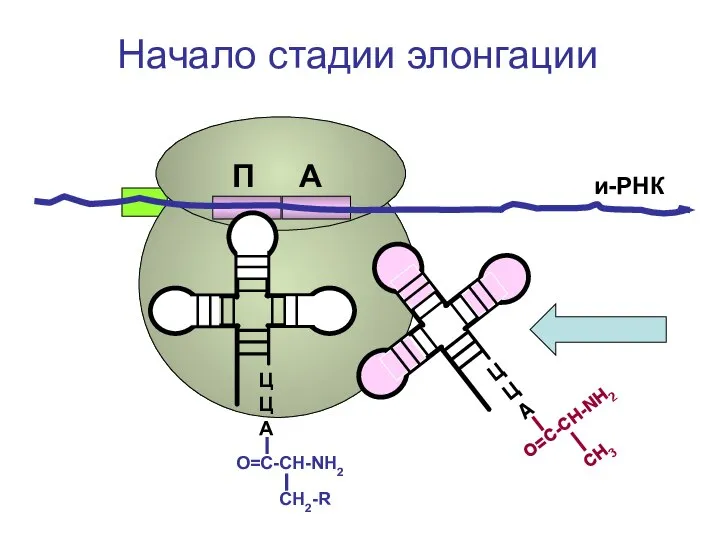
- 95. ЦЦА О=С-СН-NH2 СН2-R ЦЦА О=С-СН-NH2 CH3 и-РНК Начало стадии элонгации П А
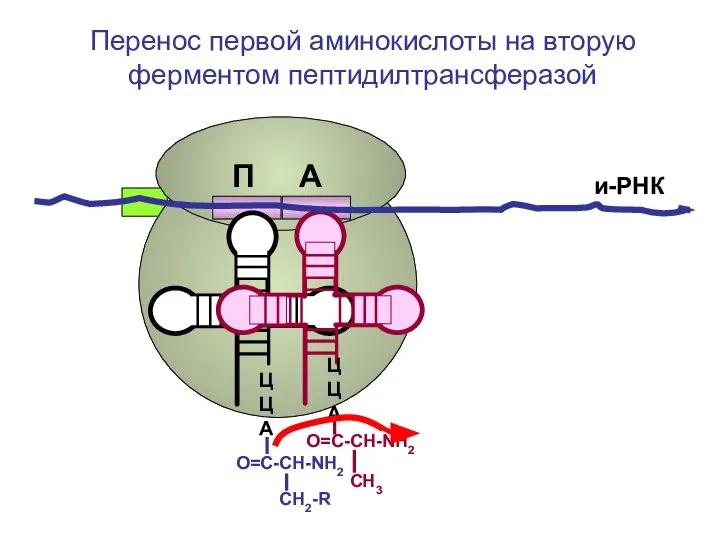
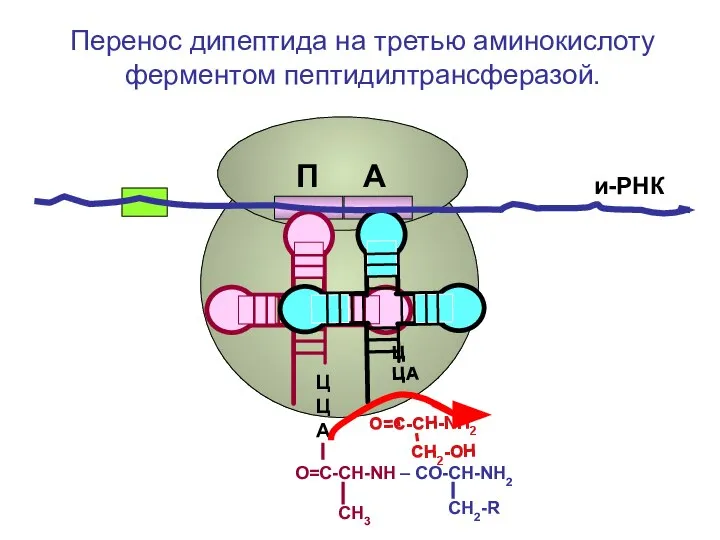
- 96. ЦЦА О=С-СН-NH2 СН2-R ЦЦА О=С-СН-NH2 СН3 и-РНК Перенос первой аминокислоты на вторую ферментом пептидилтрансферазой П А
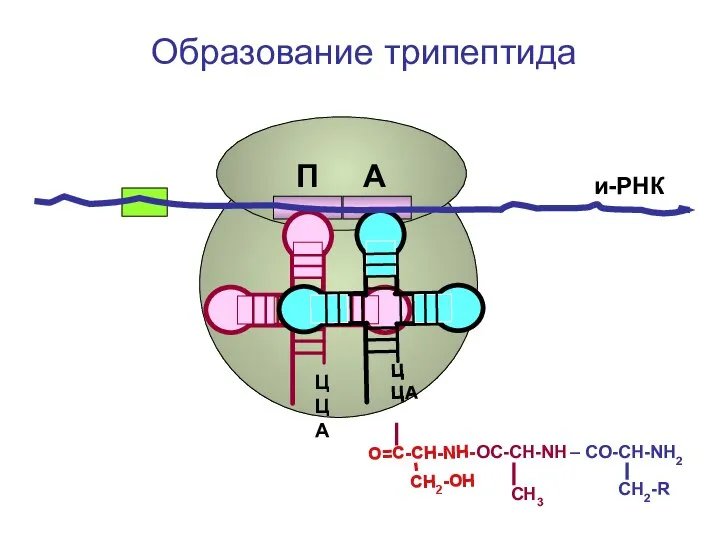
- 97. ЦЦА СН2-R ЦЦА О=С-СН-NH – CO-CH-NH2 СН3 и-РНК Образование дипептида П А
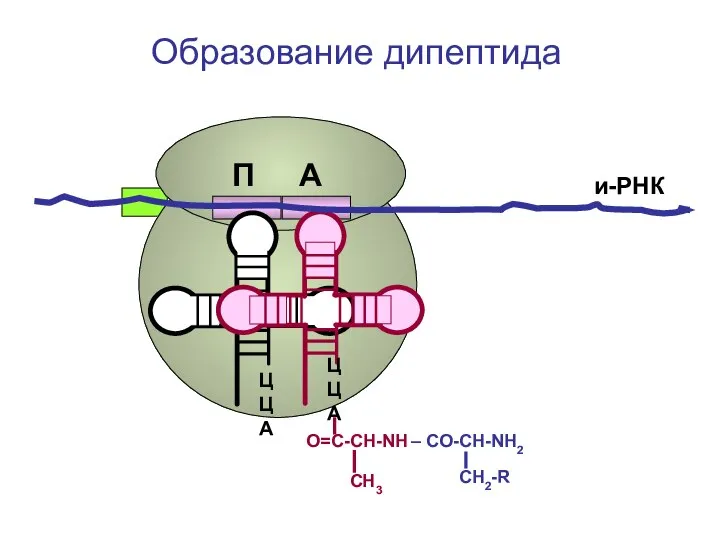
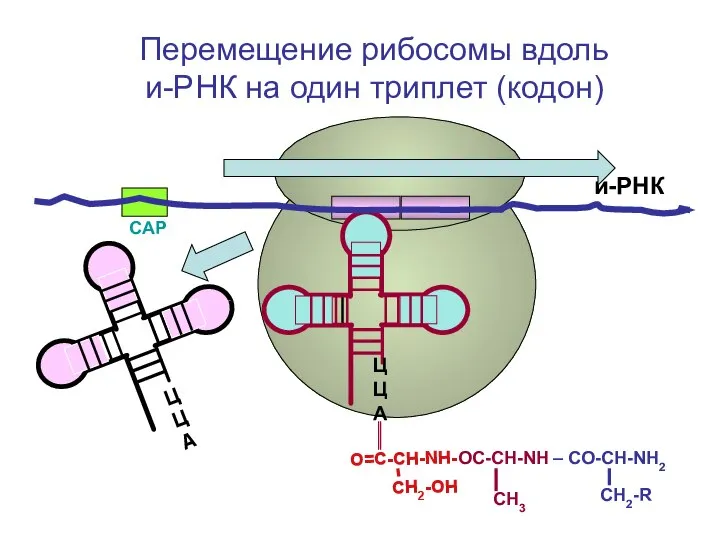
- 98. СAP СН2-R и-РНК ЦЦА О=С-СН-NH – CO-CH-NH2 СН3 Перемещение рибосомы вдоль и-РНК на один триплет (кодон)
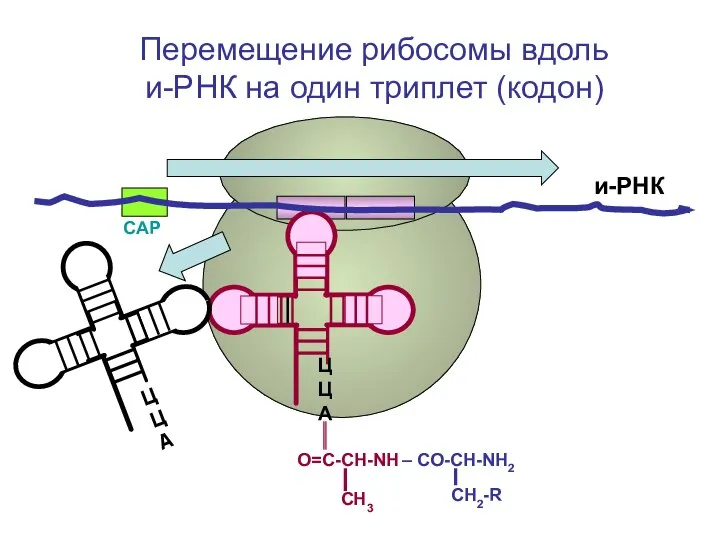
- 99. СН2-R и-РНК ЦЦА О=С-СН-NH – CO-CH-NH2 СН3 ЦЦА О=С-СН-NH2 CH2-OH Повторение цикла элонгации. Присоединение третьей т-РНК
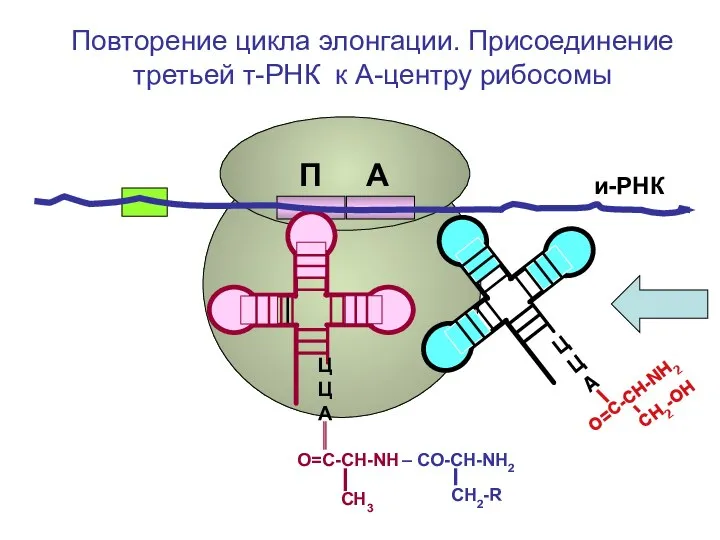
- 100. СН2-R ЦЦА О=С-СН-NH – CO-CH-NH2 СН3 ЦЦА О=С-СН-NH2 CH2-OH и-РНК П А Перенос дипептида на третью
- 101. СН2-R ЦЦА ОС-СН-NH – CO-CH-NH2 СН3 ЦЦА О=С-СН-NH- CH2-OH и-РНК П А Образование трипептида
- 102. СAP и-РНК ЦЦА Перемещение рибосомы вдоль и-РНК на один триплет (кодон) ЦЦА СН2-R ОС-СН-NH – CO-CH-NH2
- 103. Стадия терминации
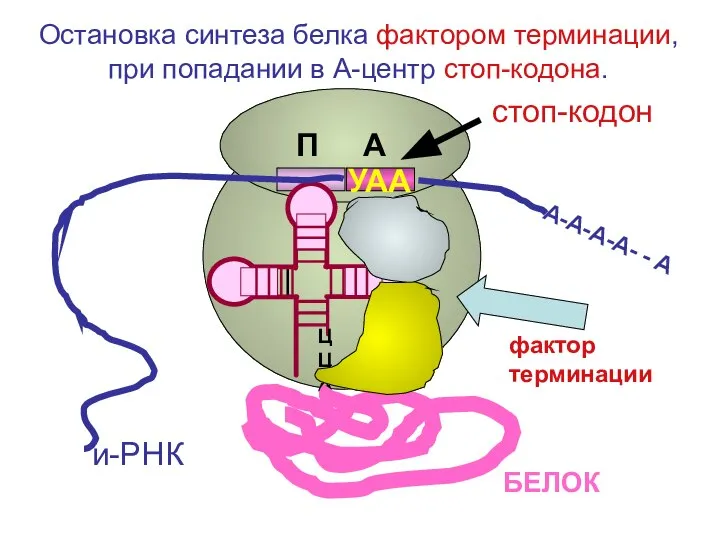
- 104. ЦЦА УАА А-А-А-А- - А и-РНК фактор терминации БЕЛОК стоп-кодон Остановка синтеза белка фактором терминации, при
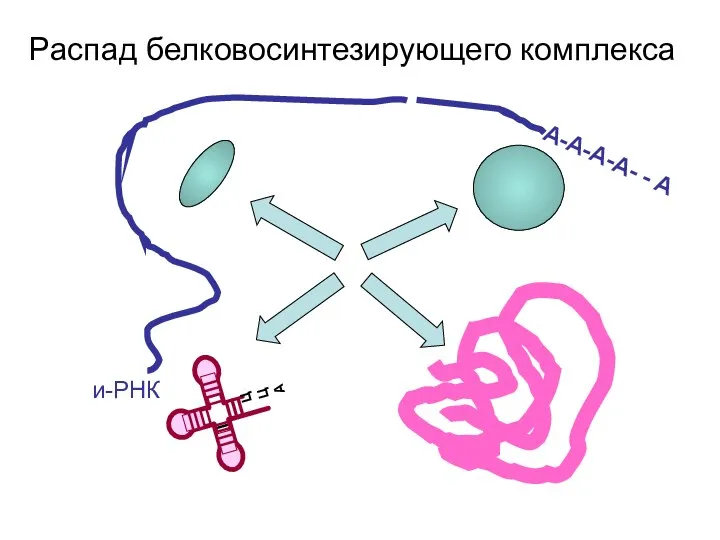
- 105. А-А-А-А- - А и-РНК Распад белковосинтезирующего комплекса
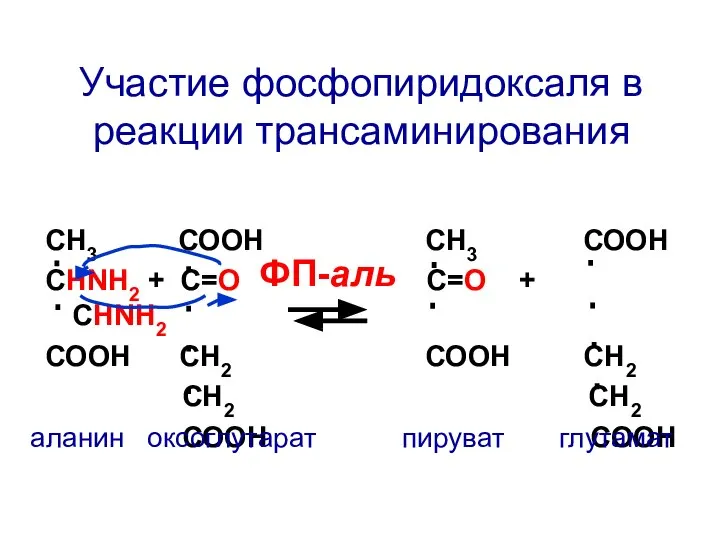
- 106. Трансамини-рование аминокислот
- 107. Биологическая ценность аминокислот заменимые пируват ----------------------→ аланин глицерин- ---------------------→ серин серин -------------------------→ глицин аланин-----------------------→ цистеин щук
- 108. СН3 СООН СН3 СООН СНNH2 + C=О С=О + СНNH2 СООН СН2 СООН СН2 СН2 СН2
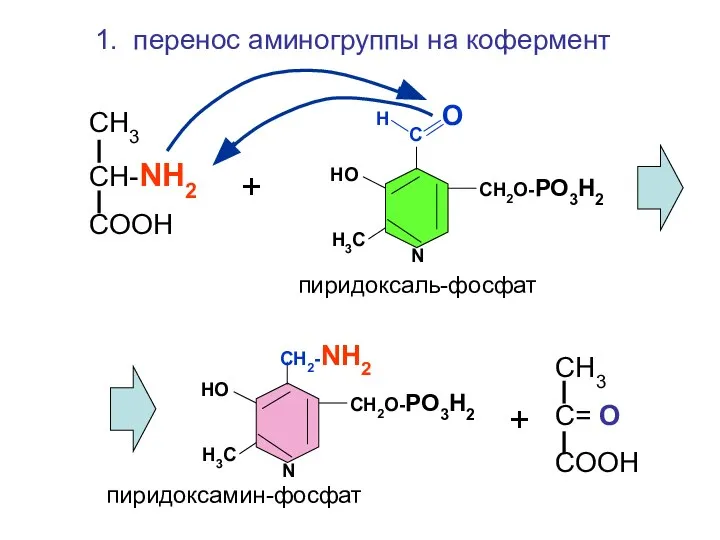
- 109. Н О С СН2О-РО3Н2 НО Н3С N СН2-NH2 СН2О-РО3Н2 НО Н3С N пиридоксаль-фосфат пиридоксамин-фосфат СН3 СН-NH2
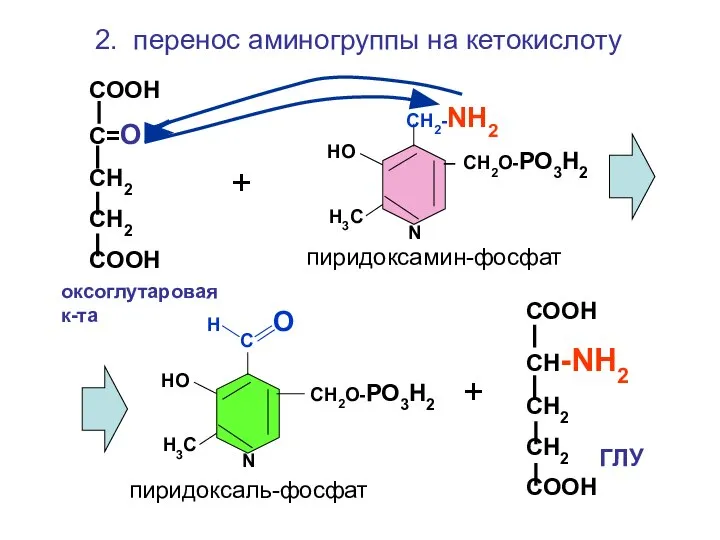
- 110. Н О С СН2О-РО3Н2 НО Н3С N СН2-NH2 СН2О-РО3Н2 НО Н3С N пиридоксаль-фосфат пиридоксамин-фосфат СООН С=О
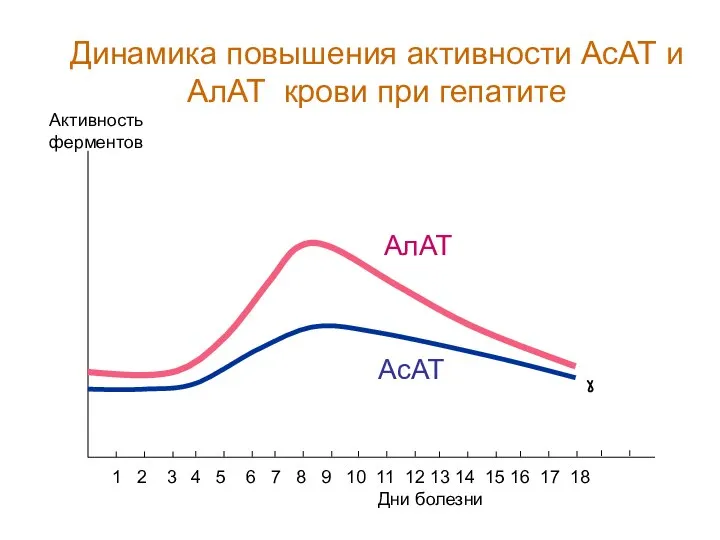
- 111. Дни болезни Активность ферментов 1 2 3 4 5 6 7 8 9 10 11 12
- 112. Декарбоксилирование аминокислот (образование биологически-активных аминов)
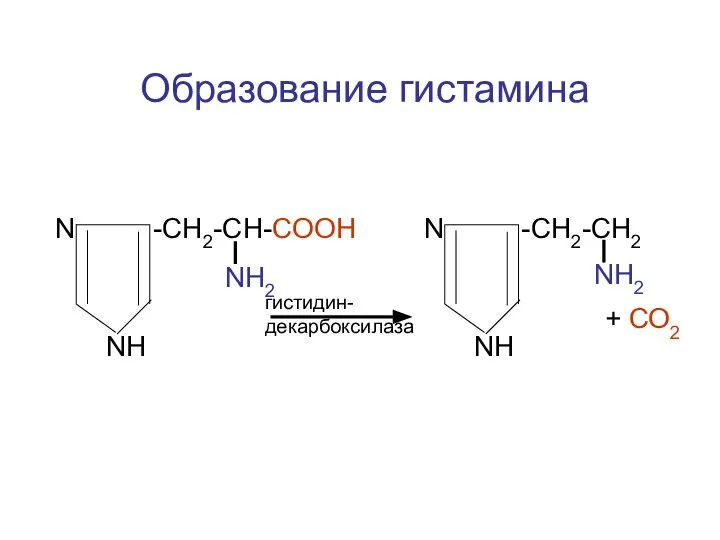
- 113. N -CH2-CH-COOH NH2 NH N -CH2-CH2 NH2 NH гистидин-декарбоксилаза + СО2 Образование гистамина
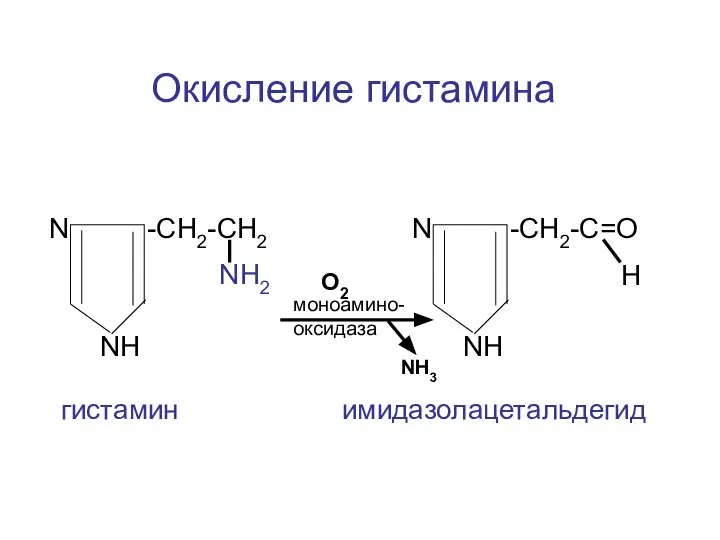
- 114. N -CH2-CH2 NH2 NH N -CH2-C=О Н NH моноамино-оксидаза гистамин имидазолацетальдегид Окисление гистамина NH3 O2
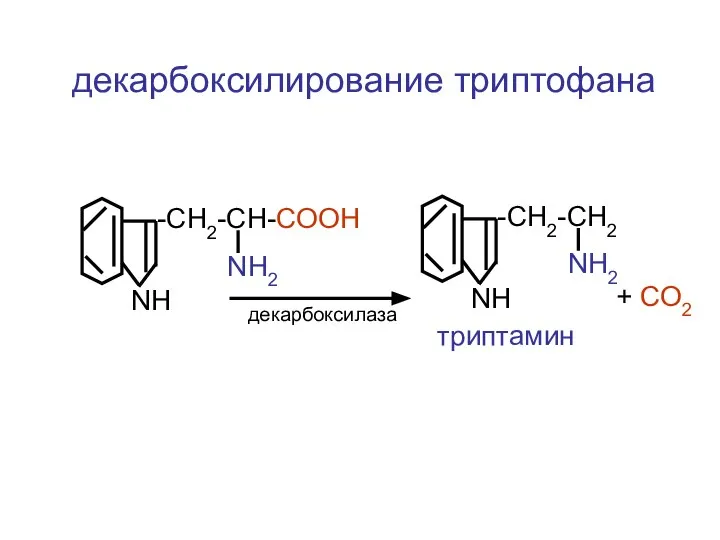
- 115. -CH2-CH-COOH NH2 NH -CH2-CH2 NH2 NH триптамин декарбоксилаза + СО2 декарбоксилирование триптофана
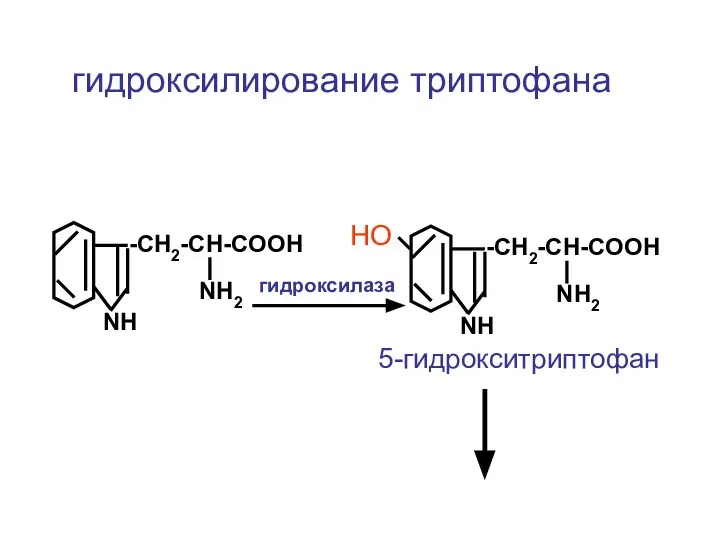
- 116. -CH2-CH-COOH NH2 NH гидроксилирование триптофана -CH2-CH-COOH NH2 NH НО гидроксилаза 5-гидрокситриптофан
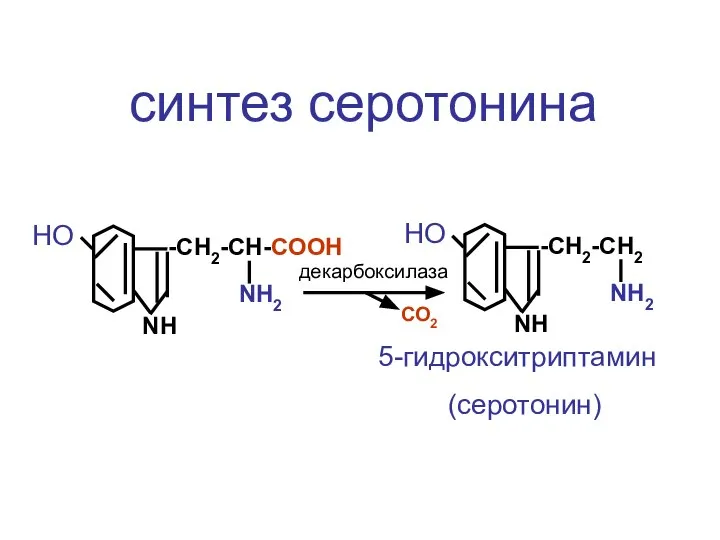
- 117. -CH2-CH-COOH NH2 NH НО -CH2-CH2 NH2 NH НО 5-гидрокситриптамин (серотонин) декарбоксилаза синтез серотонина СО2
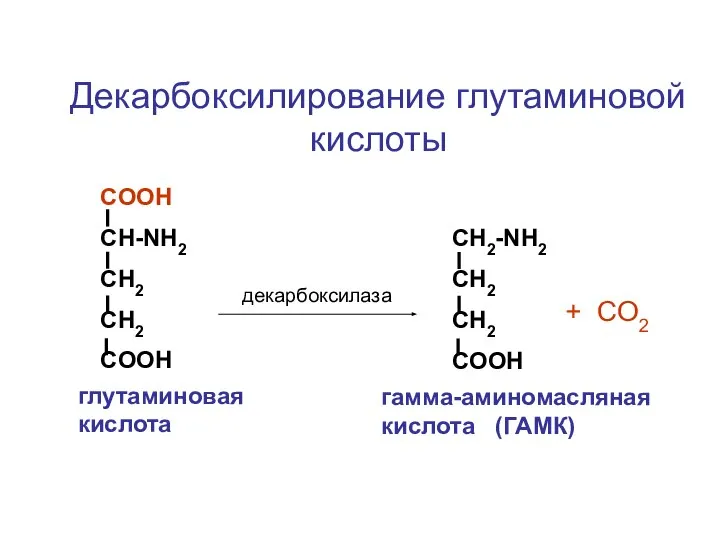
- 118. СOOH CH-NH2 CH2 CH2 COOH CH2-NH2 CH2 CH2 COOH декарбоксилаза + CO2 глутаминовая кислота гамма-аминомасляная кислота
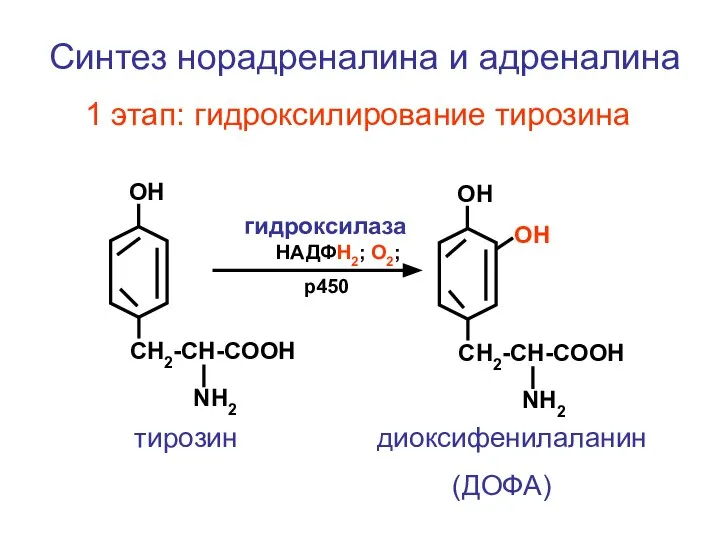
- 119. CH2-CH-COOH NH2 ОН CH2-CH-COOH NH2 ОН Синтез норадреналина и адреналина 1 этап: гидроксилирование тирозина НАДФН2; О2;
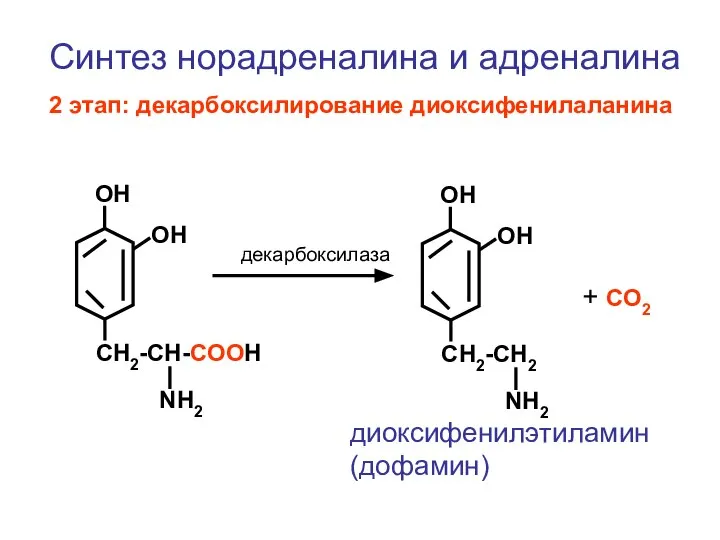
- 120. CH2-CH-COOH NH2 ОН ОН CH2-CH2 NH2 ОН ОН + СО2 декарбоксилаза Синтез норадреналина и адреналина 2
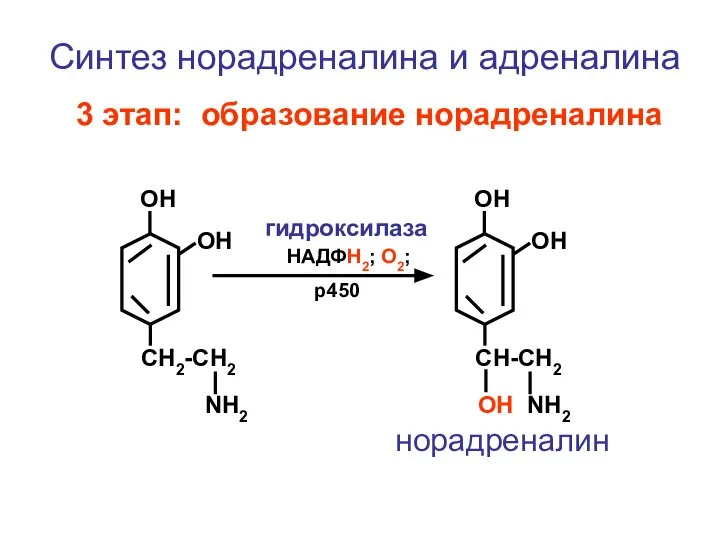
- 121. CH2-CH2 NH2 ОН ОН Синтез норадреналина и адреналина 3 этап: образование норадреналина CH-CH2 ОН NH2 ОН
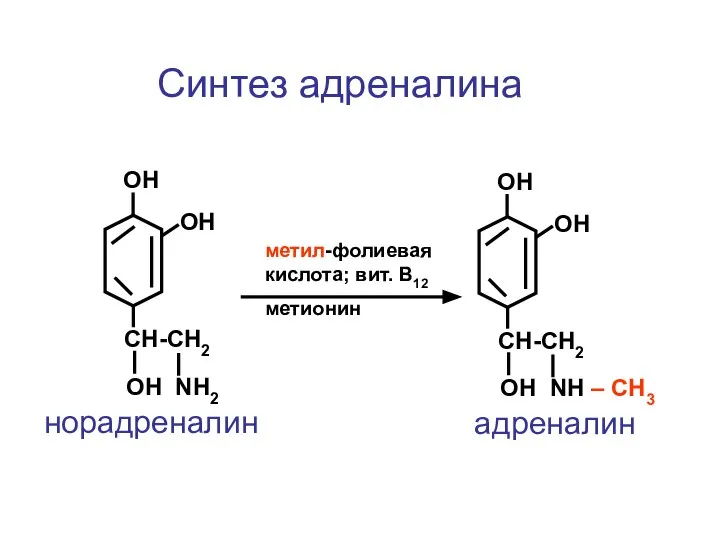
- 122. CH-CH2 ОН NH2 ОН ОН норадреналин CH-CH2 ОН NH – СН3 ОН ОН адреналин метил-фолиевая кислота;
- 123. Окислительное дезаминирование аминокислот
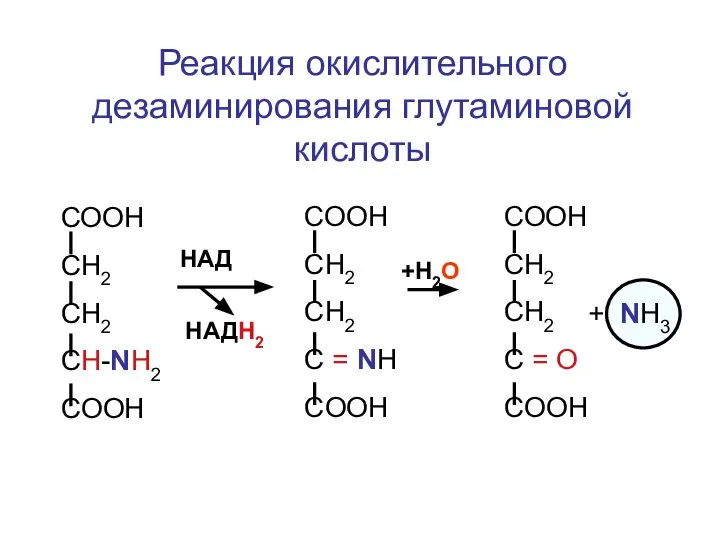
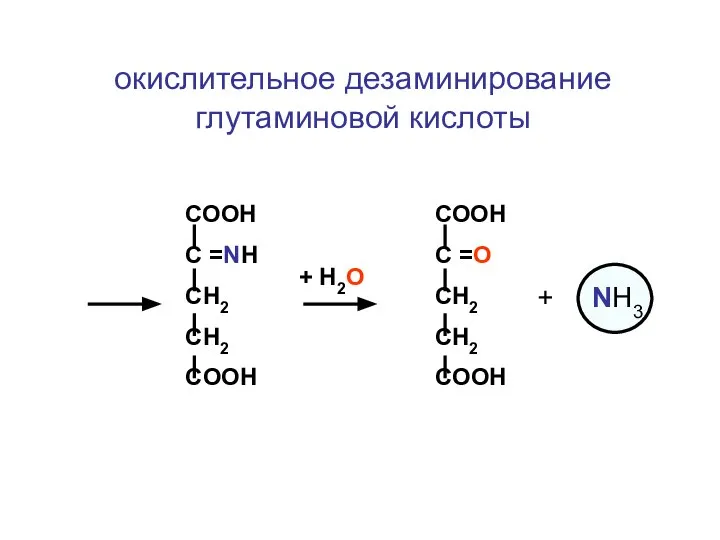
- 124. Реакция окислительного дезаминирования глутаминовой кислоты СООН СН2 СН2 CH-NH2 COOH HАД HАДН2 +Н2О СООН СН2 СН2
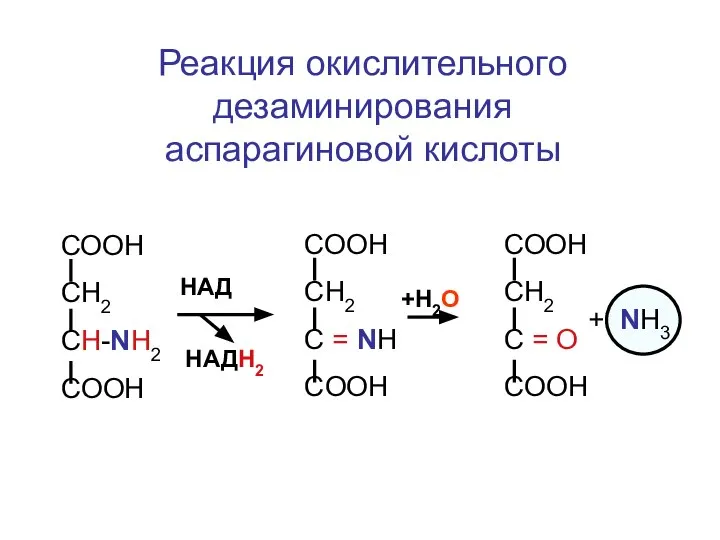
- 125. Реакция окислительного дезаминирования аспарагиновой кислоты СООН СН2 CH-NH2 COOH HАД HАДН2 +Н2О СООН СН2 C =
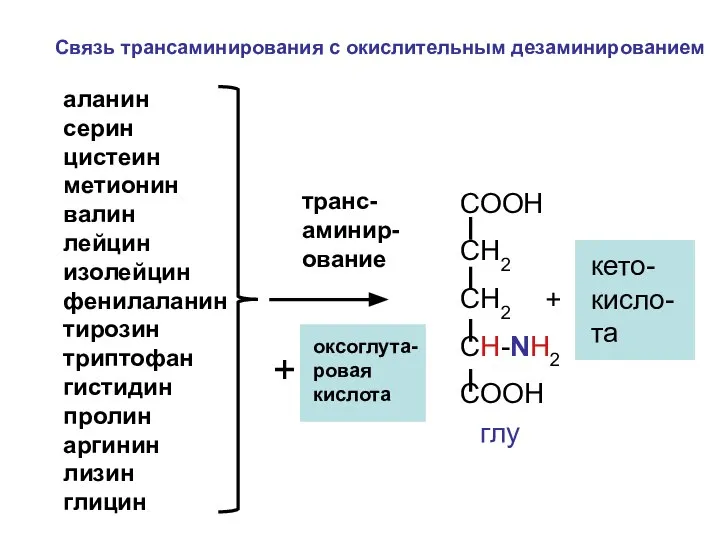
- 126. аланин серин цистеин метионин валин лейцин изолейцин фенилаланин тирозин триптофан гистидин пролин аргинин лизин глицин транс-аминир-ование
- 127. СН3 СООН СН3 СООН СНNH2 + C=О С=О + СНNH2 СООН СН2 СООН СН2 СН2 СН2
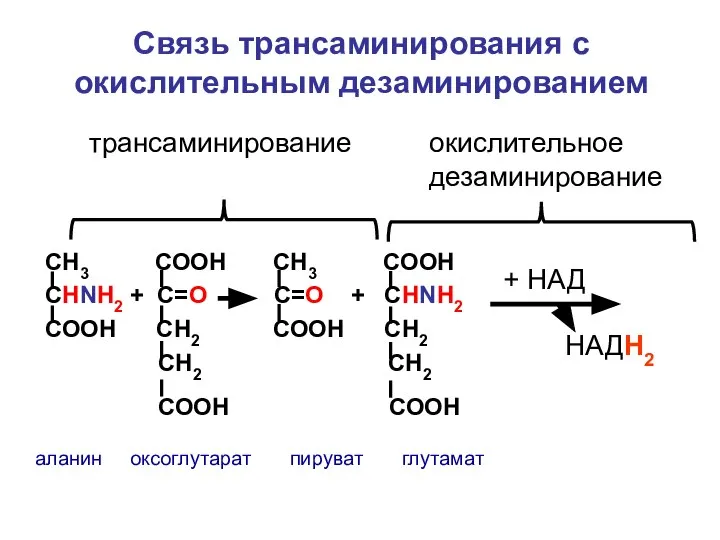
- 128. окислительное дезаминирование глутаминовой кислоты + Н2О СООН С =NH СН2 CH2 COOH СООН С =O СН2
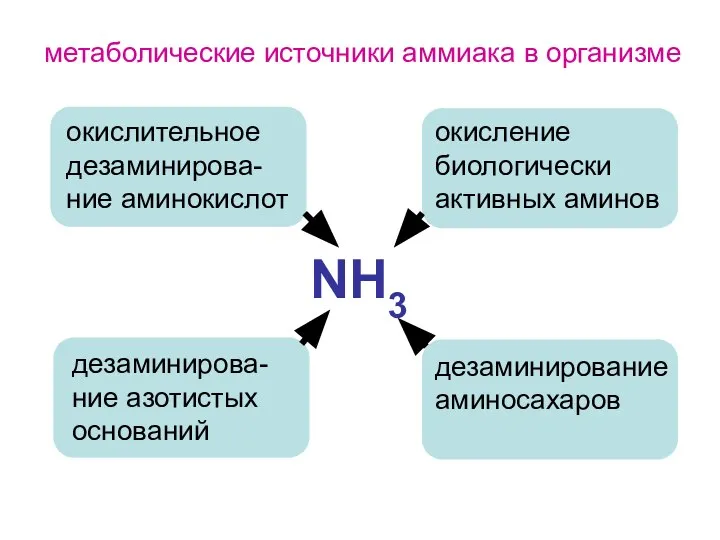
- 129. NH3 окислительное дезаминирова-ние аминокислот дезаминирова-ние азотистых оснований окисление биологически активных аминов дезаминирование аминосахаров метаболические источники аммиака
- 130. главный механизм обезвреживания аммиака в организме
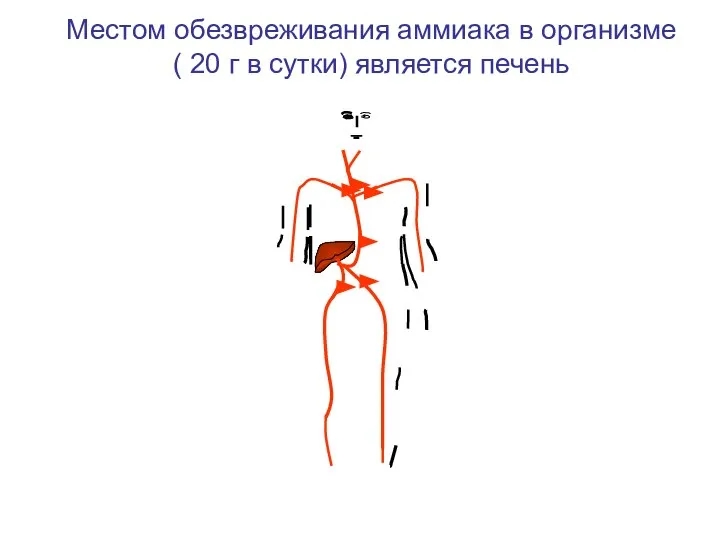
- 131. • • Местом обезвреживания аммиака в организме ( 20 г в сутки) является печень
- 132. НО – С – ОН О NH2 – C – NH2 O структурные формулы угольной кислоты
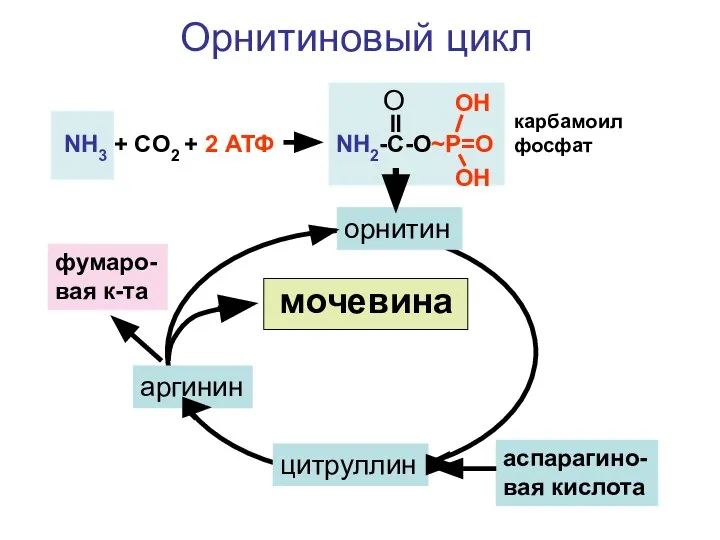
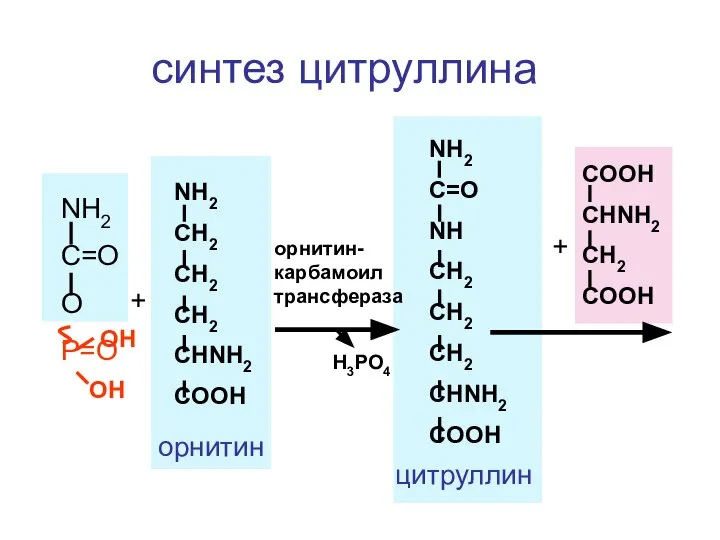
- 133. синтез мочевины
- 134. NH3 + CO2 + 2 АТФ NH2-C-O~P=O O OH OH орнитин цитруллин аспарагино-вая кислота аргинин фумаро-вая
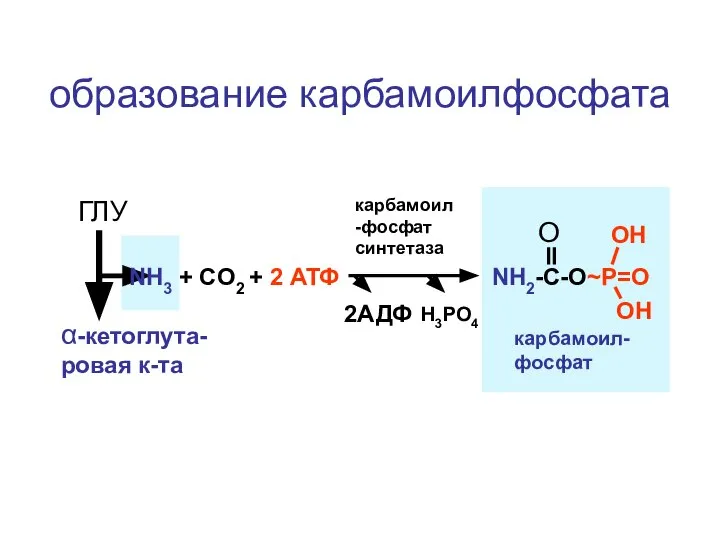
- 135. образование карбамоилфосфата ГЛУ α-кетоглута-ровая к-та NH3 + CO2 + 2 АТФ карбамоил-фосфат синтетаза 2АДФ H3PO4 NH2-C-O~P=O
- 136. NH2 C=O O P=O OH OH + NH2 CH2 CH2 CH2 CHNH2 COOH орнитин орнитин-карбамоил трансфераза
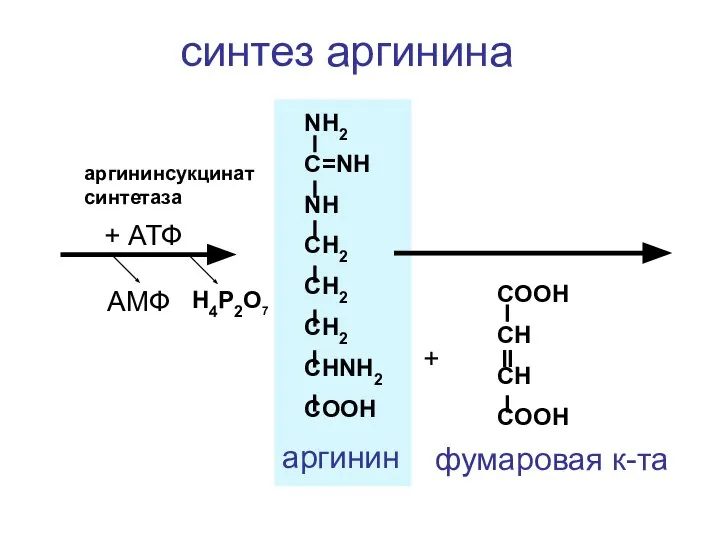
- 137. NH2 C=NH NH CH2 CH2 CH2 CHNH2 COOH + COOH CH CH COOH фумаровая к-та +
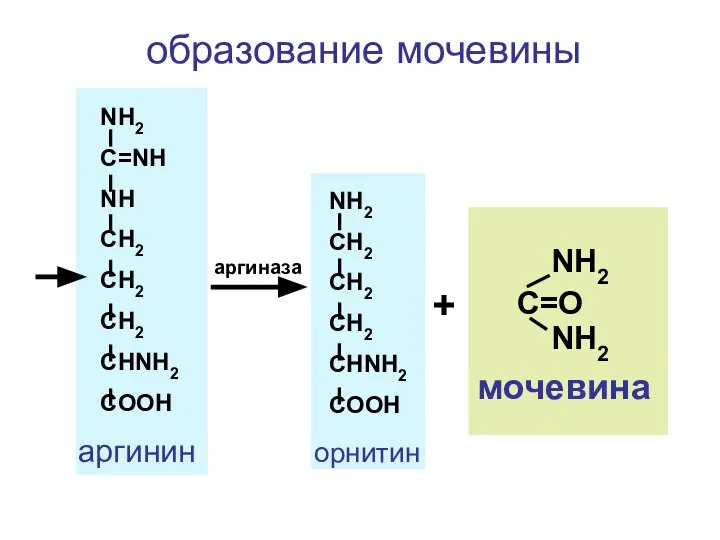
- 138. NH2 CH2 CH2 CH2 CHNH2 COOH C=O NH2 NH2 мочевина NH2 C=NH NH CH2 CH2 CH2
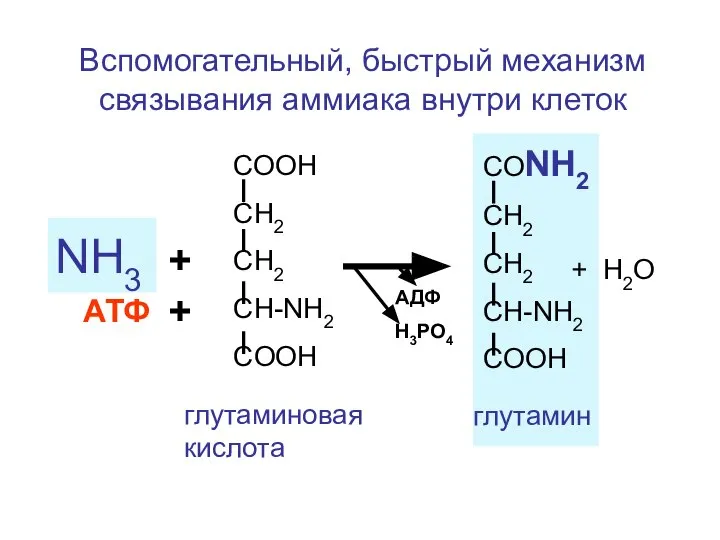
- 139. Вспомогательный, быстрый механизм связывания аммиака внутри клеток СООН СН2 СН2 CH-NH2 COOH NH3 + СОNH2 СН2
- 140. СООН СН2 СН2 CH-NH2 COOH NH3 + СОNH2 СН2 СН2 CH-NH2 COOH + H2O глутамино-вая кислота
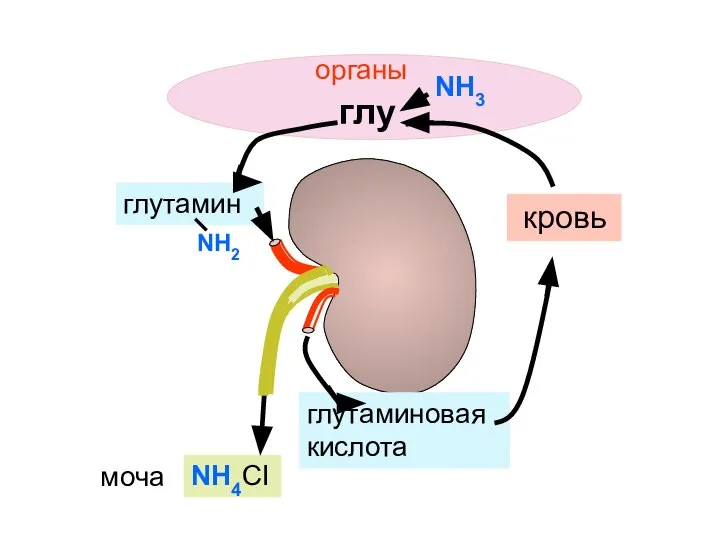
- 141. глутамин глутаминовая кислота NH4CI кровь органы глу NH3 моча NH2
- 142. Содержание мочевины в крови 2,5 – 8,3 ммоль/л сыворотки (За сутки с мочой выделяется 20-35 г)
- 143. Регуляция обмена белков
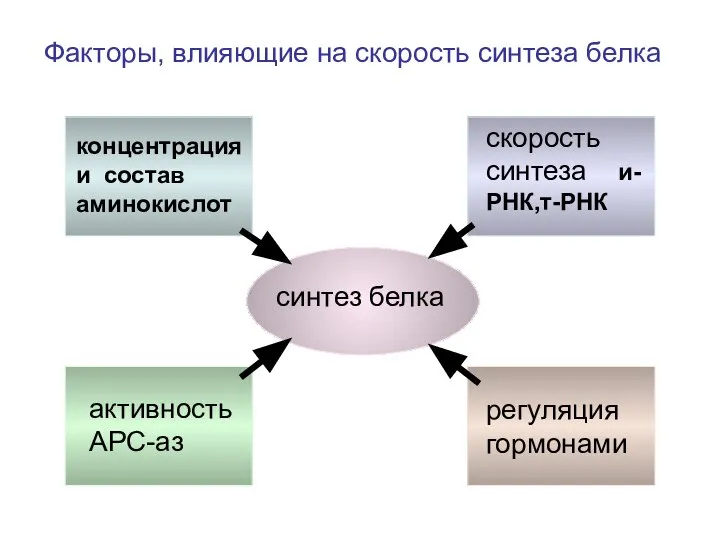
- 144. синтез белка концентрация и состав аминокислот скорость синтеза и-РНК,т-РНК активность АРС-аз регуляция гормонами Факторы, влияющие на
- 145. Влияние некоторых факторов на концентрацию и состав аминокислот Доступность в белковой диете; 2. Наличие полноценных белков
- 146. Влияние некоторых факторов на активность АРС-аз Активность белково-синтезирующей системы; 2. Кислотно-основное состояние в организме; 3. Состояние
- 147. Факторы, влияющие на скорость синтеза и-РНК и т-РНК Наличие нуклеотидного фонда; Состояние биоэнергетических процессов; 3. Влияние
- 148. Гормональная регуляция скорости синтеза белка Соматотропин, половые гормоны (индукторы транскрипции и биосинтеза белка); 2. Тироксин (активатор
- 149. На скорость дезаминирования аминокислот влияют: Соотношение НАДН2 /НАД. При гипоксии увеличивается концентрация НАДН2. Недостаток НАД служит
- 150. Взаимосвязь между обменом белков, углеводов и липидов.
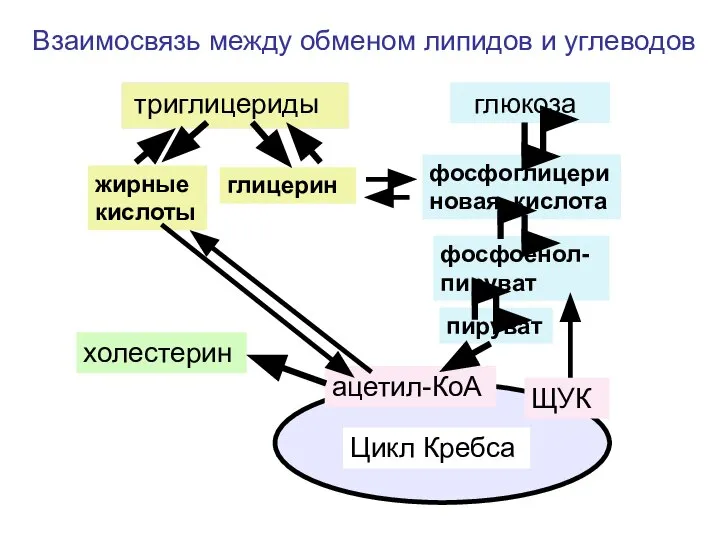
- 151. триглицериды глюкоза жирные кислоты глицерин фосфоглицериновая кислота фосфоенол-пируват пируват ацетил-КоА холестерин Цикл Кребса ЩУК Взаимосвязь между
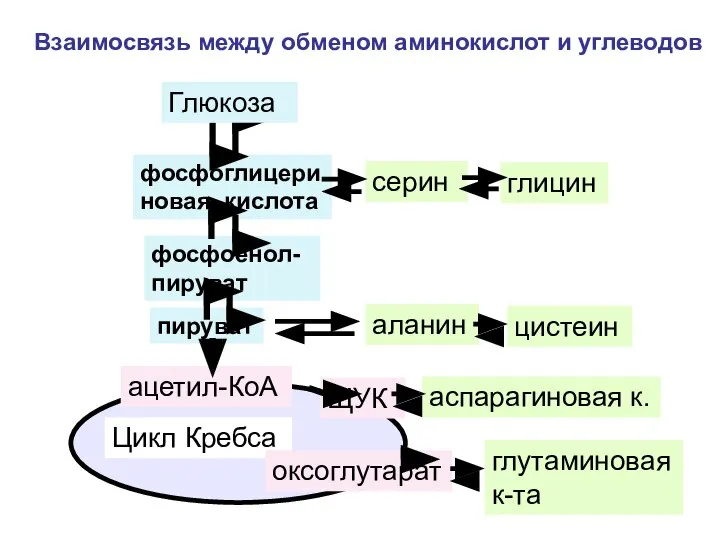
- 152. фосфоглицериновая кислота фосфоенол-пируват пируват ацетил-КоА Цикл Кребса ЩУК Взаимосвязь между обменом аминокислот и углеводов Глюкоза оксоглутарат
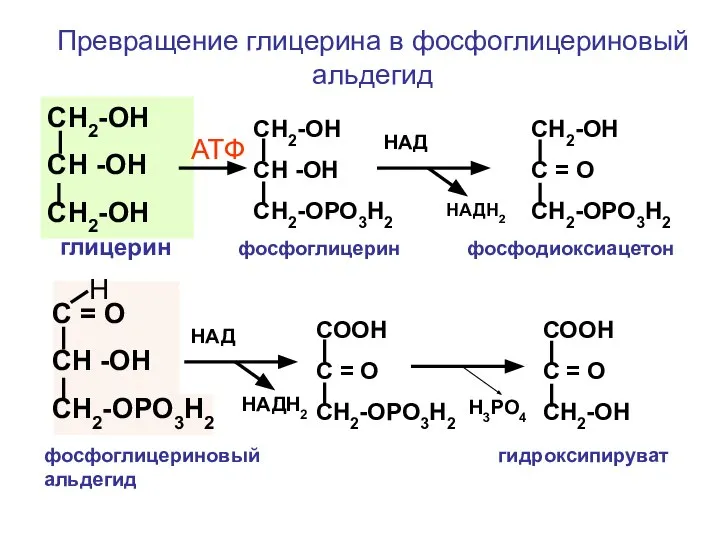
- 153. СН2-ОН СН -ОН СН2-ОН СН2-ОН СН -ОН СН2-ОРО3Н2 СН2-ОН С = О СН2-ОРО3Н2 АТФ НАД НАДН2
- 155. Скачать презентацию















































 Дисперсные системы (продолжение)
Дисперсные системы (продолжение) Короткі відомості з історії хімії. Становлення хімії як науки
Короткі відомості з історії хімії. Становлення хімії як науки Солнечные батареи в космосе. (Задача 2)
Солнечные батареи в космосе. (Задача 2)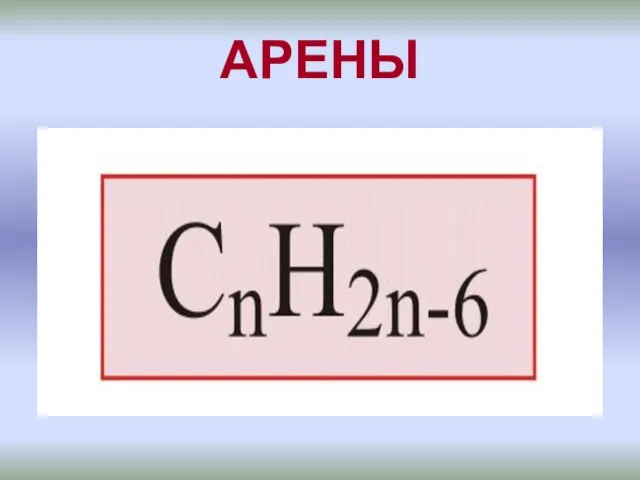 Бензоидные ароматические углеводороды - арены
Бензоидные ароматические углеводороды - арены Молекулярная биология. Белки нервной системы
Молекулярная биология. Белки нервной системы Катарометрический метод контроля
Катарометрический метод контроля Производство стекла
Производство стекла Процессы комплексообразования
Процессы комплексообразования Нефть. Состав и свойства
Нефть. Состав и свойства ФГОУ СПО «ЧПК» Выполнила: Гараева Оксана, студент группы №43 Руководители: Хасанова В.К., Чеснокова П.В.
ФГОУ СПО «ЧПК» Выполнила: Гараева Оксана, студент группы №43 Руководители: Хасанова В.К., Чеснокова П.В. Производные пурина
Производные пурина СЕРА S
СЕРА S Как осуществить цепочку превращений на основании положений теории электролитической диссоциации?
Как осуществить цепочку превращений на основании положений теории электролитической диссоциации? Применение этанола
Применение этанола Классификация химических реакций
Классификация химических реакций Великие химики России
Великие химики России Оксид азота(2) NO
Оксид азота(2) NO Повторение и обобщение знаний по темам "Металлы и сплавы."
Повторение и обобщение знаний по темам "Металлы и сплавы." Значение окислительно-восстановительных реакций в жизни человека
Значение окислительно-восстановительных реакций в жизни человека Аминокислоты Модели молекул
Аминокислоты Модели молекул Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Отрицательное влияние азотных минеральных удобрений на почву
Отрицательное влияние азотных минеральных удобрений на почву Green chemistry application to intermolecular forces
Green chemistry application to intermolecular forces Химическая связь
Химическая связь Неорганические соединения галогенов
Неорганические соединения галогенов Особенности формирования естественно-научной картины мира на уроках географии и химии
Особенности формирования естественно-научной картины мира на уроках географии и химии Камни и Козерог
Камни и Козерог Хімія і медицина
Хімія і медицина