Содержание
- 2. ИСТОРИЯ Оксид азота впервые был получен в 1772 году Джозефом Пристли, который назвал его «дефлогистированным нитрозным
- 3. СВОЙСТВА ОКСИДА АЗОТА Оксид азота – это бесцветный газ, трудно сжимающий при низких температурах-голубая жидкость, с
- 4. ПОЛУЧЕНИЕ ОКСИДА АЗОТА В лабораторных условиях получение оксида азота возможно путем проведения реакции разбавленной азотной кислоты
- 5. ПРИМЕНЕНИЕ ОКСИДА АЗОТА Оксид азота используется в медицине для расширения кровеносных сосудов при ишемической болезни сердца
- 7. Скачать презентацию
Слайд 2
ИСТОРИЯ
Оксид азота впервые был получен в 1772 году Джозефом Пристли, который
ИСТОРИЯ
Оксид азота впервые был получен в 1772 году Джозефом Пристли, который
назвал его «дефлогистированным нитрозным воздухом». В 1799 г. его исследовал Г. Дэви.
Оксид азота – химическое соединение группы окисей азота, в котором азот присутствует во II степени окисления. Он имеет один непарный радикальный электрон, следовательно, является нестабильным, имеет высокую реакционную способность и обладает свойствами свободного радикала. Оксид азота или окись азота, а также известный как монооксид азота представляет собой молекулу с химической формулой NO. Это свободные радикалы, которые является важным промежуточным продуктом химических реакций. В организмах млекопитающих и человека оксид азота является важной составляющей клеточных сигнальных молекул, участвующих во многих физиологических и патологических процессах. Это мощный вазодилататор с коротким, в несколько секунд, периодом полураспада в крови. В конце 80-х годов было доказано, что особые ферментные системы организмов способны синтезировать газ оксида азота. Это происходит в результате окисления гуанидиновой группы аминокислоты L-аргинина с одновременным синтезом цитруллина. Получение оксида азота В лабораторных условиях получение оксида азота возможно путем проведения реакции разбавленной азотной кислоты с медью или восстановлением азотистой кислоты в виде нитрита натрия или нитрита калия. Основным природным источником оксида азота являются электрические разряды молний в грозу. Оксид азота является побочным продуктом, возникающим при сгорании веществ в автомобильных двигателях и топлива на электростанциях. Также получение оксида азота возможно из свободных элементов, для этого необходимо при температуре 1200-1300°C провести соединение азота с кислородом.
Оксид азота – химическое соединение группы окисей азота, в котором азот присутствует во II степени окисления. Он имеет один непарный радикальный электрон, следовательно, является нестабильным, имеет высокую реакционную способность и обладает свойствами свободного радикала. Оксид азота или окись азота, а также известный как монооксид азота представляет собой молекулу с химической формулой NO. Это свободные радикалы, которые является важным промежуточным продуктом химических реакций. В организмах млекопитающих и человека оксид азота является важной составляющей клеточных сигнальных молекул, участвующих во многих физиологических и патологических процессах. Это мощный вазодилататор с коротким, в несколько секунд, периодом полураспада в крови. В конце 80-х годов было доказано, что особые ферментные системы организмов способны синтезировать газ оксида азота. Это происходит в результате окисления гуанидиновой группы аминокислоты L-аргинина с одновременным синтезом цитруллина. Получение оксида азота В лабораторных условиях получение оксида азота возможно путем проведения реакции разбавленной азотной кислоты с медью или восстановлением азотистой кислоты в виде нитрита натрия или нитрита калия. Основным природным источником оксида азота являются электрические разряды молний в грозу. Оксид азота является побочным продуктом, возникающим при сгорании веществ в автомобильных двигателях и топлива на электростанциях. Также получение оксида азота возможно из свободных элементов, для этого необходимо при температуре 1200-1300°C провести соединение азота с кислородом.
Слайд 3
СВОЙСТВА ОКСИДА АЗОТА
Оксид азота – это бесцветный газ, трудно сжимающий
СВОЙСТВА ОКСИДА АЗОТА
Оксид азота – это бесцветный газ, трудно сжимающий
при низких температурах-голубая жидкость, с температурой плавления -163,6°С и температурой кипения -151,7°С. Молекулярная формула оксида азота – NO, молярная масса – 30.01 грамм/моль, плотность – 1,3402 г дм, растворимость в воде – 74 см3/дм3, показатель преломления – 1.0002697. Не растворим в воде.
Слайд 4
ПОЛУЧЕНИЕ ОКСИДА АЗОТА
В лабораторных условиях получение оксида азота возможно путем проведения
ПОЛУЧЕНИЕ ОКСИДА АЗОТА
В лабораторных условиях получение оксида азота возможно путем проведения
реакции разбавленной азотной кислоты с медью или восстановлением азотистой кислоты в виде нитрита натрия или нитрита калия. Основным природным источником оксида азота являются электрические разряды молний в грозу. Оксид азота является побочным продуктом, возникающим при сгорании веществ в автомобильных двигателях и топлива на электростанциях. Также получение оксида азота возможно из свободных элементов, для этого необходимо при температуре 1200-1300°C провести соединение азота с кислородом.
Слайд 5
ПРИМЕНЕНИЕ ОКСИДА АЗОТА
Оксид азота используется в медицине для расширения кровеносных сосудов
ПРИМЕНЕНИЕ ОКСИДА АЗОТА
Оксид азота используется в медицине для расширения кровеносных сосудов
при ишемической болезни сердца путем уменьшения нагрузки на сердце. Оксид азота используется при неотложной помощи для содействия капиллярному расширению легких для лечения первичной легочной гипертензии у новорожденных, связанной с врожденными дефектами. Терапия оксидом азота значительно повышает качество жизни и, в некоторых случаях, спасает жизнь детей с риском развития заболевания сосудов легких. Оксид азота также вводится в виде спасительной терапии у больных с острой правожелудочковой недостаточностью, которая является вторичной по отношению к легочной эмболии. В пищевой промышленности оксид азота известен под названием пищевая добавка Е942 и используется в качестве пропеллента и упаковочного газа. Свойства оксида азота Оксид азота – это бесцветный газ с температурой плавления -163,6°С и температурой кипения -151,7°С. Молекулярная формула оксида азота – NO, молярная масса – 30.01 грамм/моль, плотность – 1,3402 г дм, растворимость в воде – 74 см3/дм3, показатель преломления – 1.0002697.
- Предыдущая
Минералы и горные породы, методы их определенияСледующая -
Реакции при участии катализатора



 Возникновение органической химии, как науки
Возникновение органической химии, как науки Коллоидты жүйелердің коагуляциялық және кристаллизациялық құрылымдары
Коллоидты жүйелердің коагуляциялық және кристаллизациялық құрылымдары Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості.
Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості.  VI группа периодической системы. VIA-группа
VI группа периодической системы. VIA-группа Установка кристаллов
Установка кристаллов ЕГЭ Химия. Задание №5
ЕГЭ Химия. Задание №5 Изделия на основе углеволокон
Изделия на основе углеволокон Презентация по Химии "Получение водорода в лаборатории" - скачать смотреть
Презентация по Химии "Получение водорода в лаборатории" - скачать смотреть  Растворы. Общая характеристика растворов
Растворы. Общая характеристика растворов Токсикология и анализ спиртов
Токсикология и анализ спиртов Физические свойства металлов
Физические свойства металлов Биохимия витаминов. Классификация витаминов. Жирорастворимые витамины. (Лекция 20)
Биохимия витаминов. Классификация витаминов. Жирорастворимые витамины. (Лекция 20) Законы химии. Массовая доля вещества в растворе. Решение задач. (Лекция 3)
Законы химии. Массовая доля вещества в растворе. Решение задач. (Лекция 3) Эмульсии, микроэмульсии и пены. Производство и применение
Эмульсии, микроэмульсии и пены. Производство и применение Роль химии в нашей жизни
Роль химии в нашей жизни Положение атомов - металлов в ПСХЭ Д.И.Менделеева. 9 класс
Положение атомов - металлов в ПСХЭ Д.И.Менделеева. 9 класс Soluţiile sunt amestecuri omogene de două sau mai multe substanţe
Soluţiile sunt amestecuri omogene de două sau mai multe substanţe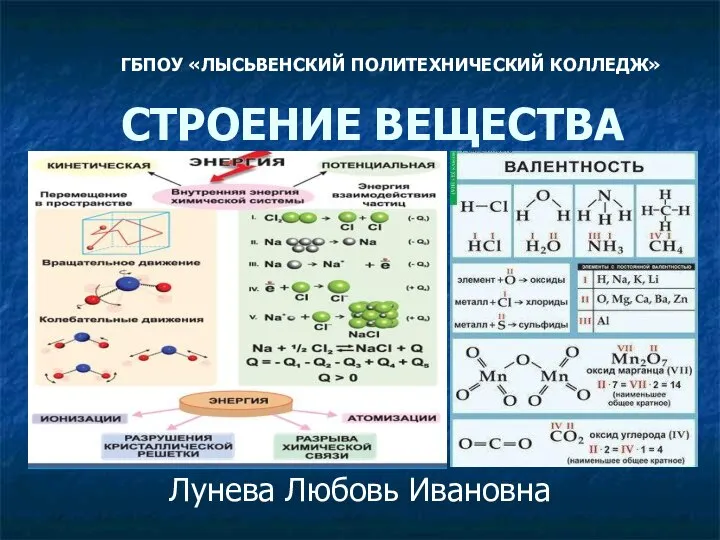 Строение вещества
Строение вещества Нефть. Состав и свойства
Нефть. Состав и свойства Этилен. Действие этилена на рост проростков гороха
Этилен. Действие этилена на рост проростков гороха Полиморфизм. Аллотропия
Полиморфизм. Аллотропия Буландырғыш аппараттарының құрылымдары
Буландырғыш аппараттарының құрылымдары Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой
Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой Бериллий: основные свойства, технологии получения, применение
Бериллий: основные свойства, технологии получения, применение Поняття про лікарські препарати Підготували Стебко Марія, Бондар Аліна 11-Ф
Поняття про лікарські препарати Підготували Стебко Марія, Бондар Аліна 11-Ф  Катализдің түрлері жене маңызы
Катализдің түрлері жене маңызы Наносеребрянные носки
Наносеребрянные носки Аминокислоты. Классификация. Реакционная способность
Аминокислоты. Классификация. Реакционная способность