Содержание
- 2. Что читать? А.П. Чупахин «ИОННЫЕ ПРОЦЕССЫ В ВОДНЫХ РАСТВОРАХ ЧАСТЬ 2» НГУ, 2015 И.В. Морозов, А.И.
- 3. ОВР = окислительно- восстановительные реакции Окислительно-восстановительные реакции (ОВР) – это такие химические реакции, в которых происходит
- 4. Важные понятия! Степень окисления (СО) – формальный заряд, который можно приписать атому, входящему в состав какой-либо
- 5. Важные понятия! Окислитель (Ox) – частица, которая в ходе ОВР приобретает электроны. Восстановитель (Red) – частица,
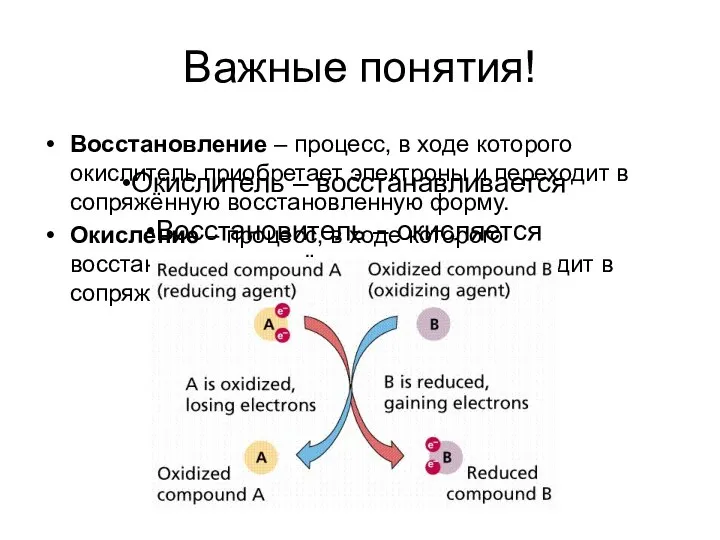
- 6. Важные понятия! Восстановление – процесс, в ходе которого окислитель приобретает электроны и переходит в сопряжённую восстановленную
- 7. Важные понятия! В любой ОВР всегда принимают участие две пары конкурирующих за электроны сопряженных окислителей и
- 8. Правила расчета степени окисления Сумма СО всех атомов в частице равна заряду этой частицы (в простых
- 9. Уравнивание ОВР Электронный баланс. Метод полуреакций. Разберем на примерах.
- 10. Алгоритм метода электронного баланса Найти атомы у которых меняются степени окисления. Уровнять электронный баланс. (умножить на
- 11. FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + KHSO4 Fe2+ - e → Fe3+
- 12. CoS + O2 → Co3O4 + SO2 Co2+ - 2/3e → Co8/3+ S2- - 6e →
- 13. Co2+ - e → Co3+ S2- - 6e → S4+ O0 + 2e → O2- CoS
- 14. Метод полуреакций Найти атомы у которых меняются степени окисления. Составить (а лучше выписать из справочника) полуреакции.
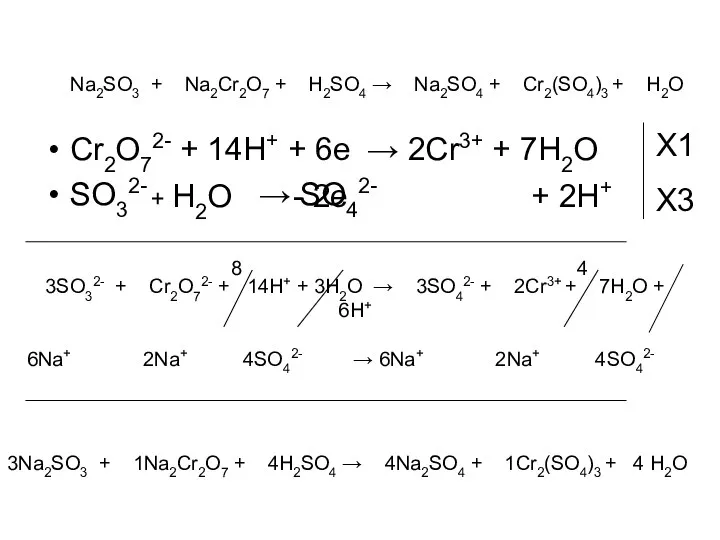
- 15. Na2SO3 + Na2Cr2O7 + H2SO4 → Na2SO4 + Cr2(SO4)3 + H2O Для составления полуреакций в водной
- 16. Cr2O72- + 14H+ + 6e → 2Cr3+ + 7H2O SO32- → SO42- Na2SO3 + Na2Cr2O7 +
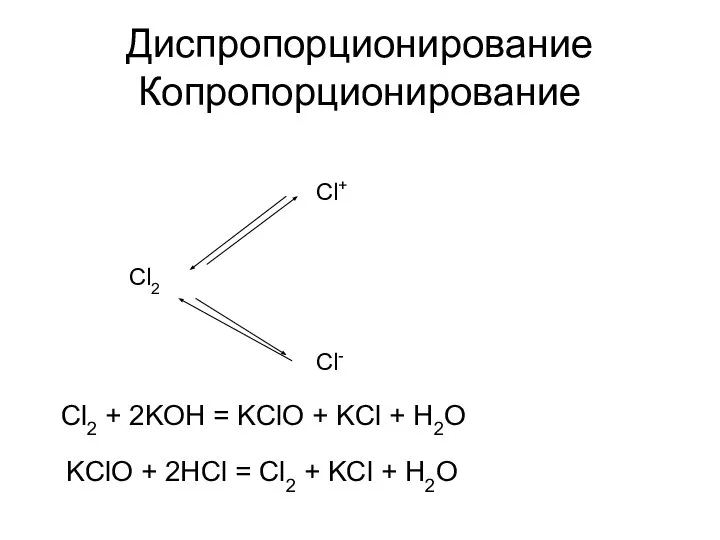
- 17. Диспропорционирование Копропорционирование Cl2 Cl+ Cl- Cl2 + 2KOH = KClO + KCl + H2O KClO +
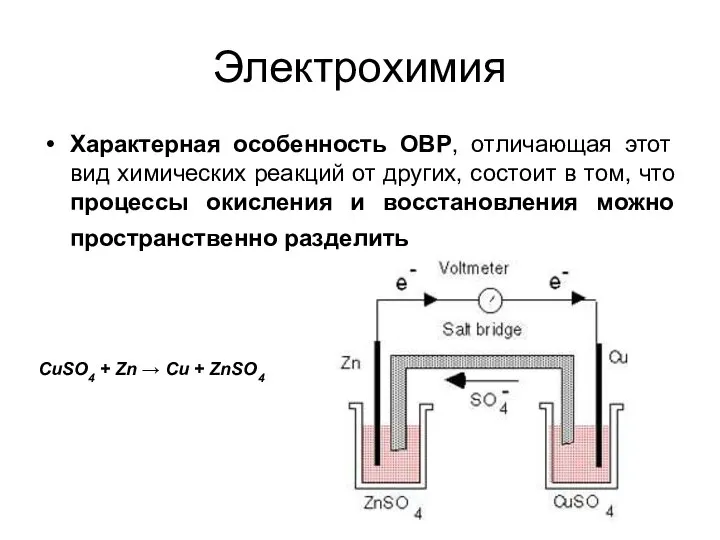
- 18. Электрохимия Характерная особенность ОВР, отличающая этот вид химических реакций от других, состоит в том, что процессы
- 19. Вперед – гальванический, Назад - электролитический Если ОВР в электрохимической цепи протекает самопроизвольно, то такая цепь
- 20. Классификация ХИТов гальванические элементы (первичные ХИТ), которые из-за необратимости протекающих в них реакций, невозможно перезарядить; электрические
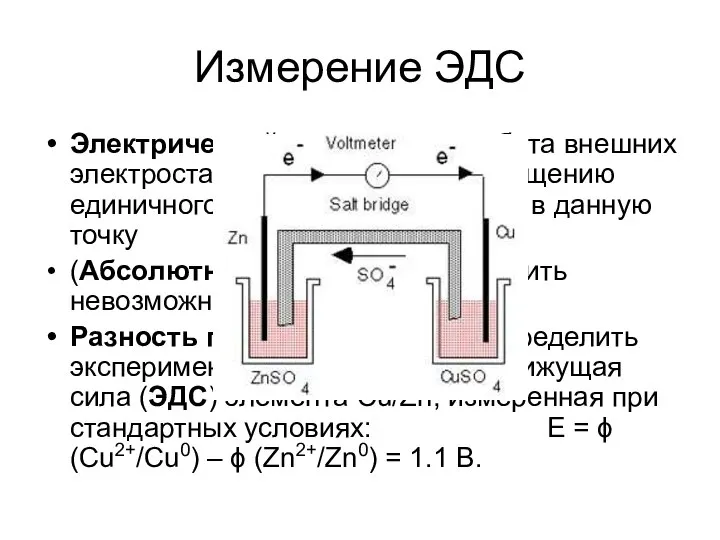
- 21. Измерение ЭДС Электрический потенциал – работа внешних электростатических сил по перемещению единичного заряда из точки с
- 22. ЭДС и работа(энергия) При взаимодействии 1 моль Zn и 1 моль CuSO4 переносится n = 2
- 23. ЭДС и энергия Гиббса ΔG = -Аэ/х ΔG = -n·F·ΔE Определение направления процесса ΔG ΔE >
- 24. Установление «нуля» «Дайте мне точку опоры и я переверну Землю» АРХИМЕД Archimedes ок. 287 - 212
- 25. Пример определения направления процесса 2FeCl3 + Cu → CuCl2 + 2FeCl2 2Fe3+ + Cuo → Cu2+
- 26. Энергия Гиббса и К 2FeCl3 + Cu → CuCl2 + 2FeCl2 Е0 = 0,77 - 0,34
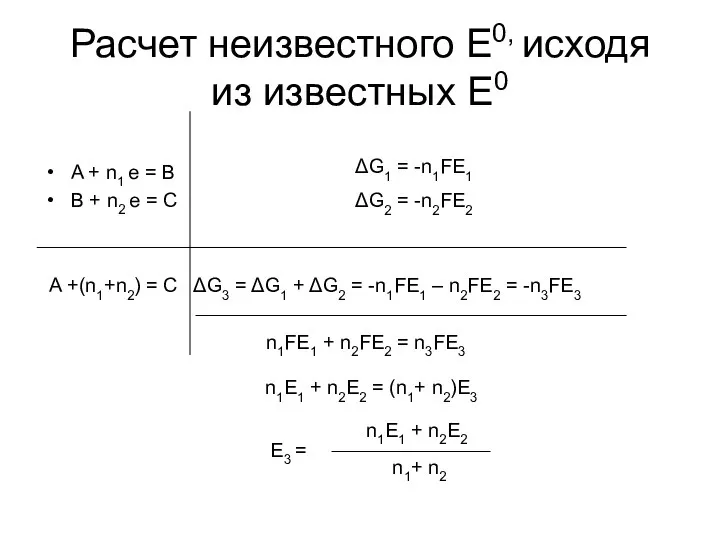
- 27. Расчет неизвестного E0, исходя из известных E0 A + n1 e = B B + n2
- 28. Пример расчета Е0 3IO- + 3H2O + 4e → I3- + 6OH- 3I- - 2e →
- 29. Диаграмма Латимера
- 30. Диаграмма Латимера 2+ 4+ 6+ 6+ 7+ 7+ 7+ 7+ MnO4- → MnO42- → MnO2 →
- 31. 2+ 4+ 6+ 6+ 7+ 7+ 7+ 7+ Диаграмма Латимера В щелочной (ОН-) MnO4- → MnO42-
- 32. Диспропорционирование Копропорционирование по диаграмме Латимера E = 2.26 – 0.59 = 1.6 > 0 E =
- 33. Как при помощи Е рассчитывают ПР (KL) ? ПР(HgS) = 4*10-53 C(Hg2+)=C(S2-)= 6.3*10-27 М В одном
- 34. Как при помощи Е рассчитывают ПР (KL) ? Хлорсере́бряный электро́д (ХСЭ) благодаря стабильности потенциала (ХСЭ) благодаря
- 35. Как при помощи Е рассчитывают ПР (KL) ? Hg2+ + 2e = Hg E0 = 0.85
- 36. Уравнение Нернста Вальтер Герман Нернст Walther Hermann Nernst, 18641864, — 1941 Лауреат Нобелевской премии
- 37. Электрохимический вариант уравнения изотермы химической реакции. ΔG = ΔG0 + RTlnП E = E0 – lnП
- 38. Зависимость Е от рН. Одним из наиболее важных факторов, влияющих на величину электродного потенциала, является кислотность
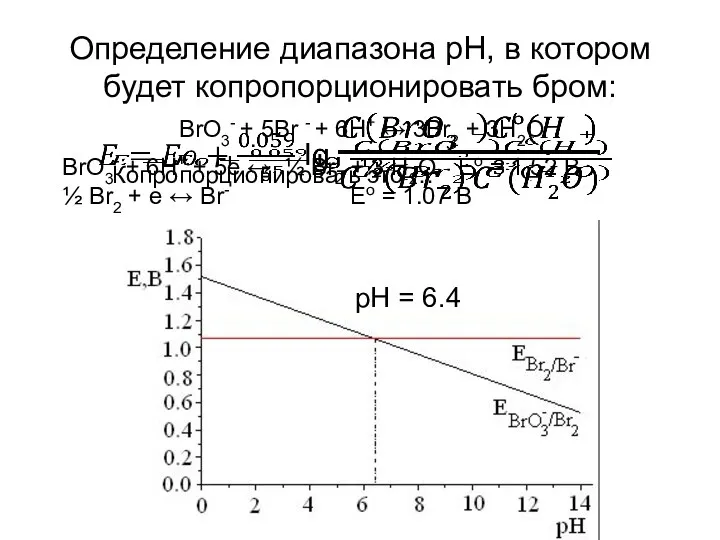
- 39. Определение диапазона рН, в котором будет копропорционировать бром: Копропорционировать это … Диспропорционировать это … BrO3- +
- 41. Скачать презентацию









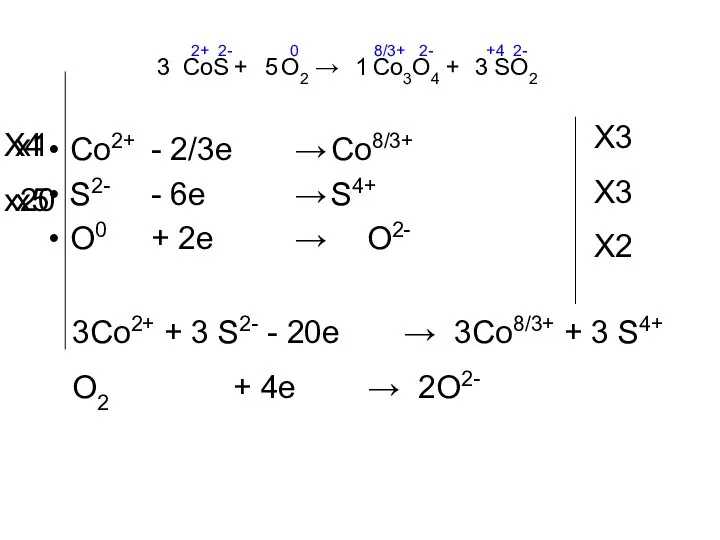





















 Изучение десорбции лантаноидов и иттирия из сульфокатионита КУ-2 с применением сульфата аммония
Изучение десорбции лантаноидов и иттирия из сульфокатионита КУ-2 с применением сульфата аммония Неорганические лекарственные средства. Соединения элементов V и VI группы периодической системы
Неорганические лекарственные средства. Соединения элементов V и VI группы периодической системы Презентация по Химии "«Основные химические понятия»" - скачать смотреть
Презентация по Химии "«Основные химические понятия»" - скачать смотреть  Химия элементов IVA группы
Химия элементов IVA группы Юный химик. Интерактивная интеллектуальная игра
Юный химик. Интерактивная интеллектуальная игра Природный и попутный нефтяной газы
Природный и попутный нефтяной газы Бензилиденкетоны в синтезе замещённых бензимидазолопиримидинов
Бензилиденкетоны в синтезе замещённых бензимидазолопиримидинов Презентация Качество продукции
Презентация Качество продукции  Презентация Подгруппа углерода и азота
Презентация Подгруппа углерода и азота Производство HNO3
Производство HNO3 Химия көшбасшысы
Химия көшбасшысы Өтмө металлдар
Өтмө металлдар Химия белков Функции и классификация белков
Химия белков Функции и классификация белков  Диаграммы бинарных систем, образующих твердые растворы
Диаграммы бинарных систем, образующих твердые растворы Основные классы неорганических соединений
Основные классы неорганических соединений Қышқылдық негіздік тепе теңдік
Қышқылдық негіздік тепе теңдік Химия и производство. Химическая промышленность и химические технологии
Химия и производство. Химическая промышленность и химические технологии Карбоновые кислоты
Карбоновые кислоты Гальванический элемент
Гальванический элемент Циклоалканы. Лекция 4
Циклоалканы. Лекция 4 Обмен простых белков. Дезаминирование и трансаминирование аминокислот
Обмен простых белков. Дезаминирование и трансаминирование аминокислот Криптонит для растений
Криптонит для растений Гидроксид натрия
Гидроксид натрия Жёсткость воды и способы её устранения
Жёсткость воды и способы её устранения Состояние атмосферного воздуха в Ярославской области
Состояние атмосферного воздуха в Ярославской области Лекарственные растения и сырье, содержащие бициклические монотерпены в составе эфирных масел. (Лекция 6)
Лекарственные растения и сырье, содержащие бициклические монотерпены в составе эфирных масел. (Лекция 6) Кирпичики наноструктуры. Занятие 8
Кирпичики наноструктуры. Занятие 8 Задачи к экзамену по дисциплине «ИПР и ОП»
Задачи к экзамену по дисциплине «ИПР и ОП»