Содержание
- 2. Цель лекции Понять сущность окислительно-восстановительных реакций через понятия сопряженная редокс пара и её редокс потенциал Обосновать
- 3. План лекции Актуальность темы Понятие сопряженной окислительно-восстановительной пары и её редокс потенциал. Механизм возникновения электродных потенциалов.
- 4. Актуальность Окислительно-восстановительных процессы лежат в основе понимания взаимопревращения разных форм энергии (химической в электрическую и обратно,
- 5. Основные понятия Атом, который принимает электроны – акцептор электронов – называется окислителем. При этом его степень
- 6. Основные понятия (продолжение) Атом, который отдает электроны – донор электронов, - называется восстановителем. При этом его
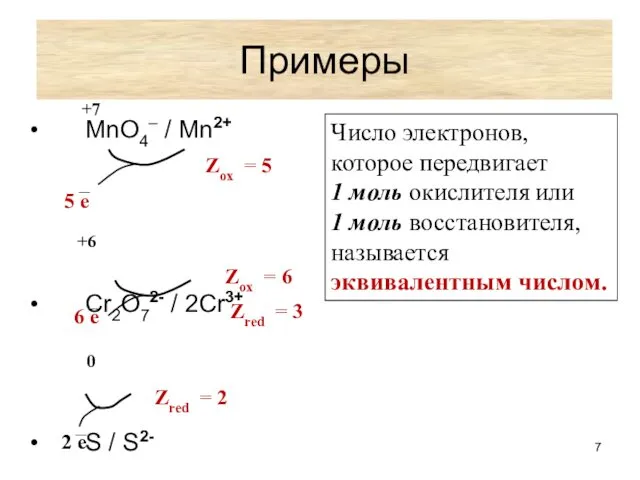
- 7. Примеры MnO4– / Mn2+ Cr2O72- / 2Cr3+ S / S2- 5 e – Zox = 5
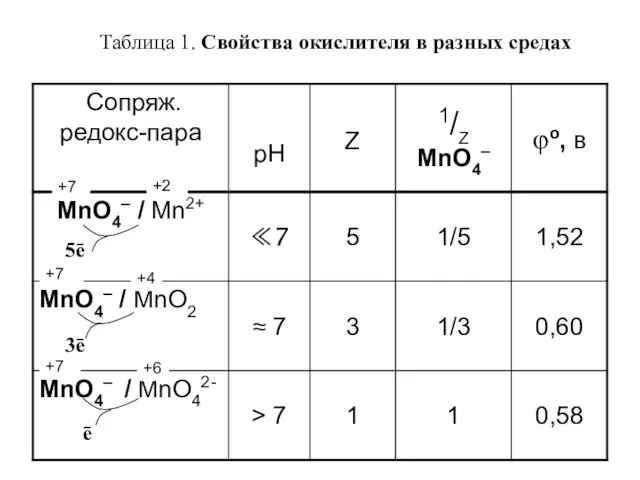
- 8. Таблица 1. Свойства окислителя в разных средах
- 9. Редокс-потенциал ϕ измеряется с помощью гальванического элемента Если измерения проведены в стандартных условиях : to =
- 10. Редокс-потенциал (продолжение) Окислительно-восстановительный потенциал – это напряжение, которое вызывает в гальваническом элементе одна редокс пара по
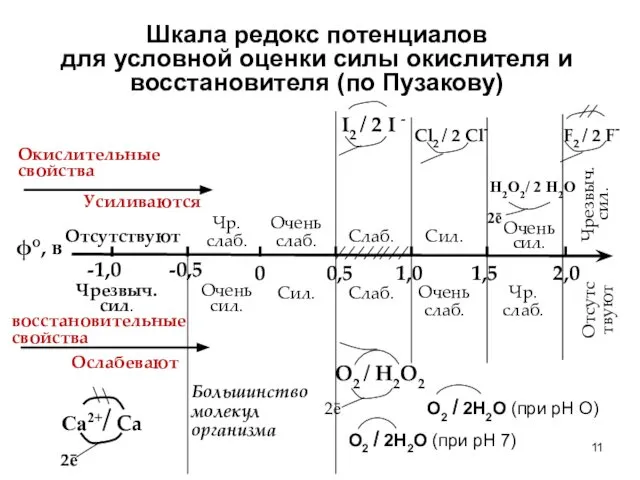
- 11. Шкала редокс потенциалов для условной оценки силы окислителя и восстановителя (по Пузакову) О2 / 2Н2О (при
- 12. Судя по потенциалу редокс пар, биомолекулы – сильные восстановители; они отдают свой электрон даже слабым окислителям,
- 13. Жесткие (сильные) окислители Заметим, что при рН 0 кислород является жестким окислителем. ϕо (О2 / 2Н2О
- 14. Водородный электрод как гетерогенная редокс пара 2Н+(р)│Н2 (Pt)
- 15. ЭДС реакции Разность потенциалов двух сопряженных редокс пар называется электродвижущей силой (ℰ) окислительно-восстановительной реакции.
- 16. ℰ реакции может быть только положительной величиной (отрицательная лишена физического смысла), т.е. ℰ > 0. ℰ
- 17. Сопряженная редокс пара может быть записана в виде полуреакций
- 18. Уравнение Нернста В нестандартных условиях потенциалы редокс пар подсчитывают по формуле Нернста: где R = 8,31
- 19. Уравнение Нернста (продолжение) Заменяя ln→lg (коэффициент 2,3), получим a, b, c – стехиометрические коэффициенты реакции: а·ox
- 20. Расстановка коэффициентов в ОВР методом ЭИБ (м. полуреакций) Пишут полуреакции для окислителя и восстановителя в ионном
- 21. Расстановка коэффициентов методом ЭИБ (м. полуреакций) Затем полуреакции суммируют и получают суммарное уравнение в ионном виде.
- 22. Баланс по «О»
- 23. Примеры КMnO4 + Na2SO3 + H2SO4 → MnSO4 + Na2SO4 + K2SO4 + H2O 2× MnO4–
- 24. Примеры КMnO4 + Na2SO3 + H2O → MnO2↓ + Na2SO4 + KOH 2× MnO4– + 2
- 25. Методы количественного определения окислителей или восстановителей В основе методов оксидиметрии лежат окислительно-восстановительные реакции Рабочими реактивами являются
- 26. Перманганатометрия (ПМ) Основная реакция метода (точнее, полуреакция): MnO4– + 8H+ + 5ē = Mn2+ + 4H2O
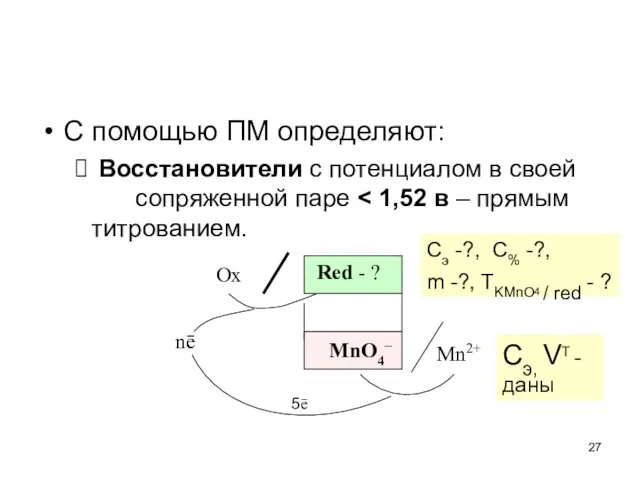
- 27. C помощью ПМ определяют: Восстановители с потенциалом в своей сопряженной паре Red - ? MnO4– Ox
- 28. Расчеты m(red) = M(1/z red) · n(1/z red) = = M(1/z red) · n(1/z MnO4–) =
- 29. Т = = = = =
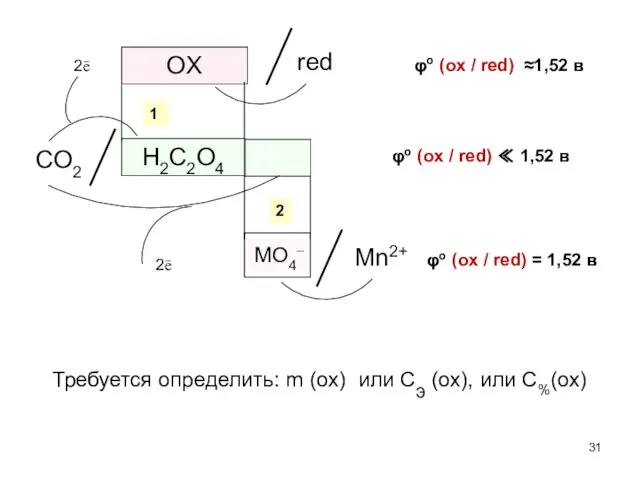
- 30. Определение окислителей ПМ-й Окислители с потенциалом в сопряженной паре, близким к 1,52 в определяют методом обратного
- 31. Требуется определить: m (ox) или Сэ (ox), или С%(ox)
- 32. Расчеты при обратном титровании в ПМ m (ox) = M(1/z ox) · Cэ (H2C2O4) · Vмл1
- 33. Примечание # Вместо щавелевой кислоты в качестве вспомогательного реактива при обратном титровании в ПМ можно использовать
- 34. Йодометрия Основная реакция метода (точнее, полуреакция): I2 + 2ē ⇄ 2I– φo(I2/ 2I–) = + 0,54
- 35. # I2 плохо растворяется в воде, но хорошо в KI благодаря реакции комплексообразования с I–: I2
- 36. Йодометрия (продолжение) Рабочими растворами метода являются: I2 в KI, сам KI, а также тиосульфат натрия Na2S2O3·5H2O.
- 37. φo(S4O62-/2S2O32-) ≈ 0,2 в ℰреакции=Δφo = Δφo (I2/2I-) – Δφo(S4O62-/2S2O32-)= = 0,54 – 0,2 = 0,34
- 38. Прямым титрованием определяют восстановители с φo (ox/red) ≪ 0,54 в Их титруют раствором I2 в присутствии
- 39. Расчеты При прямом титровании m (red) = M (1/z red)·Cэ·Vл(I2) = = M (1/z red)·Cэ·Vмл·10-3 (I2),
- 40. Обратным титрованием определяют Восстановители с потенциалом в сопряженной паре К ним добавляют фиксированный избыток вспомогательного раствора
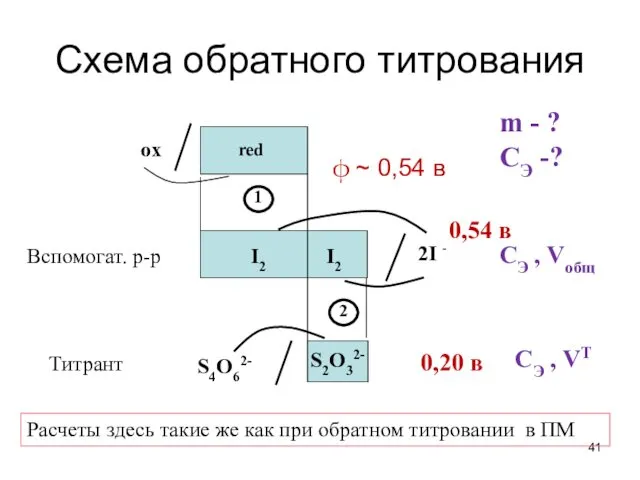
- 41. Схема обратного титрования ϕ ~ 0,54 в Вспомогат. р-р 0,54 в Расчеты здесь такие же как
- 42. Расчеты При обратном титровании m (red) = M (1/z red)·Cэ·Vл1(I2) = V1(I2) = Vобщ.- V2 =
- 43. Косвенным титрованием определяют окислители с φo 0,54 в Cуть: к окислителю добавляют нефиксированный избыток вспомогательного раствора
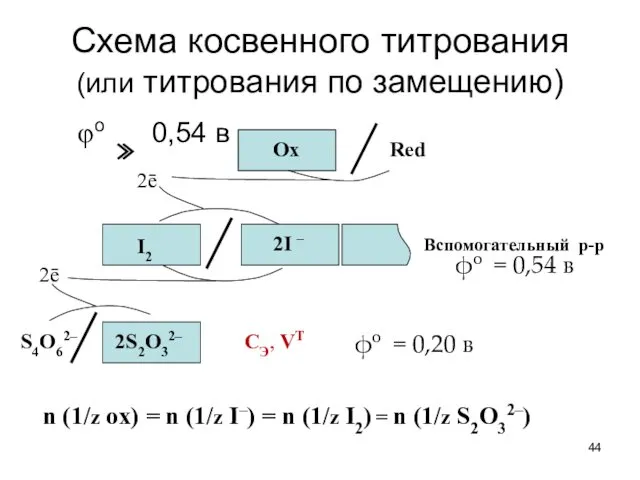
- 44. Схема косвенного титрования (или титрования по замещению) φo 0,54 в Red Ox ≫ 2I – I2
- 45. Поэтому рассчеты массы При косвенном титровании cходны с таковыми при прямом титровании: m (ox) = M
- 46. Выводы При косвенном титровании количество эквивалентов окислителя равно количеству эквивалентов восстановителя Na2S2O3, хотя в прямой контакт
- 47. Косвенным титрованием в ЙМ можно определять и кислоты HCl, CH3COOH 6HCl + KIO3 + 5KI (разб.)
- 48. Основные выводы Данные по окислительно-восстановительным потенциалам сопряженных редокс пар позволяют подобрать участников реакции – окислитель и
- 49. Литература Основная: Слесарев В.И. – Химия: Основы химии живого: Учебник для вузов. – 3-е изд., испр.
- 51. Скачать презентацию









































 Мыло
Мыло  Крохмаль і целюлоза
Крохмаль і целюлоза  Введение в предмет. Классификация композитов
Введение в предмет. Классификация композитов Кремний және оның қосылыстары
Кремний және оның қосылыстары Нуклеиновые кислоты
Нуклеиновые кислоты Презентация Электролиз
Презентация Электролиз Биоэнергетика. Энергетическое сопряжение
Биоэнергетика. Энергетическое сопряжение Углерод Carboneum происходит от лат. carbo — уголь.
Углерод Carboneum происходит от лат. carbo — уголь. Полимеры, пластмассы и товары на их основе
Полимеры, пластмассы и товары на их основе Получение силикагеля, модифицированного бензоксазолами
Получение силикагеля, модифицированного бензоксазолами Химия вокруг нас
Химия вокруг нас Презентация по Химии "Нафта і нафтопродукти" - скачать смотреть бесплатно
Презентация по Химии "Нафта і нафтопродукти" - скачать смотреть бесплатно Презентация по Химии "Окрашивание пластмасс" - скачать смотреть
Презентация по Химии "Окрашивание пластмасс" - скачать смотреть  Химический элемент сера
Химический элемент сера Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные
Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ
Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ Сказка о Круговороте Азота
Сказка о Круговороте Азота Исследование влияния изменения технических параметров на производительность установки замедленного коксования
Исследование влияния изменения технических параметров на производительность установки замедленного коксования Характеристика переходного металла на основании его положения в Периодической системе. Амфотерность
Характеристика переходного металла на основании его положения в Периодической системе. Амфотерность Повышение огнестойкости деревянных конструкций методом поверхностной и объёмной пропитки
Повышение огнестойкости деревянных конструкций методом поверхностной и объёмной пропитки Полимеры. Основные понятия
Полимеры. Основные понятия Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В.
Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В. Топливо и топливосжигающие устройства. Горение топлива
Топливо и топливосжигающие устройства. Горение топлива Минералы группы кварца. Скрытокристаллические формы
Минералы группы кварца. Скрытокристаллические формы Метан и его свойства
Метан и его свойства  Відкриття радіоактивності. У 1896 р. французький учений Антуан Анрі Беккерель (1852-1908) відкрив радіоактивність солей Урану – явище са
Відкриття радіоактивності. У 1896 р. французький учений Антуан Анрі Беккерель (1852-1908) відкрив радіоактивність солей Урану – явище са Фазовые равновесия. Физическая и коллоидная химия
Фазовые равновесия. Физическая и коллоидная химия Вольфрам W
Вольфрам W