Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В.
Содержание
- 2. Цель Сформировать представление о строении периодической системы Рассмотреть закономерности свойств химических элементов Меню
- 3. Содержание Историческая справка Структура периодической системы Закономерности изменения свойств элементов в периодах Закономерности изменения свойств элементов
- 4. Историческая справка Открыта 1 марта 1969 Д. И. Менделеевым Является графическим отображением периодического закона Известны более
- 5. Длинный вариант периодической системы Меню
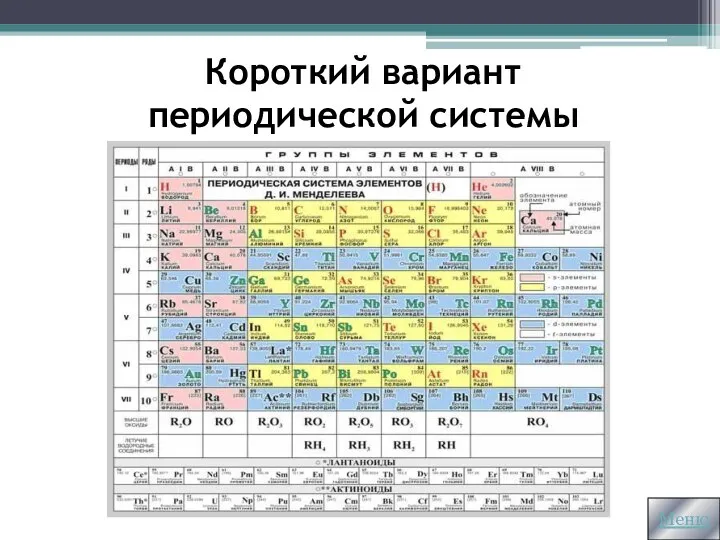
- 6. Короткий вариант периодической системы Меню
- 7. Структура периодической системы Периодическая система Периоды Группы Меню
- 8. Периоды Горизонтальные ряды, сходных по свойствам элементов Всего 7 Обозначаются римскими цифрами Делятся на малые и
- 9. Изменение свойств элементов в периодах Увеличивается: Заряд ядра; 2) Радиус атома; 3) Число электронов на внешнем
- 10. Группы Горизонтальные ряды сходных по свойствам элементов. Всего 8 Делятся на главные (A) и побочные (B)
- 11. Изменение свойств элементов в группах Увеличивается: Заряд ядра; 2) Радиус атома; 3) Число энергетических уровней; 4)
- 12. Проверочная работа Сравните: Заряд ядра: Na * Mg Радиус атома N * O Число энергетических уровней
- 13. Проверь ответ Сравните: Заряд ядра: Na Радиус атома N Число энергетических уровней S = P Число
- 15. Скачать презентацию











 Гелий
Гелий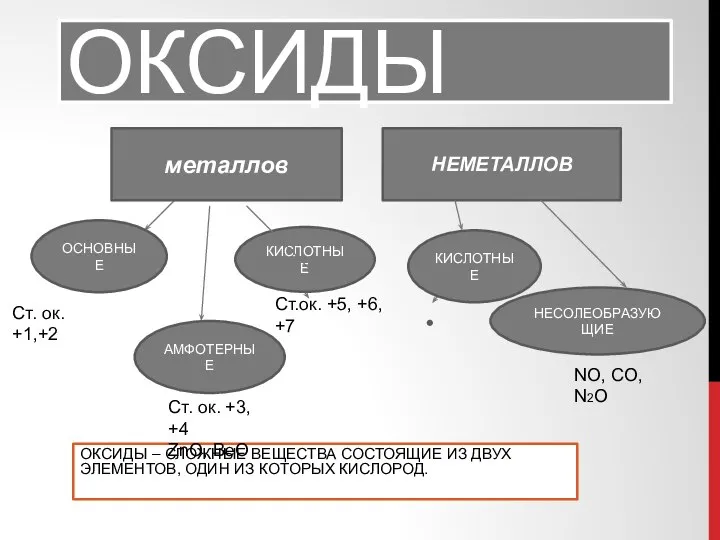 Оксиды
Оксиды History of radioactivity
History of radioactivity Презентация по химии Сахароза 10 класс
Презентация по химии Сахароза 10 класс Реакции замещения. Электрохимический ряд напряжений.
Реакции замещения. Электрохимический ряд напряжений. Норми радіаційної безпеки (НРБУ-97)
Норми радіаційної безпеки (НРБУ-97) Кремний и его соединения
Кремний и его соединения Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Композиционные материалы
Композиционные материалы Путешествие по континенту Химия познавательная игра по химии, 8 класс Автор: Лаврентьева Снежана Павловна, учитель химии и би
Путешествие по континенту Химия познавательная игра по химии, 8 класс Автор: Лаврентьева Снежана Павловна, учитель химии и би Поверхностное натяжение. Поверхности раздела фаз
Поверхностное натяжение. Поверхности раздела фаз Термоэластопласты. Классификация ТЭП
Термоэластопласты. Классификация ТЭП Амины. Анилин. Учитель химии МБОУ СОШ № 20 г.Королева Московской области Баранова Ирина Александровна
Амины. Анилин. Учитель химии МБОУ СОШ № 20 г.Королева Московской области Баранова Ирина Александровна Композиционные или композитные материалы
Композиционные или композитные материалы Композиты. Полимерные композиционные материалы
Композиты. Полимерные композиционные материалы Природные источники углеводородов и топливные ресурсы Западной Сибири
Природные источники углеводородов и топливные ресурсы Западной Сибири Микроэлементы
Микроэлементы Дослід Ознайомлення зі змістом етикеток харчових продуктів
Дослід Ознайомлення зі змістом етикеток харчових продуктів  Предмет химии. Вещества и их физические свойства. (8 класс)
Предмет химии. Вещества и их физические свойства. (8 класс) Сопряжение электронной плотности, как фактор обеспечения стабильности молекул
Сопряжение электронной плотности, как фактор обеспечения стабильности молекул Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Геохимия природных процессов. Метеориты
Геохимия природных процессов. Метеориты Личный опыт сортировки мусора
Личный опыт сортировки мусора Презентация по химии Удобрения и их классификация
Презентация по химии Удобрения и их классификация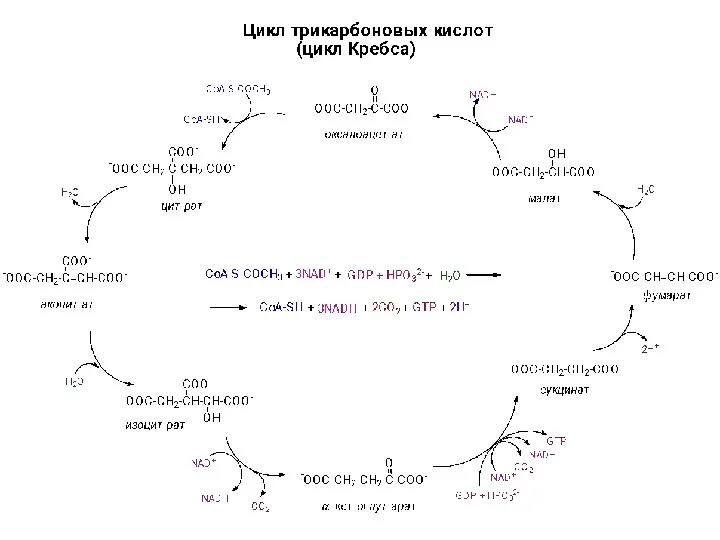 Цикл трикарбоновых кислот
Цикл трикарбоновых кислот Этилен. Углеводороды ряда этилена
Этилен. Углеводороды ряда этилена Пластмаси та полімери
Пластмаси та полімери Основные задачи токсикологической химии в аналитической диагностике наркотических и психотропных веществ (Продолжение)
Основные задачи токсикологической химии в аналитической диагностике наркотических и психотропных веществ (Продолжение)