Содержание
- 2. Окислительно-восстановительные реакции (ОВР) План: 1. Понятие ОВР 2. Типичные окислители и восстановители 3. Окислительно-восстановительная двойственность (ОВД)
- 3. Понятие ОВР I. ОВР – реакции, протекающие с изменением степени окисления элементов. Окислители принимают электроны и
- 4. Типичные окислители: Элементы в max степени окисления ( HNO3, KMnO4, K2Cr2O7) степень окисления = номер группы.
- 5. Типичные восстановители: Элементы в минимальной степени окисления (KI, H2S, NH3) Ме0 (металлы) (Zn0, Mg0) H20
- 6. Окислительно-восстановительная двойственность (ОВД) Элементы в промежуточной степени окисления (HNO2, Na2SO3) Ионы Mem+ в промежуточной степени окисления
- 7. IV. Метод электронного баланса Метод используется, если реакция протекает в газах или в твердой фазе. Пример:
- 8. V. Метод полуреакций Метод полуреакций используется для ОВР, протекающих в водном растворе. В нем выписывается не
- 9. Правила уравнивания атомов «O» и «Н»: а) кислая среда: в той части полуреакции, где мало атомов
- 10. б) нейтральная среда: если справа и слева в полуреакции разное количество атомов «О», то слева всегда
- 12. Скачать презентацию








 Серебро
Серебро Химический элемент - фосфор
Химический элемент - фосфор Классификация кислых пород
Классификация кислых пород Происхождение химических элементов
Происхождение химических элементов Основные свойства кристаллов
Основные свойства кристаллов Химическая промышленность России
Химическая промышленность России Изучение строения и свойств глюкозы. Разработка урока учителя химии Ерёменко Елены Борисовны
Изучение строения и свойств глюкозы. Разработка урока учителя химии Ерёменко Елены Борисовны  Каталитический крекинг. Промышленные установки
Каталитический крекинг. Промышленные установки Предельные углеводороды. (9 класс)
Предельные углеводороды. (9 класс) Соединения щелочноземельных металлов
Соединения щелочноземельных металлов Основные особенности композитов по сравнению с традиционными материалами
Основные особенности композитов по сравнению с традиционными материалами Общая характеристика неметаллов
Общая характеристика неметаллов Эпоксидті полимер материалдарының қасиеттерін зерттеу
Эпоксидті полимер материалдарының қасиеттерін зерттеу Роль хімії в сучасному житті
Роль хімії в сучасному житті Пищевые добавки
Пищевые добавки Презентация по Химии "Органическая химия" - скачать смотреть бесплатно
Презентация по Химии "Органическая химия" - скачать смотреть бесплатно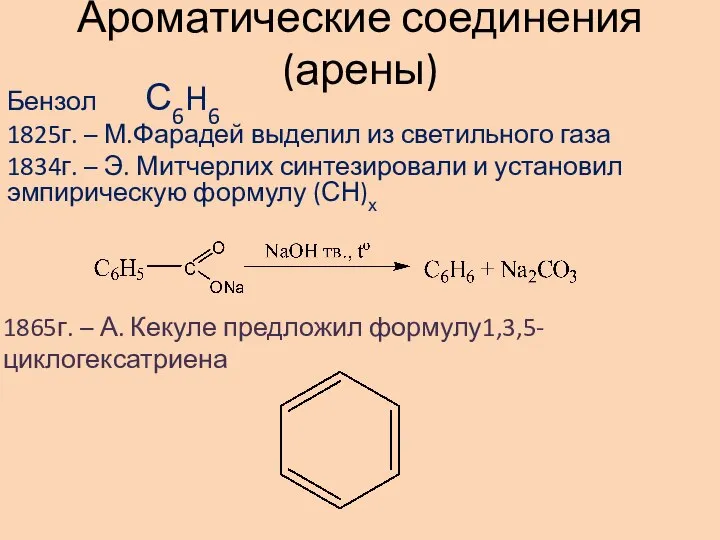 Ароматические соединения (арены)
Ароматические соединения (арены) Нафтены
Нафтены Органическая химия
Органическая химия Teoria hibridizării orbitalilor atomici
Teoria hibridizării orbitalilor atomici Машиностроительные материалы
Машиностроительные материалы Қанықпаған көмірсутектердің реакцияға түсу қабілеттілігі
Қанықпаған көмірсутектердің реакцияға түсу қабілеттілігі Вклад М.В. Ломоносова в развитие науки химия
Вклад М.В. Ломоносова в развитие науки химия Химическое образование в современной средней (полной) общеобразовательной школе
Химическое образование в современной средней (полной) общеобразовательной школе Общие представления о строении и реакционной способности органических соединений
Общие представления о строении и реакционной способности органических соединений Количество вещества. Единица измерения вещества моль
Количество вещества. Единица измерения вещества моль Силикатная промышленность
Силикатная промышленность Уравнение состояния идеального газа
Уравнение состояния идеального газа