Периодический закон и периодическая система химических элементов д.и.менделеева в свете учения о строении атома
Содержание
- 2. ОСНОВНЫЕ СВЕДЕНИЯ О СТРОЕНИИ АТОМА В результате химических реакций атомы не разрушаются, а лишь перегруппировываются: из
- 4. МОДЕЛЬ СТРОЕНИЯ АТОМА ДЖ. ТОМСОНА В 1904 г. в работе «О структуре атома» Дж.Томсон дал описание
- 5. ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА Э. РЕЗЕРФОРДА согласно которой атом состоит из положительно заряженного ядра и электронов, движущихся
- 6. КВАНТОВАЯ МОДЕЛЬ Н. БОРА Первый постулат. Электрон движется вокруг ядра по строго определенным замкнутым стационарным орбитам
- 7. ПРОТОННО-НЕЙТРОННАЯ ТЕОРИЯ ЯДРА В 1932 г. была разработана протонно-нейтронная теория ядра, согласно которой ядра атомов состоят
- 9. Атомное ядро каждого химического элемента характеризуется строго определенным, данным природой числом протонов в нем (порядковым номером
- 10. ЭЛЕКТРОННОЕ СТРОЕНИЕ АТОМА Под электронной оболочкой понимают совокупность всех электронов атома. Важнейшей характеристикой электрона является энергия
- 12. Электрон в атоме не имеет траектории движения, т.е. можно говорить лишь о вероятности нахождения его в
- 13. ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ В атомах химических элементов первый уровень составляет одна s-орбяталь, на которой находятся два s-электрона.
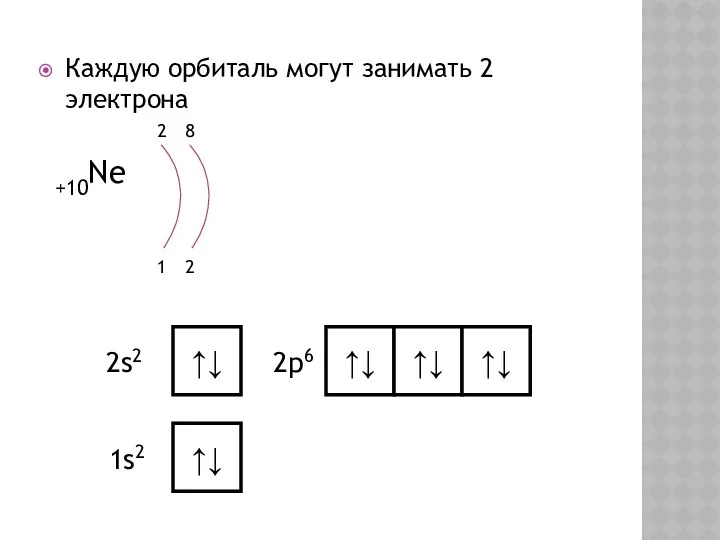
- 14. Каждую орбиталь могут занимать 2 электрона +10Ne 1 2 2 8 ↑↓ ↑↓ ↑↓ ↑↓ ↑↓
- 15. Атомы элементов одного периода Периодической таблицы Д.И.Менделеева отличаются тем, что заряды их ядер возрастают на единицу
- 16. к s-элементам относят элементы главных подгрупп I и II групп Периодической системы химических элементов Д. И.
- 18. ОТКРЫТИЕ ПЕРИОДИЧЕСКОГО ЗАКОНА Д. И. МЕНДЕЛЕЕВЫМ Открытию Периодического закона предшествовало накопление знаний о веществах и их
- 19. В 1862 г. профессор Парижской высшей школы А.Шанкуртуа попробовал расположить химические элементы в порядке возрастания их
- 21. В отличие от работ предшественников предложенная русским химиком Д. И. Менделеевым Периодическая таблица химических элементов имела
- 23. В основу своей работы по классификации химических элементов Д. И. Менделеев положил два их основных и
- 24. На основании своих наблюдений 1 марта 1869 г. Д. И. Менделеев сформулировал Периодический закон: Свойства простых
- 25. ВЫВОДЫ В результате мы пришли к нескольким важным выводам. Свойства химических элементов находятся в периодической зависимости
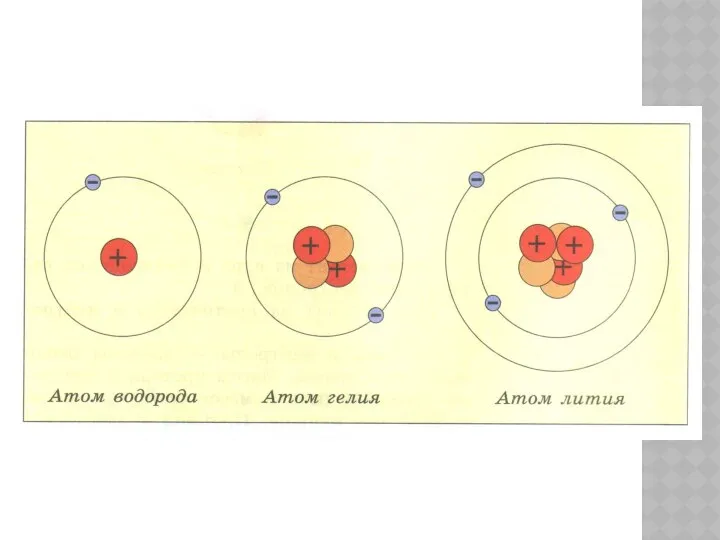
- 26. По горизонтали таблица Менделеева делится на семь периодов: период I включает два элемента: водород Н и
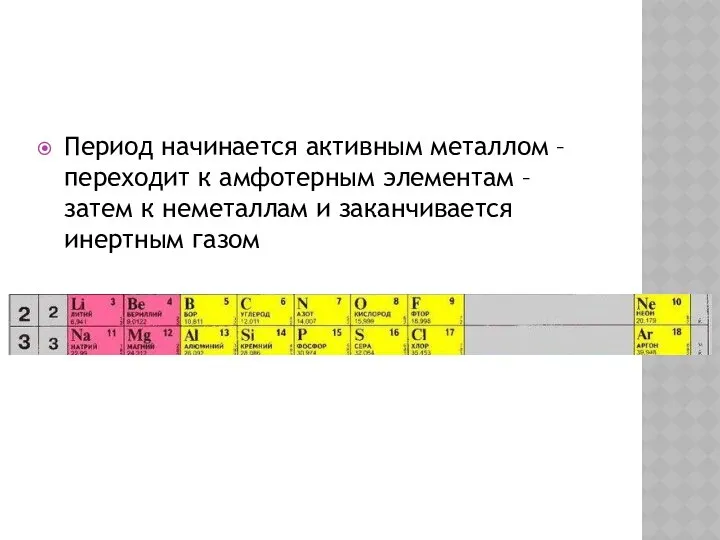
- 27. Период начинается активным металлом – переходит к амфотерным элементам – затем к неметаллам и заканчивается инертным
- 28. По вертикали химические элементы распределены по восьми группам. Каждая группа состоит из двух подгрупп — главной
- 30. Скачать презентацию
























 Спирты: классификация, изомерия, номенклатура
Спирты: классификация, изомерия, номенклатура Стратегії дослідження хімічних сполук з використанням сучасних фізичних методів (частина перша)
Стратегії дослідження хімічних сполук з використанням сучасних фізичних методів (частина перша) Свойства идеального газа на примере воздуха
Свойства идеального газа на примере воздуха Урок – КВН «Подгруппа углерода и азота»
Урок – КВН «Подгруппа углерода и азота»  Ақуыздардың құрылысы мен қызыметі
Ақуыздардың құрылысы мен қызыметі Изотопы, их свойства и применение
Изотопы, их свойства и применение Выполнил: Выполнил: учитель химии первой квалификационной категории Сафиканов Ахат Файзрахманович
Выполнил: Выполнил: учитель химии первой квалификационной категории Сафиканов Ахат Файзрахманович  Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований
Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований Количество вещества (8 класс)
Количество вещества (8 класс) Презентация по Химии "Химическая посуда" - скачать смотреть бесплатно
Презентация по Химии "Химическая посуда" - скачать смотреть бесплатно Обмен аминокислот и белков
Обмен аминокислот и белков Карбид кремния
Карбид кремния Кристаллы. Формирование кристаллов
Кристаллы. Формирование кристаллов Алканы. Хлороформ
Алканы. Хлороформ Йододефицит. Выполнила Кириллова Анастасия.
Йододефицит. Выполнила Кириллова Анастасия.  Кислородсодержащие органические вещества. Фенолы
Кислородсодержащие органические вещества. Фенолы Совместимость электродных материалов в новой электрохимической системе Li4Ti5O12/Li3V2(PO4)3 с традиционным электролитом для
Совместимость электродных материалов в новой электрохимической системе Li4Ti5O12/Li3V2(PO4)3 с традиционным электролитом для Группа веществ, изолируемых экстракцией органическими растворителями (пестициды или ядохимикаты)
Группа веществ, изолируемых экстракцией органическими растворителями (пестициды или ядохимикаты) Презентация Неорганические полимеры
Презентация Неорганические полимеры  Щелочно-земельные металлы
Щелочно-земельные металлы Количество вещества
Количество вещества Аминокислоты алифатического ряда и их производные
Аминокислоты алифатического ряда и их производные Взаимодействие солей аммония со щелочами
Взаимодействие солей аммония со щелочами Презентация по Химии "Определение рода вещества (жидкости) по его плотности" - скачать смотреть
Презентация по Химии "Определение рода вещества (жидкости) по его плотности" - скачать смотреть  Значение органической химии в жизни людей
Значение органической химии в жизни людей Тела. Вещества. Частицы. Разнообразие веществ
Тела. Вещества. Частицы. Разнообразие веществ Chem-квест. Химический диктант
Chem-квест. Химический диктант Acid-base equilibrium in biological systems
Acid-base equilibrium in biological systems