Содержание
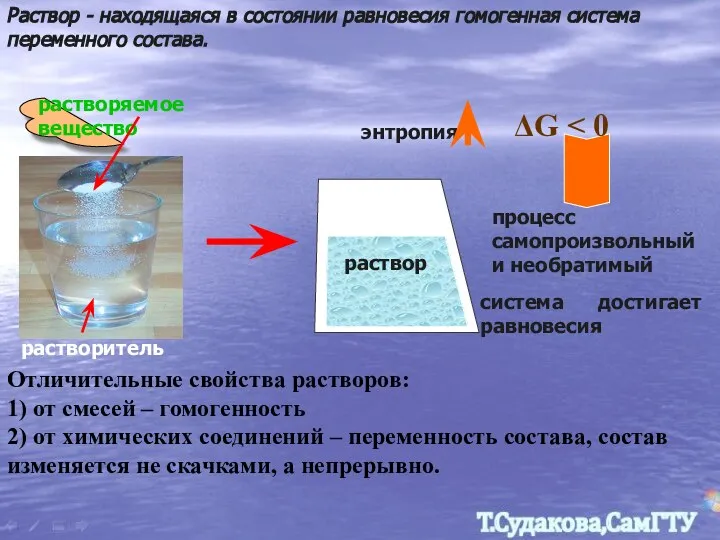
- 2. Раствор - находящаяся в состоянии равновесия гомогенная система переменного состава. растворитель растворяемое вещество раствор энтропия система
- 3. водка Раствор спирта в воде, т.к. содержание спирта 40% раствор воды в спирте, т.к. содержание спирта
- 4. Жидкие: жидкость – газ (СО2 в воде, HCl, NH3 в воде) жидкость – жидкость (спирт С2Н5ОН
- 5. РАСТВОРЫ: - концентрированные – содержание растворенного вещества свыше 5% массовых; - разбавленные – содержание до 5%.
- 6. РАСТВОРИМОСТЬ - способность растворяться! коэффициент растворимости – масса вещества, при растворении которой в 100 г растворителя
- 7. Кристаллы KCl в его пересыщенном водном растворе
- 8. эмпирическое правило растворения: Подобное растворяется в подобном: полярное – в полярном, неполярное – в неполярном. йод
- 9. Концентрация вещества в растворе – количество растворенного вещества в определенной массе или объеме раствора или растворителя.
- 10. При растворении происходят процессы: 1. смачивание 2. разрушение кристаллической решетки твердого вещества 3. сольватация (гидратация, если
- 11. В водных растворах гидратация - 1 стадия диссоциации и главная ее причина!!! 2 стадия – поляризация
- 12. СИЛЬНЫЕ ЭЛЕКТРОЛИТЫ: хорошо диссоциируют на ионы, α>30% почти все соли; кислоты (H2SO4, HCl, HBr, HI, HNO3),
- 13. Степень диссоциации зависит: - Природа электролита; - природа растворителя: чем ↑ε растворителя, тем ↑α; - концентрация
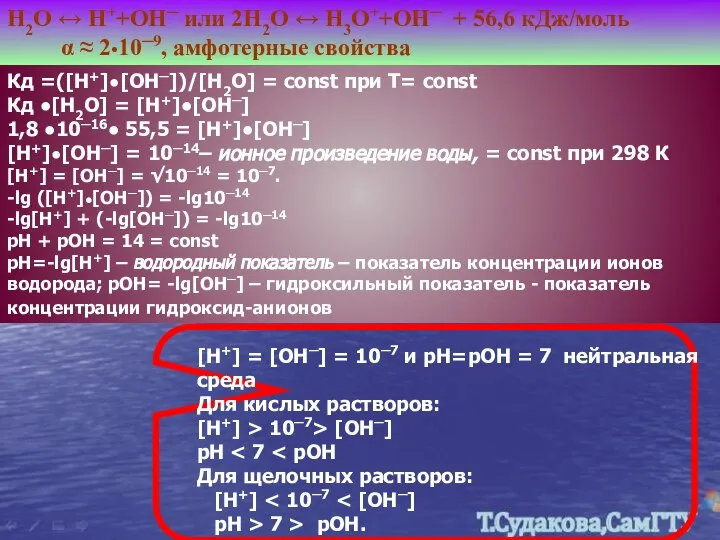
- 14. Н2О ↔ Н++ОН─ или 2Н2О ↔ Н3О++ОН─ + 56,6 кДж/моль α ≈ 2•10─9, амфотерные свойства Кд
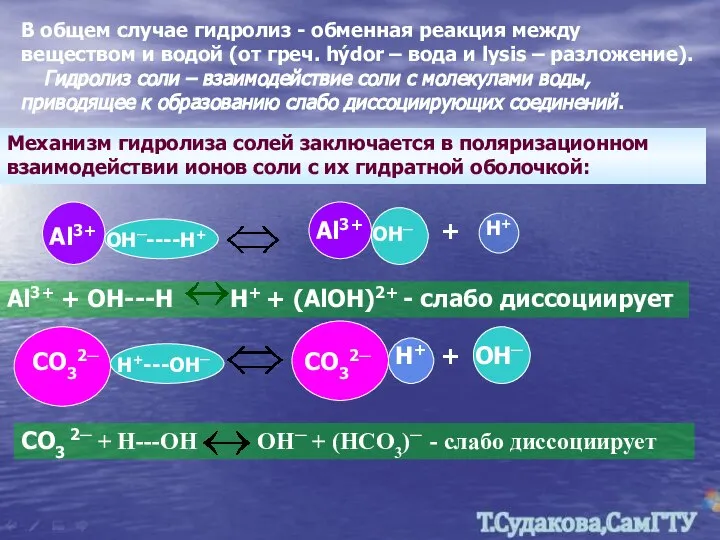
- 15. В общем случае гидролиз - обменная реакция между веществом и водой (от греч. hýdor – вода
- 16. Сильным поляризующим действием обладают: катионы d-элементов (Al3+, Zn2+, Cr3+, Cu2+, Ag+, Au3+ и др.), анионы слабых
- 17. ТИПЫ ГИДРОЛИЗА: 1) Гидролиз по катиону – гидролиз солей, образованных слабым основанием и сильной кислотой: NH4Cl
- 18. 3) Полный гидролиз – гидролиз солей, образованных слабой кислотой и слабым основанием: NH4CN + HOH ↔
- 19. Равновесие между осадком малорастворимого сильного электролита и насыщенным раствором: Произведение растворимости: AgCl ↔ Ag+ + Cl─
- 20. ПР (CaCO3) = 4,8 • 10─9 Пример: [Ca2+] [CO32─] > ПР [Ca2+] [CO32─] > 4,8•10─9 Выпадает
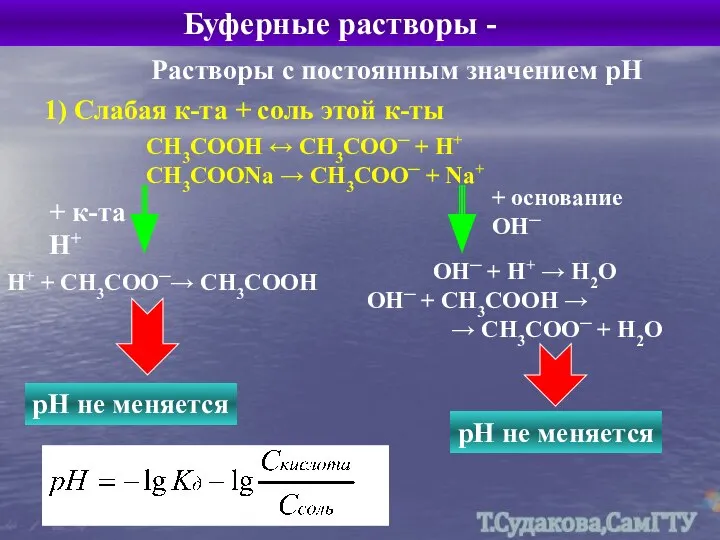
- 21. Буферные растворы - Растворы с постоянным значением рН 1) Слабая к-та + соль этой к-ты СН3СООН
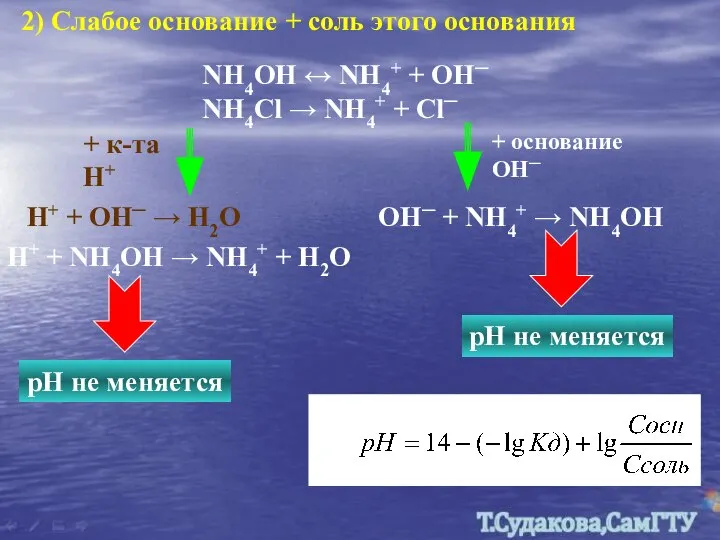
- 22. 2) Слабое основание + соль этого основания NH4OH ↔ NH4+ + OH─ NH4Cl → NH4+ +
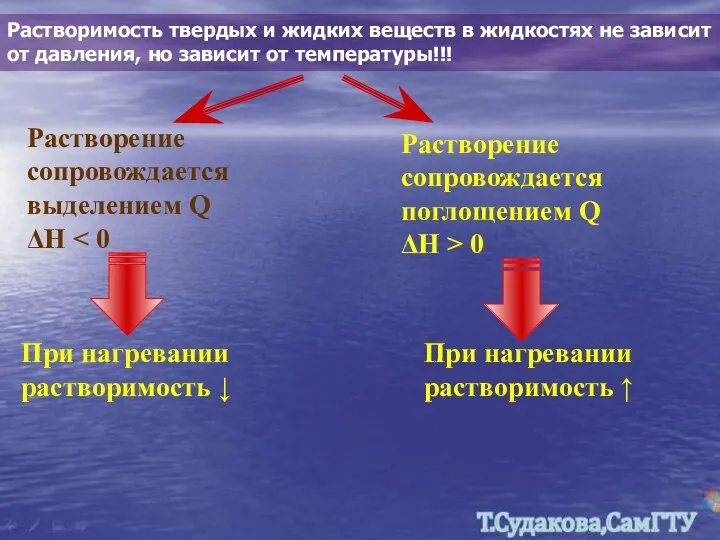
- 23. Растворимость твердых и жидких веществ в жидкостях не зависит от давления, но зависит от температуры!!! Растворение
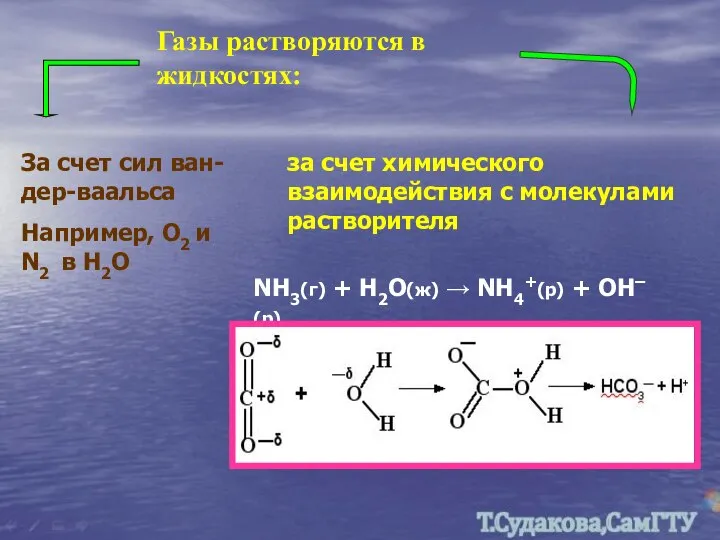
- 24. Газы растворяются в жидкостях: За счет сил ван-дер-ваальса Например, О2 и N2 в Н2О за счет
- 25. Растворимость газов в жидкостях зависит от давления!!! закон Генри: С (Х) = Кг (Х)• р (Х)
- 26. независящие от природы растворенного вещества, а только от количества растворенных частиц – коллигативные свойства. Основная причина
- 27. Осмотическое давление – мера стремления растворителя к переходу через полупроницаемую перегородку в данный раствор. Оно численно
- 28. Чем больше число молекул или ионов в растворе, тем больше осмотическое давление раствора!!! Для растворов не
- 29. Куриные яйца после эксперимента по осмосу
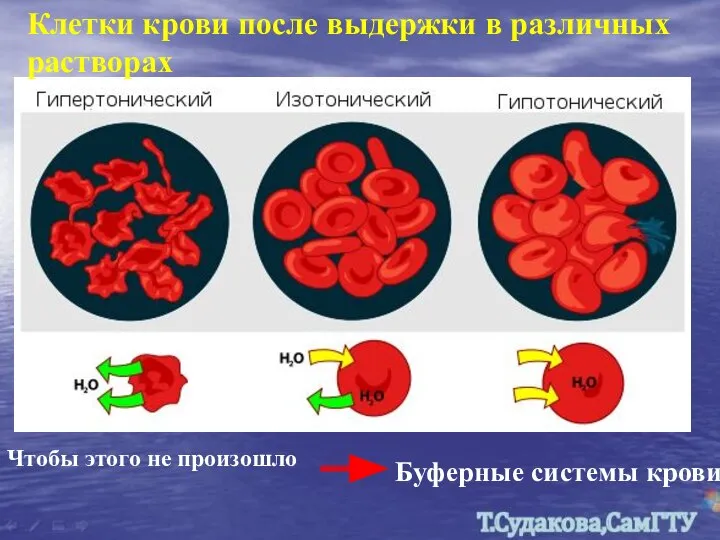
- 30. Клетки крови после выдержки в различных растворах Чтобы этого не произошло Буферные системы крови
- 31. Понижение давления пара растворителя над раствором - закон Рауля: Δp/p0 = nв/(nв + n0) Δp –
- 32. Температура замерзания растворов ниже, чем температура замерзания чистого растворителя; понижение температуры ΔТз = Ккр• Сm Сm
- 34. Скачать презентацию















![ПР (CaCO3) = 4,8 • 10─9 Пример: [Ca2+] [CO32─] > ПР](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396062/slide-19.jpg)







 Мыло
Мыло  Крохмаль і целюлоза
Крохмаль і целюлоза  Введение в предмет. Классификация композитов
Введение в предмет. Классификация композитов Кремний және оның қосылыстары
Кремний және оның қосылыстары Нуклеиновые кислоты
Нуклеиновые кислоты Презентация Электролиз
Презентация Электролиз Биоэнергетика. Энергетическое сопряжение
Биоэнергетика. Энергетическое сопряжение Углерод Carboneum происходит от лат. carbo — уголь.
Углерод Carboneum происходит от лат. carbo — уголь. Полимеры, пластмассы и товары на их основе
Полимеры, пластмассы и товары на их основе Получение силикагеля, модифицированного бензоксазолами
Получение силикагеля, модифицированного бензоксазолами Химия вокруг нас
Химия вокруг нас Презентация по Химии "Нафта і нафтопродукти" - скачать смотреть бесплатно
Презентация по Химии "Нафта і нафтопродукти" - скачать смотреть бесплатно Презентация по Химии "Окрашивание пластмасс" - скачать смотреть
Презентация по Химии "Окрашивание пластмасс" - скачать смотреть  Химический элемент сера
Химический элемент сера Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные
Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ
Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ Сказка о Круговороте Азота
Сказка о Круговороте Азота Исследование влияния изменения технических параметров на производительность установки замедленного коксования
Исследование влияния изменения технических параметров на производительность установки замедленного коксования Характеристика переходного металла на основании его положения в Периодической системе. Амфотерность
Характеристика переходного металла на основании его положения в Периодической системе. Амфотерность Повышение огнестойкости деревянных конструкций методом поверхностной и объёмной пропитки
Повышение огнестойкости деревянных конструкций методом поверхностной и объёмной пропитки Полимеры. Основные понятия
Полимеры. Основные понятия Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В.
Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В. Топливо и топливосжигающие устройства. Горение топлива
Топливо и топливосжигающие устройства. Горение топлива Минералы группы кварца. Скрытокристаллические формы
Минералы группы кварца. Скрытокристаллические формы Метан и его свойства
Метан и его свойства  Відкриття радіоактивності. У 1896 р. французький учений Антуан Анрі Беккерель (1852-1908) відкрив радіоактивність солей Урану – явище са
Відкриття радіоактивності. У 1896 р. французький учений Антуан Анрі Беккерель (1852-1908) відкрив радіоактивність солей Урану – явище са Фазовые равновесия. Физическая и коллоидная химия
Фазовые равновесия. Физическая и коллоидная химия Вольфрам W
Вольфрам W