Содержание
- 2. Фаза и ее отличие от агрегатного состояния Правило фаз Гиббса Фазовые диаграммы однокомпонентных систем Фазовые равновесия
- 3. Гомогенная система – ТД система, внутри которой нет поверхностей раздела, отделяющих друг от друга части системы,
- 4. Твердое вещество характеризуется способностью сохранять объём и форму Жидкость характеризуется способностью сохранять объём. Жидкость принимает форму
- 5. Фаза - гомогенная часть гетерогенной системы Компонент – вещество, которое может быть выделено из системы и
- 6. С=К-Ф+N – в общем случае С=К-Ф+2 – для систем, на которые влияют Т, Р Число степеней
- 7. - графическое отображение равновесного состояния бесконечной физико-химической системы Обычными координатами для построения фазовой диаграммы являются термодинамические
- 8. На фазовых диаграммах однокомпонентных систем поля, по правилу фаз, соответствуют однофазным состояниям, линии, разграничивающие их —
- 9. Физические явления, происходящие без протекания химических реакций: Плавление и кристаллизация (твердое вещество ↔ жидкость) Кипение (испарение)
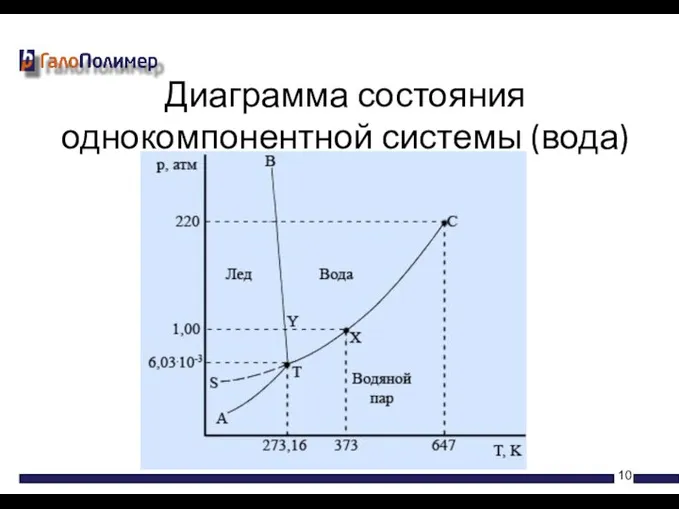
- 10. Диаграмма состояния однокомпонентной системы (вода)
- 11. Диаграммы состояния однокомпонентных систем (углерод, сера)
- 12. Классификация растворов Виды концентрации растворов Закон Рауля и следствия из него. Коллигативные свойства растворов Термодинамика жидких
- 13. Раствор – однофазная (гомогенная) система, состоящая из двух и более веществ Растворитель – компонент раствора, находящийся
- 14. Истинный раствор – однофазная (гомогенная) система, состоящая из двух и более веществ. Например, раствор хлористого водорода
- 15. Концентрированный раствор имеет большое содержание растворенного вещества Разбавленный раствор содержит растворенное вещество в низкой концентрации Насыщенный
- 16. Массовая доля, ω равна отношению массы растворенного вещества к массе раствора. Измеряется в долях единицы (от
- 17. Объемная доля, ϕ равна отношению объема растворенного вещества к объему раствора. Измеряется в долях единицы (от
- 18. Молярная концентрация CM равна отношению количества растворенного вещества к объему раствора. Измеряется в моль/дм3 (моль/л), М.
- 19. Молярная концентрация эквивалента CН (старое название - нормальная концентрация) равна отношению количества эквивалентов растворенного вещества к
- 20. Моляльная концентрация Cm равна отношению количества растворенного вещества к массе раствора. Измеряется в моль/кг Cm =
- 21. Титр по растворённому веществу (просто титр) равен отношению массы растворённого вещества (титранта) к объему раствора. Измеряется
- 22. С какими растворами Вы сталкиваетесь в ходе работы на предприятии ООО «ГалоПолимер Кирово-Чепецк»? Для получения хлора
- 23. Давление пара растворителя над раствором меньше, чем над чистым растворителем P1=P10*X1 Относительное понижение давления пара растворителя
- 24. Понижение температуры замерзания раствора по сравнению с чистым растворителем, ΔТзам=Ккр*Cm Повышение температуры кипения раствора по сравнению
- 25. Следствия из закона Рауля (коллигативные свойства растворов)
- 26. Растворитель и растворенное вещество –летучие жидкости Разделение перегонкой (простой, фракционной, ректификацией) за счет различия Ткип Кипение
- 27. Метан CH4, Ткип= -161,5 °С Хлор Сl2, Ткип= -34,06 °С Хлористый метил CH3Cl, Ткип= -24,2 °С
- 28. Жидкости закипают тогда, когда давление пара над ними становится равным атмосферному давлению. Чистые жидкости кипят при
- 29. Равновесие жидкость-пар
- 30. Экстремумы на диаграмме кипения соответствуют такому равновесию раствора и насыщенного пара, при котором составы обеих фаз
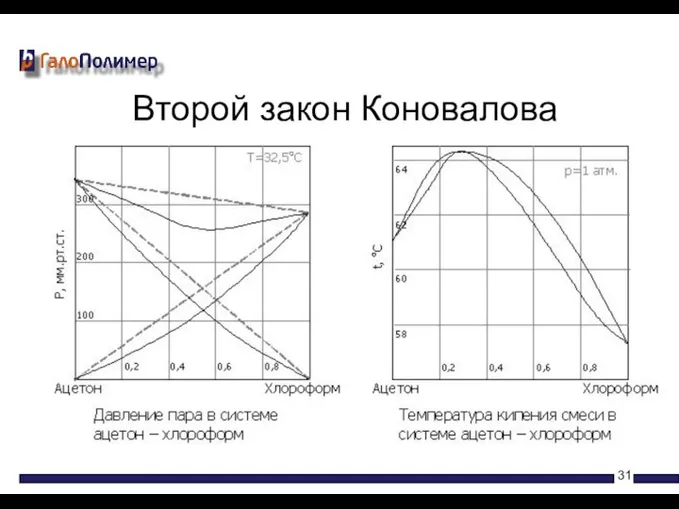
- 31. Второй закон Коновалова
- 32. Азеотропные смеси на основе хлороформа
- 33. – процесс разделения жидких летучих смесей путем испарения жидкости с последующим охлаждением и конденсацией паров. Разделение
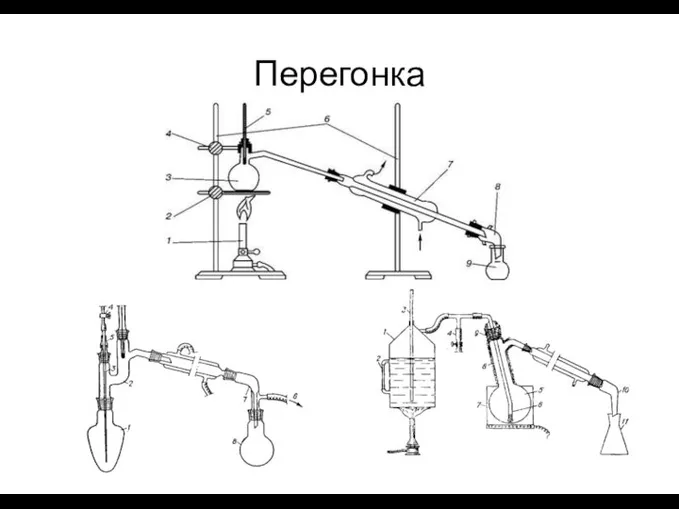
- 34. Перегонка
- 35. – наиболее эффективный вид дистилляции, особенность которого состоит в многократном взаимодействии пара и жидкости за счет
- 36. Ректификация
- 37. Ректификация
- 39. Скачать презентацию

































 Вирощування кристалів в додомашніх умовах
Вирощування кристалів в додомашніх умовах Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине
Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине Определение валентности элементов
Определение валентности элементов V група періодичної системи Менделєєва
V група періодичної системи Менделєєва Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады) Альдегидтер және кетондар
Альдегидтер және кетондар Кристаллические решетки
Кристаллические решетки Получение и установление состава кристаллогидрата фосфата цинка
Получение и установление состава кристаллогидрата фосфата цинка Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Теоретические основы органической химии
Теоретические основы органической химии Железо и его соединения.
Железо и его соединения. Beryllium. The physical properties of beryllium
Beryllium. The physical properties of beryllium Физический процесс и химическая реакция.
Физический процесс и химическая реакция. Общая и неорганическая химия
Общая и неорганическая химия Химические свойства алканов
Химические свойства алканов Расчёт равновесного состава
Расчёт равновесного состава Викторина. Дмитрий Иванович Менделеев
Викторина. Дмитрий Иванович Менделеев Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары
Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары Уран. Получение урана
Уран. Получение урана Значение основных химических элементов в жизни человека
Значение основных химических элементов в жизни человека Сведения о воде
Сведения о воде Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs
Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs Буровые технологические жидкости для бурения и крепления горизонтальных скважин
Буровые технологические жидкости для бурения и крепления горизонтальных скважин Имеет ли вода форму
Имеет ли вода форму Методы хроматографии. Ионообменная хроматография
Методы хроматографии. Ионообменная хроматография Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Кислород. Получение кислорода и его физические свойства
Кислород. Получение кислорода и его физические свойства