Содержание
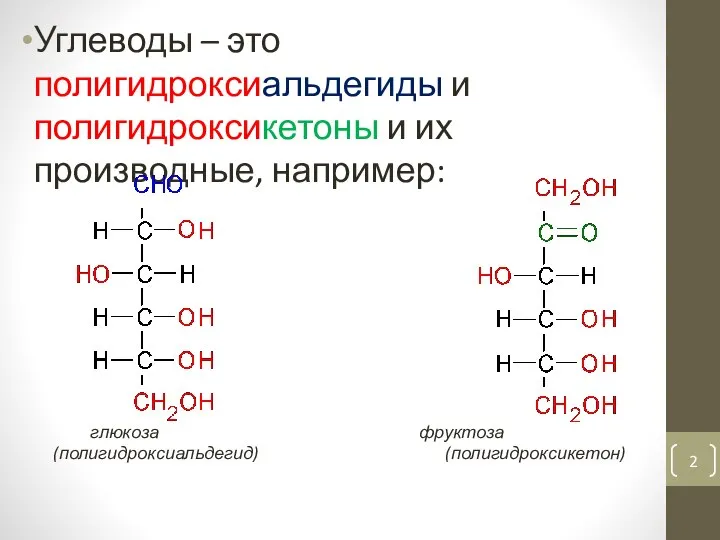
- 2. Углеводы – это полигидроксиальдегиды и полигидроксикетоны и их производные, например: глюкоза фруктоза (полигидроксиальдегид) (полигидроксикетон)
- 3. Общая формула простых моносахаридов может быть представлена как Cn(H2O)m поэтому ранее сахара считали гидратированными формами углерода,
- 4. Биологическая роль углеводов Энергетическая. Пластическая. Резервная. Защитная. Специфическая. Регуляторная.
- 5. Классификация углеводов Моносахариды (простые сахара, например, глюкоза) Олигосахариды (углеводы, содержащие 2-10 остатков моносахаридов, например сахароза). Полисахариды
- 6. 1. Моносахариды Моносахариды – простейшие углеводы, не гидролизующиеся на более простые углеводы (греч. μονος – один)
- 7. тривиальная номенклатура: 1.2. Номенклатура название D-глюкозы по номенклатуре IUPAC : (2R, 3S, 4R, 5R) – 2,3,4,5,6-гексагидроксигексаналь.
- 10. 1.3. Изомерия явление существования химических соединений (изомеров), одинаковых по составу и молекулярной массе, различающихся по строению
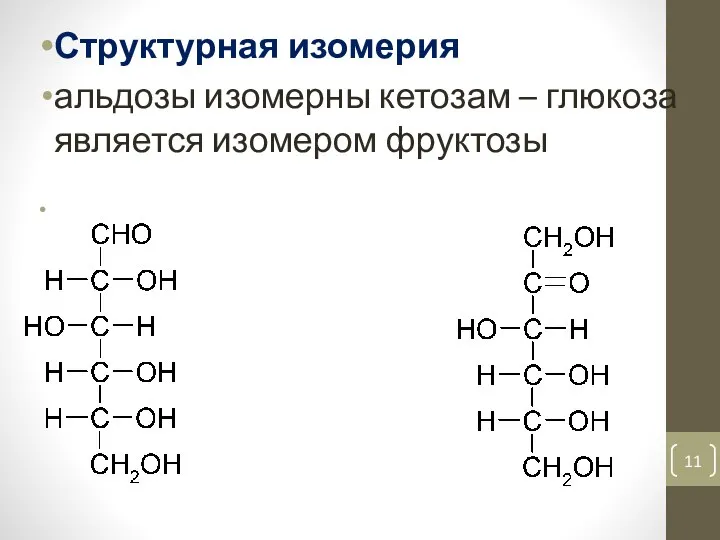
- 11. Структурная изомерия альдозы изомерны кетозам – глюкоза является изомером фруктозы
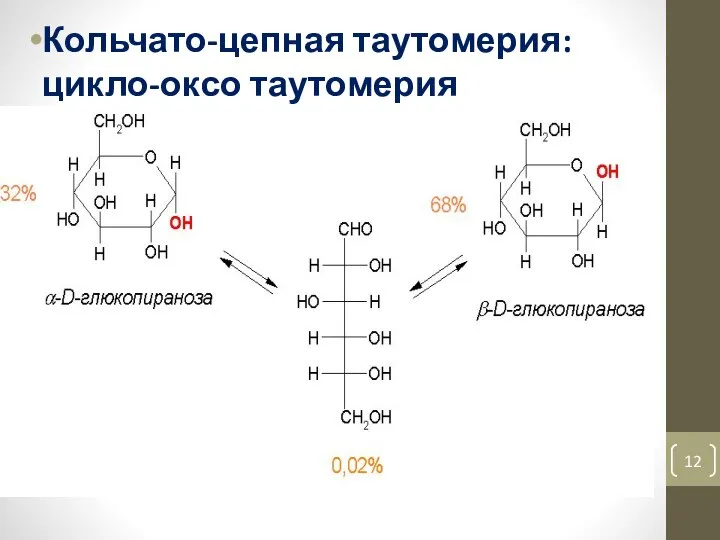
- 12. Кольчато-цепная таутомерия: цикло-оксо таутомерия
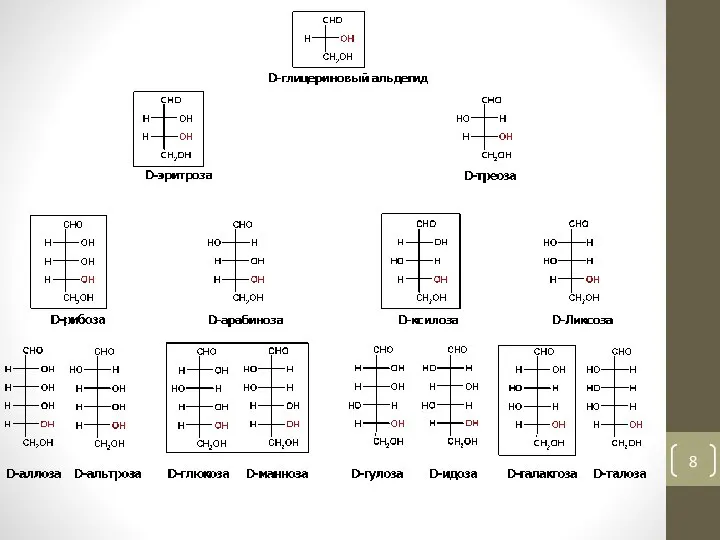
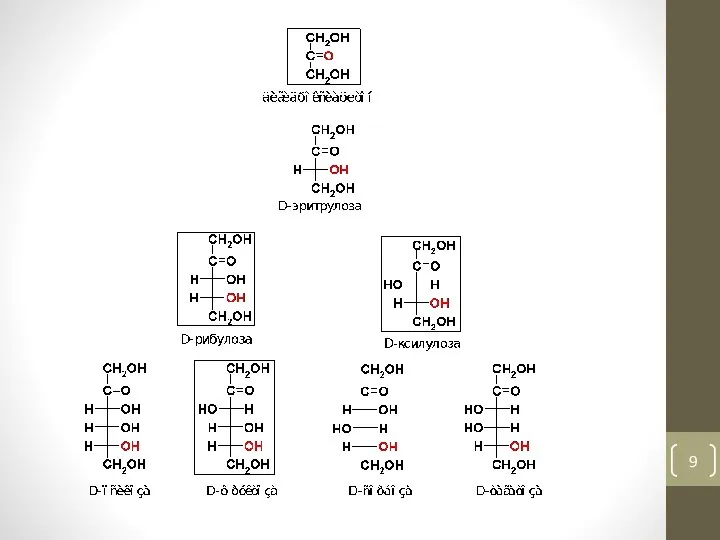
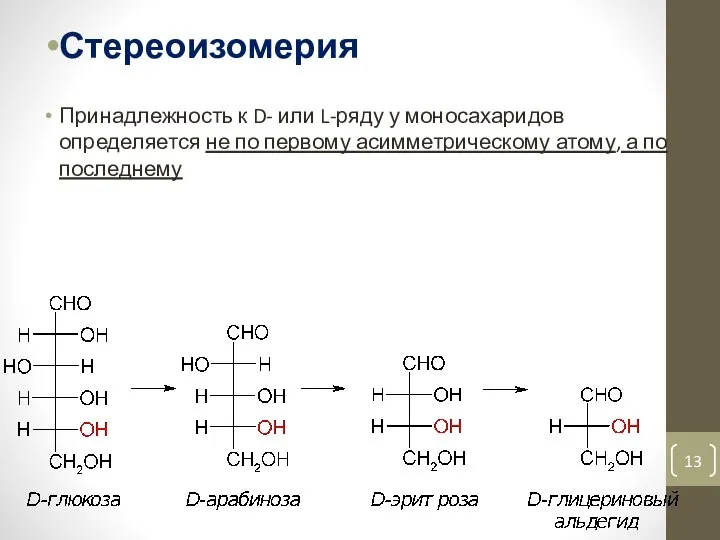
- 13. Стереоизомерия Принадлежность к D- или L-ряду у моносахаридов определяется не по первому асимметрическому атому, а по
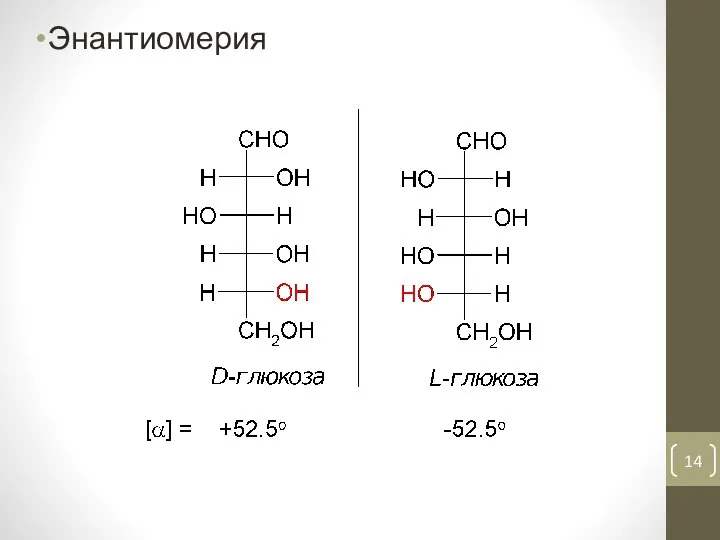
- 14. Энантиомерия
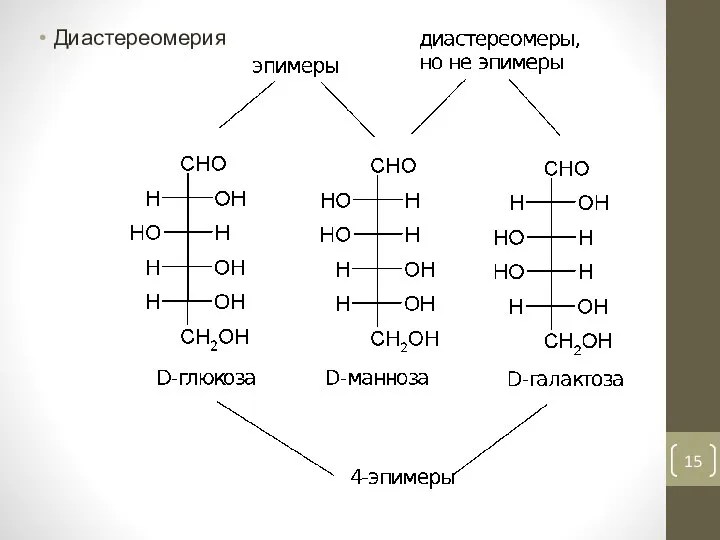
- 15. Диастереомерия
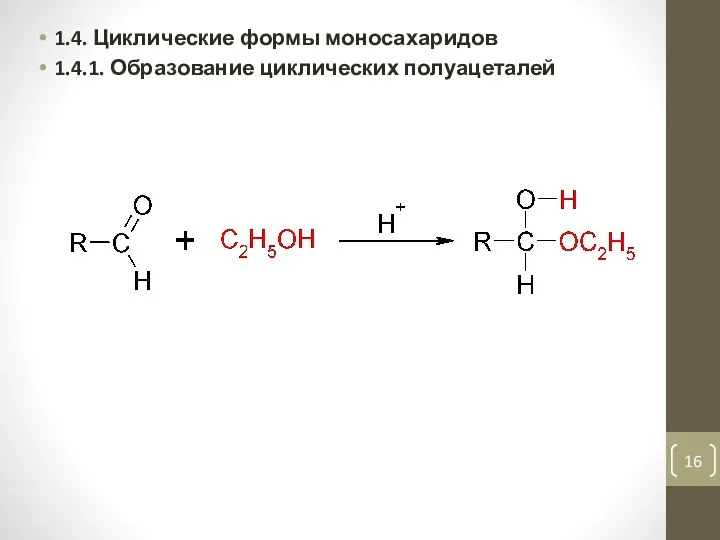
- 16. 1.4. Циклические формы моносахаридов 1.4.1. Образование циклических полуацеталей
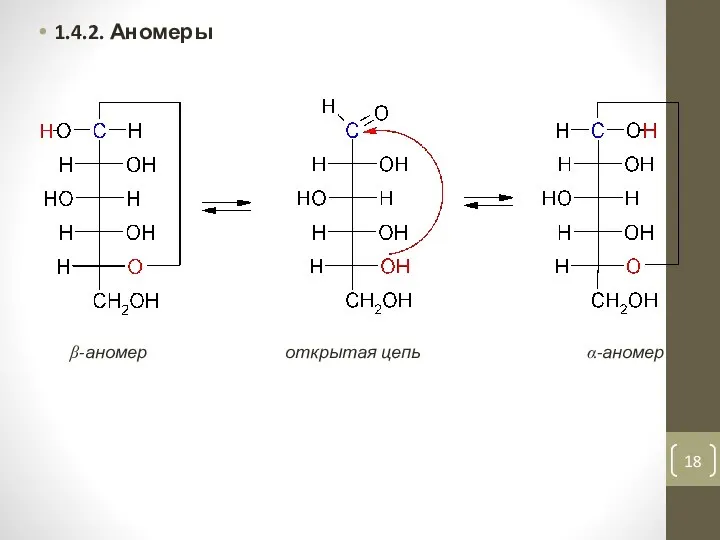
- 18. 1.4.2. Аномеры β-аномер открытая цепь α-аномер
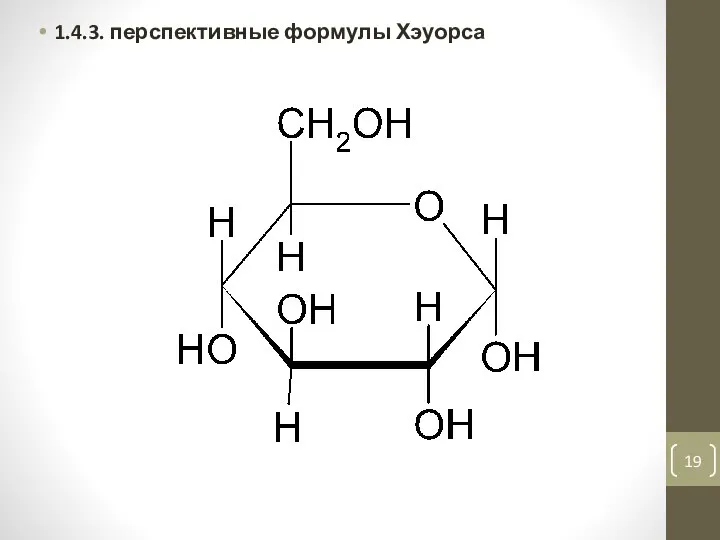
- 19. 1.4.3. перспективные формулы Хэуорса
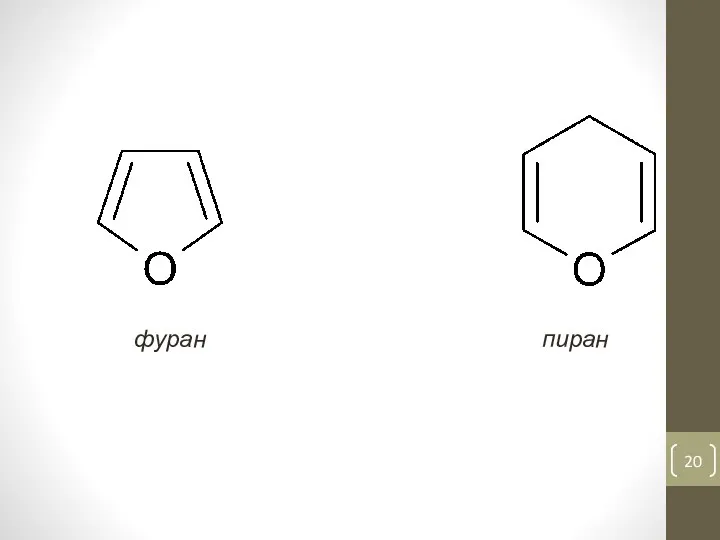
- 20. фуран пиран
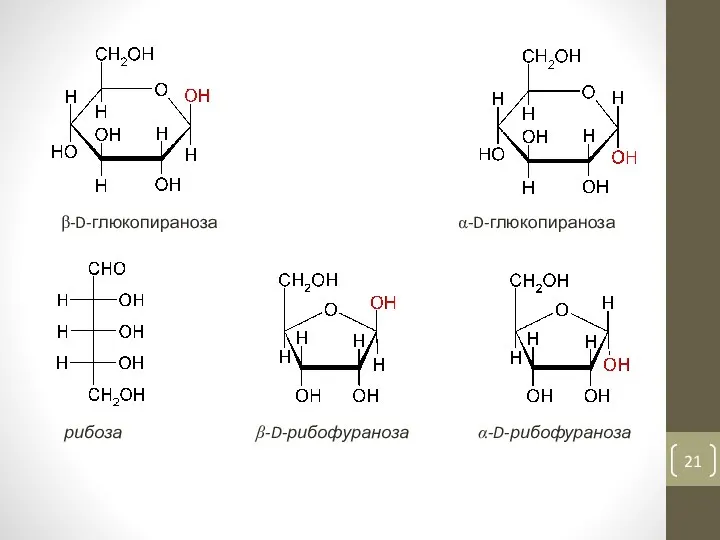
- 21. β-D-глюкопираноза α-D-глюкопираноза рибоза β-D-рибофураноза α-D-рибофураноза
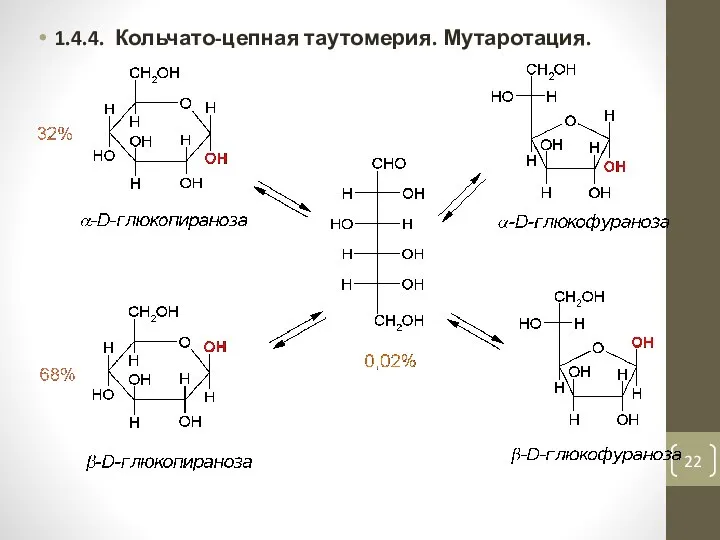
- 22. 1.4.4. Кольчато-цепная таутомерия. Мутаротация.
- 23. Кольчато-цепная таутомерия сопровождается закономерным явлением – мутаротацией. Мутаротация (лат. mutare – изменять, rotatio – вращение) в
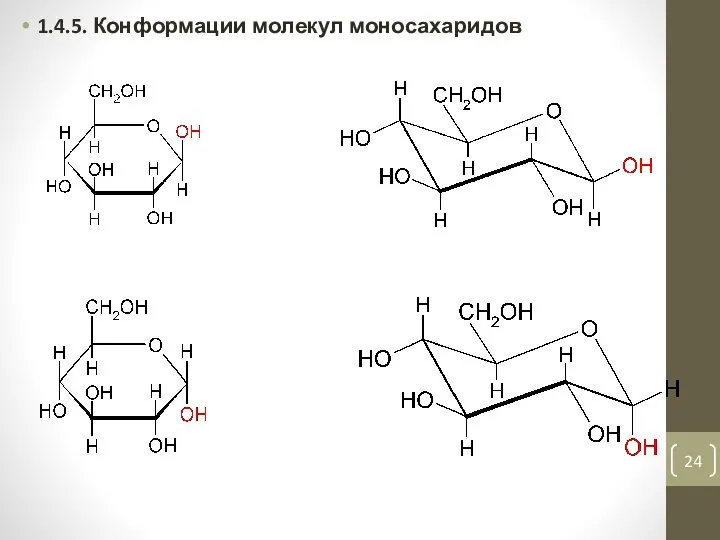
- 24. 1.4.5. Конформации молекул моносахаридов
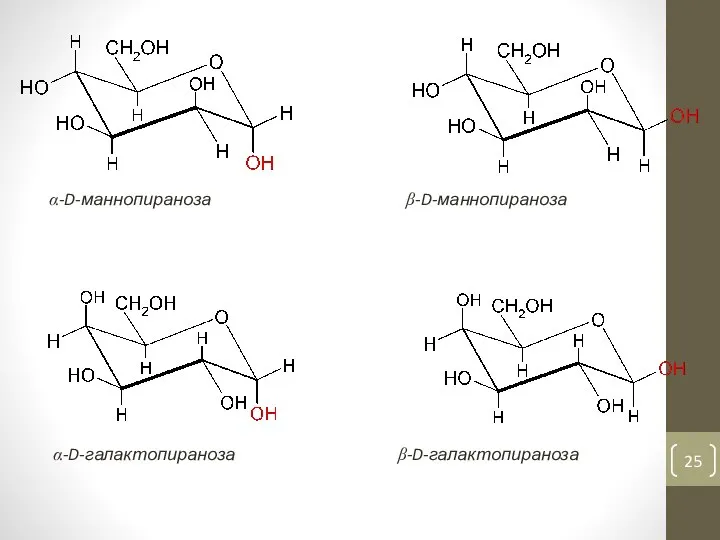
- 25. α-D-маннопираноза β-D-маннопираноза α-D-галактопираноза β-D-галактопираноза
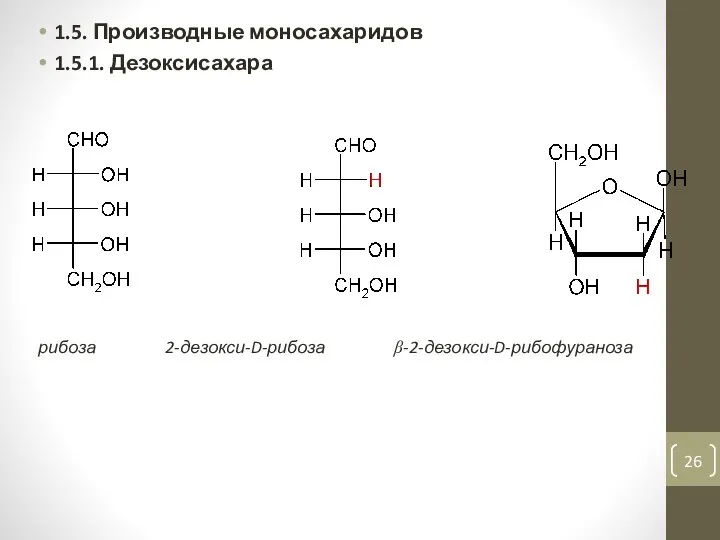
- 26. 1.5. Производные моносахаридов 1.5.1. Дезоксисахара рибоза 2-дезокси-D-рибоза β-2-дезокси-D-рибофураноза
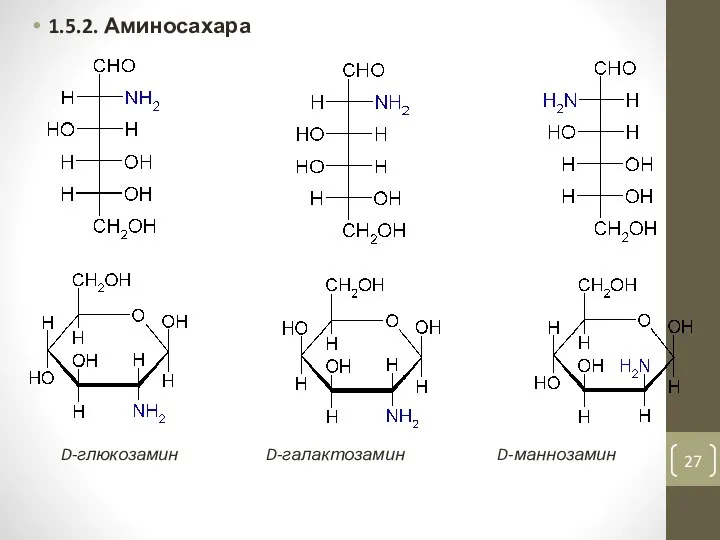
- 27. 1.5.2. Аминосахара D-глюкозамин D-галактозамин D-маннозамин
- 28. 1.6. Физические свойства Моносахариды представляют собой бесцветные кристаллические вещества очень хорошо растворимые в воде. Моносахариды трудно
- 29. 1.7. Биологические свойства и значение 1.7.1 Метаболическое значение и энергетическая функция 1.7.2. Структурная функция 1.7.3. Сладкий
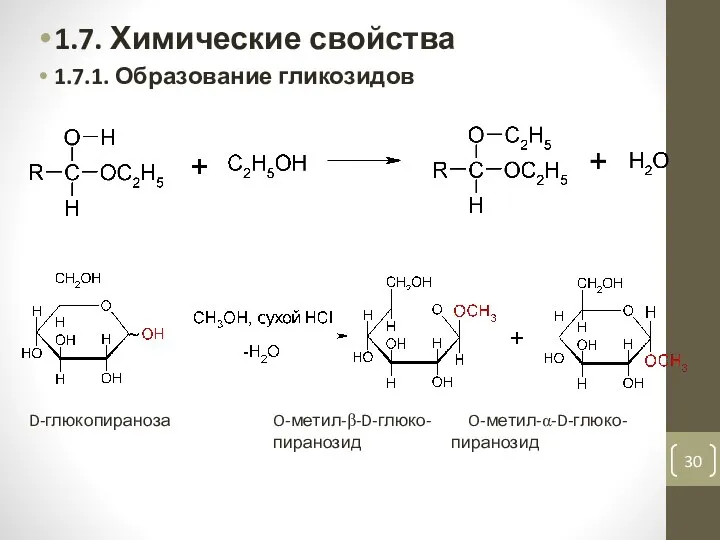
- 30. 1.7. Химические свойства 1.7.1. Образование гликозидов D-глюкопираноза O-метил-β-D-глюко- O-метил-α-D-глюко- пиранозид пиранозид
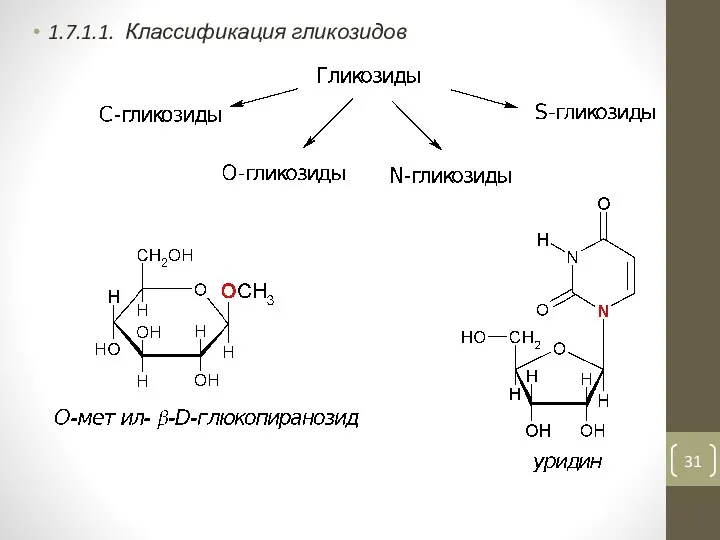
- 31. 1.7.1.1. Классификация гликозидов
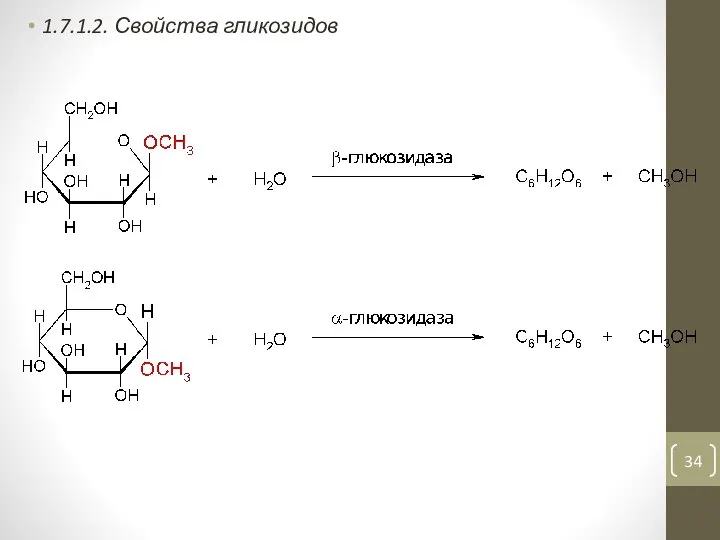
- 34. 1.7.1.2. Свойства гликозидов
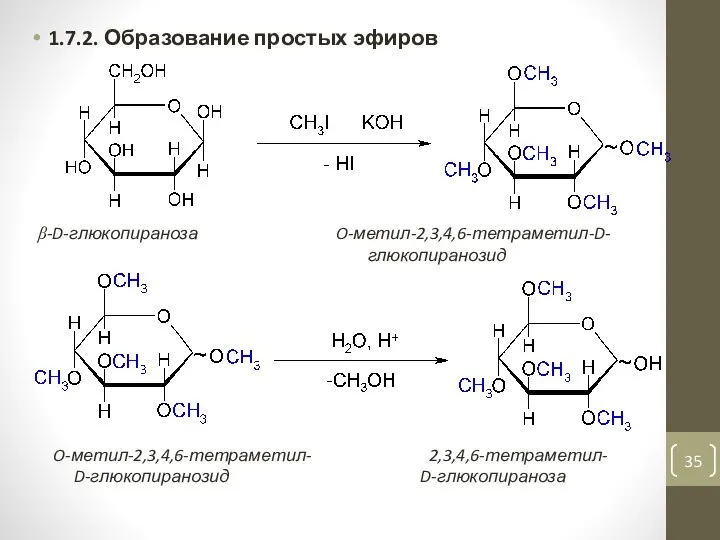
- 35. 1.7.2. Образование простых эфиров β-D-глюкопираноза O-метил-2,3,4,6-тетраметил-D- глюкопиранозид O-метил-2,3,4,6-тетраметил- 2,3,4,6-тетраметил- D-глюкопиранозид D-глюкопираноза
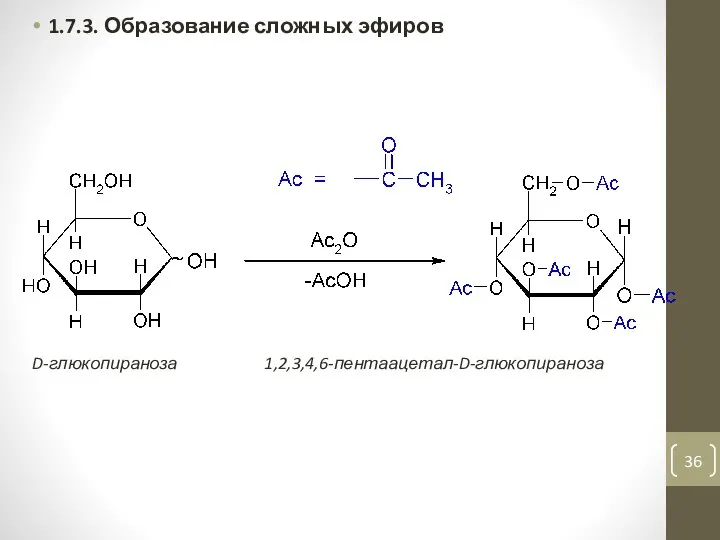
- 36. 1.7.3. Образование сложных эфиров D-глюкопираноза 1,2,3,4,6-пентаацетал-D-глюкопираноза
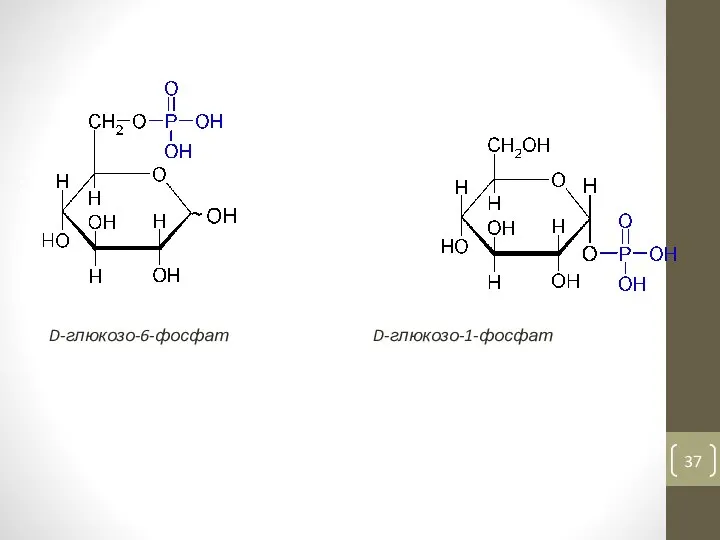
- 37. D-глюкозо-6-фосфат D-глюкозо-1-фосфат
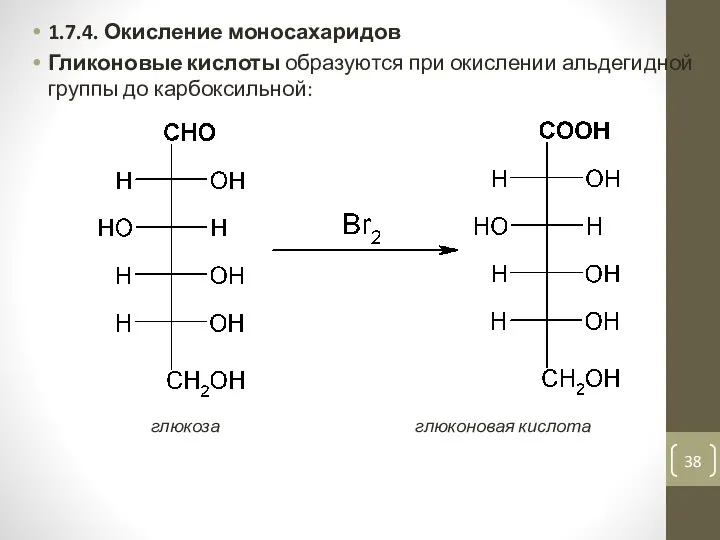
- 38. 1.7.4. Окисление моносахаридов Гликоновые кислоты образуются при окислении альдегидной группы до карбоксильной: глюкоза глюконовая кислота
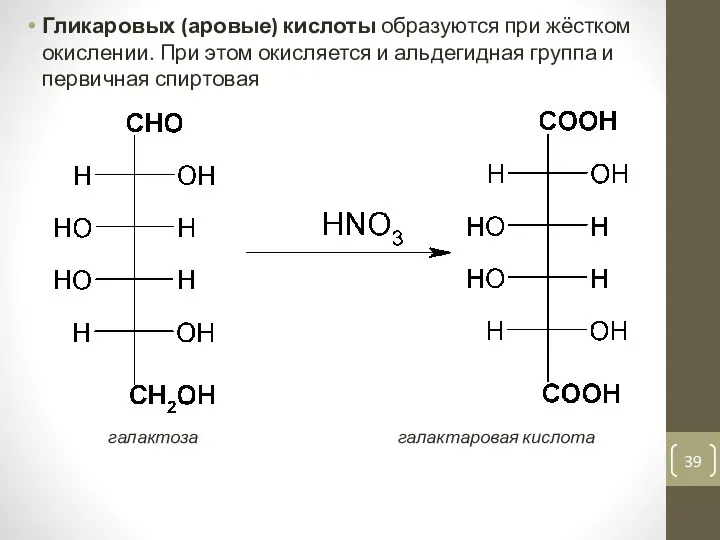
- 39. Гликаровых (аровые) кислоты образуются при жёстком окислении. При этом окисляется и альдегидная группа и первичная спиртовая
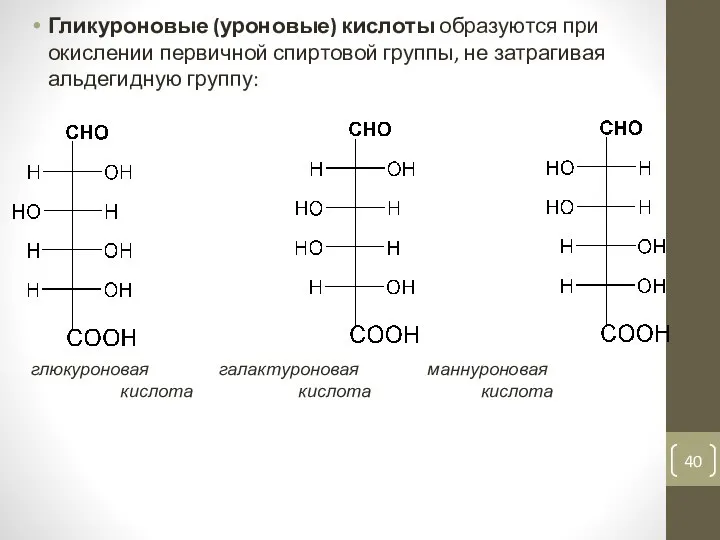
- 40. Гликуроновые (уроновые) кислоты образуются при окислении первичной спиртовой группы, не затрагивая альдегидную группу: глюкуроновая галактуроновая маннуроновая
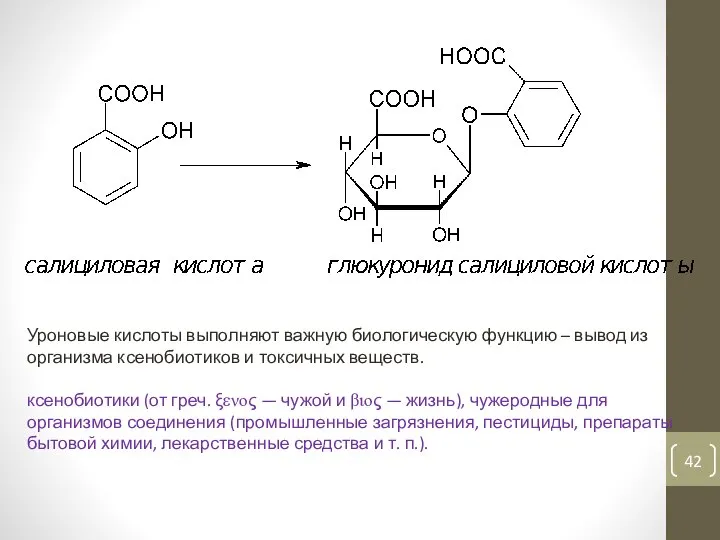
- 42. Уроновые кислоты выполняют важную биологическую функцию – вывод из организма ксенобиотиков и токсичных веществ. ксенобиотики (от
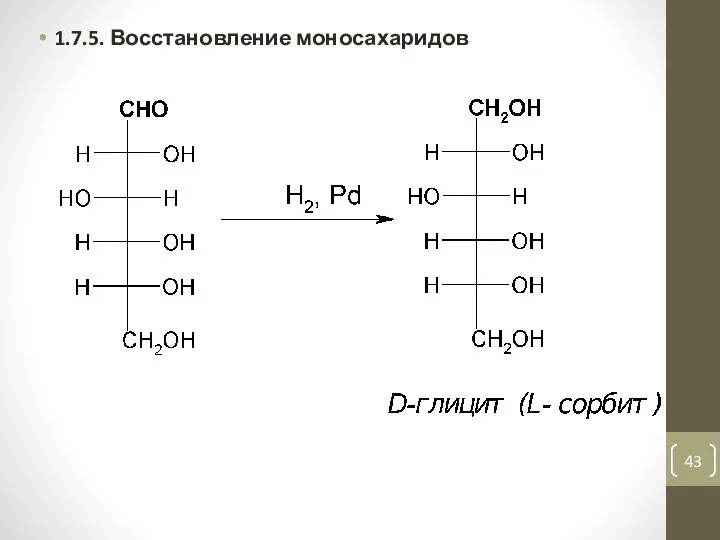
- 43. 1.7.5. Восстановление моносахаридов
- 44. Ксилоза → ксилит (E967) Манноза → маннит Глюкоза → глицит(сорбит) E420 http://www.sorbit.ru/
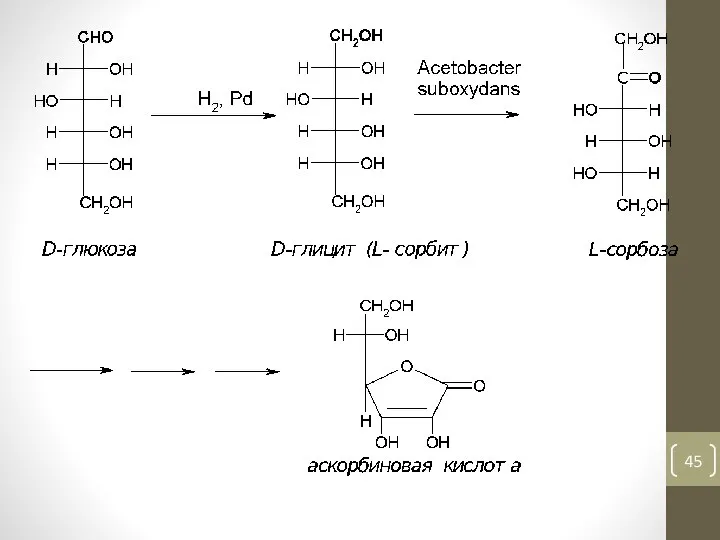
- 46. Аскорбиновая кислота (витамин С), С6Н8О6, водорастворимый витамин. Отсутствие аскорбиновой кислоты в пище человека понижает сопротивляемость к
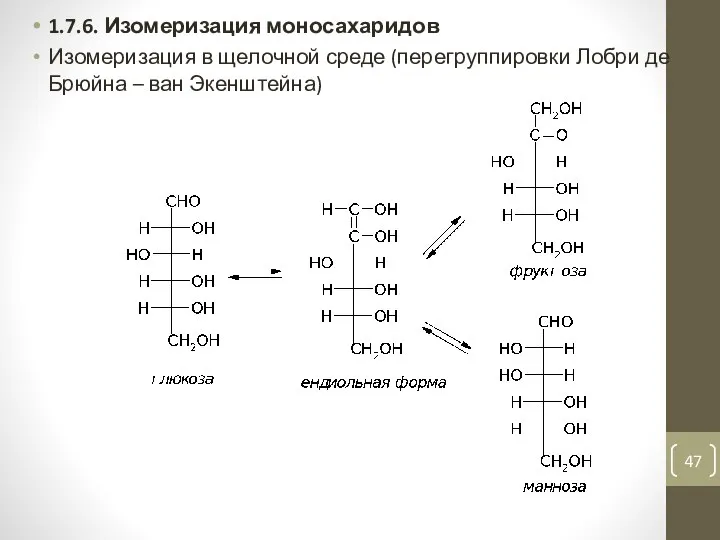
- 47. 1.7.6. Изомеризация моносахаридов Изомеризация в щелочной среде (перегруппировки Лобри де Брюйна – ван Экенштейна)
- 48. 1.8. Получение моносахаридов 1.8.1. Природные источники 6 CO2 + 6 H2O → C6H12O6 + 6 O2
- 49. 1.8.2. Гидролиз дисахаридов, олигосахаридов и полисахаридов Сахароза + H2O → глюкоза + фруктоза Мальтоза + H2O
- 51. Скачать презентацию

















 Повторение основных вопросов курса неорганической химии 8 класса
Повторение основных вопросов курса неорганической химии 8 класса Реакции замещения и реакции обмена
Реакции замещения и реакции обмена Defect in solid
Defect in solid Лекция №4. Строение металлических сплавов
Лекция №4. Строение металлических сплавов Компоненты химического производства
Компоненты химического производства Ванадатты фосфаттар. Орынбасар фосфаттар. Төменгі оксоқышқылдар
Ванадатты фосфаттар. Орынбасар фосфаттар. Төменгі оксоқышқылдар Physical chemistry of surface phenomena. Basics of adsorptive therapy
Physical chemistry of surface phenomena. Basics of adsorptive therapy Лекарственные растения, содержащие простые фенолы, лигнаны и кумарины
Лекарственные растения, содержащие простые фенолы, лигнаны и кумарины Будова електронних оболонок і властивості хіиічних елементів. (8 клас)
Будова електронних оболонок і властивості хіиічних елементів. (8 клас) Periodic Table: It’s Elementary
Periodic Table: It’s Elementary Яковлева Татьяна Алексеевна Ярославль, 2009 г.
Яковлева Татьяна Алексеевна Ярославль, 2009 г.  Растворение сплавов. Коррозия
Растворение сплавов. Коррозия Protecting-Group-Free Enantioselective Synthesis of (-)-Pallavicinin and (+)-Neopallavicinin
Protecting-Group-Free Enantioselective Synthesis of (-)-Pallavicinin and (+)-Neopallavicinin Radical Approach to the Chiral Quaternary Center in Asperaculin A: Synthesis of 9‑Deoxyasperaculin A
Radical Approach to the Chiral Quaternary Center in Asperaculin A: Synthesis of 9‑Deoxyasperaculin A Презентация по Химии "Азот. Подгруппа азота" - скачать смотреть
Презентация по Химии "Азот. Подгруппа азота" - скачать смотреть  Оксид серы (VI). Серная кислота
Оксид серы (VI). Серная кислота Технология поликристаллического кремния. Его применение
Технология поликристаллического кремния. Его применение Введение в химию. 8 класс
Введение в химию. 8 класс Галогены. Галогеноводородные кислоты и их соли
Галогены. Галогеноводородные кислоты и их соли Переробка горючих сланців підготував учень 11-В класу Котенко Роман
Переробка горючих сланців підготував учень 11-В класу Котенко Роман  Презентация ГЛАДКИХ КСЕНИИ НА ТЕМУ: «СЕРНАЯ КИСЛОТА. ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ»
Презентация ГЛАДКИХ КСЕНИИ НА ТЕМУ: «СЕРНАЯ КИСЛОТА. ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ»  Химические элементы
Химические элементы Углерод. Физические свойства
Углерод. Физические свойства Изучение свойств пластичных масс для лепки
Изучение свойств пластичных масс для лепки Липосомы
Липосомы Презентация по Химии "Застосування скла" - скачать смотреть бесплатно
Презентация по Химии "Застосування скла" - скачать смотреть бесплатно Реакции ионного обмена. Теория химического строения органических соединений. 9 класс
Реакции ионного обмена. Теория химического строения органических соединений. 9 класс Карбоновые кислоты
Карбоновые кислоты