Содержание
- 2. Чистые вещества и смеси Выпишите в два столбика названия чистых веществ и смесей: спиртовой раствор йода,
- 3. Химический элемент и простое вещество В каком высказывании речь идёт о химическом элементе, а в каком
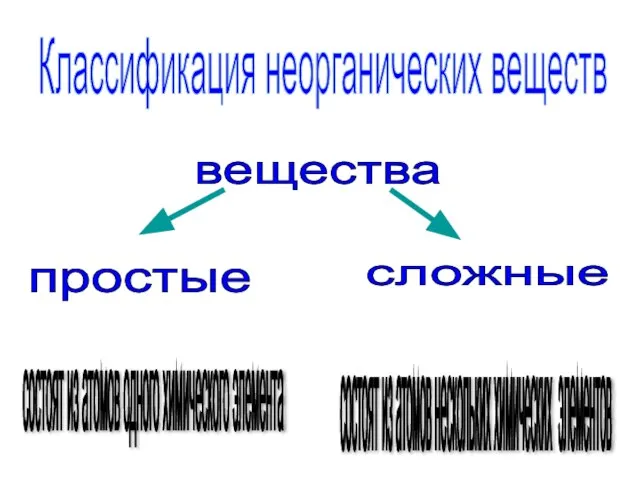
- 4. Классификация неорганических веществ вещества простые сложные состоят из атомов одного химического элемента состоят из атомов нескольких
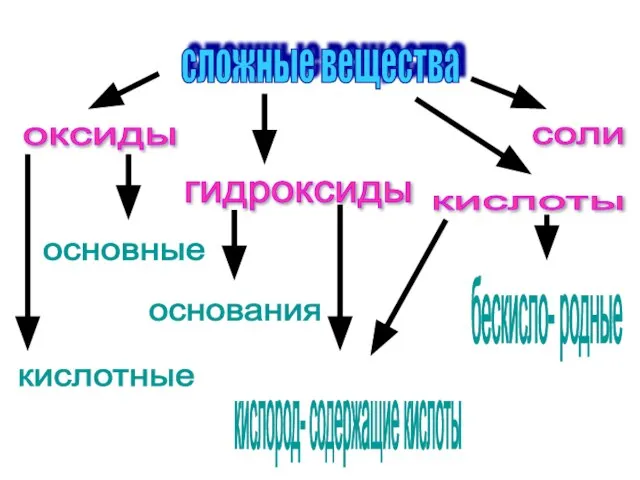
- 5. сложные вещества оксиды основные кислотные соли гидроксиды кислоты основания кислород- содержащие кислоты бескисло- родные
- 6. 1. Определите принадлежность веществ к определённым классам. Ответ объясните. CuO, H2SO4 , Fe(OH)2 , Al2O3, NaCl,
- 7. Домашнее задание Напишите формулы веществ, названия которых: оксид натрия, гидроксид меди (II), силикат натрия, угольная кислота,
- 8. Химические свойства основных оксидов 1. + вода → растворимое основание 2. + кислотный оксид → соль
- 9. Какие оксиды взаимодействуют между собой? Напишите уравнения реакций. SO3 и СO2 CO2 и H2O Al2O3 и
- 10. Химические свойства основных и амфотерных гидроксидов + кислота → соль + вода ( реакция нейтрализации )
- 11. Химические свойства кислот + Ме (до Н) → соль + Н2↑ + основные и амфотерные оксиды
- 12. Химические свойства солей 1. Соль + щёлочь → соль’ + гидроксид Ме ( один из продуктов
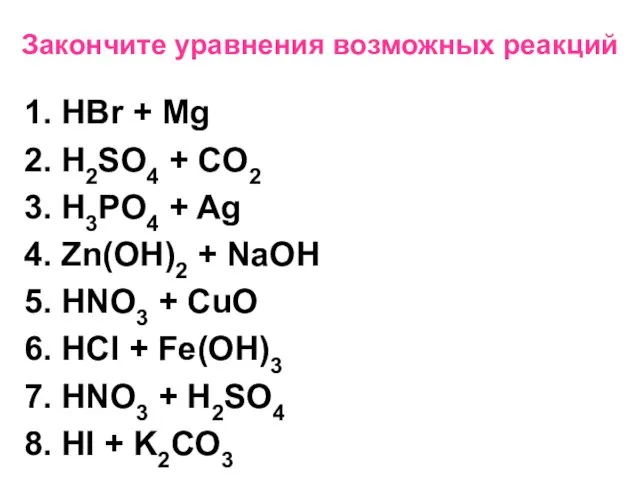
- 13. Закончите уравнения возможных реакций 1. HBr + Mg 2. H2SO4 + CO2 3. H3PO4 + Ag
- 14. Pb, NaOH, CO2 , Na2S, Cu(OH)2 , Zn, H3PO4, KCl, MgO, KOH, HCl. Напишите уравнения возможных
- 15. Определите вещество Х в цепочках превращений. Напишите уравнения соответствующих реакций. Ca → CaO → X →
- 16. Домашнее задание Какие из веществ могут реагировать друг с другом? Напишите уравнения возможных реакций. Оксид алюминия,
- 17. Решите задачи: Какова массовая доля кислорода в веществах : а) оксид магния; б) карбонат натрия. В
- 18. 4. Объём углекислого газа, полученного при разложении 8,4 г карбоната магния, равен ____ л. 5. Какова
- 19. Рассчитайте массовую долю натрия в веществах: а) оксид натрия; б) фосфат натрия. Масса воды, необходимая для
- 21. Скачать презентацию















 Презентация по Химии "Бинарные соединения" - скачать смотреть
Презентация по Химии "Бинарные соединения" - скачать смотреть  Тұздар химиялық қосылыстар класы
Тұздар химиялық қосылыстар класы Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі
Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі Идеальный газ в молекулярно-кинетической теории. Среднее значение квадрата скорости молекул
Идеальный газ в молекулярно-кинетической теории. Среднее значение квадрата скорости молекул Стадии онтогенеза почв
Стадии онтогенеза почв Каучук и резина
Каучук и резина Типы химической связи
Типы химической связи Gas hydrates
Gas hydrates Строение и функция белков
Строение и функция белков Тест по теме «Альдегиды и кетоны»
Тест по теме «Альдегиды и кетоны» Углерод
Углерод Enantioselective Total Synthesis of (+)-Vittatalactone
Enantioselective Total Synthesis of (+)-Vittatalactone Диоксины, глобальные экотоксиканты
Диоксины, глобальные экотоксиканты Биохимия нуклеиновых кислот
Биохимия нуклеиновых кислот Аминокислотный спектр плазмы крови у пациентов с острым миелобластным лейкозом
Аминокислотный спектр плазмы крови у пациентов с острым миелобластным лейкозом Вырожденные фазовые равновесия на экспериментальных t-x диаграммах
Вырожденные фазовые равновесия на экспериментальных t-x диаграммах Химия, как наука. Основные понятия и законы
Химия, как наука. Основные понятия и законы Кристаллохимические радиусы
Кристаллохимические радиусы Презентация по Химии "Кто хочет стать отличником" - скачать смотреть бесплатно
Презентация по Химии "Кто хочет стать отличником" - скачать смотреть бесплатно Углеводы – структура, функции, свойства
Углеводы – структура, функции, свойства Строение вещества. Молекулы
Строение вещества. Молекулы Растворы. Классификация дисперсных систем
Растворы. Классификация дисперсных систем Анализ качества лекарственных и косметических веществ из группы алифатических кислот и аминокислот
Анализ качества лекарственных и косметических веществ из группы алифатических кислот и аминокислот Адсорбционные равновесия и процессы на подвижных и неподвижных границах раздела фаз
Адсорбционные равновесия и процессы на подвижных и неподвижных границах раздела фаз Вторичное квантование. Применение оболочечной модели. Метод Хартри - Фока
Вторичное квантование. Применение оболочечной модели. Метод Хартри - Фока Программа повышения квалификации. Каталитические процессы в глубокой переработке нефти
Программа повышения квалификации. Каталитические процессы в глубокой переработке нефти Механизмы трансформации энергии в фотосинтезе
Механизмы трансформации энергии в фотосинтезе Строение атома
Строение атома