Содержание
- 2. * ORGANIZACJA ZAJĘĆ WYKŁAD (II semestr) – 15 godzin I połowa semestru– 2 godziny/tydzień LABORATORIUM (II
- 3. * LITERATURA Zdzisław Celiński, „Materiałoznawstwo elektrotechniczne”, Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa 1998 (2005) Karol Radecki i
- 4. *
- 5. * TEMATYKA ZAJĘĆ Jak działają układy (urządzenia) elektroniczne ? Jak projektować urządzenia/układy? Z czego budować? (materiały)
- 6. * TEMATYKA ZAJĘĆ Podstawy budowy materii struktura atomu i wiązania chemiczne struktura krystaliczna Materiały i elementy
- 7. * PODSTAWY BUDOWY MATERII Kryterium podstawowe - oddziaływanie materiału z falą elektromagnetyczną Hz
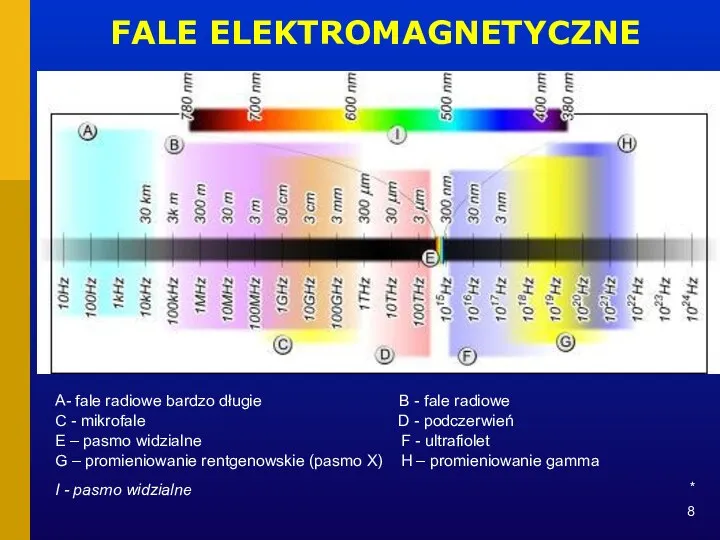
- 8. * FALE ELEKTROMAGNETYCZNE A- fale radiowe bardzo długie B - fale radiowe C - mikrofale D
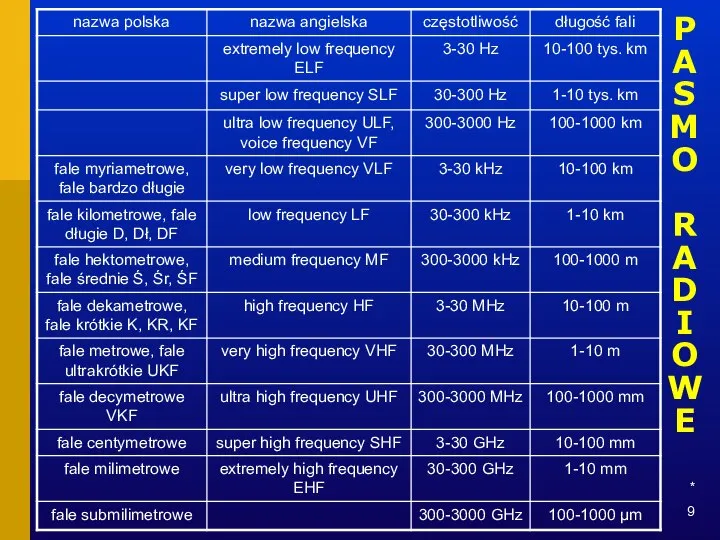
- 9. * PASMO RADIOWE
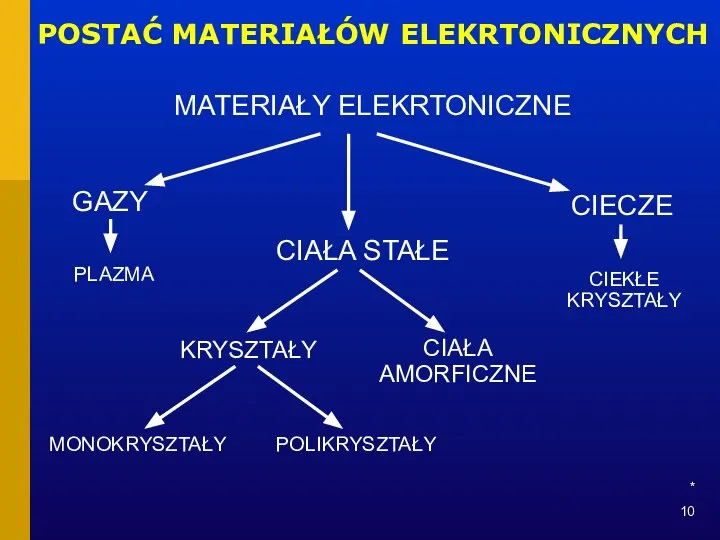
- 10. * POSTAĆ MATERIAŁÓW ELEKRTONICZNYCH MATERIAŁY ELEKRTONICZNE GAZY CIECZE CIAŁA STAŁE KRYSZTAŁY CIEKŁE KRYSZTAŁY CIAŁA AMORFICZNE MONOKRYSZTAŁY
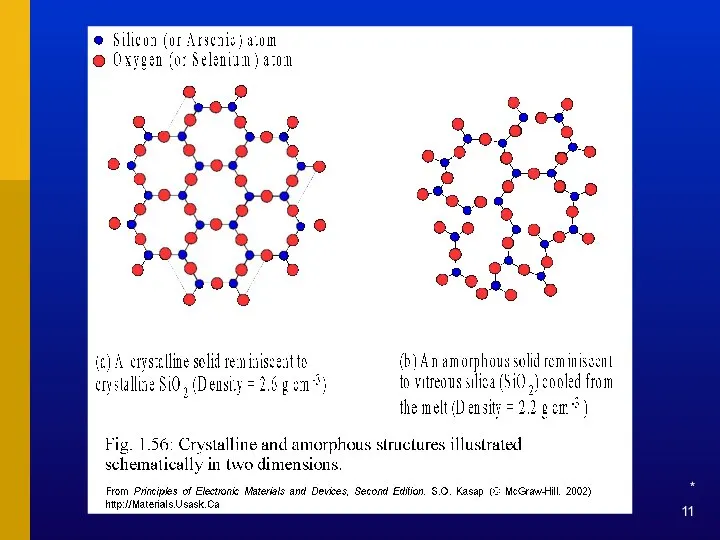
- 11. *
- 12. * PODSTAWY BUDOWY MATERII Pojęcie struktury materiału obejmuje: Charakterystykę uporządkowania atmowego Opis wielkości, kształtu i jednorodności,
- 13. * BUDOWA ATOMU
- 14. * BUDOWA ATOMU Główna liczba kwantowa n określa numer porządkowy powłoki elektronowej i rozmiary orbity; przybiera
- 15. * ORBITALNA LICZBA KWANTOWA Zdzisław Celiński, „Materiałoznawstwo elektrotechniczne”, Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa 1998 (2005)
- 16. * BUDOWA ATOMU Główna liczba kwantowa n określa numer porządkowy powłoki elektronowej i rozmiary orbity; przybiera
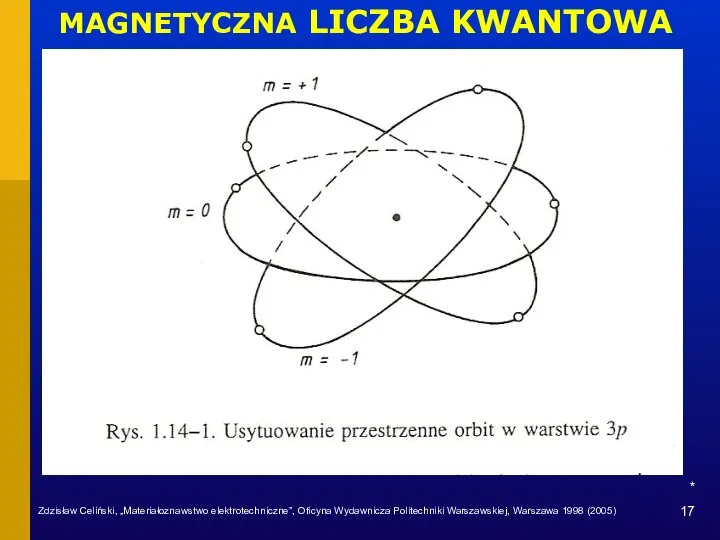
- 17. * MAGNETYCZNA LICZBA KWANTOWA Zdzisław Celiński, „Materiałoznawstwo elektrotechniczne”, Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa 1998 (2005)
- 18. * BUDOWA ATOMU Główna liczba kwantowa n określa numer porządkowy powłoki elektronowej i rozmiary orbity; przybiera
- 19. * Table 1.1 Maximum possible number of electrons in the shells and subshells of an atom.
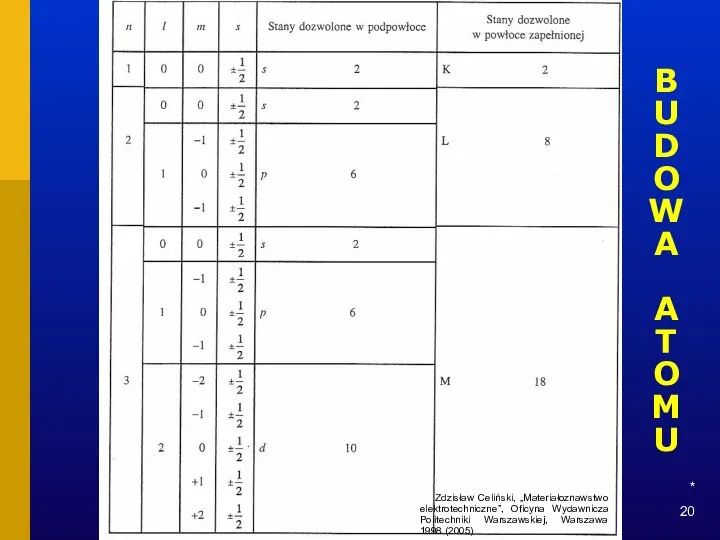
- 20. * BUDOWA ATOMU Zdzisław Celiński, „Materiałoznawstwo elektrotechniczne”, Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa 1998 (2005)
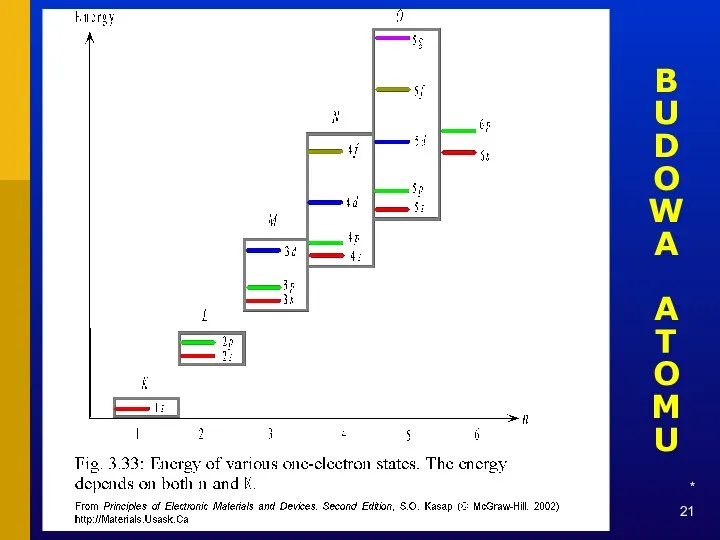
- 21. * BUDOWA ATOMU
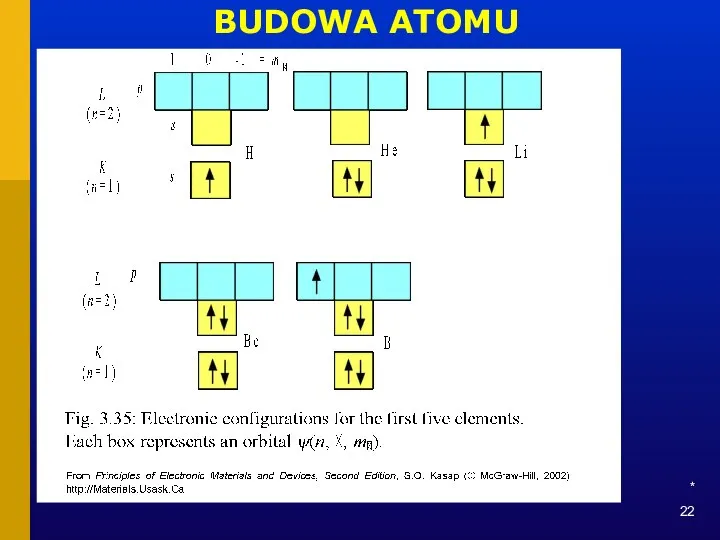
- 22. * BUDOWA ATOMU
- 23. * BUDOWA ATOMU
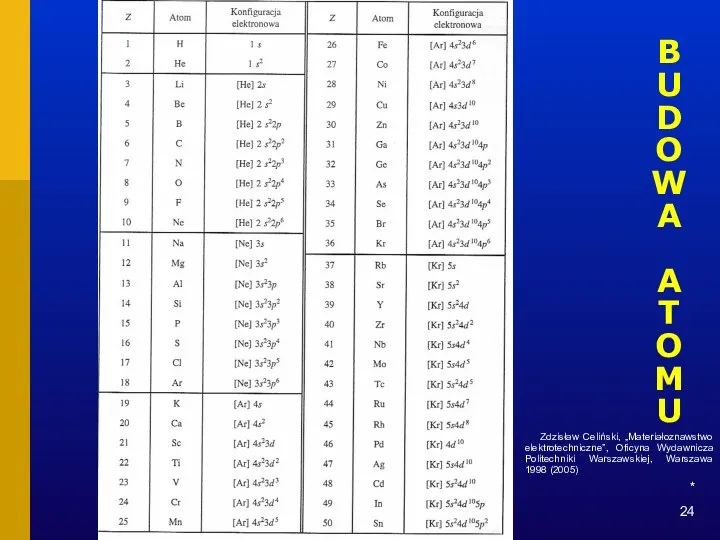
- 24. * BUDOWA ATOMU Zdzisław Celiński, „Materiałoznawstwo elektrotechniczne”, Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa 1998 (2005)
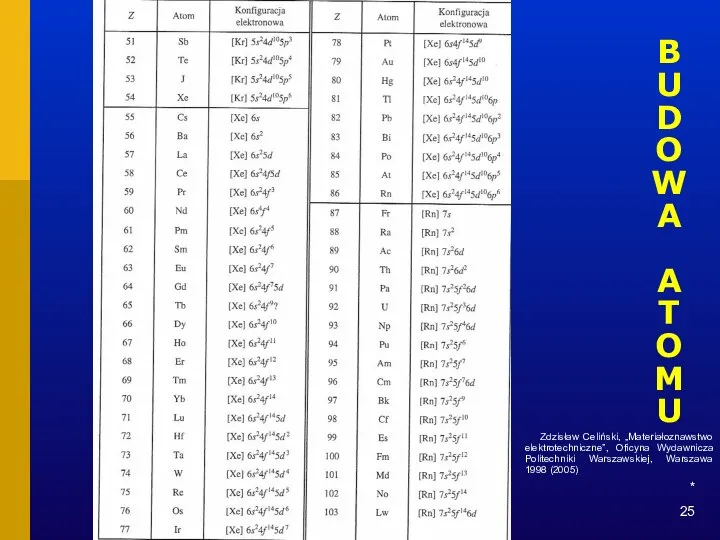
- 25. * BUDOWA ATOMU Zdzisław Celiński, „Materiałoznawstwo elektrotechniczne”, Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa 1998 (2005)
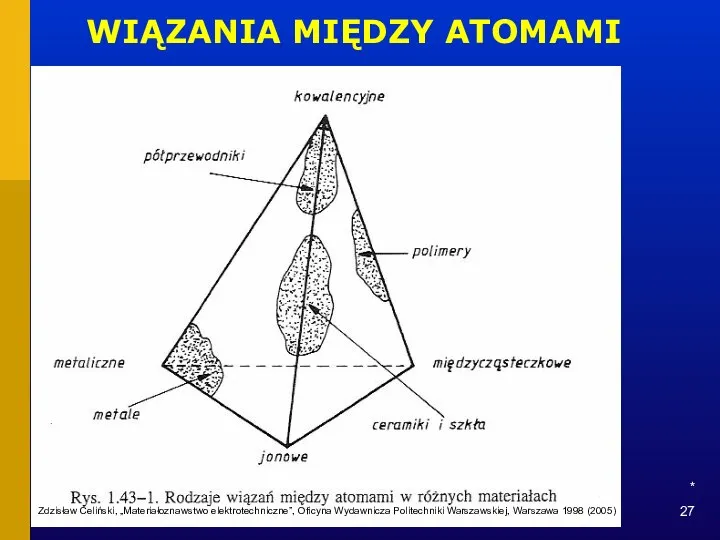
- 26. * WIĄZANIA MIĘDZY ATOMAMI Wiązania metaliczne metale Wiązania kowalencyjne półprzewodniki, polimery, ceramiki i szkła Wiązania jonowe
- 27. * WIĄZANIA MIĘDZY ATOMAMI Zdzisław Celiński, „Materiałoznawstwo elektrotechniczne”, Oficyna Wydawnicza Politechniki Warszawskiej, Warszawa 1998 (2005)
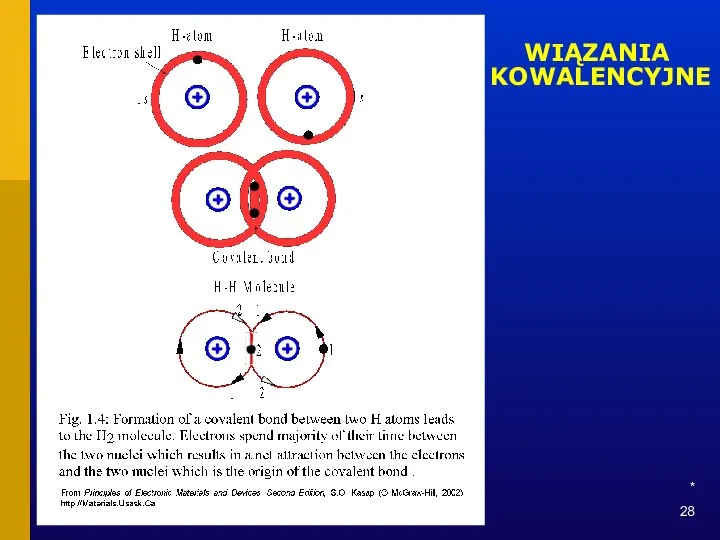
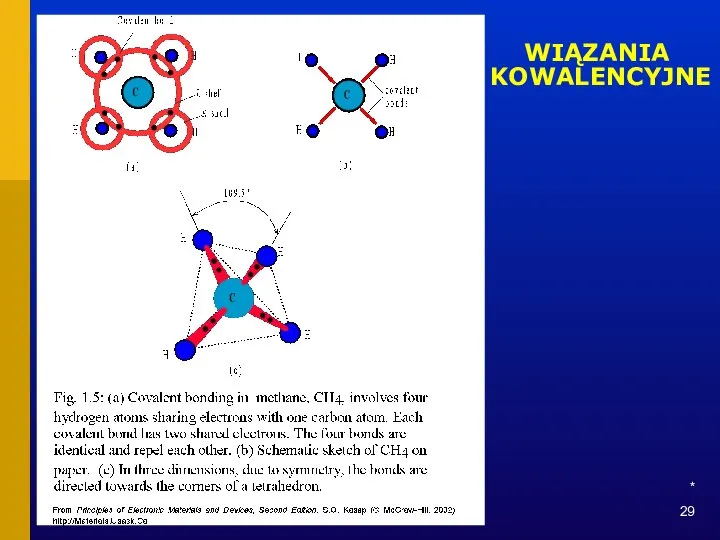
- 28. * WIĄZANIA KOWALENCYJNE
- 29. * WIĄZANIA KOWALENCYJNE
- 30. * WIĄZANIA METALICZNE
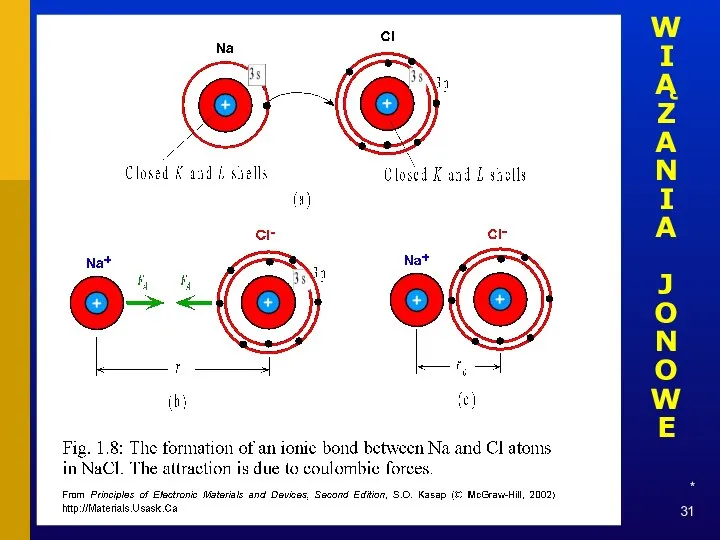
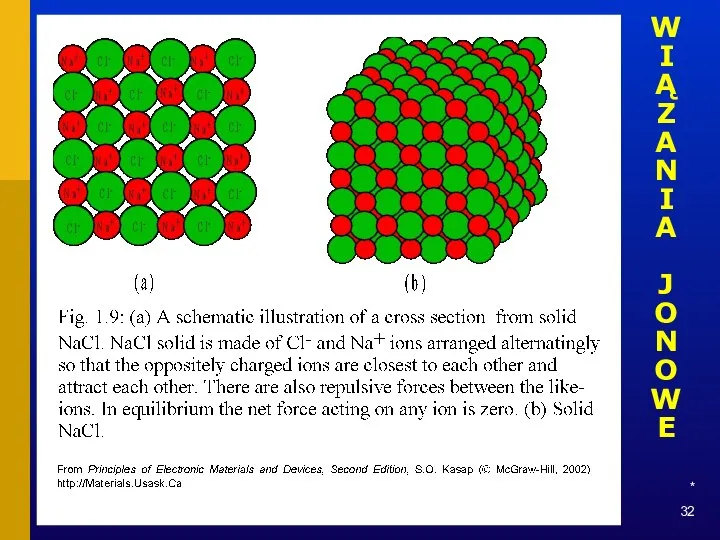
- 31. * WIĄZANIA JONOWE
- 32. * WIĄZANIA JONOWE
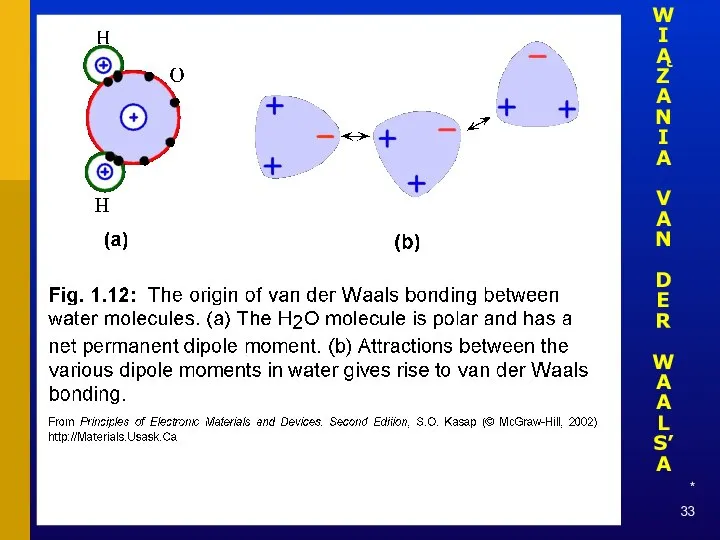
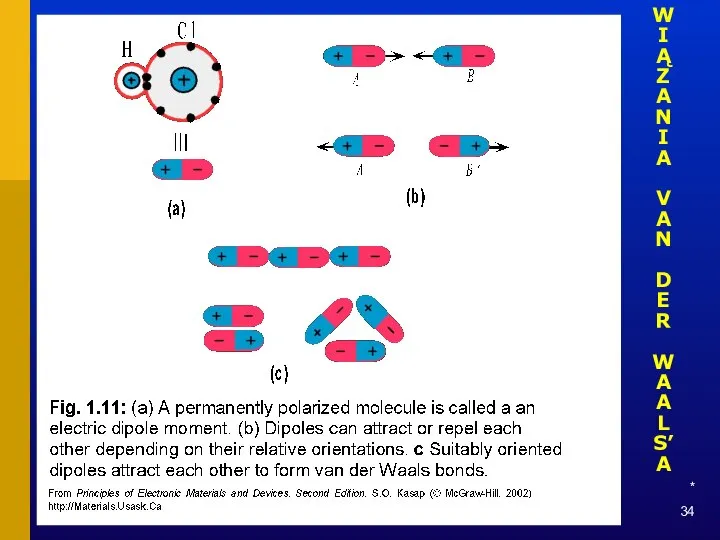
- 33. * WIĄZANIA VAN DER WAALS’A
- 34. * WIĄZANIA VAN DER WAALS’A
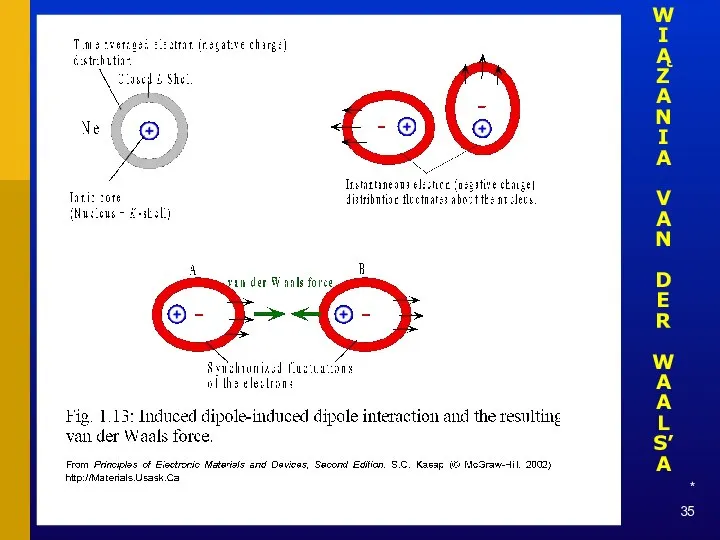
- 35. * WIĄZANIA VAN DER WAALS’A
- 36. *
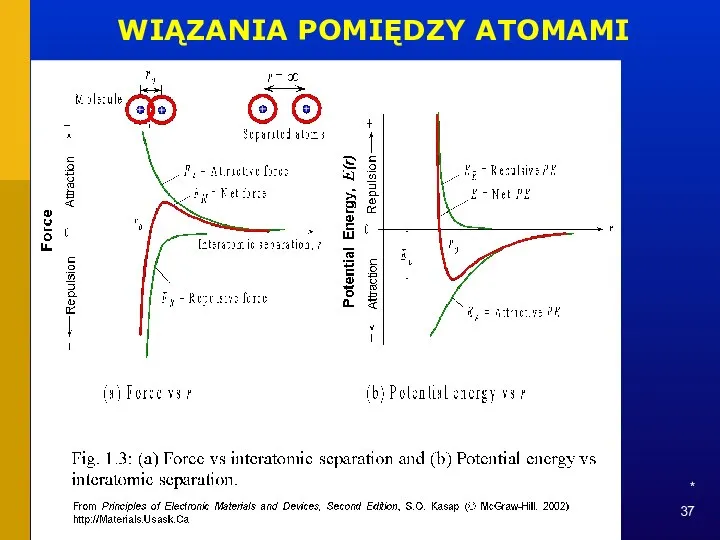
- 37. * WIĄZANIA POMIĘDZY ATOMAMI
- 38. * STRUKTURA KRYSTALICZNA Monokryształy – pojedyńcze duże kryształy. Polikryształy – ciała składające się z wielu zrośniętych
- 39. * STRUKTURA KRYSTALICZNA
- 40. * STRUKTURA KRYSTALICZNA
- 41. * STRUKTURA KRYSTALICZNA
- 42. * STRUKTURA KRYSTALICZNA
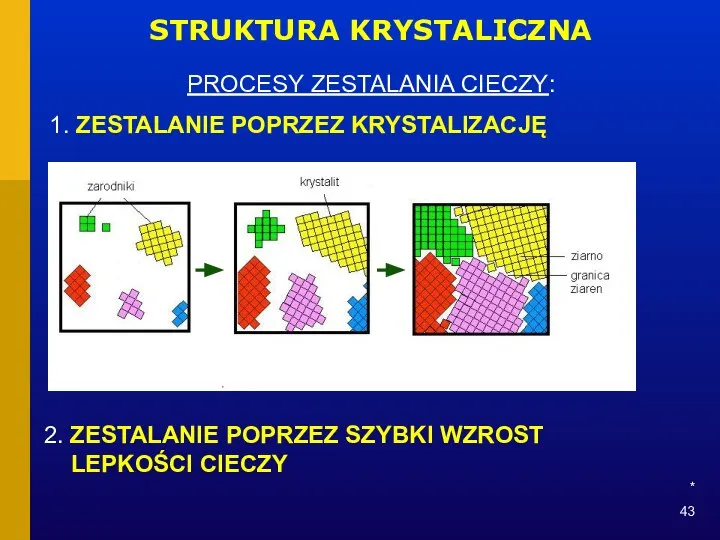
- 43. * STRUKTURA KRYSTALICZNA PROCESY ZESTALANIA CIECZY: 1. ZESTALANIE POPRZEZ KRYSTALIZACJĘ 2. ZESTALANIE POPRZEZ SZYBKI WZROST LEPKOŚCI
- 44. * IZOTROPIA i ANIZOTROPIA Anizotropia (an- 'nie'; gr. isos 'równy, jednakowy'; gr. trópos 'zwrot, obrót') –
- 45. * IZOTROPIA i ANIZOTROPIA Materiał izotropowy: j1 = σE1, j2 = σE2, j3 = σE3 Kryształ
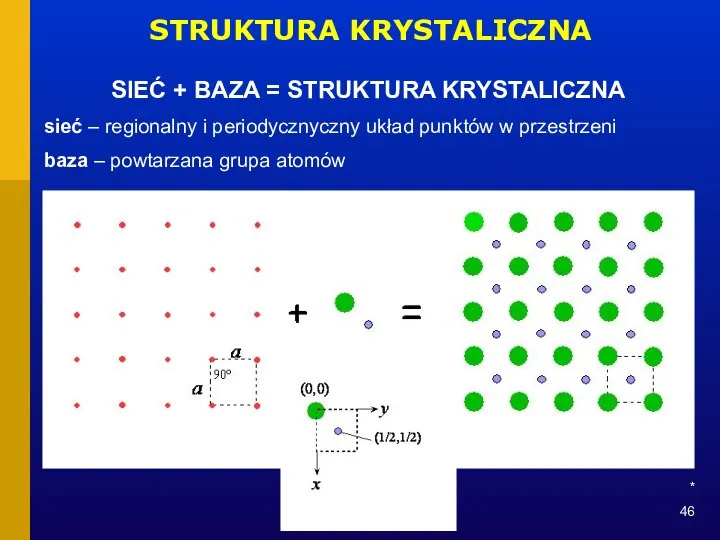
- 46. * STRUKTURA KRYSTALICZNA SIEĆ + BAZA = STRUKTURA KRYSTALICZNA sieć – regionalny i periodycznyczny układ punktów
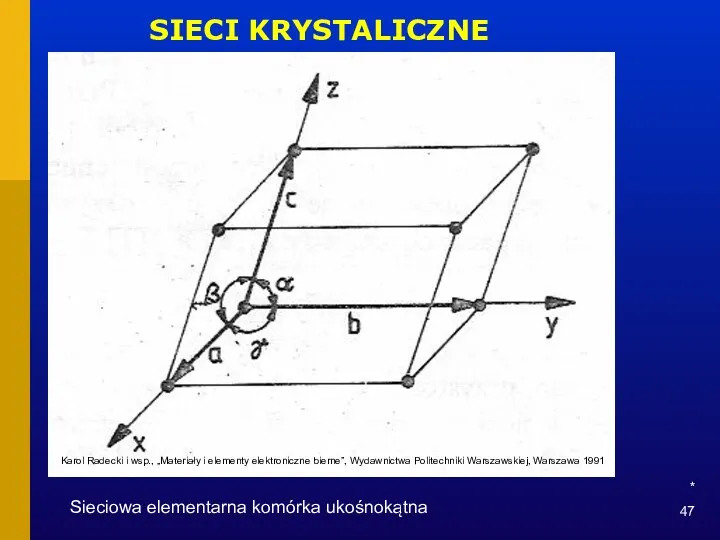
- 47. * SIECI KRYSTALICZNE Sieciowa elementarna komórka ukośnokątna Karol Radecki i wsp., „Materiały i elementy elektroniczne bierne”,
- 48. * OPIS STRUKTURY KRYSTALICZNEJ Parametry komórki elementarnej; Liczba koordynacyjna – ilość sąsiadów dla każdego atomu w
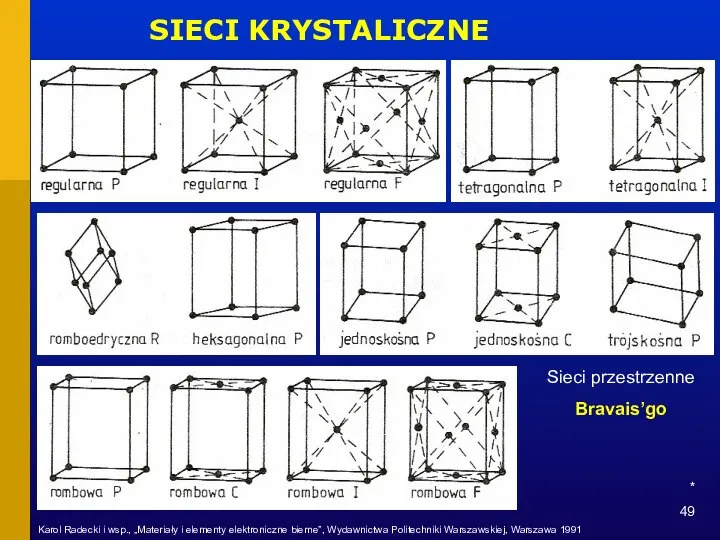
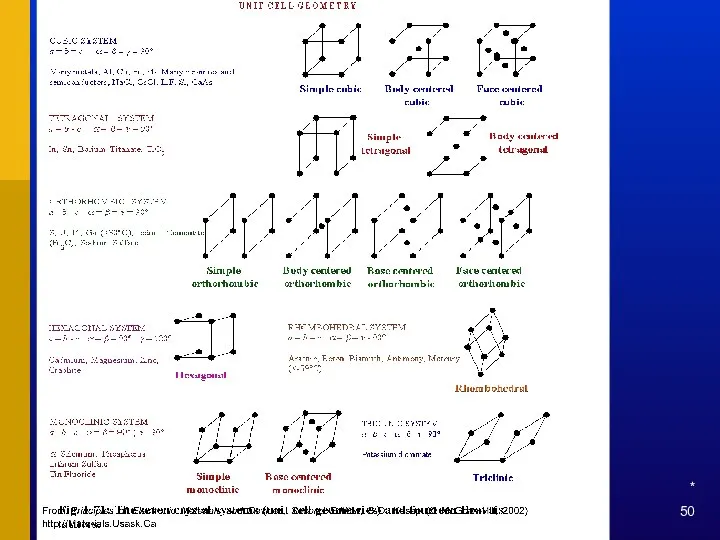
- 49. * SIECI KRYSTALICZNE Sieci przestrzenne Bravais’go Karol Radecki i wsp., „Materiały i elementy elektroniczne bierne”, Wydawnictwa
- 50. *
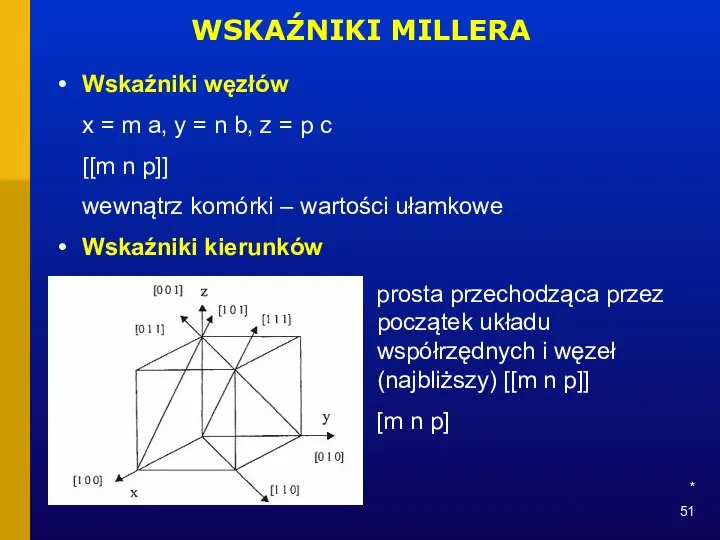
- 51. * WSKAŹNIKI MILLERA Wskaźniki węzłów x = m a, y = n b, z = p
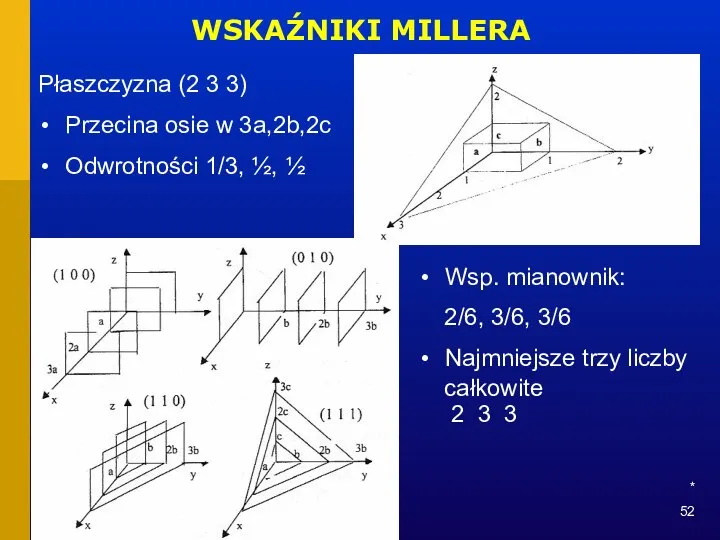
- 52. * WSKAŹNIKI MILLERA Płaszczyzna (2 3 3) Przecina osie w 3a,2b,2c Odwrotności 1/3, ½, ½ Wsp.
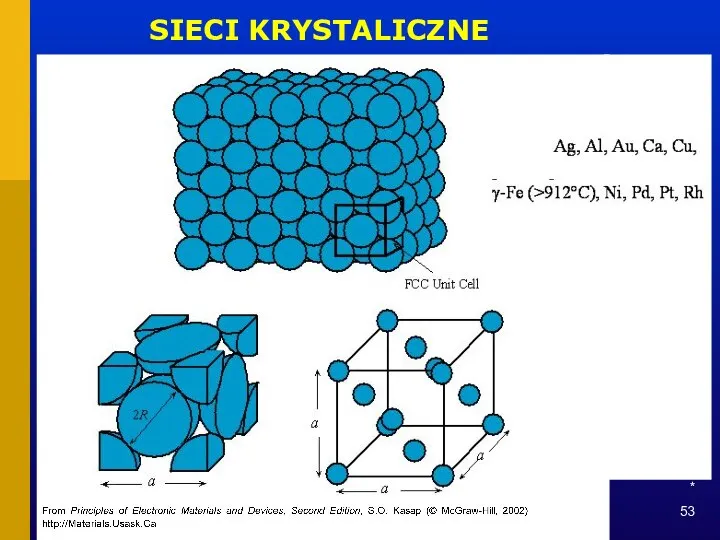
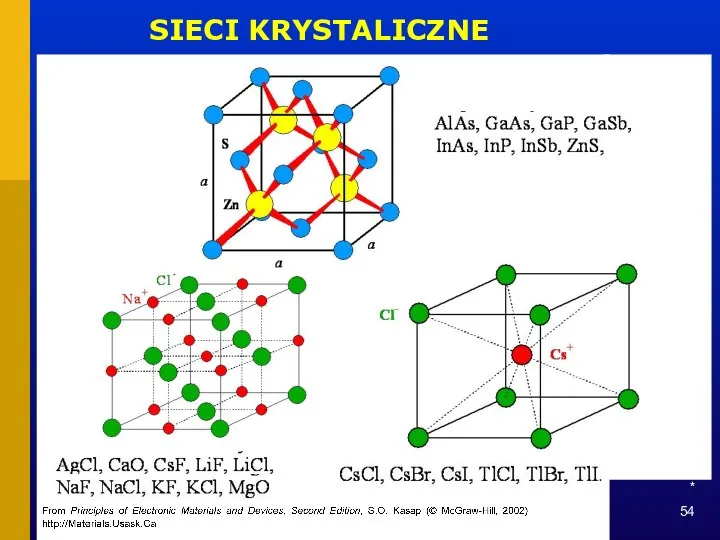
- 53. * SIECI KRYSTALICZNE
- 54. * SIECI KRYSTALICZNE
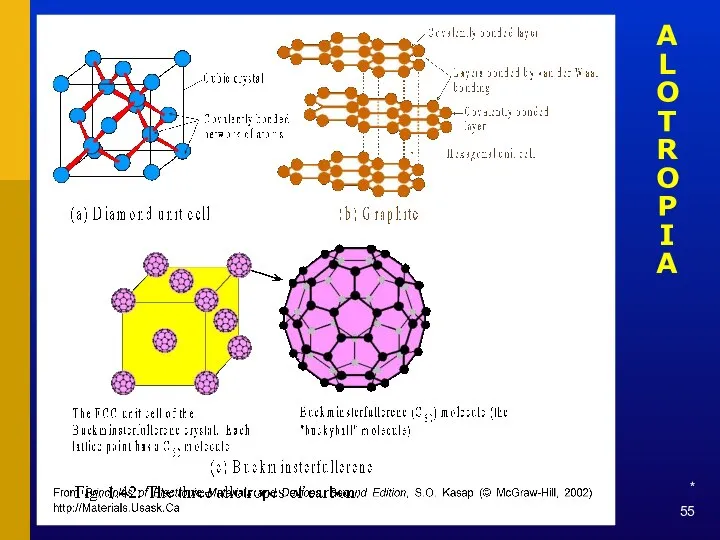
- 55. * ALOTROPIA
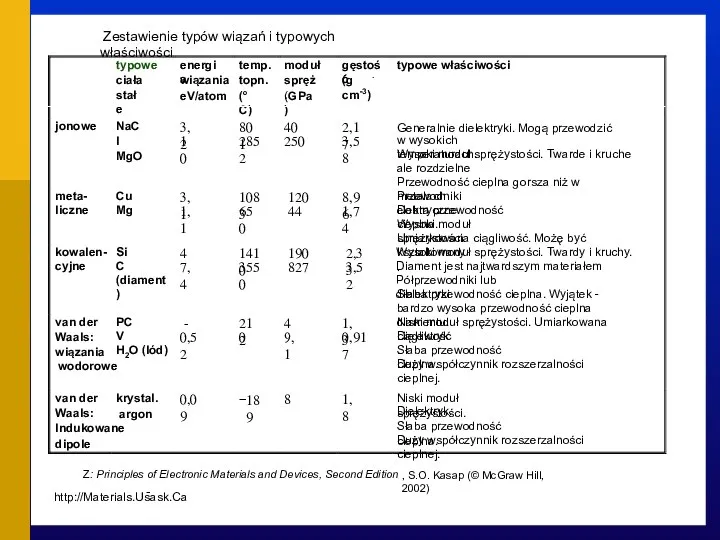
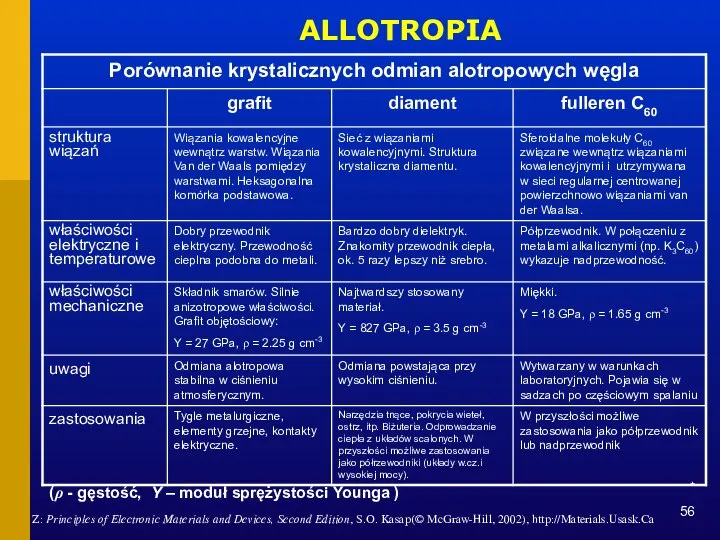
- 56. * Z: Principles of Electronic Materials and Devices, Second Edition, S.O. Kasap(© McGraw-Hill, 2002), http://Materials.Usask.Ca ALLOTROPIA
- 57. * DEFEKTY SIECI KRYSTALICZNYCH Defekty powierzchniowe powierzchnie zewnętrzne, powierzchnie wewnętrzne, granice ziaren, itp. Defekty liniowe dyslokacje
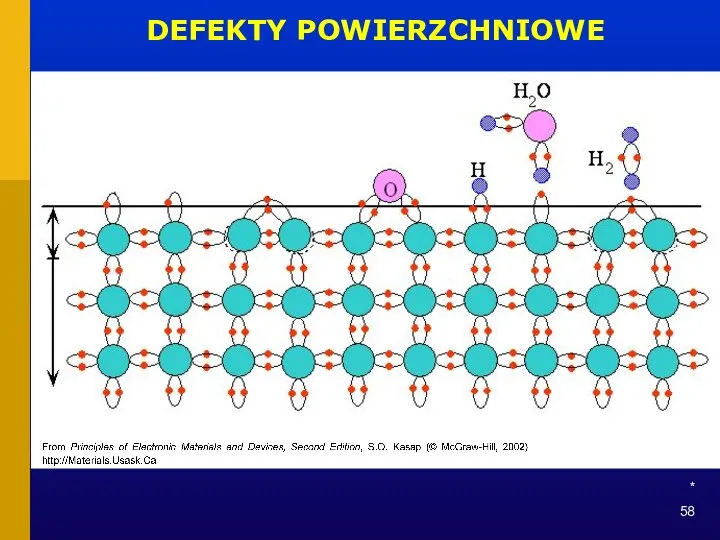
- 58. * DEFEKTY POWIERZCHNIOWE
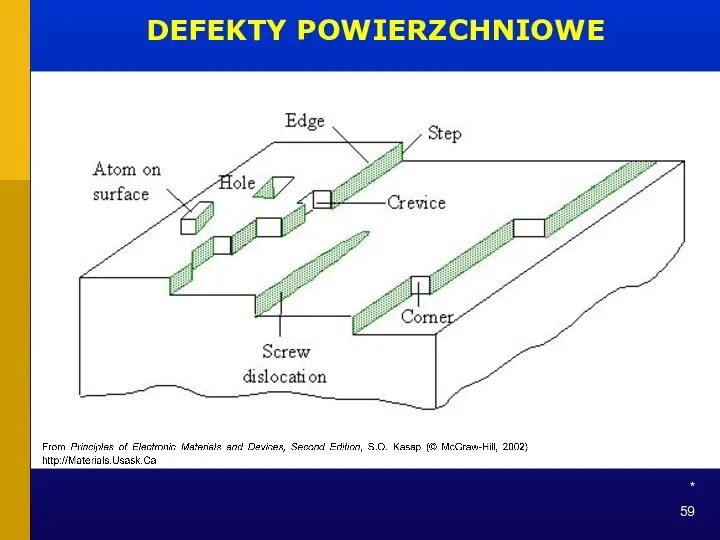
- 59. * DEFEKTY POWIERZCHNIOWE
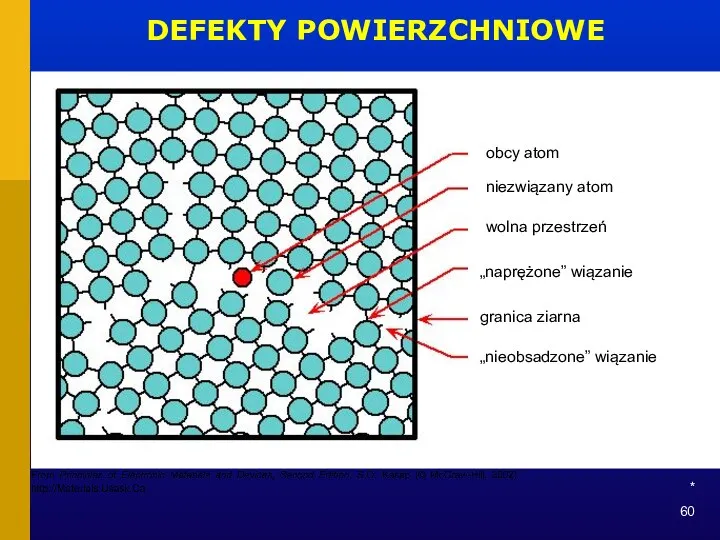
- 60. * DEFEKTY POWIERZCHNIOWE „nieobsadzone” wiązanie granica ziarna obcy atom „naprężone” wiązanie niezwiązany atom wolna przestrzeń
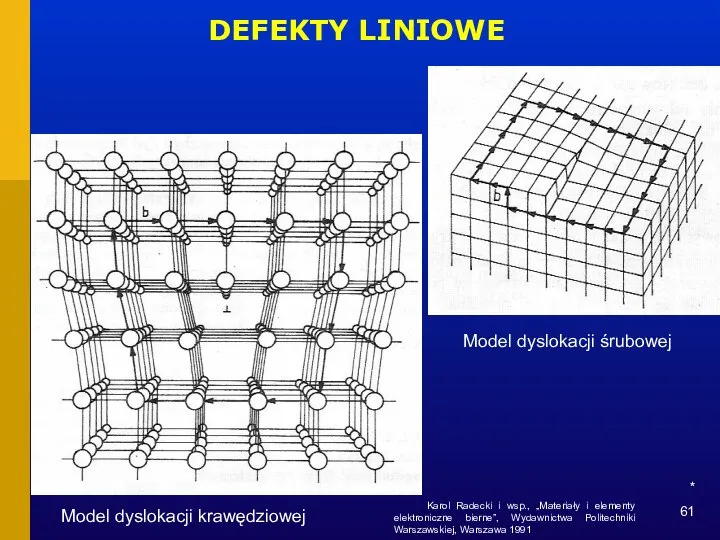
- 61. * DEFEKTY LINIOWE Model dyslokacji krawędziowej Model dyslokacji śrubowej Karol Radecki i wsp., „Materiały i elementy
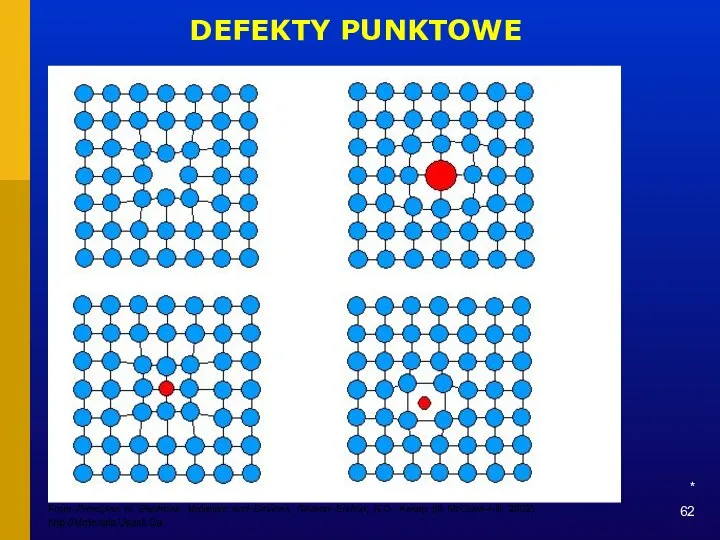
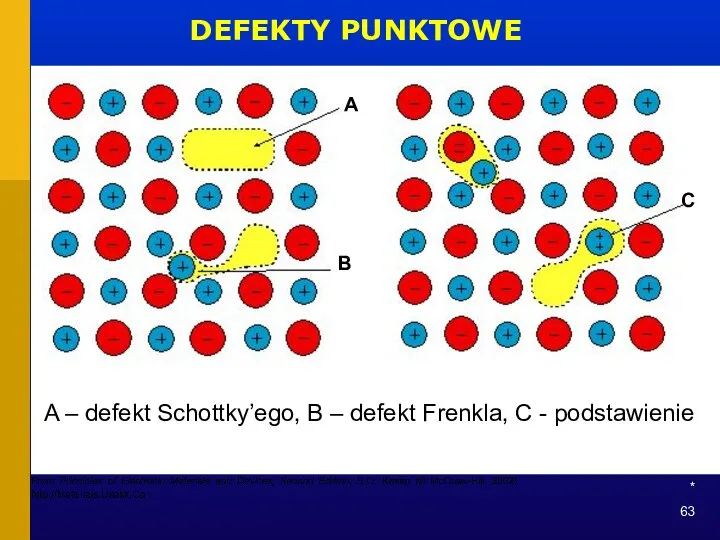
- 62. * DEFEKTY PUNKTOWE
- 63. * DEFEKTY PUNKTOWE A B C A – defekt Schottky’ego, B – defekt Frenkla, C -
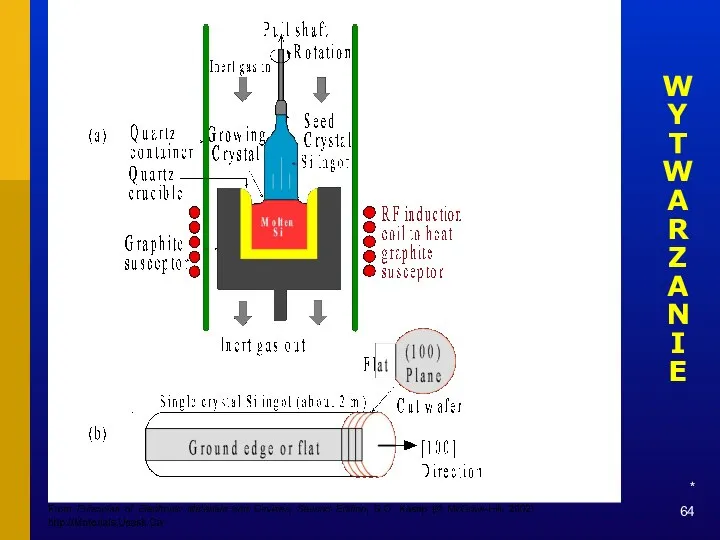
- 64. * WYTWARZANIE
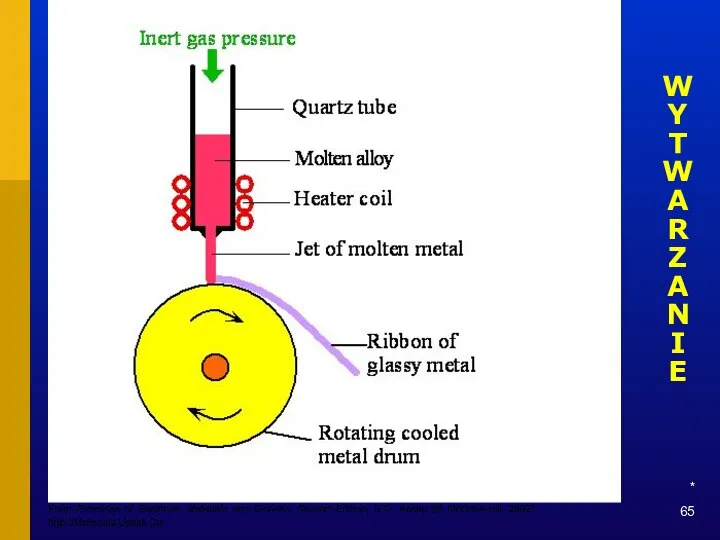
- 65. * WYTWARZANIE
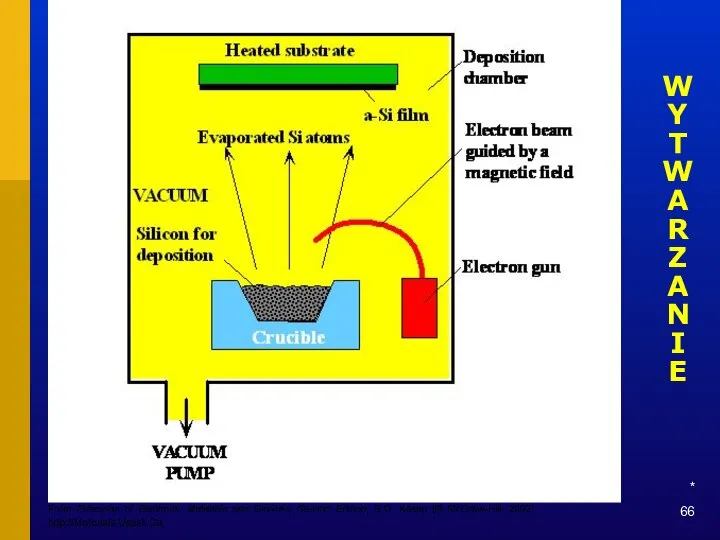
- 66. * WYTWARZANIE
- 68. Скачать презентацию

























 Девочка, которая стала храмом
Девочка, которая стала храмом bfa8-ebdc91bc
bfa8-ebdc91bc aleksandrsilovpobediteli (1)
aleksandrsilovpobediteli (1) 1
1 Итоги выполнения диагностического обследования объектов КС
Итоги выполнения диагностического обследования объектов КС 20160201_ispolzovanie_metafory
20160201_ispolzovanie_metafory Calculation of the optimal location of the wind turbines
Calculation of the optimal location of the wind turbines Отгадай персонажа из аниме 4
Отгадай персонажа из аниме 4 Сократические странствия
Сократические странствия Analisi di bilancio Riclassificazione e quozienti
Analisi di bilancio Riclassificazione e quozienti Виды симметрии в архитектуре г. Санкт-Петербурга
Виды симметрии в архитектуре г. Санкт-Петербурга Киностудия Чебовский дельрус представляет
Киностудия Чебовский дельрус представляет Ходырев2
Ходырев2 Вера православных христиан
Вера православных христиан Времена года в искусстве
Времена года в искусстве Права и обязанности школьника
Права и обязанности школьника Je vais vous présenter une super -famille
Je vais vous présenter une super -famille Презентация к 5 заданию
Презентация к 5 заданию Село Бурабай
Село Бурабай Виды роботов
Виды роботов Sales order type & ship mode
Sales order type & ship mode Классификация средств обработки документов
Классификация средств обработки документов Особенности возведения зданий в условиях городской застройки
Особенности возведения зданий в условиях городской застройки Молодежь в современном обществе
Молодежь в современном обществе Аптечные книги
Аптечные книги 20160306_prezentatsiya_po_chssh
20160306_prezentatsiya_po_chssh Миссия среди молодежи в условиях пандемии: духовные уроки и их осмысление
Миссия среди молодежи в условиях пандемии: духовные уроки и их осмысление Резюме. Ушаков Антон Анатольевич
Резюме. Ушаков Антон Анатольевич