Содержание
- 2. La segnalazione intercellulare L’evoluzione degli organismi multicellulari dipende dalla capacità delle cellule di comunicare una con
- 3. La segnalazione intercellulare Molte cellule secernono una o più molecole segnale che funzionano come mediatori chimici
- 4. MEDIATORI ENDOGENI Mediatori a basso peso molecolare: Aminoacidi: glutammato, glicina, acido gamma-amino-butirrico (GABA) Monoamine: catecolamine (dopamina,
- 5. Recettori Classificazione in base alla localizzazione: Recettori di membrana Recettori intracellulari I primi rispondono a mediatori
- 6. Recettori Classificazione in base alla localizzazione: Recettori di membrana Recettori intracellulari I secondi trasducono il segnale
- 7. Recettori intracellulari Divisi in due classi: I) citoplasmatici, formano omodimeri o dimeri con il ligando. Ne
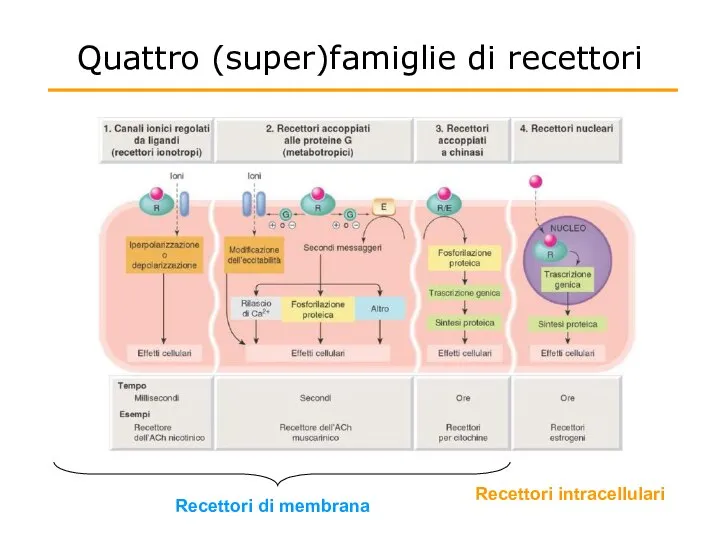
- 8. Quattro (super)famiglie di recettori Recettori di membrana Recettori intracellulari
- 9. Aspetti quantitativi delle risposte ai farmaci: analisi delle curve La relazione fra CONCENTRAZIONE di un FARMACO
- 10. In molti modelli sperimentali la risposta che si misura è graduabile e direttamente correlabile con la
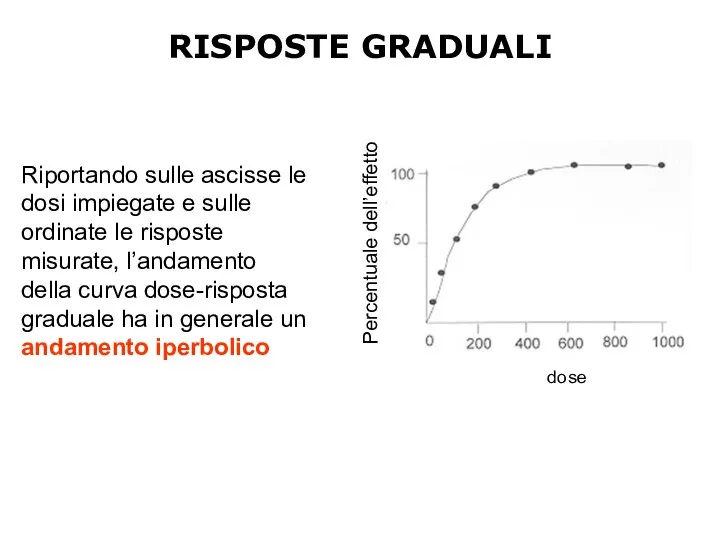
- 11. Riportando sulle ascisse le dosi impiegate e sulle ordinate le risposte misurate, l’andamento della curva dose-risposta
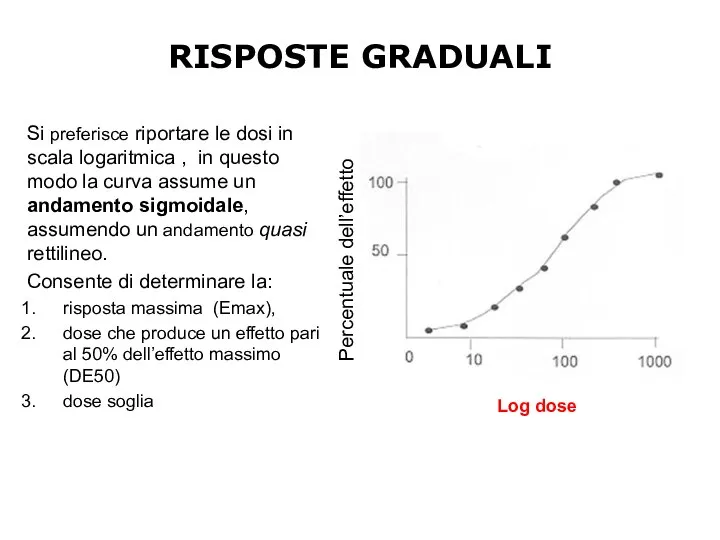
- 12. Si preferisce riportare le dosi in scala logaritmica , in questo modo la curva assume un
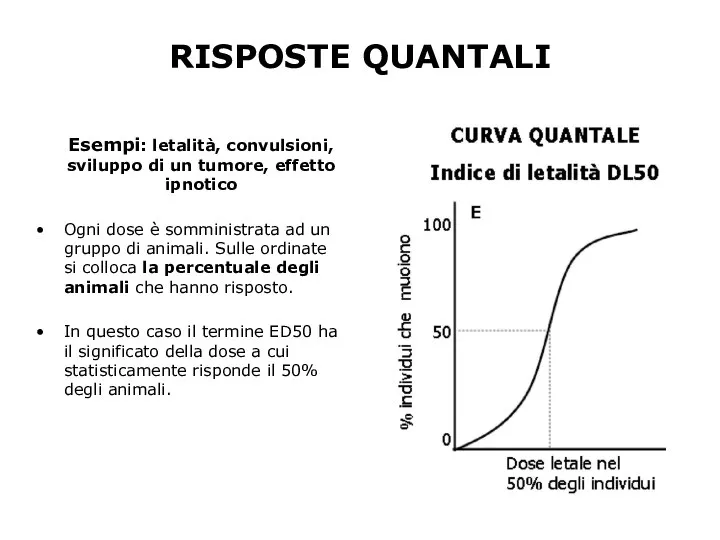
- 13. Esempi: letalità, convulsioni, sviluppo di un tumore, effetto ipnotico Ogni dose è somministrata ad un gruppo
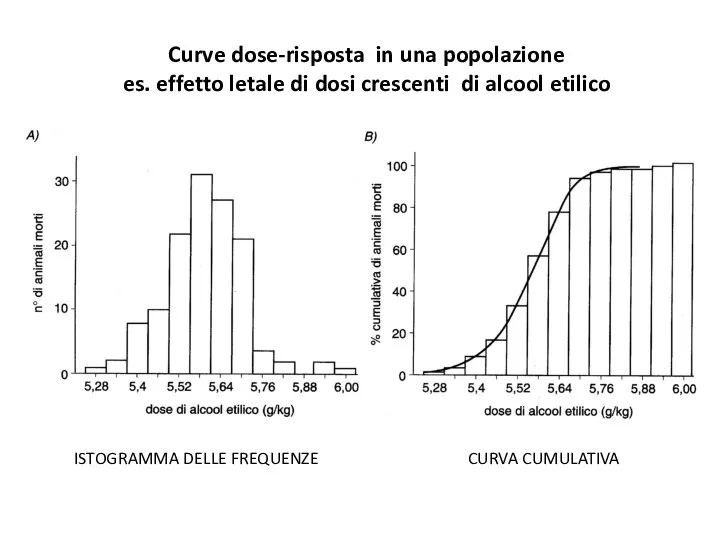
- 14. Curve dose-risposta in una popolazione es. effetto letale di dosi crescenti di alcool etilico ISTOGRAMMA DELLE
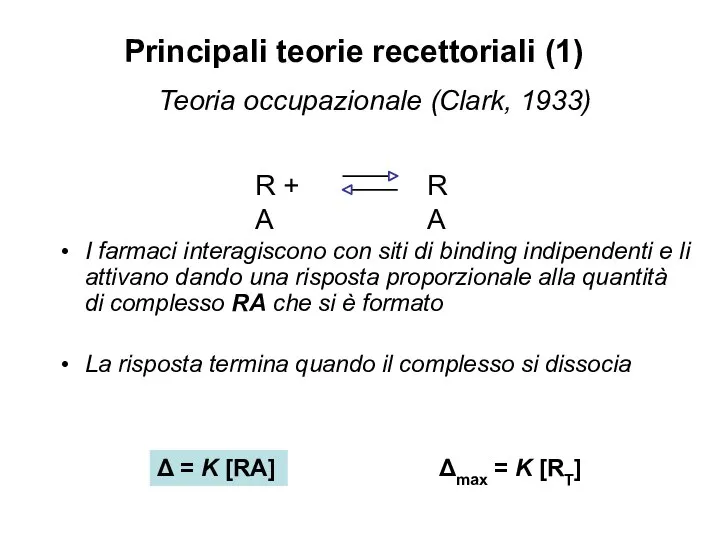
- 15. Principali teorie recettoriali (1) Teoria occupazionale (Clark, 1933) I farmaci interagiscono con siti di binding indipendenti
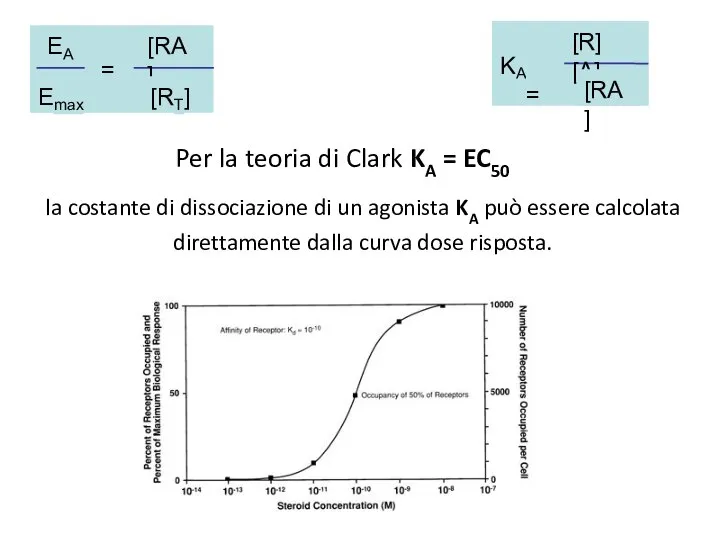
- 16. Per la teoria di Clark KA = EC50 la costante di dissociazione di un agonista KA
- 17. Il contributo di Ariens (1954) Non tutti gli agonisti producono la stessa risposta massimale Principali teorie
- 18. Attività intrinseca E’ la capacità del farmaco di indurre una risposta biologica (α) La risposta biologica
- 19. gli agonisti si legano ai recettori producendo effetti di vario tipo gli antagonisti si legano ai
- 20. Farmaci agonisti Generalmente un agonista riproduce gli effetti dei ligandi endogeni. agonista pieno (α = 1)
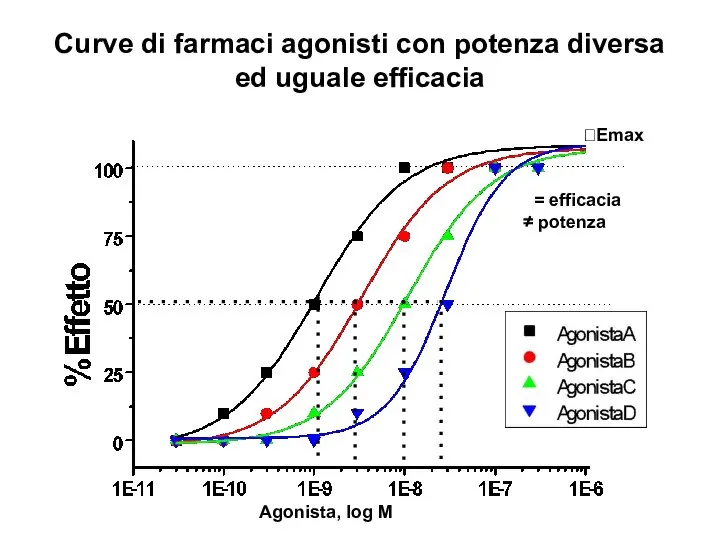
- 21. Curve di farmaci agonisti con potenza diversa ed uguale efficacia Agonista, log M = efficacia potenza
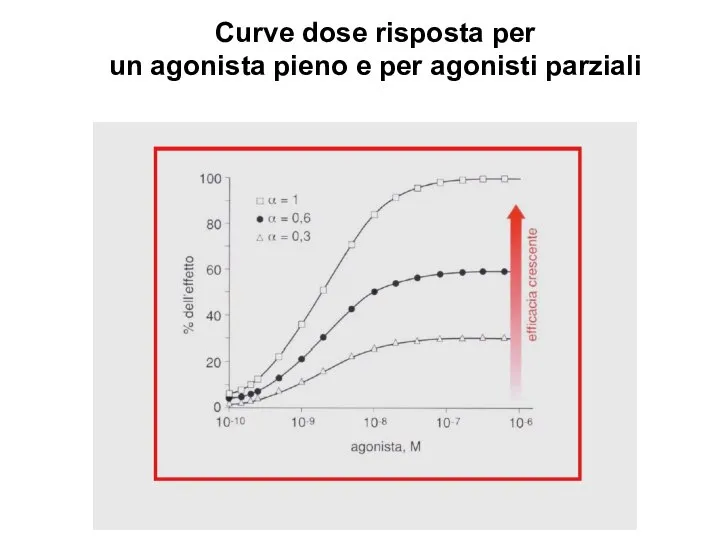
- 22. Curve dose risposta per un agonista pieno e per agonisti parziali
- 23. Farmaci antagonisti Si legano con alta affinità ai recettori, ma non sono in grado di indurre
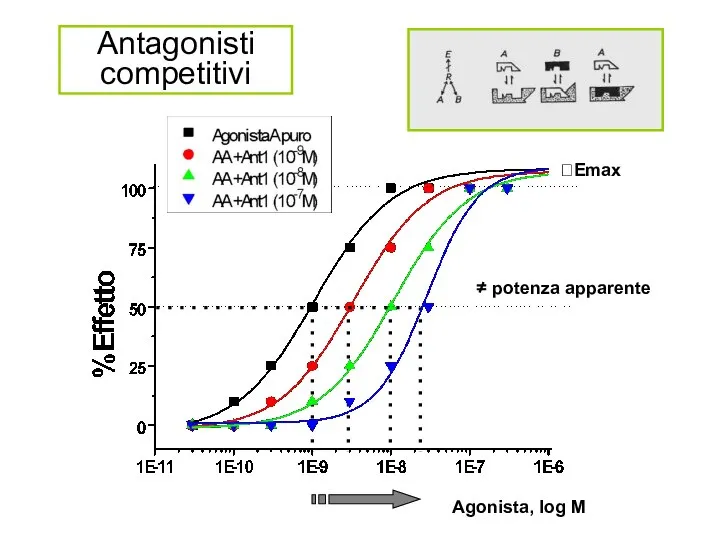
- 24. Antagonisti competitivi Agonista, log M ?Emax potenza apparente
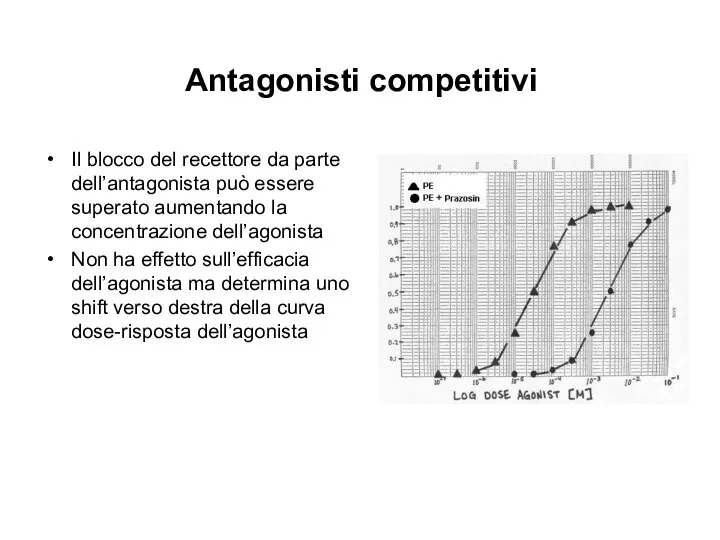
- 25. Antagonisti competitivi Il blocco del recettore da parte dell’antagonista può essere superato aumentando la concentrazione dell’agonista
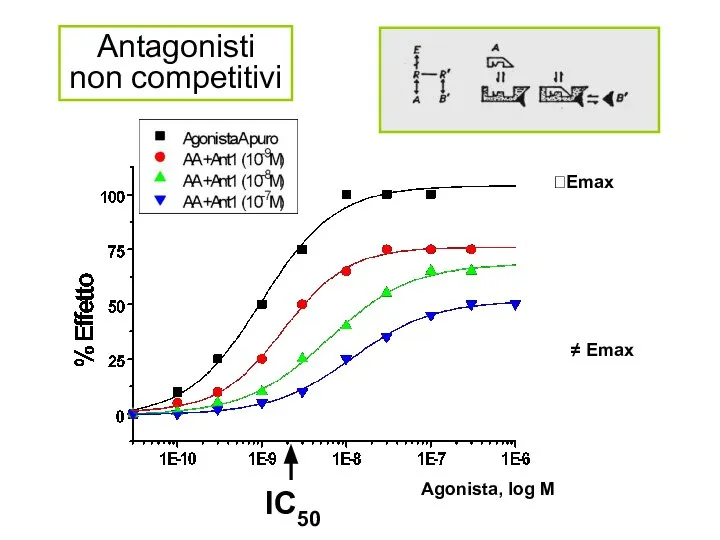
- 26. Antagonisti non competitivi ?Emax ≠ Emax IC50 Agonista, log M
- 27. Antagonisti non competitivi o irreversibili Un antagonista non competitivo sposta la curva dell’agonista verso destra in
- 28. Il contributo di Stephenson (1954) La risposta farmacologica non è linearmente proporzionale al numero di recettori
- 29. Il contributo di Furchgott (1966) Fornì l’evidenza sperimentale dell’esistenza degli spare receptors Principali teorie recettoriali (4)
- 30. Caratteristiche dell’interazione di un farmaco con il suo recettore AFFINITA’: esprime la forza con cui il
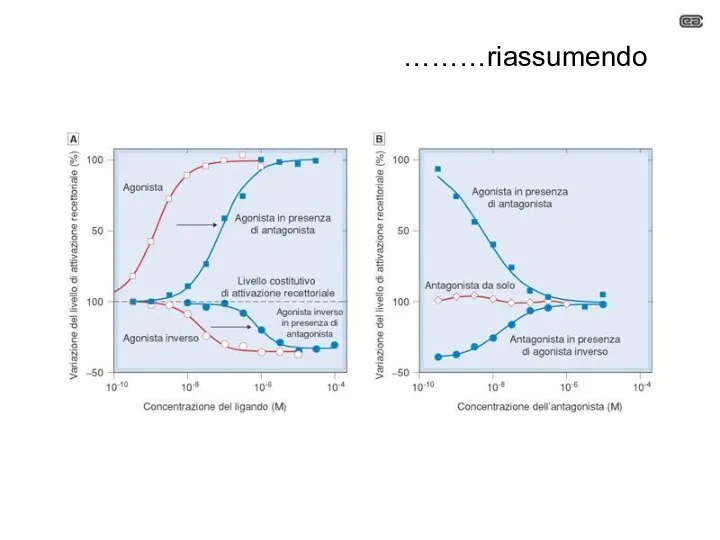
- 31. ………riassumendo
- 32. La tecnica del binding recettoriale Metodi semplici e rapidi per lo screening farmacologico di numerose molecole.
- 33. Si procede incubando un omogenato di tessuto opportunamente diluito e di cui si dovrà determinare la
- 34. Preparazione del tessuto Semplice omogenato (es. di cervello) Frazione subcellulare arricchita della componente rappresentata dalle membrane
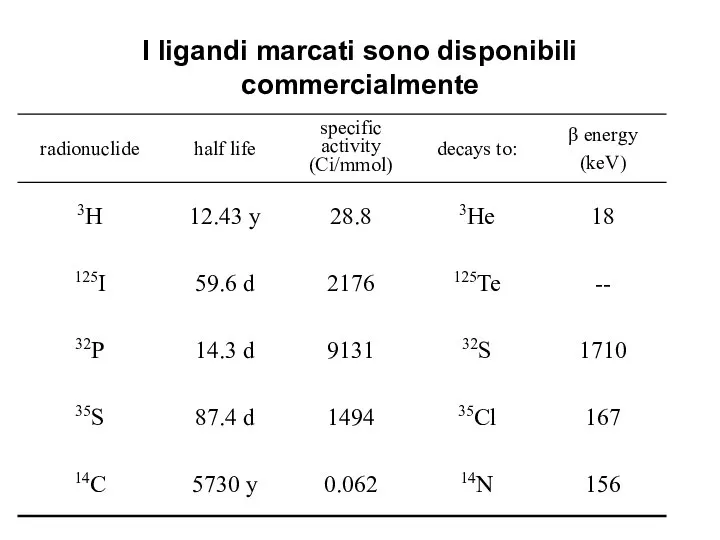
- 35. I ligandi marcati sono disponibili commercialmente
- 36. Durante l’incubazione si forma il complesso ligando-recettore, che segue la legge d’azione di massa. Tale reazione
- 37. Si termina l’incubazione con una procedura che permetta di separare il ligando legato al recettore dal
- 38. Al termine dell’esperimento, la radioattività legata ai filtri o presente nel pellet viene quantificata mediante spettrofotometria
- 39. Binding misurato per concentrazioni crescenti di legante radioattivo fino alla saturazione dei siti di binding. Es.
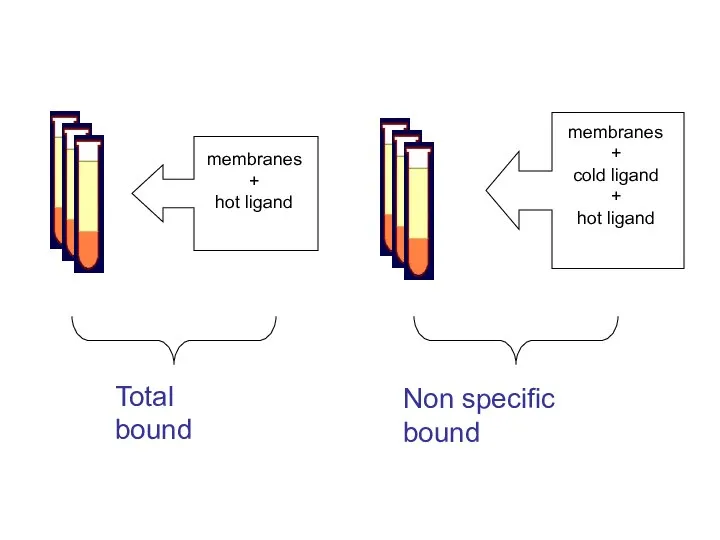
- 40. membranes + hot ligand membranes + cold ligand + hot ligand Total bound Non specific bound
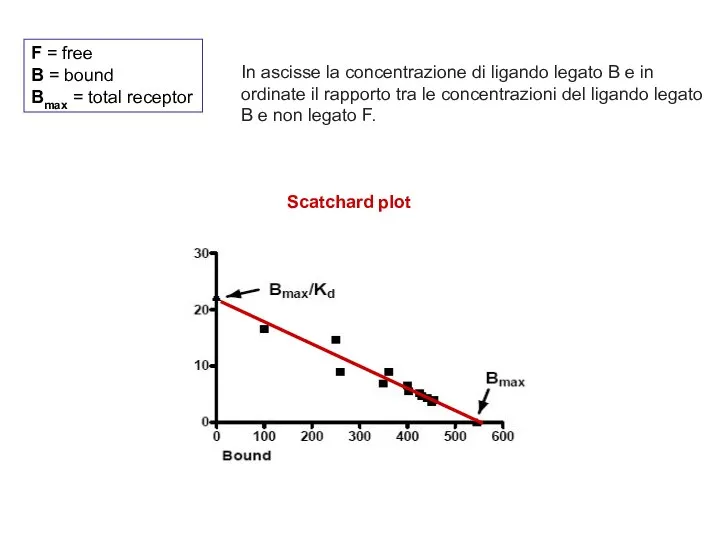
- 41. F = free B = bound Bmax = total receptor In ascisse la concentrazione di ligando
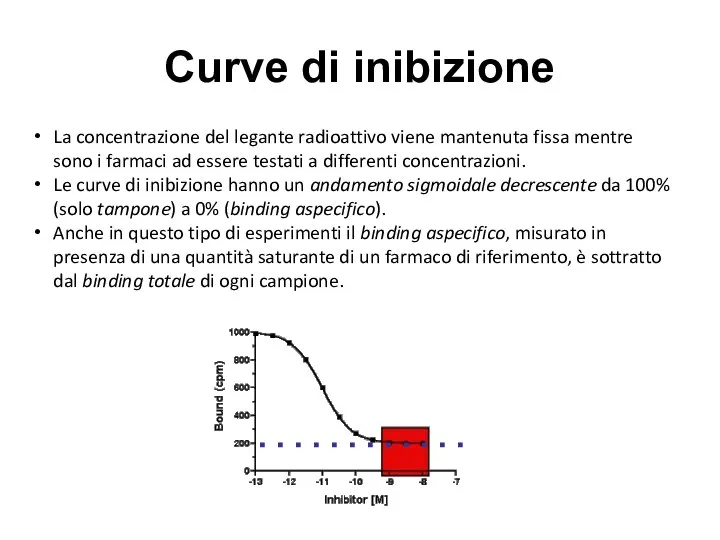
- 42. La concentrazione del legante radioattivo viene mantenuta fissa mentre sono i farmaci ad essere testati a
- 43. In questi esperimenti, il binding di un legante marcato è misurato in presenza di concentrazioni crescenti
- 44. Saturabilità – il numero di recettori è finito Reversibilità – il legame ligando-recettore non è covalente
- 45. Recettori accoppiati a proteine G Definiti anche come recettori metabotropici. Costituti da unico filamento che attraversa
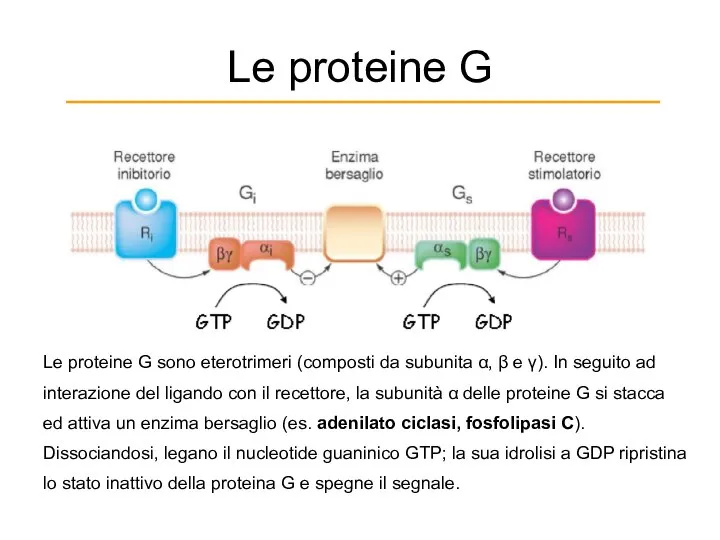
- 46. Le proteine G Le proteine G sono eterotrimeri (composti da subunita α, β e γ). In
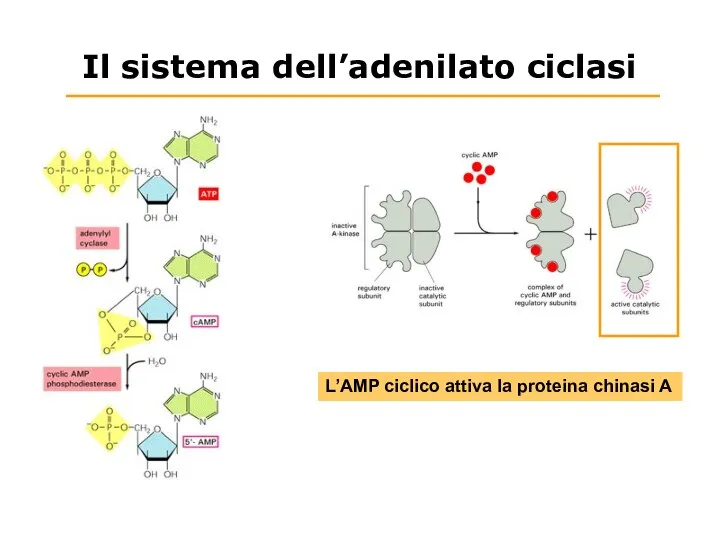
- 47. Il sistema dell’adenilato ciclasi L’AMP ciclico attiva la proteina chinasi A
- 48. Il sistema della fosfolipasi C La fosfolipasi C scinde il PIP3 a DAG ed inositolo tri
- 51. Скачать презентацию




























 Trouble Shooting Guide <Hardware Issues>
Trouble Shooting Guide <Hardware Issues> Ржев – город воинской славы
Ржев – город воинской славы День педагога. Зі святом. дорогі колеги
День педагога. Зі святом. дорогі колеги
 Wigilia bożego narodzeniaWigilia Bożego Narodzenia
Wigilia bożego narodzeniaWigilia Bożego Narodzenia 20151117_usloviya_prorastaniya_semyan
20151117_usloviya_prorastaniya_semyan Своя игра. Веков минувших достояние…
Своя игра. Веков минувших достояние… Foundmate помоги себе и другим
Foundmate помоги себе и другим Изготовление декоративной вазы для карандашей и кисточек (из подручных материалов)
Изготовление декоративной вазы для карандашей и кисточек (из подручных материалов) Конструкции гражданских зданий
Конструкции гражданских зданий Неорганические вяжущие вещества. Лекция №8
Неорганические вяжущие вещества. Лекция №8 бизнес план
бизнес план Індуїзм. Храм
Індуїзм. Храм Схема Медведевского ДК
Схема Медведевского ДК Going shopping
Going shopping Тесты Фармакология спорта
Тесты Фармакология спорта Определение содержания ионов меди и железа в различных фракциях крови в норме и при патологии(ССЗ)
Определение содержания ионов меди и железа в различных фракциях крови в норме и при патологии(ССЗ) Подготовка инструмента к работе
Подготовка инструмента к работе Рисунок, геометрические фигуры
Рисунок, геометрические фигуры Lead the way!
Lead the way! 20170211_prilozhenie_no2
20170211_prilozhenie_no2 Закрепление изученного. Что узнали. Чему научились
Закрепление изученного. Что узнали. Чему научились Продукция НЛМК
Продукция НЛМК Детский совет в ДОУ по ФГОС
Детский совет в ДОУ по ФГОС листание 8
листание 8 c794b18c6edbeb069a3764451eb9c0a0
c794b18c6edbeb069a3764451eb9c0a0 Шаблон проекта. Территория 2020
Шаблон проекта. Территория 2020 Проект размера рубок ухода в сосновых лесах ГЛХУ Щучинский лесхоз с использованием ГИС-технологий
Проект размера рубок ухода в сосновых лесах ГЛХУ Щучинский лесхоз с использованием ГИС-технологий