Содержание
- 2. ЭНТРОПИЯ. ВТОРОЕ И ТРЕТЬЕ НАЧАЛА ТЕРМОДИНАМИКИ Приведенная теплота. Энтропия Изменение энтропии 3. Поведение энтропии в процессах
- 3. 1. Приведенная теплота. Энтропия Равные между собой отношения теплот к температурам, при которых они были получены
- 4. Отношение теплоты Q в изотермическом процессе к температуре, при которой происходила передача теплоты, называется приведенной теплотой
- 5. Суммируя приведенную теплоту на всех участках процесса, получим: Тогда в обратимом цикле Карно имеем:
- 6. Этот результат справедлив для любого обратимого процесса. Таким образом, для процесса, происходящего по замкнутому циклу Из
- 7. Это позволяет ввести новую функцию состояния S: Функция состояния, полный дифференциал которой равен , называется энтропией.
- 8. Понятие энтропии было впервые введено Рудольфом Клаузиусом в 1865 г. Для обратимых процессов изменение энтропии: -
- 9. Клаузиус Рудольф Юлиус Эмануэль (1822 – 1888) – немецкий физик-теоретик, один из создателей термодинамики и кинетической
- 10. В 1850 г. получил общие соотношения между теплотой и механической работой (первое начало термодинамики) и разработал
- 11. 2. Изменение энтропии в изопроцессах Энтропия системы является функцией ее состояния, определенная с точностью до произвольной
- 12. Таким образом, по этой формуле можно определить энтропию лишь с точностью до аддитивной постоянной, т.е. начало
- 13. Изменение энтропии ΔS1→2 идеального газа при переходе его из состояния 1 в состояние 2 не зависит
- 14. 3. Поведение энтропии в процессах изменения агрегатного состояния Существует три агрегатных состояния: твердое, жидкое и газообразное
- 15. 1. Переход вещества из твердого состояния (фазы) в жидкое называется плавлением, а обратный – кристаллизация. 2.
- 16. 4. Закон плавления: количество тепла ∂Q, которое необходимо для плавления вещества массой dm, пропорционально этой массе:
- 17. Этот закон справедлив и для кристаллизации, правда, с одним отличием: ∂Q в этом случае – тепло
- 18. Изменение энтропии в процессе этого фазового перехода можно найти просто, если считать процесс равновесным. Это вполне
- 19. Тогда можно использовать термодинамический смысл энтропии: с точки зрения термодинамики энтропия – это такая функция состояния
- 20. Так как температура системы в данном фазовом переходе не меняется и равна температуре плавления, то подынтегральное
- 21. Из этой формулы следует, что при плавлении энтропия возрастает, а при кристаллизации уменьшается. Физический смысл этого
- 22. Поэтому при равной температуре энтропия твердого тела меньше энтропии жидкости. Это означает, что твердое тело представляет
- 23. Фазовый переход «жидкость – газ» Этот переход обладает всеми свойствами перехода «твердое тело – жидкость». Существует
- 24. 2: при испарении система поглощает тепло, при конденсации – теряет. 3: процессы испарения и конденсации протекают
- 25. В процессе фазового перехода «жидкость – газ» температура остается постоянной и равной температуре кипения до тех
- 26. Коэффициент пропорции r в этом выражении, есть константа, зависящая от вещества системы, называемая удельной теплотой испарения.
- 27. Изменение энтропии в этом процессе можно найти просто, считая процесс равновесным. И опять это вполне допустимое
- 28. Из формулы следует, что при испарении энтропия возрастает, а при конденсации уменьшается.
- 29. Физический смысл этого результата состоит в различии фазовой области молекулы в жидкости и газе. Хотя в
- 30. занятой жидкостью, но не имеет возможности «оторваться от коллектива» остальных молекул: стоит ей оторваться от одной
- 31. Молекулы газа ведут себя иначе. У них гораздо больше свободы, среднее расстояние между ними таково, что
- 32. Поэтому при равных температурах фазовая область молекул газа значительно больше фазовой области молекул жидкости, и энтропия
- 33. 4. Изменения энтропии при обратимых и необратимых процессах Итак, энтропия – отношение полученной или отданной системой
- 34. Обратимый цикл Карно В тепловой машине, работающей по принципу Карно, имеются три тела: холодильник, нагреватель, рабочее
- 35. или Это неравенство Клаузиуса. При любом необратимом процессе в замкнутой системе энтропия возрастает (dS > 0).
- 36. Тогда для замкнутой системы – математическая запись второго начала термодинамики. Для произвольного процесса, где, знак равенства
- 37. 5. Второе начало термодинамики Термодинамика, это наука о тепловых процессах, о превращении тепловой энергии. Для описания
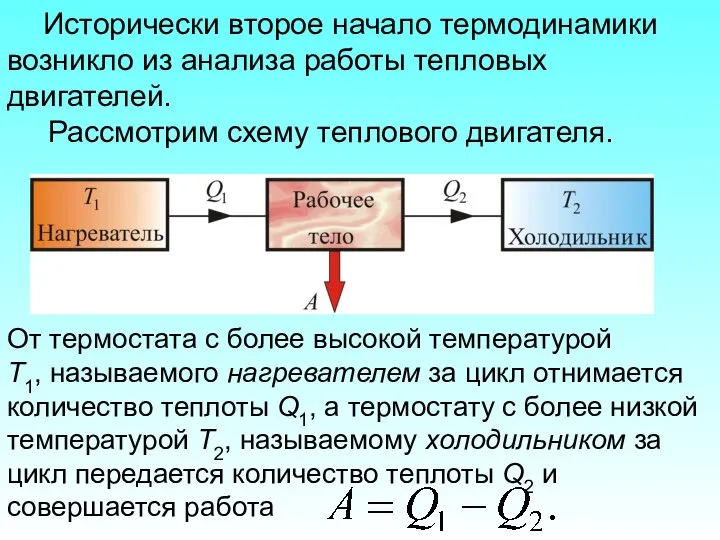
- 38. Исторически второе начало термодинамики возникло из анализа работы тепловых двигателей. Рассмотрим схему теплового двигателя. От термостата
- 40. Чтобы термический коэффициент полезного действия теплового двигателя был , должно быть выполнено условие , т.е. тепловой
- 41. 1. Невозможен процесс, единственным результатом которого является превращение всей теплоты, полученной от нагревателя в эквивалентную ей
- 42. Математической формулировкой второго начала является выражение Энтропия замкнутой системы при любых происходивших в ней процессах не
- 43. При обратимомном процессе При необратимом процессе, как доказал Клаузиус − изменение энтропии больше приведенной теплоты. Тогда
- 44. Первое и второе начала термодинамики в объединенной форме имеют вид:
- 45. 6. Свободная и связанная энергии Как следует из первого и второго начала термодинамики в объединенной форме
- 46. Обозначим, , где F – разность двух функций состояний, поэтому сама является также функцией состояния. Ее
- 47. следовательно свободная энергия есть та работа, которую могло бы совершить тело в обратимом изотермическом процессе или,
- 48. Связанная энергия – та часть внутренней энергии, которая не может быть превращена в работу – это
- 49. В термодинамике есть еще понятие – энергетическая потеря в изолированной системе
- 50. При любом необратимом процессе энтропия увеличивается до того, пока не прекратятся какие-либо процессы, т.е. пока не
- 51. Макросостояние – это состояние вещества, характеризуемое его термодинамическими параметрами. Состояние же системы, характеризуемое состоянием каждой входящей
- 52. Термодинамической вероятностью или статистическим весом макросостояния W − называется число микросостояний, осуществляющих данное макросостояние (или число
- 53. В состоянии равновесия в термодинамике и вероятность максимальна и энтропия максимальна. Из этого можно сделать вывод,
- 54. Энтропия – вероятностная статистическая величина. Утверждение о возрастании энтропии потеряло свою категоричность. Её увеличение вероятно, но
- 55. Российские физики Я.Б. Зельдович и И.Д. Новиков, так же опровергли эту теорию, и показали, что Р.
- 56. 7. Третье начало термодинамики Недостатки первого и второго начал термодинамики в том, что они не позволяют
- 57. Нернст Вальтер Фридрих Герман (1864 – 1941) – немецкий физик и физико- химик, один из основоположников
- 58. Согласно Нернсту, изменение энтропии ΔS стремится к нулю при любых обратимых изотермических процессах, совершаемых между двумя
- 59. Как первое и второе начала термодинамики, теорема Нернста может рассматриваться как результат обобщения опытных фактов, поэтому
- 60. Отсюда следует, что при T → 0 интеграл сходится на нижнем пределе, т.е. имеет конечное значение
- 61. При T = 0, внутренняя энергия и тепловая функция системы прекращают зависеть от температуры, кроме того,
- 62. Третье начало термодинамики иногда формулируют следующим образом: при абсолютном нуле температуры любые изменения термодинамической системы происходят
- 63. Принцип Нернста был развит Планком, предположившим, что при абсолютном нуле температуры энергия системы минимальна (но не
- 65. Скачать презентацию





























































 Классификация схем совмещения литья и прокатки
Классификация схем совмещения литья и прокатки !!! САЙТ выпуск 2019
!!! САЙТ выпуск 2019 Гордость - чувство собственного достоинства
Гордость - чувство собственного достоинства Методы измерения температуры при испытаниях
Методы измерения температуры при испытаниях Маршруты создания ИС. Технология изготовления КМОП схем с p-карманом
Маршруты создания ИС. Технология изготовления КМОП схем с p-карманом Презентация Государственное регулирование внутреннего и внешнего долга
Презентация Государственное регулирование внутреннего и внешнего долга Конструкктор классный уголок
Конструкктор классный уголок Экономические и правовые основы предпринимательства
Экономические и правовые основы предпринимательства  Презентация Привлечение иностранных инвестиций
Презентация Привлечение иностранных инвестиций  Закон о создании дополнительных условий для расселения граждан из жилых помещений в домах, признанных аварийными
Закон о создании дополнительных условий для расселения граждан из жилых помещений в домах, признанных аварийными Политический конфликт
Политический конфликт Deutsche autos
Deutsche autos Стиль богатых девушек. Дресскоды
Стиль богатых девушек. Дресскоды Культура архаической Греции
Культура архаической Греции Свято-Троицкий женский монастырь города Муром
Свято-Троицкий женский монастырь города Муром Ноосфера В.И. Вернадского
Ноосфера В.И. Вернадского наложение ареста на почтово-телеграфные отправления, их осмотр и выемка
наложение ареста на почтово-телеграфные отправления, их осмотр и выемка Przeznaczenie
Przeznaczenie Урок алгебры в 8 классе - презентация по Алгебре
Урок алгебры в 8 классе - презентация по Алгебре Жан Батист Ламарк
Жан Батист Ламарк AutoCAD. Примеры работ. Расписание занятий
AutoCAD. Примеры работ. Расписание занятий Нижегородский Кремль- чудо России!!! Над проектом работали: Башкурова Диана Юрина Екатерина Платонова Анастасия Рылова Анастаси
Нижегородский Кремль- чудо России!!! Над проектом работали: Башкурова Диана Юрина Екатерина Платонова Анастасия Рылова Анастаси Урок2 среды обитания
Урок2 среды обитания Інженерія якості. Ядро професійних знань
Інженерія якості. Ядро професійних знань Макроэкономическое равновесие на товарном рынке. Кейнсианская модель доходов и расходов.
Макроэкономическое равновесие на товарном рынке. Кейнсианская модель доходов и расходов. Искусство Древней Греции Афинский Акрополь
Искусство Древней Греции Афинский Акрополь  Действия над обыкновенными дробями - презентация по Алгебре_
Действия над обыкновенными дробями - презентация по Алгебре_ Геодезист
Геодезист