Содержание
- 2. План 5.1. Реакции SE для бензоидных ароматических соединений 5.2. Ориентирующее влияние заместителей 5.3. Реакции SE в
- 3. Электрофильное замещение при атоме углерода в sp2-гибридизации наиболее характерно для ароматических соединений 5.1. Реакции SE для
- 4. Соединения с двойными связями неароматического характера гораздо легче вступают в реакции электрофильного присоединения, чем замещения
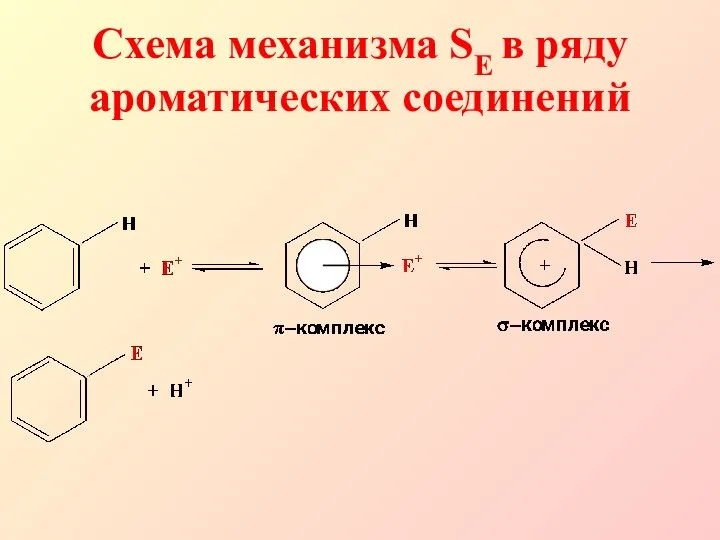
- 5. Схема механизма SE в ряду ароматических соединений
- 6. Электрофильное замещение в ароматическом ряду начинается с атаки π-электронной системы ароматического кольца электрофильной частицей (для этого
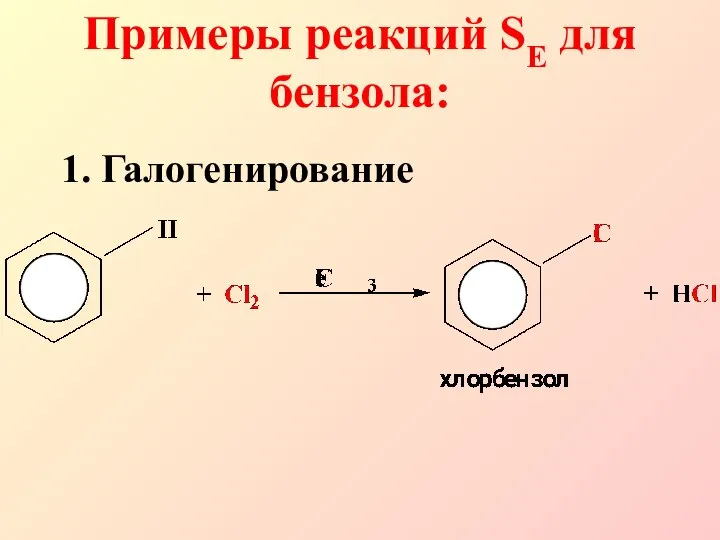
- 7. 1. Галогенирование Примеры реакций SE для бензола:
- 8. В качестве электрофила выступает либо комплекс галогена с кислотой Льюиса (FeCl3), либо катион, образующийся в результате
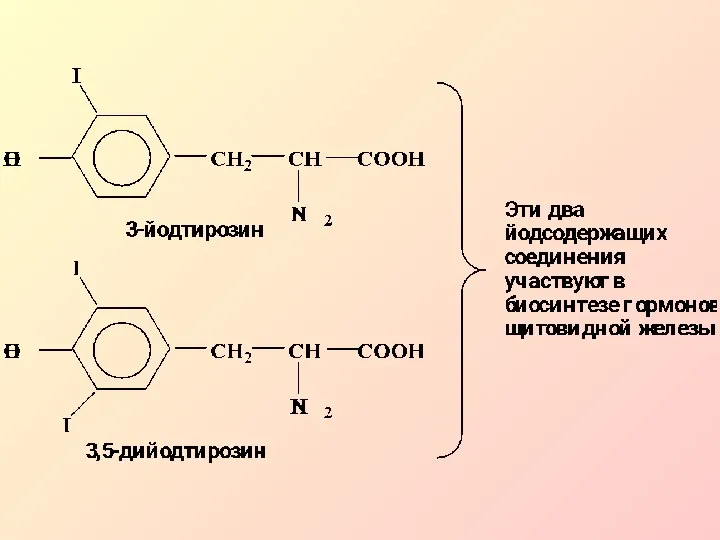
- 9. В организме по механизму SЕ протекает очень важная реакция иодирования. Гормоны щитовидной железы имеют в своем
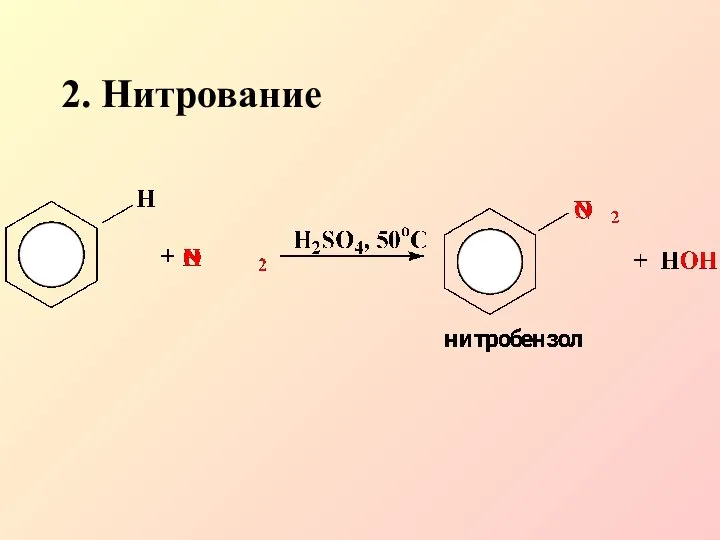
- 11. 2. Нитрование
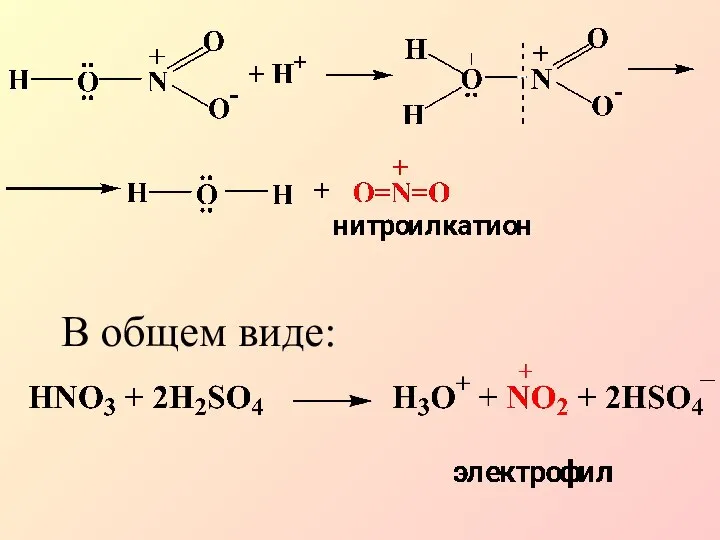
- 12. В общем виде:
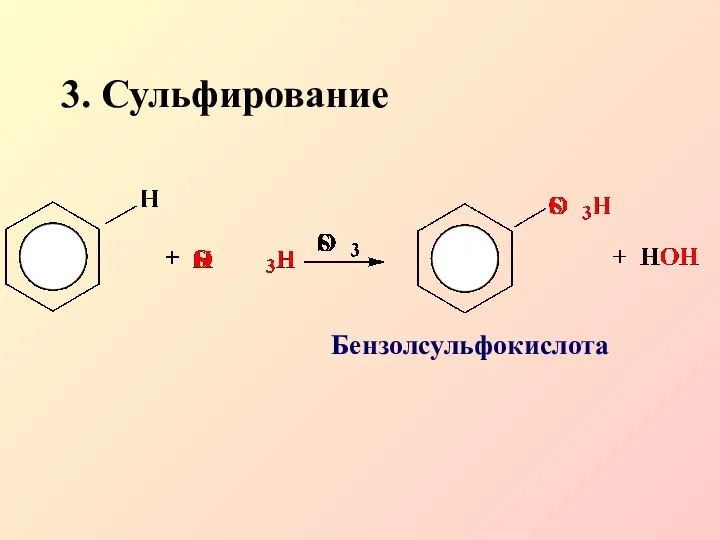
- 13. 3. Сульфирование Бензолсульфокислота
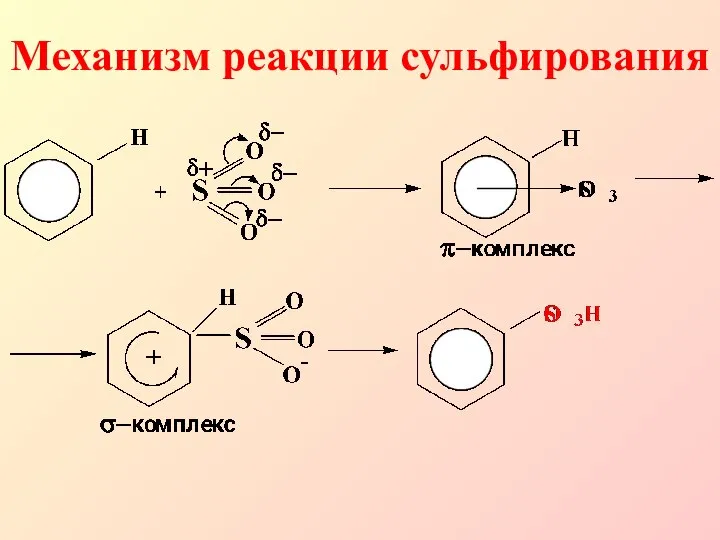
- 14. Механизм реакции сульфирования
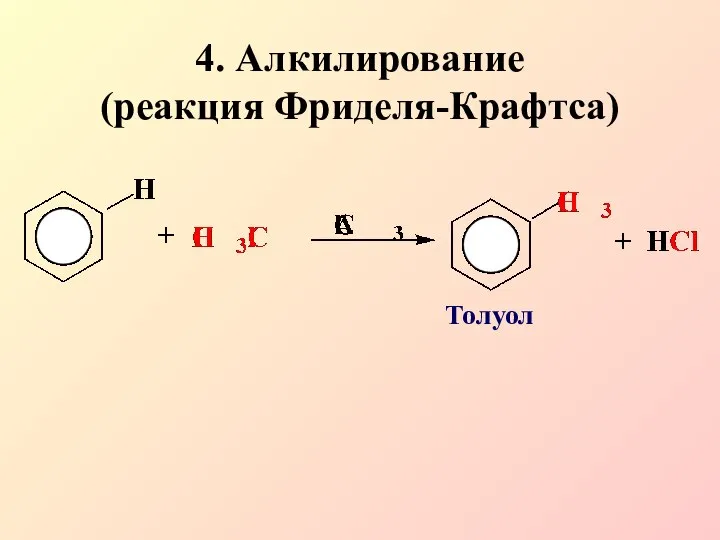
- 15. 4. Алкилирование (реакция Фриделя-Крафтса) Толуол
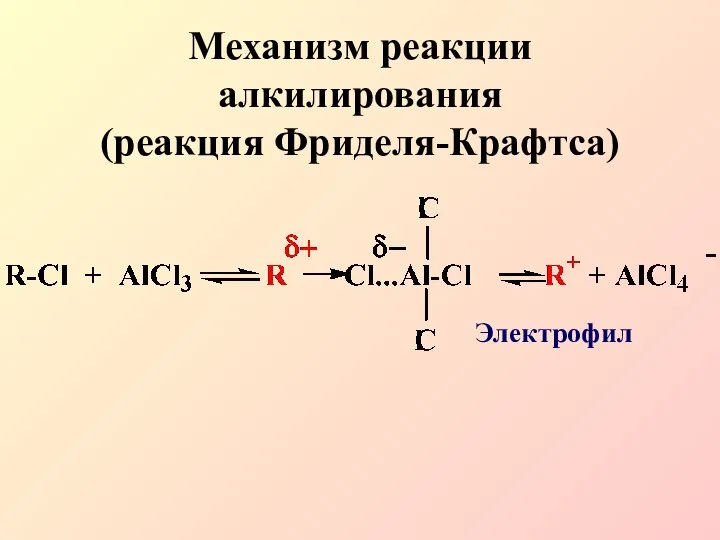
- 16. Механизм реакции алкилирования (реакция Фриделя-Крафтса) Электрофил
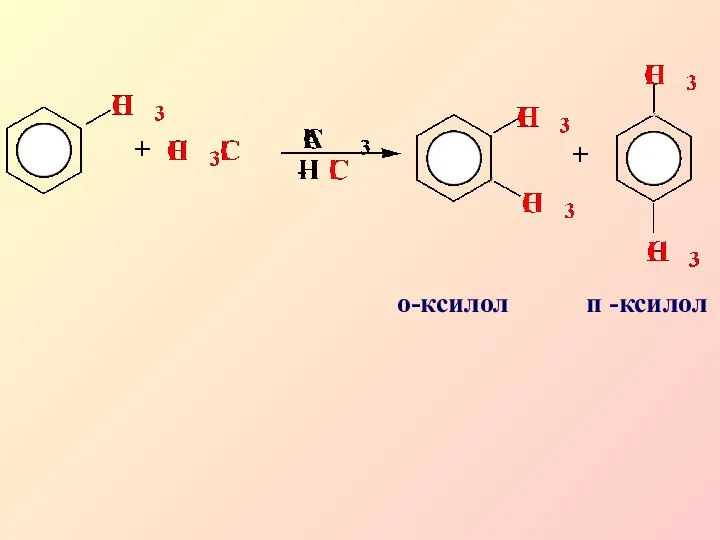
- 17. о-ксилол п -ксилол
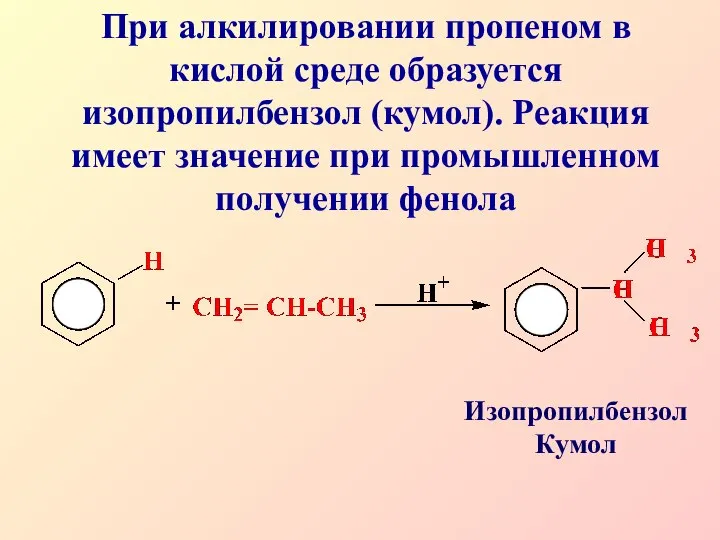
- 18. При алкилировании пропеном в кислой среде образуется изопропилбензол (кумол). Реакция имеет значение при промышленном получении фенола
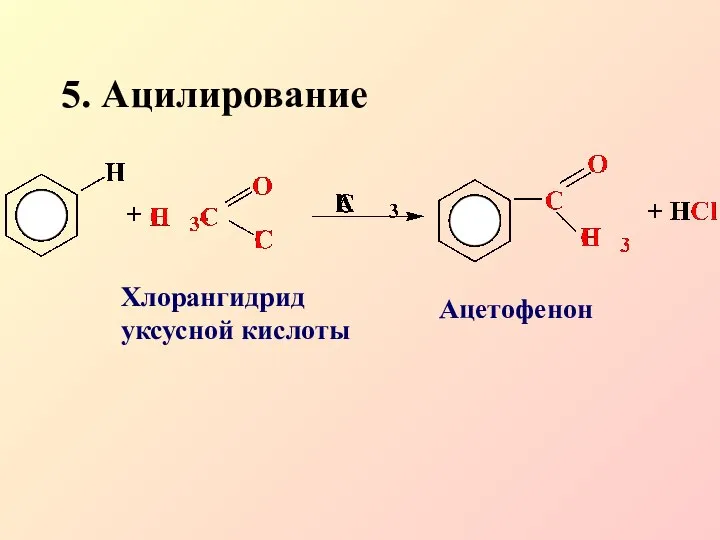
- 19. 5. Ацилирование Хлорангидрид уксусной кислоты Ацетофенон
- 20. 5.2. Ориентирующее влияние заместителей Заместители делят на две группы:
- 21. 1. Ориентанты I-рода, электронодонорные заместители алкильные группы, проявляющие +I эффект и группы, проявляющие +М эффект: –ОН;
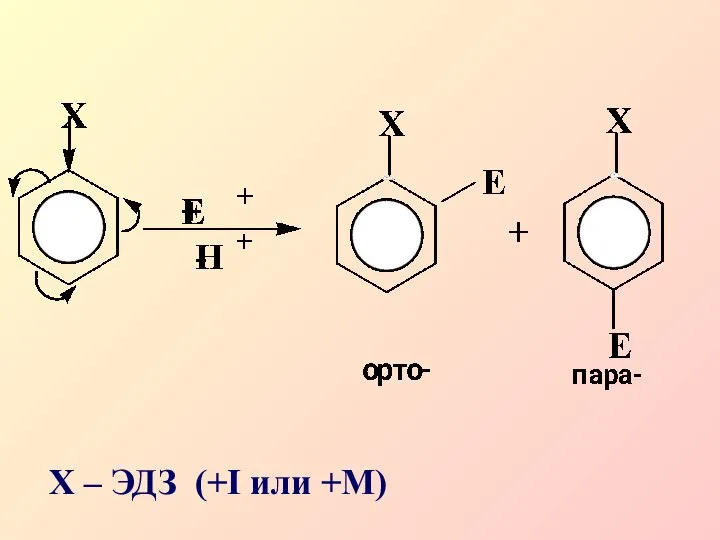
- 22. Заместители I рода облегчают электрофильное замещение по сравнению с незамещенным бензолом и направляют новые заместители в
- 23. Х – ЭДЗ (+I или +M)
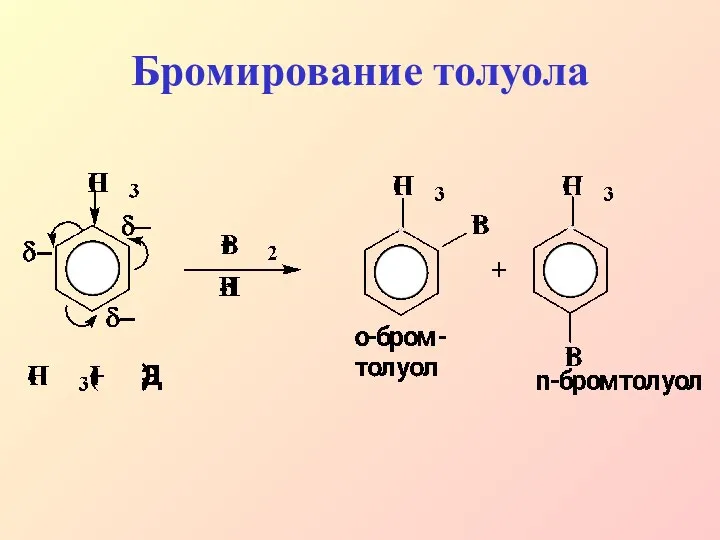
- 24. Бромирование толуола
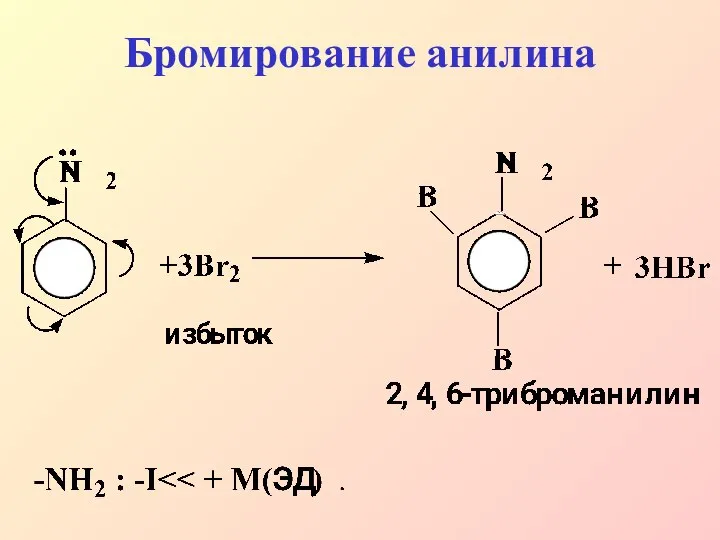
- 25. Бромирование анилина
- 26. 2.Ориентанты II рода, электроноакцепторные заместители проявляют –I и –М эффекты: –NO2; –SO3H; –CN; –CHO; –COOH
- 27. Заместители II рода затрудняют реакции электрофильного замещения по сравнению с незамещенным бензолом, причем входящая группа вступает
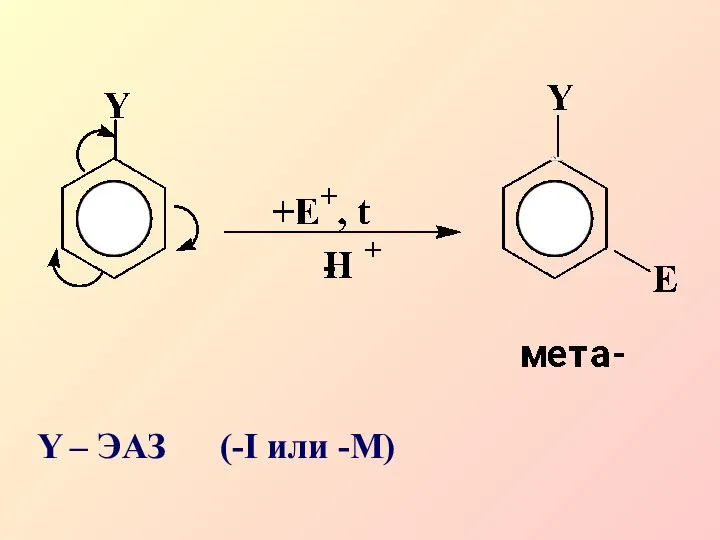
- 28. Y – ЭАЗ (-I или -M)
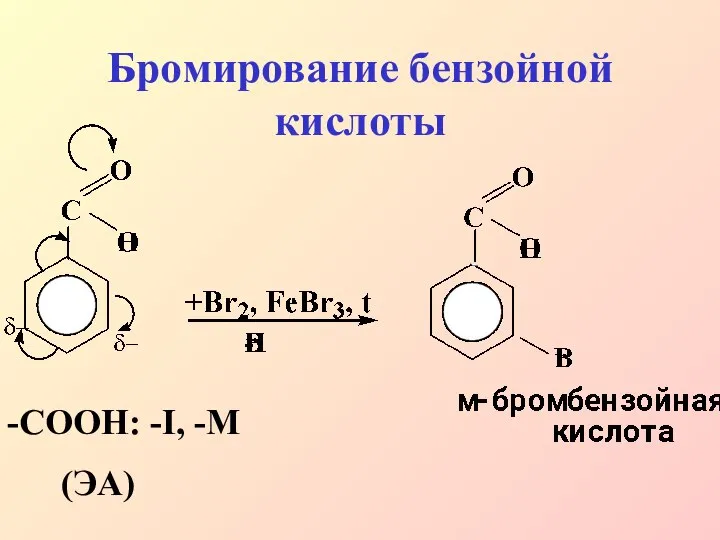
- 29. Бромирование бензойной кислоты -СООН: -I, -M (ЭА)
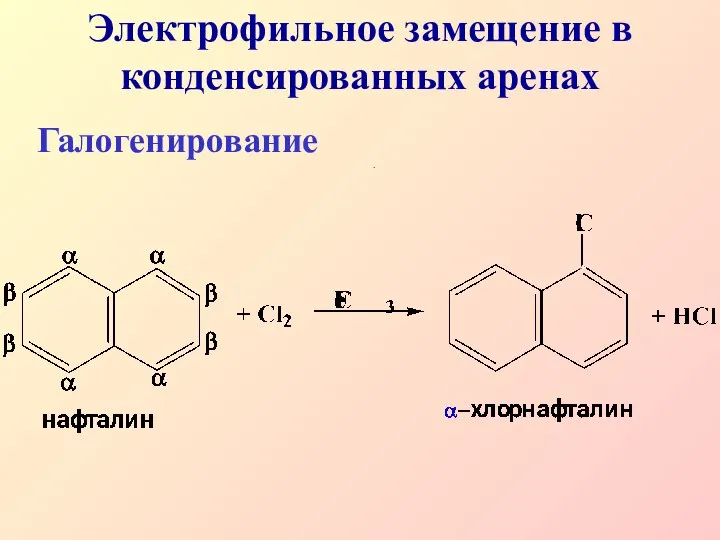
- 30. Электрофильное замещение в конденсированных аренах Галогенирование .
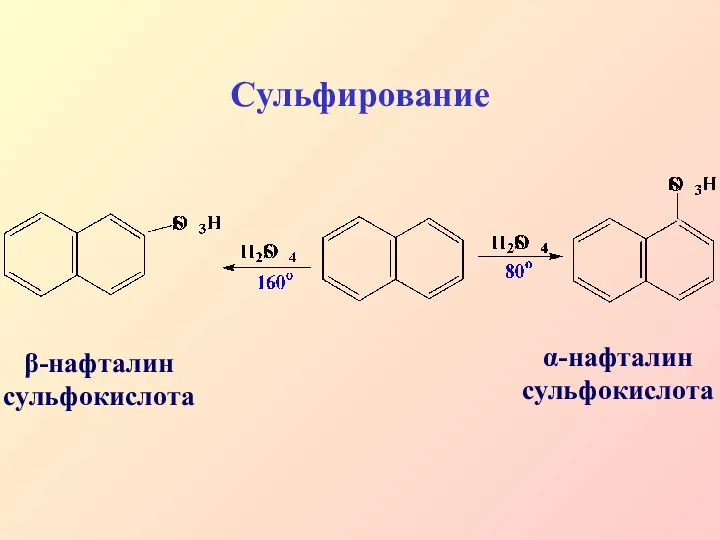
- 31. Сульфирование α-нафталин сульфокислота β-нафталин сульфокислота
- 32. 5.3. Реакции SE в гетероциклических соединениях . Гетероатомы в ароматических системах могут оказывать активирующее (пиррол, фуран,
- 33. Пиррол, фуран и тиофен по сравнению с бензолом являются π-избыточными (суперарома-тическими системами), следствием этого является их
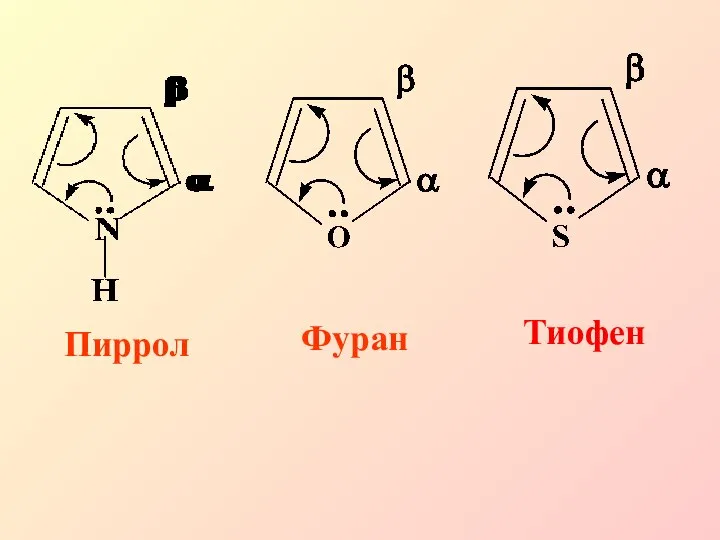
- 34. Пиррол Фуран Тиофен
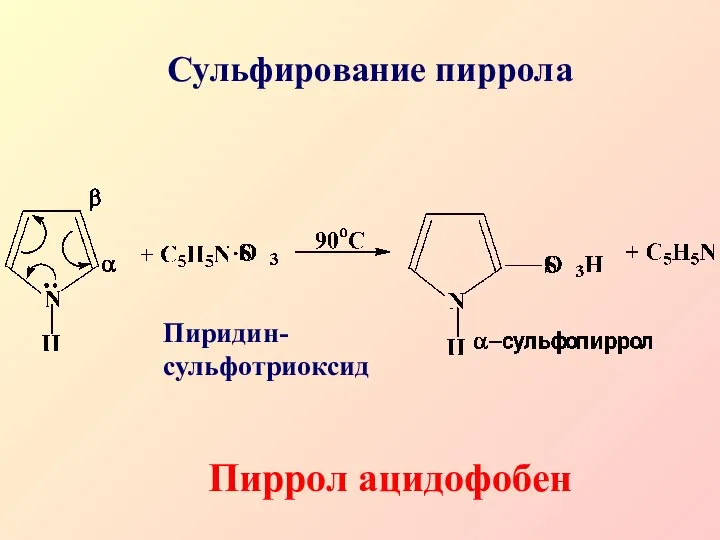
- 35. Сульфирование пиррола Пиридин- сульфотриоксид Пиррол ацидофобен
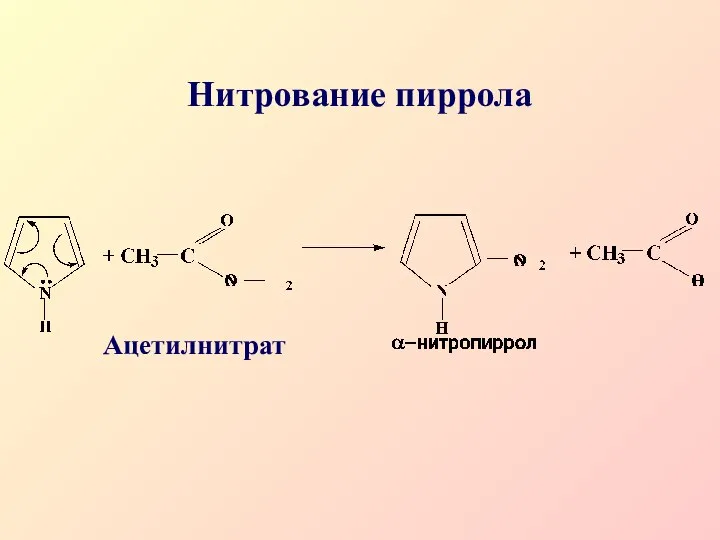
- 36. Нитрование пиррола Ацетилнитрат
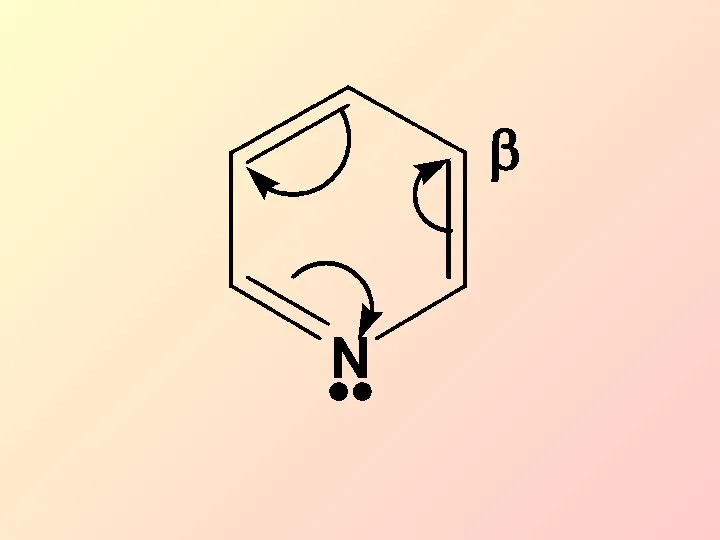
- 37. Пиридин является π-недостаточной ароматической системой. Общая электронная плотность в ароматическом кольце понижена по сравнению с бензолом
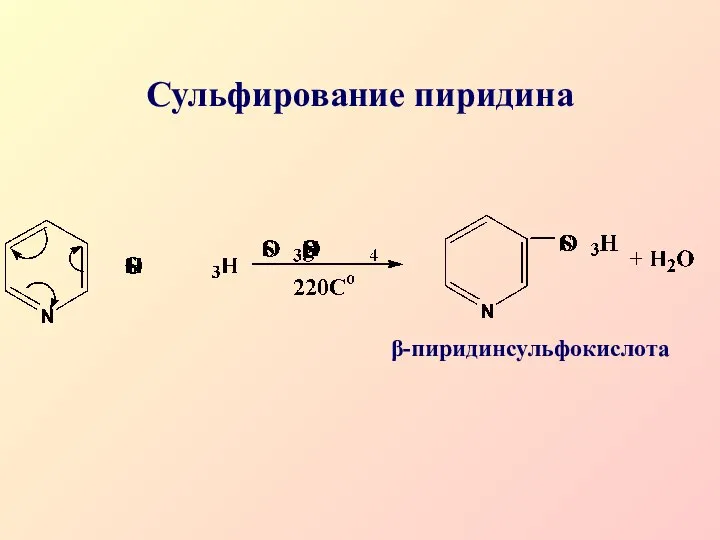
- 39. Сульфирование пиридина β-пиридинсульфокислота
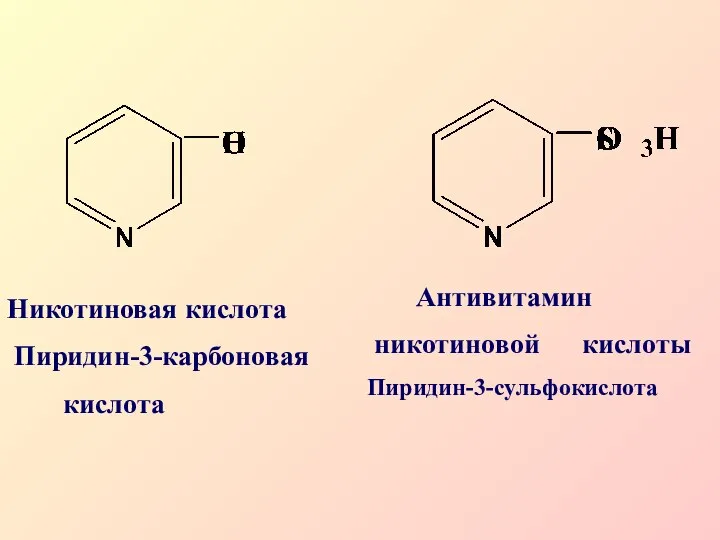
- 40. Никотиновая кислота Пиридин-3-карбоновая кислота Антивитамин никотиновой кислоты Пиридин-3-сульфокислота
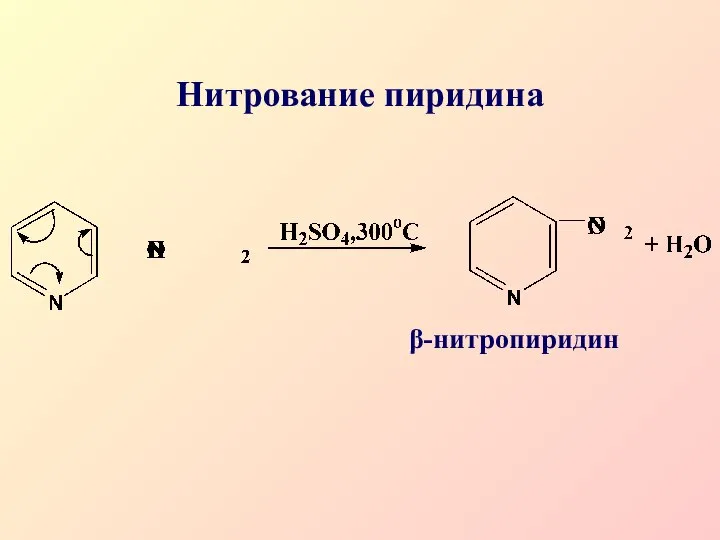
- 41. Нитрование пиридина β-нитропиридин
- 43. Скачать презентацию













 Древний Китай
Древний Китай История понятия государство. Теории возникновения государства. Основные признаки государства
История понятия государство. Теории возникновения государства. Основные признаки государства Презентація на тему Георг Сімон Ом
Презентація на тему Георг Сімон Ом Презентация Театр в 18 веке в Росиии
Презентация Театр в 18 веке в Росиии Внеклассное мероприятие в начальной школе - презентация для начальной школы
Внеклассное мероприятие в начальной школе - презентация для начальной школы Работа с базами данных
Работа с базами данных Министерство транспорта РФ
Министерство транспорта РФ «Банкир – это центральная фигура. Он держит на своих плечах весь мир.» Герберт Кэссон
«Банкир – это центральная фигура. Он держит на своих плечах весь мир.» Герберт Кэссон Разработка метеостанции на базе ATmega8 для измерения влажности, давления и CO2
Разработка метеостанции на базе ATmega8 для измерения влажности, давления и CO2 Подростковый возраст материалы для родительского собрания
Подростковый возраст материалы для родительского собрания Doping problem in sports. (Lecture 8)
Doping problem in sports. (Lecture 8) МБОУ «СОШ№12» г. Байкальск Внеклассное мероприятие По изобразительному искусству 8 класс Учитель : Грищенко Наталья Константино
МБОУ «СОШ№12» г. Байкальск Внеклассное мероприятие По изобразительному искусству 8 класс Учитель : Грищенко Наталья Константино Презентация Переход к Новой экономической политике
Презентация Переход к Новой экономической политике  Ландшафтный дизайн. Дренаж, декоративные покрытия дорожек
Ландшафтный дизайн. Дренаж, декоративные покрытия дорожек Грек-латын дублеттері
Грек-латын дублеттері Компьютер своими руками
Компьютер своими руками Износ основных фонов
Износ основных фонов Организация производства и продаж прибора для неинвазивного (чрезкожного) мониторинга содержания сахара в крови человека
Организация производства и продаж прибора для неинвазивного (чрезкожного) мониторинга содержания сахара в крови человека Индивидуализация и дифференциация обучения в современной школе. Методическая тема учителя русского языка и литературы МОУ СОШ
Индивидуализация и дифференциация обучения в современной школе. Методическая тема учителя русского языка и литературы МОУ СОШ  Числовые и символьные массивы
Числовые и символьные массивы Символическое значение животных и предметов в архитектурном декоре
Символическое значение животных и предметов в архитектурном декоре Әлем. XXI ғасыр
Әлем. XXI ғасыр Финансовая грамотность
Финансовая грамотность Построение проекций плоских фигур
Построение проекций плоских фигур Особенности деловых отношений в разных культурах
Особенности деловых отношений в разных культурах Организация занятий физической культурой с учащимися медицинских групп и детей с ОВЗ
Организация занятий физической культурой с учащимися медицинских групп и детей с ОВЗ Презентация "Эффективные способы рекламы" - скачать презентации по Экономике
Презентация "Эффективные способы рекламы" - скачать презентации по Экономике Йоганнес Кеплер
Йоганнес Кеплер