Содержание
- 2. П л а н 6.1.Кислотность органичес-ких соединений 6.2.Основность органических соединений 6.3. Амфотерность органи-ческих соединений
- 3. 6.1 Кислотность органических соединений В соответствии с протолитической теорией Бренстеда Кислота-соединение, спо-собное отдавать протоны, Кислота -
- 4. Основание-соединение, способное принимать протон, Основание -акцептор протонов
- 5. Из множества функциональных групп, входящих в состав органических соединений наиболее важны в биологическом плане - группы
- 6. Многие соединения, участвующие в процессах жизнедеятельности (белки, липиды, нуклеиновые кислоты, углеводы) являются полифункциональными соединениями, т.е. проявляют
- 7. Донорами и акцепторами протонов могут быть как нейтральные молекулы, так и заряженные ионы
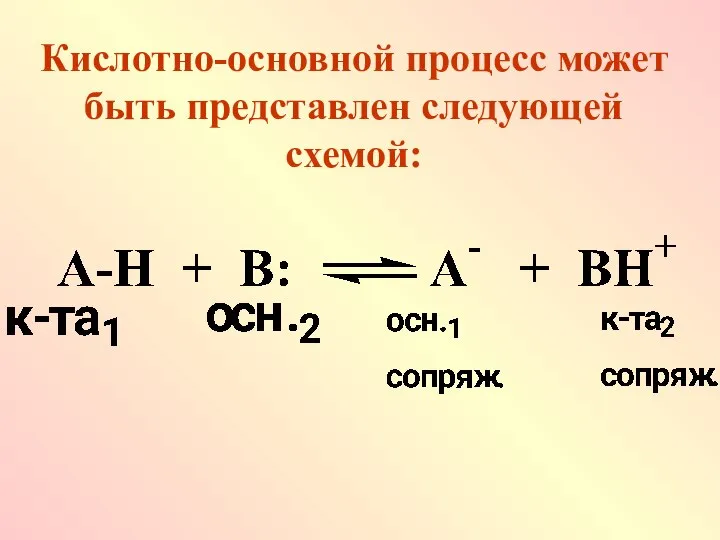
- 8. Кислотно-основной процесс может быть представлен следующей схемой:
- 9. Кислота-1 и сопряженное ей основание-1, а также основание-2 с сопряженной кислотой-2 образуют две кислотно-основные пары. В
- 10. Кислотность и основность - понятия относительные, эти свойства взаимосвязаны между собой и проявляются одновременно, т.е. соединение
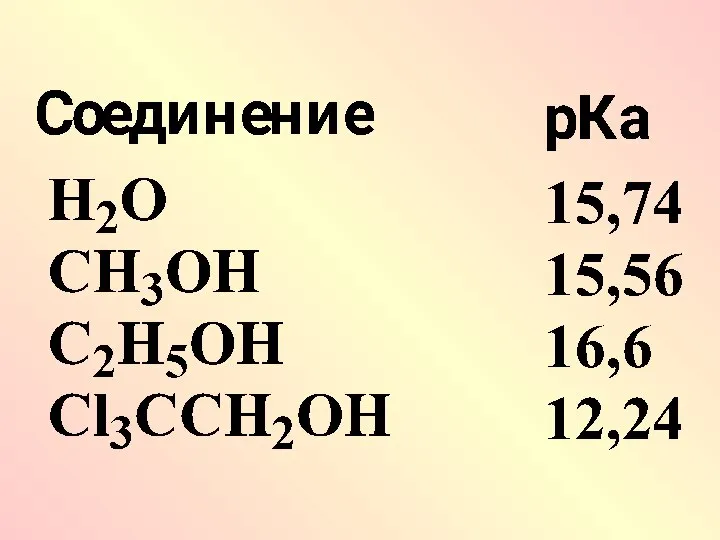
- 11. Количественно дать оценку кислот через Ка и рКа для многих биологических веществ невозможно, поэтому сравнительный анализ
- 12. Стабильность аниона определяется рядом факторов: 1. Делокализацией отрицательного заряда: чем выше степень делокализации отрицательного заряда в
- 13. 2. Электроотрицательностью элемента в кислотном центре. Чем больше электроотрицательность, тем сильнее кислотные свойства (ЭО обычно сравнивают
- 14. 3. Поляризуемостью атома в кислотном центре. Чем больше поляризуемость атома в кислотном центре, тем сильнее кислотные
- 15. 4. Сольватационные эффекты оказывают влияние на устойчивость аниона. Чем больше эффект сольватации, тем сильнее кислотные свойства
- 16. 5. Электронная природа заместителя, связанного с кислотным центром влияет на устойчивость аниона. Электроакцепторные (ЭА) заместители усиливают
- 17. Классификация кислот ОН - кислоты: карбоновые кислоты, спирты, фенолы SН - кислоты: тиолы, тиоловые кислоты NН
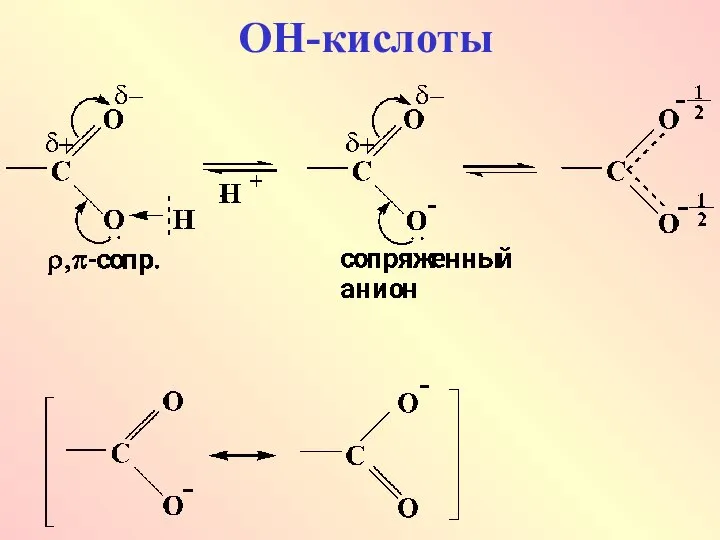
- 18. ОН-кислоты
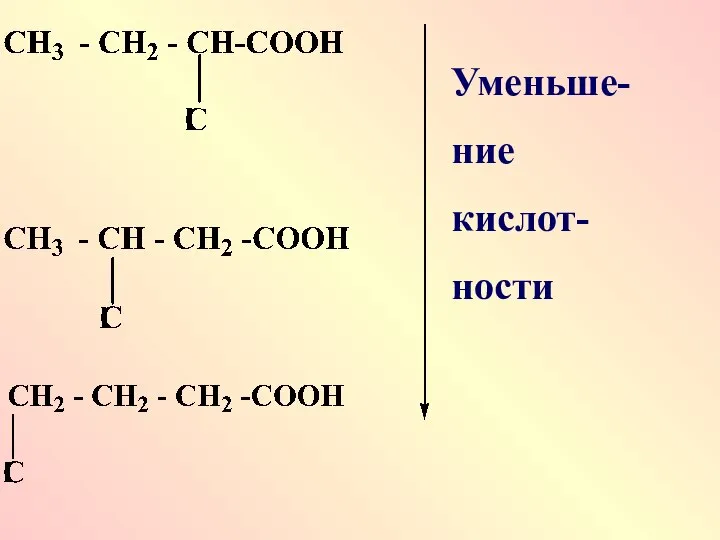
- 19. Введение электродонорных заместителей приводит к уменьшению кислотности
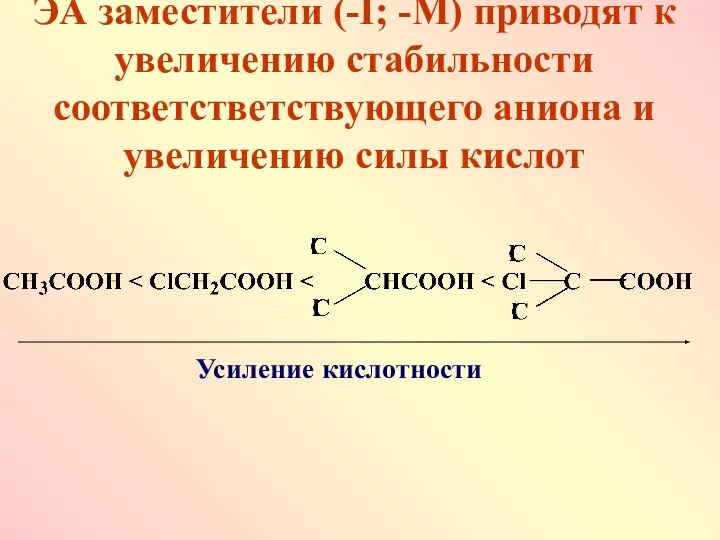
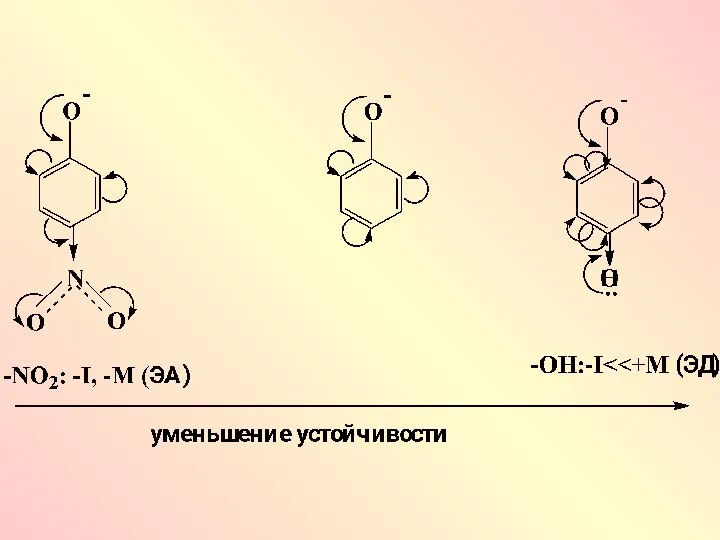
- 20. ЭА заместители (-I; -М) приводят к увеличению стабильности соответстветствующего аниона и увеличению силы кислот Усиление кислотности
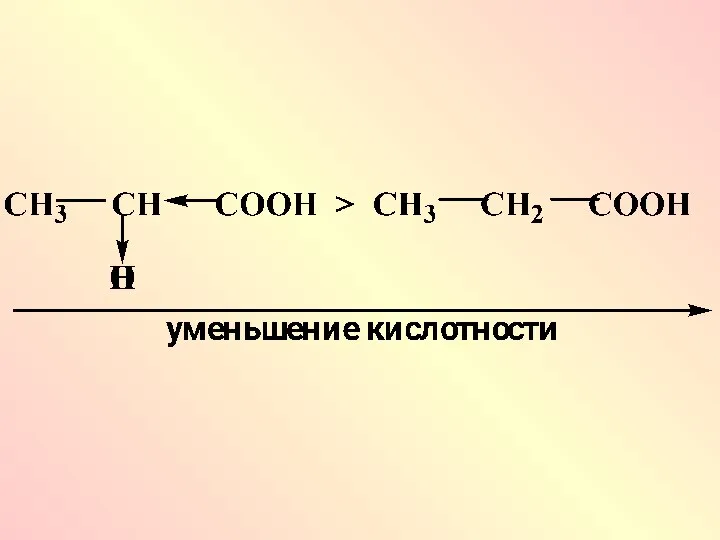
- 22. Уменьше- ние кислот- ности
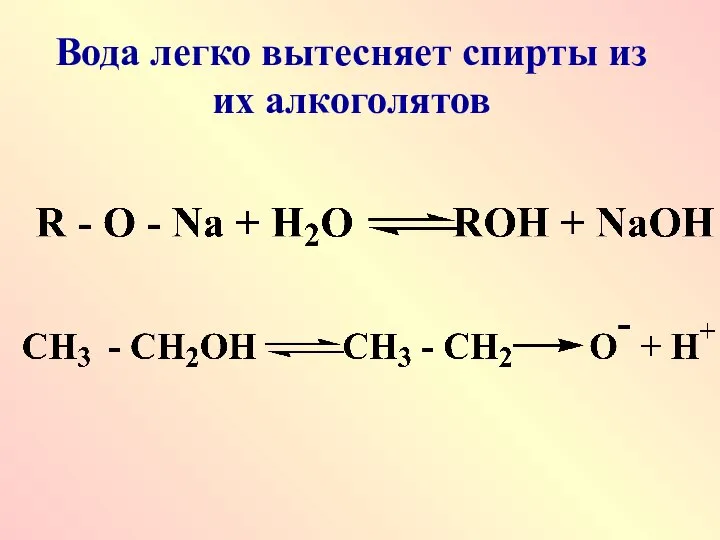
- 24. Вода легко вытесняет спирты из их алкоголятов
- 25. Слабые кислотные свойства спиртов подтверждаются реакцией с активными щелочными металлами
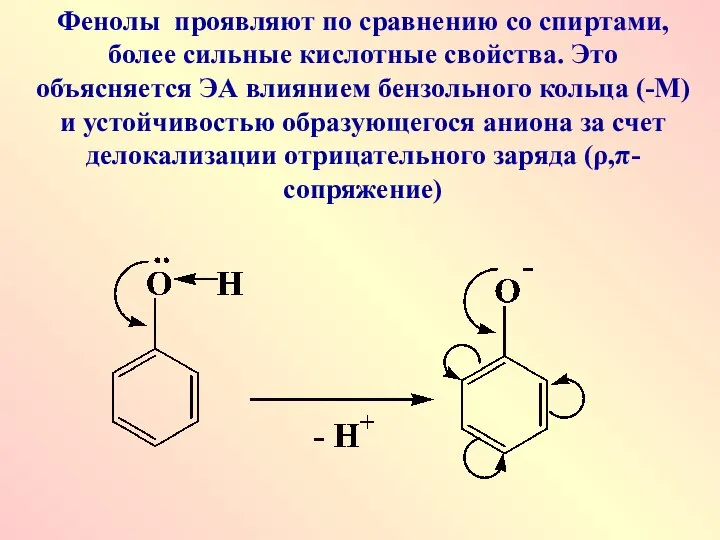
- 27. Фенолы проявляют по сравнению со спиртами, более сильные кислотные свойства. Это объясняется ЭА влиянием бензольного кольца
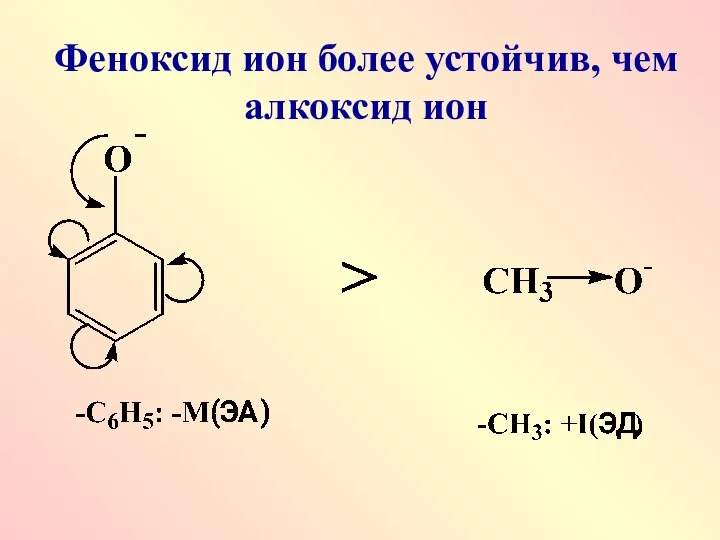
- 28. Феноксид ион более устойчив, чем алкоксид ион
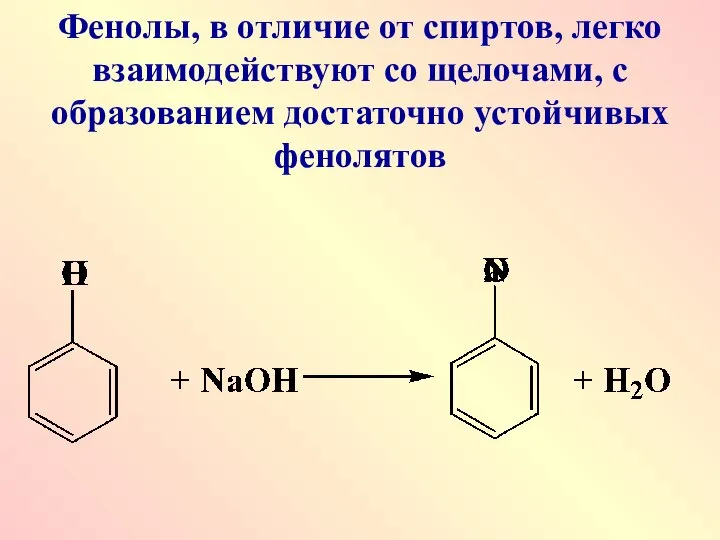
- 29. Фенолы, в отличие от спиртов, легко взаимодействуют со щелочами, с образованием достаточно устойчивых фенолятов
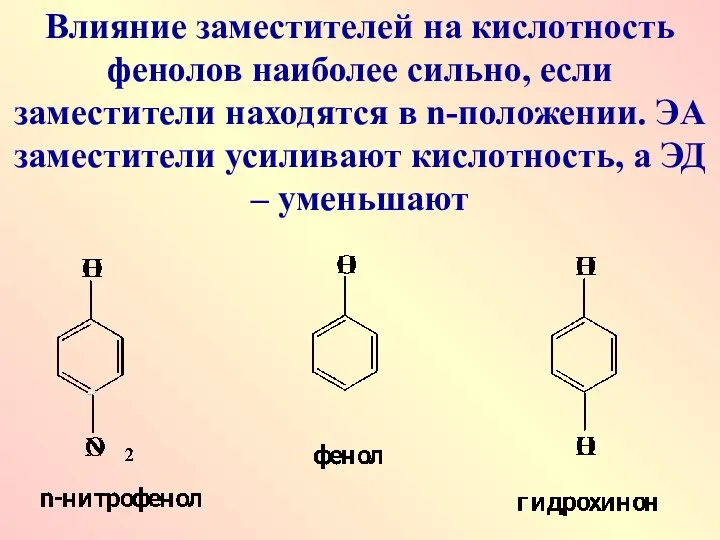
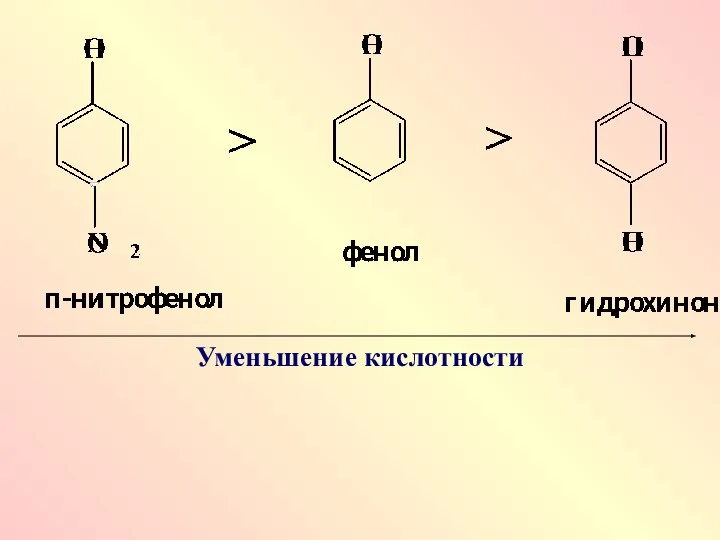
- 30. Влияние заместителей на кислотность фенолов наиболее сильно, если заместители находятся в n-положении. ЭА заместители усиливают кислотность,
- 32. Уменьшение кислотности
- 33. SH-кислоты SН-кислоты – являются более сильными кислотами по сравнению с соответствующими ОН-кислотами (спирты, фенолы). Для оценки
- 35. Тиоловые соединения – сильные кислоты, легко окисляются в организме и выполняют роль антиоксидантов, их широко используют
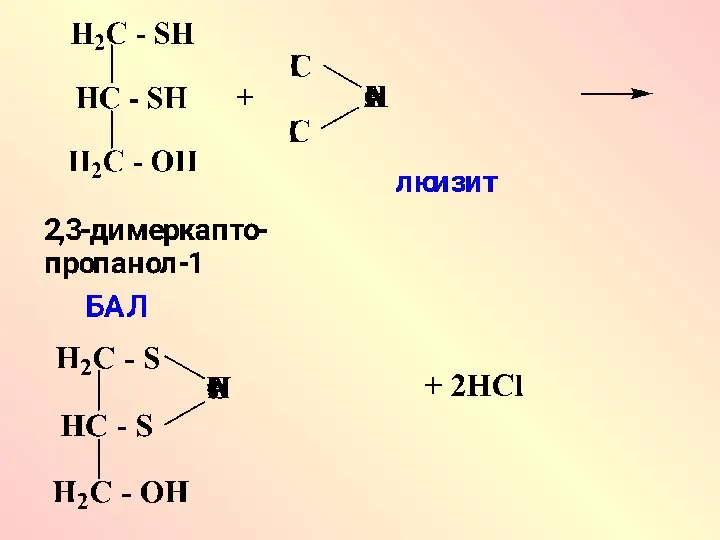
- 37. В настоящее время в лекарственной практике широко применяется унитиол для лечения острых и хронических отравлений соединениями
- 39. NH-кислоты NН-кислоты значительно слабее соответствующих ОН- и SН-кислот, что связано с меньшей ЭО азота. К NН-кислотам
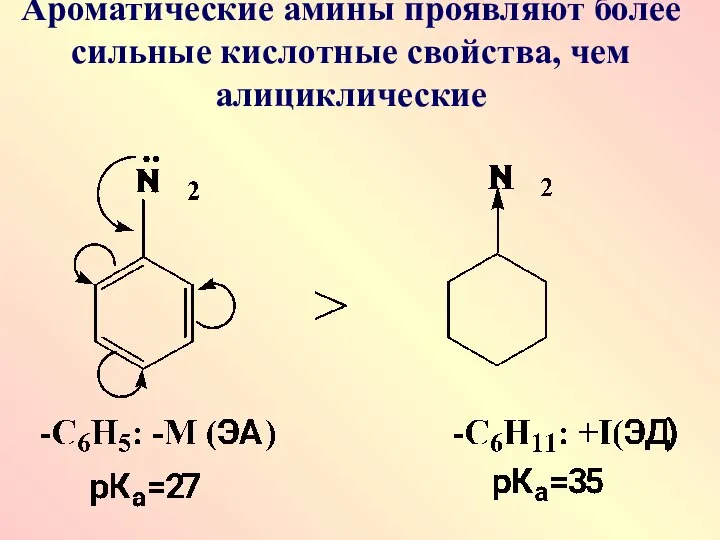
- 40. Ароматические амины проявляют более сильные кислотные свойства, чем алициклические
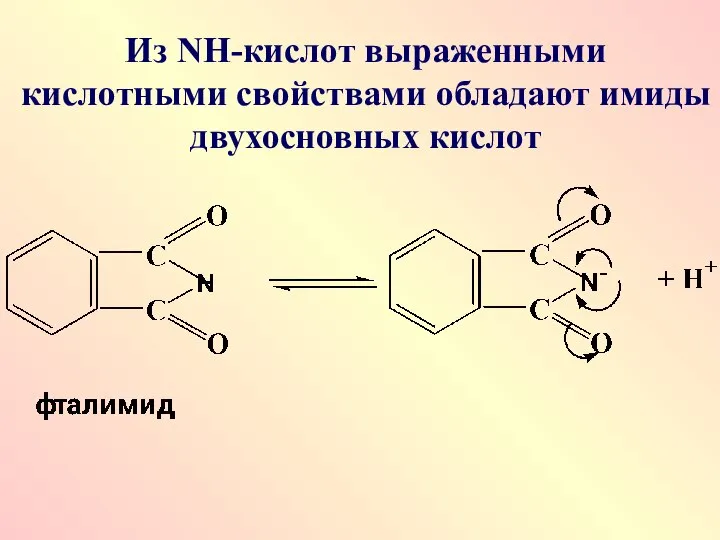
- 41. Из NН-кислот выраженными кислотными свойствами обладают имиды двухосновных кислот
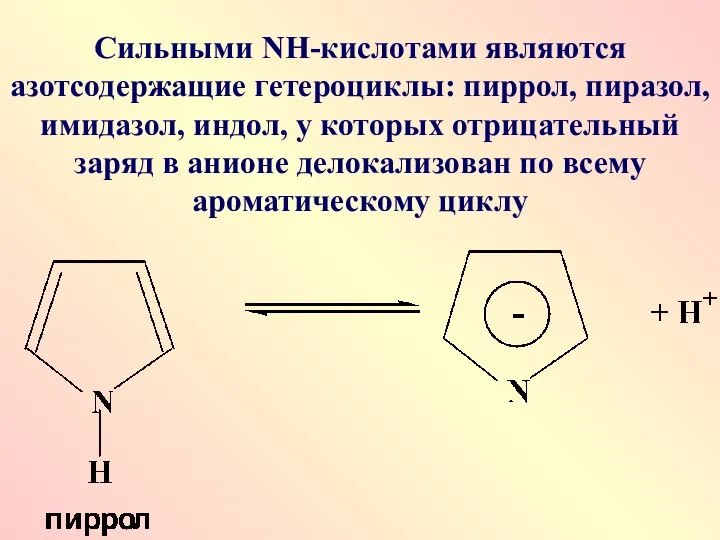
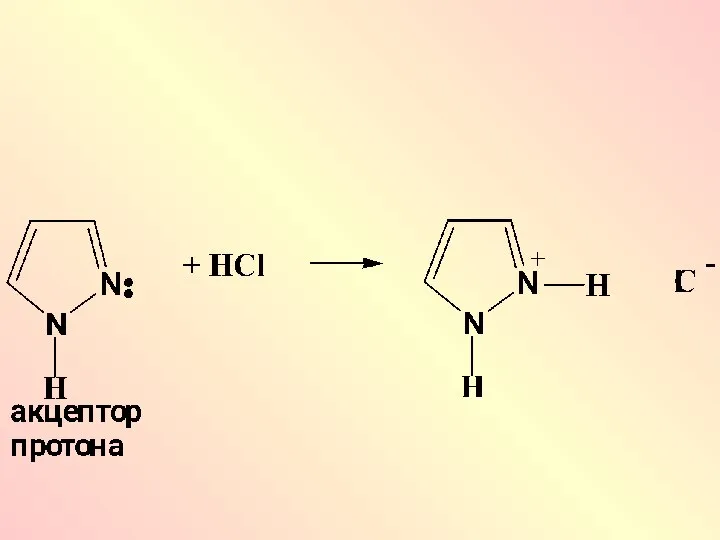
- 42. Сильными NН-кислотами являются азотсодержащие гетероциклы: пиррол, пиразол, имидазол, индол, у которых отрицательный заряд в анионе делокализован
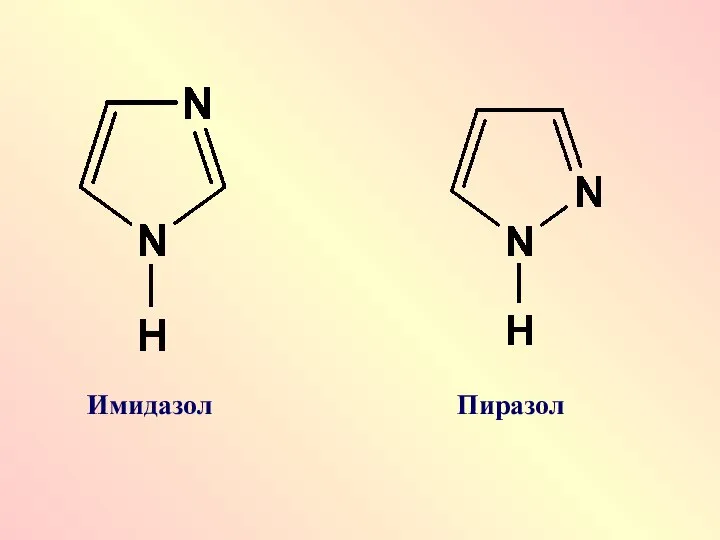
- 43. Имидазол Пиразол
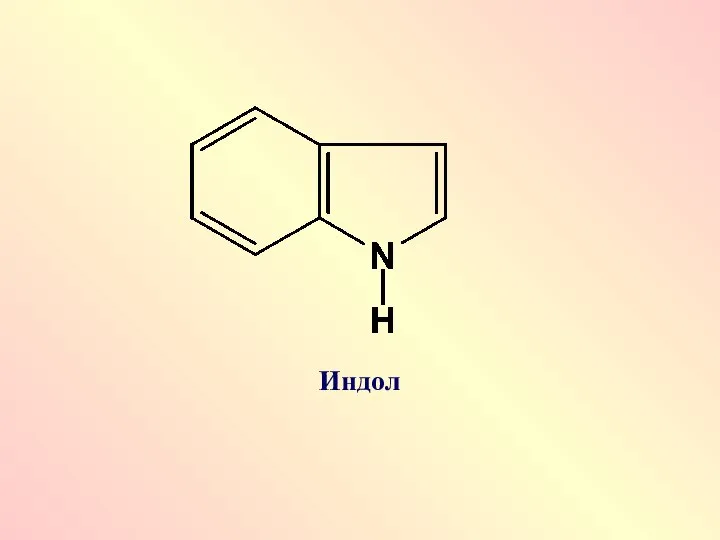
- 44. Индол
- 45. СН-кислоты СН-кислоты являются самыми слабыми из кислот
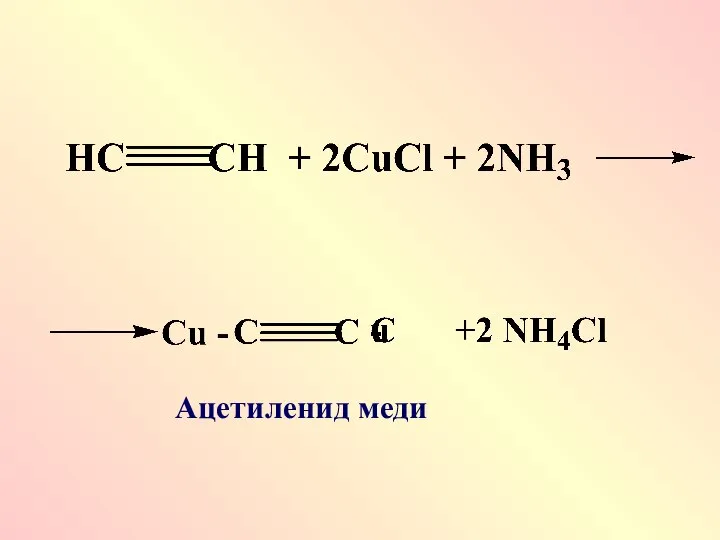
- 46. Ацетиленид меди
- 47. Кислотность соединений с одинаковыми радикалами падает в ряду
- 48. 6.2.Основность органических соединений Основание - молекула органического вещества, имеющая электронную пару, для принятия протона
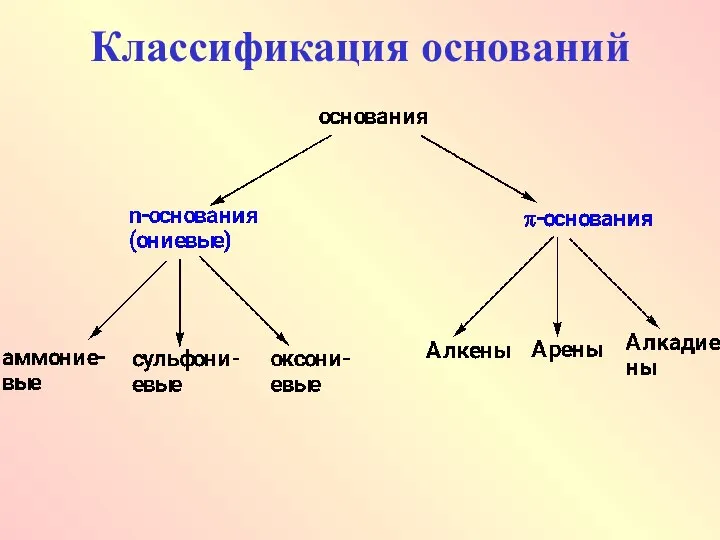
- 49. Классификация оснований
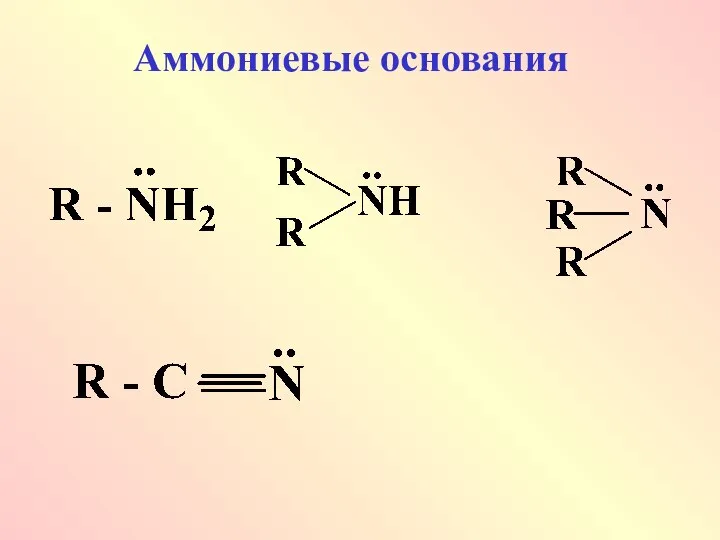
- 50. Аммониевые основания
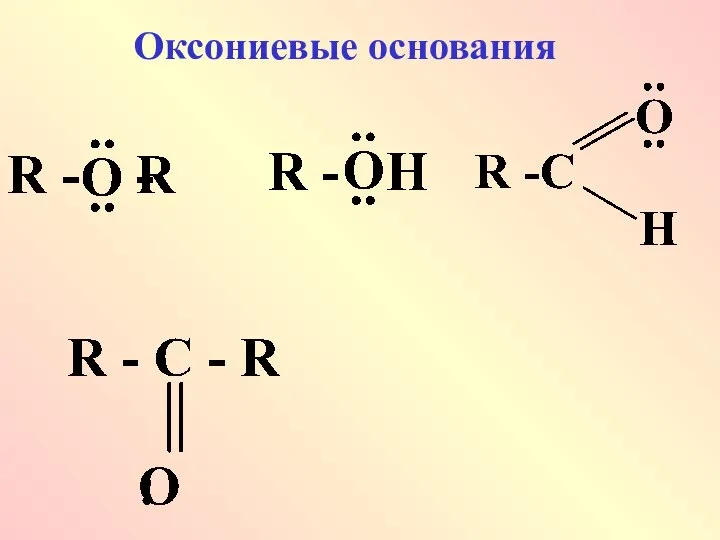
- 51. Оксониевые основания
- 52. Сульфониевые осноавния
- 54. Основность органических соединений определяется устойчивостью образовавшегося катиона или величиной электронной плотности на атоме основного центра, что
- 55. 1) Чем больше делокализация положительного заряда, тем выше основность 2) Чем выше электронная плотность на атоме
- 56. 3) Чем больше ЭО атома в основном центре, тем меньше основные свойства. Аммониевые основания проявляют более
- 57. 4)Чем больше поляризуемость атома в основном центре, тем меньше основность. Оксониевые основания более сильные, чем сульфониевые
- 58. 5) Чем выше эффект сольватации, тем более ярко выражены основные свойства
- 59. 6) ЭД-заместители усиливают основные свойства, а ЭА – уменьшают основные свойства
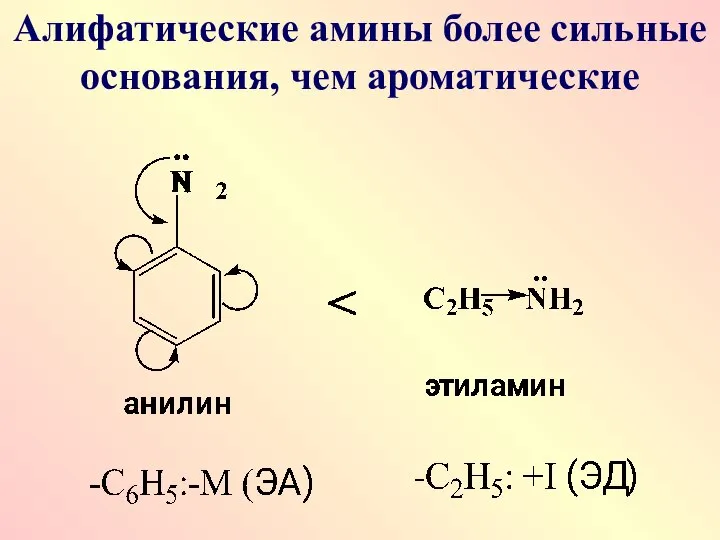
- 60. Алифатические амины более сильные основания, чем ароматические
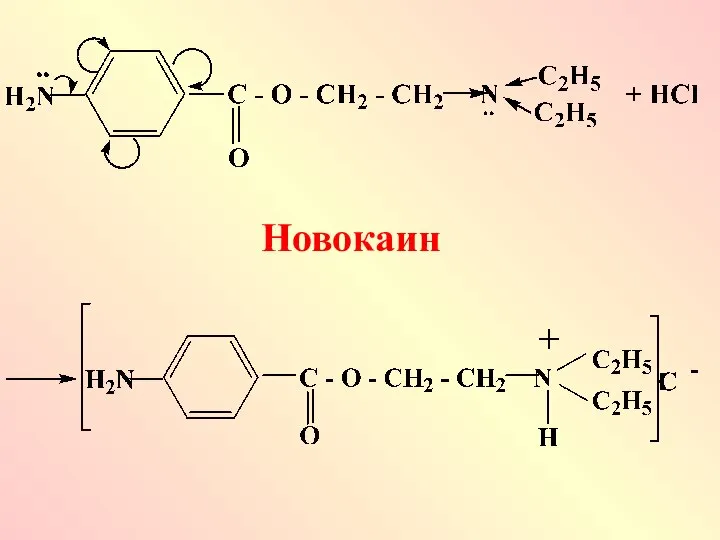
- 61. Если в молекуле сложного соединения имеется несколько основных центров, то определяют наиболее сильный основный центр и
- 62. Новокаин
- 63. 6.3.Амфотерные соединения Кислотность и основность – понятия относительные. Многие соединения, в зависимости от условий, могут выступать
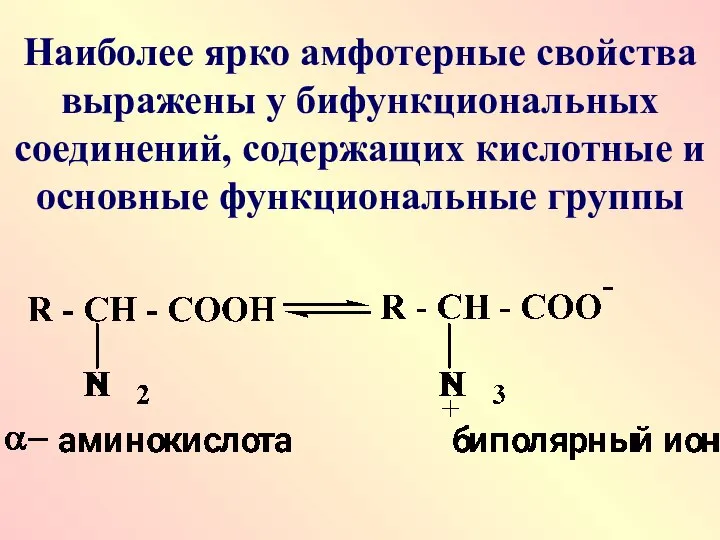
- 64. Наиболее ярко амфотерные свойства выражены у бифункциональных соединений, содержащих кислотные и основные функциональные группы
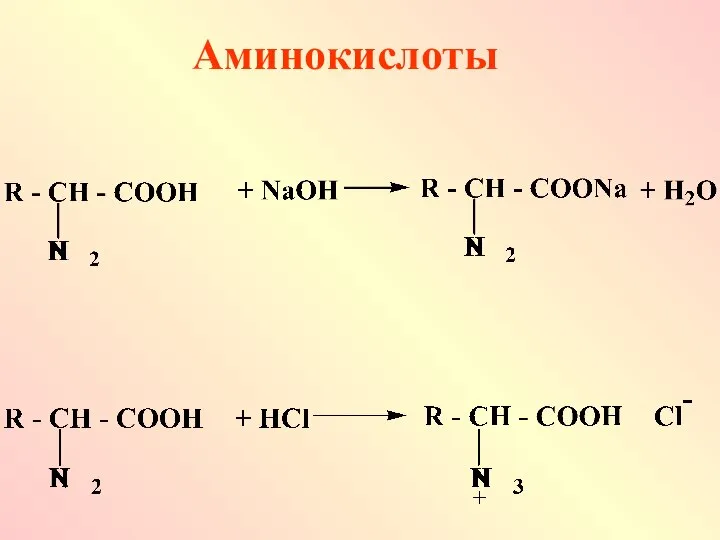
- 65. Аминокислоты
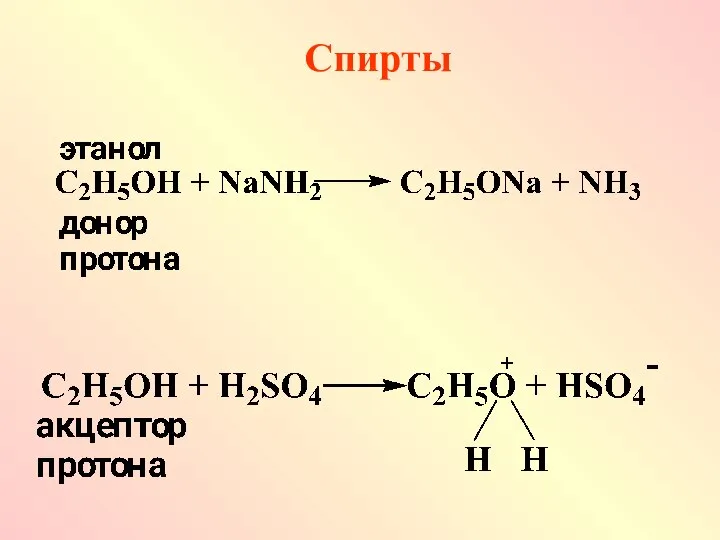
- 66. Спирты
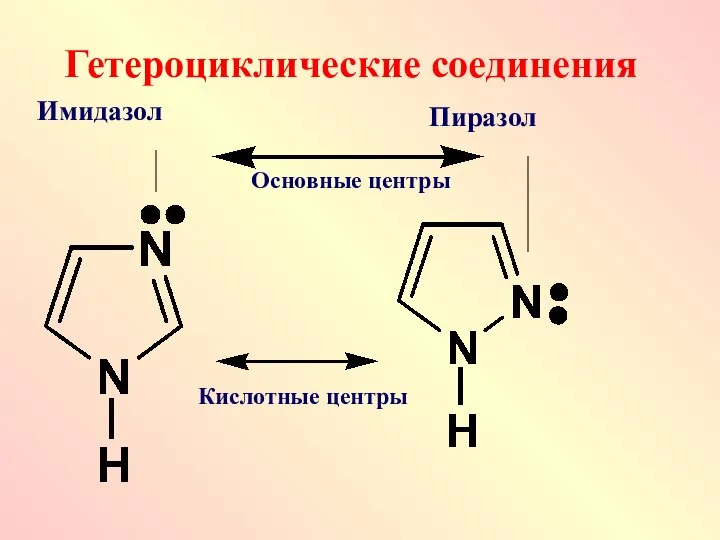
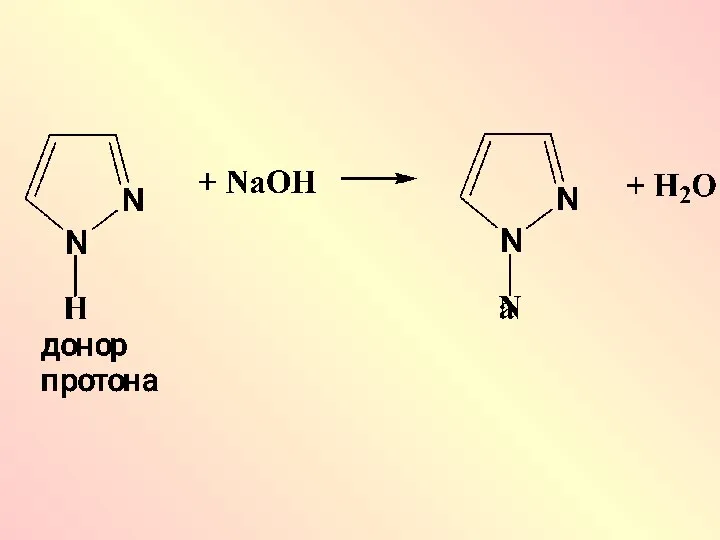
- 67. Гетероциклические соединения Имидазол Пиразол Кислотные центры Основные центры
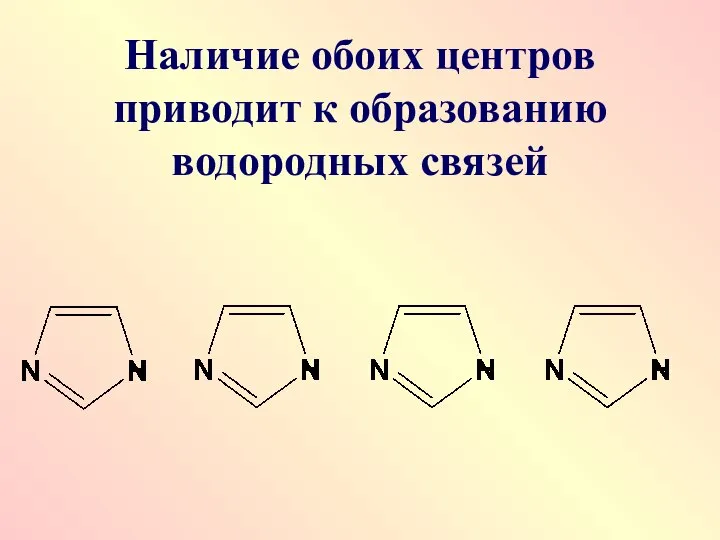
- 70. Наличие обоих центров приводит к образованию водородных связей
- 73. Кислотность и основность – важнейшие понятия, определяющие физико-химические и биологические свойства органических соединений. Кислотный и основный
- 75. Скачать презентацию

















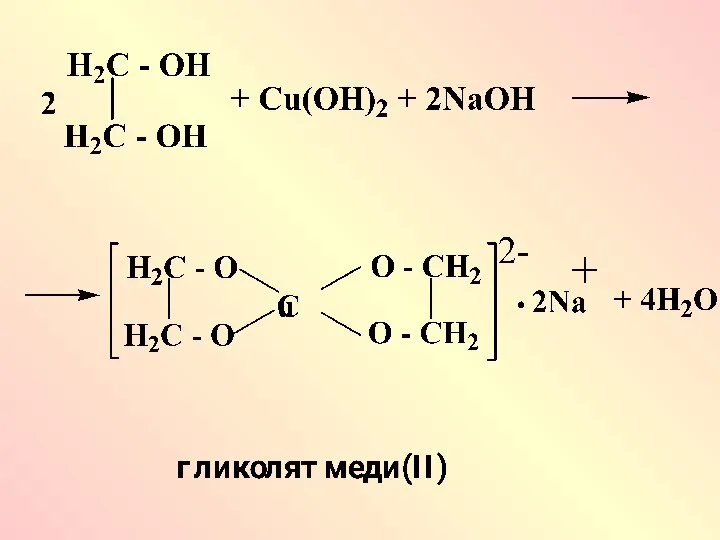

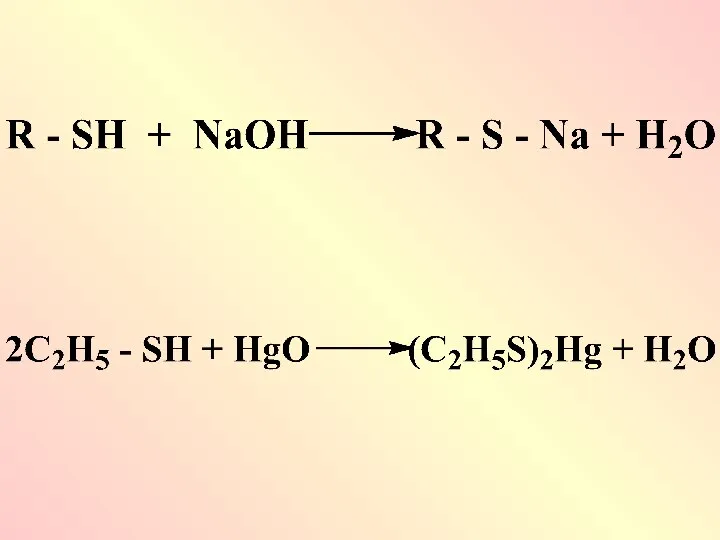

















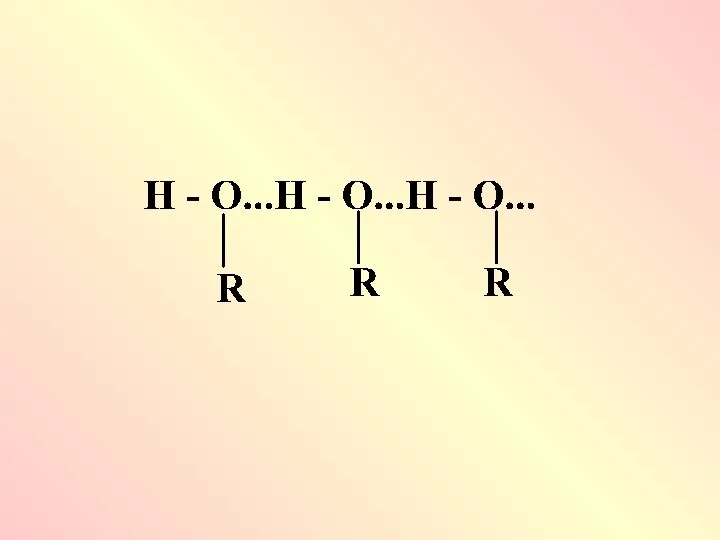


 Механическое оборудование и система вентиляции
Механическое оборудование и система вентиляции Тема: Сравнение слов-названий, слов-действий и слов-признаков со словами, которые выражают различные чувства. урок русского языка
Тема: Сравнение слов-названий, слов-действий и слов-признаков со словами, которые выражают различные чувства. урок русского языка Столовая посуда, приборы и столовое белье
Столовая посуда, приборы и столовое белье 2 класс 2 четверть Авторы: Хомутовская Л.Н., МОУ Саваслейская ср. шк. Каргина В.В., МОУ Новосельская ср. шк. 2005
2 класс 2 четверть Авторы: Хомутовская Л.Н., МОУ Саваслейская ср. шк. Каргина В.В., МОУ Новосельская ср. шк. 2005 Гимнастика после дневного сна
Гимнастика после дневного сна Использование компьютерных систем в оптимизации производства бензинов
Использование компьютерных систем в оптимизации производства бензинов Сказочное путешествие в страну Дроби - презентация для начальной школы
Сказочное путешествие в страну Дроби - презентация для начальной школы Презентация____
Презентация____ Теория пар сил
Теория пар сил Тема 15. Управление человеческими ресурсами
Тема 15. Управление человеческими ресурсами  Ручное изготовление диадемы с использованием традиционных материалов
Ручное изготовление диадемы с использованием традиционных материалов Обобщение опыта работы. Презентация опыта работы по теме самообразования « Самостоятельная работа как средство развития поз
Обобщение опыта работы. Презентация опыта работы по теме самообразования « Самостоятельная работа как средство развития поз Проектно - исследовательская работа на тему: «И С Т О Р И Я И Г Р У Ш К И. С В И С ТУ Л Ь К А .» Автор работы: Тюрина Юлия Ученица 1 «А» кл
Проектно - исследовательская работа на тему: «И С Т О Р И Я И Г Р У Ш К И. С В И С ТУ Л Ь К А .» Автор работы: Тюрина Юлия Ученица 1 «А» кл Религия. Искусство. Мораль
Религия. Искусство. Мораль Кратные интегралы
Кратные интегралы Лекція 18. Основи структурного програмування
Лекція 18. Основи структурного програмування Массовая культура (pop culture)
Массовая культура (pop culture) Практическая работа: изображение подводного мира. 6 класс
Практическая работа: изображение подводного мира. 6 класс 5 ლექცია
5 ლექცია Пьер Ферма - француз математик, физик. Мамандығы бойынша заңгер
Пьер Ферма - француз математик, физик. Мамандығы бойынша заңгер ПРОДУКТИВНОЕ И СПЕЦИФИЧЕСКОЕ ВОСПАЛЕНИЕ
ПРОДУКТИВНОЕ И СПЕЦИФИЧЕСКОЕ ВОСПАЛЕНИЕ Здоровый образ жизни
Здоровый образ жизни Красноярский медицинский университет им.проф.В.Ф.Войно-Ясенецкого.
Красноярский медицинский университет им.проф.В.Ф.Войно-Ясенецкого.  Негативні явища економічних криз
Негативні явища економічних криз Абзац.ppt
Абзац.ppt ЭЛЕКТРОННАЯ ВИКТОРИНА для детей 6-7 лет «Мы – наследники Великой Победы»
ЭЛЕКТРОННАЯ ВИКТОРИНА для детей 6-7 лет «Мы – наследники Великой Победы»  Металлические материалы
Металлические материалы Распределительный метод
Распределительный метод