Система допуска на рынок Республики Казахстан безопасных, эффективных и качественных лекарственных средств
Содержание
- 2. Содержание: Государственное регулирование в области здравоохранения в Республике Казахстан Структура системы здравоохранения в Республике Казахстан Структура
- 3. Государственное регулирование в области здравоохранения в Республике Казахстан Государственное регулирование в области здравоохранения осуществляется путем проведения
- 4. Государственное регулирование в области здравоохранения в Республике Казахстан измененийврегистрационноедосьеЛС, ИМНиМТ, отдельныхвидовпродукцииивеществ, оказывающихвредноевоздействиеназдоровьечеловека; ?6) подтверждениясоответствиятоваров(работ, услуг) вобластиздравоохранениятребованиям,
- 5. Структура системы здравоохранения в Республике Казахстан Министерство здравоохранения Республики Казахстан Комитетгосударственногосанитарно-эпидемиологическогонадзора Комитетмедицинскихуслуг Комитетконтролямедицинскойифармацевтическойдеятельности Организации, находящиесявведенииМЗ(НИИ, Медицинскиеобразовательныеорганизации,
- 6. Структура системы государственного контроля в сфере обращения ЛС Государственный контроль в сфере обращения ЛС и обеспечение
- 7. История создания. Основные функции РГП на ПХВ «Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и
- 8. Функции Национального центра Проведениеэкспертизылекарственныхсредств, изделиймедицинскогоназначенияимедицинскойтехникипригосударственнойрегистрации ОсуществлениесертификацииЛС РазработкаГосударственнойфармакопеиРК ПроведениедоклиническихиспытанийЛСииспытанийнабиоэквивалентностьЛС УчастиевфармаконадзореимониторингепобочныхдействийЛС Участитевразработкенормативныхправовыхактов Осуществлениеэкспертизырекламныхматериалов ВедениебазыданныхГосударственногореестраЛС Изданиеинформационно-аналитическогожурнала«ФармацияКазахстана» Ведениеведомственногоархиварегистрационныхдосье
- 9. Структура РГП «Национальный центр экспертизы лекарственных средств» Генеральный директор Заместитель по производственным вопросам Заместитель по экономическим
- 10. Испытательный центр ИЦ аккредитован в государственной системе технического регулирования РК на соответствие требованиям СТ РК ИСО/МЭК
- 11. Структурные подразделения ИЦ Республиканскаяиммунобиологическаялаборатория; Физико-химическаялаборатория; Микробиологическаялаборатория; Токсикологическаялаборатория; Лабораториянеклиническихиклиническихисследований; Виварий.
- 12. Фармакопейный центр Осуществлениенаучнойспециализированнойфармацевтическойэкспертизыдокументоврегистрационногодосье РазработкаиподготовкакизданиюГосударственнойфармакопеиРК ВнесениепредложенийпоизменениямидополнениямвГосударственныйреестрлекарственныхсредствРеспубликиКазахстан(внесениеновыхэффективныхибезопасныхлекарственныхсредствиисключениеустаревших, малоэффективныхпрепаратов)
- 13. Фармакологический центр ОсуществлениенаучнойспециализированнойфармакологическойэкспертизыЛСнапредметихбезопасностииэффективности; Разработкавпределахсвоейкомпетенциимер, направленныхнаобеспечениевнутреннегорынкаРКбезопасными, эффективнымиикачественнымиЛС ОсуществлениенаучногоруководстваорганизациейикоординациейработподоклиническимиклиническимисследованиямфармакологическихилекарстнныхсредстввсоответствиисGLP иGСP, включаяисследованиебиоэквивалентностивоспроизведенныхпрепаратов; Фармаконадзоримониторингпобочногодействиялекарственныхсредствиразработкамерпоснижениюрискаопасностиприменениялекарственныхсредсв;
- 14. Подтверждение соответствия лекарственных средств В соответствии со статьей 17 Кодекса РК «О здоровье народа и системе
- 15. Стандартизация лекарственных средств Издана Государственная фармакопея Республики Казахстан вдвух томах на государственном и русском языках I
- 16. Международное сотрудничество КомиссияЕвропейскойфармакопеи МеждународнаяпрограммаВОЗпомониторингупобочныхдействийЛС Межгосударственнаякомиссияпостандартизации, регистрациииконтролюкачестваЛС, ИМНиМТгосударств-участниковСНГ Евразийскоеэкономическоесообщество(ЕврАзЭС) Таможенныйсоюз ЕвропейскийДиректоратпоконтролюкачестваЛСимедицинскихуслугСоветаЕвропы(EDQM)
- 17. Научный информационно- аналитический журнал «Фармация Казахстана» Издается с 2001 года. Журнал «Фармация Казахстана» входит в перечень
- 18. Государственная регистрация ЛС, ИМН и МТ ГосударственнаярегистрацияЛС, ИМНиМТосуществляетсяККМФДМЗРК ЭкспертизуЛС, ИМНиМТпроводитРГП«НациональныйцентрэкспертизыЛС, ИМНиМТ»МЗРК. ТребованияКазахстанаприпроведениигосударственнойрегистрациилекарственныхсредствприближеныигармонизированысостандартамиЕвропейскосообщества, странСНГ–России, Украины. ТакаясистемагосударственногоконтролявРеспубликеКазахстанзаоборотомидопускомнарыноклекарственныхсредствэффективноработаетуже10 лет.
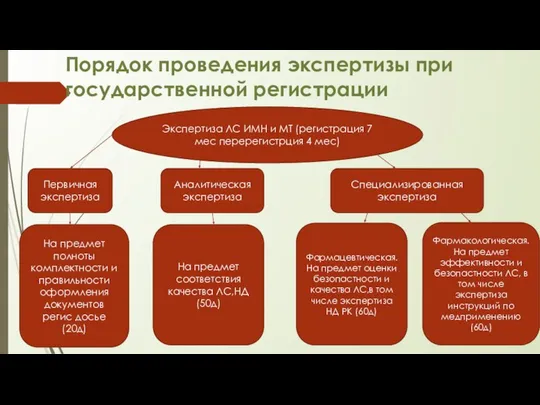
- 19. Порядок проведения экспертизы при государственной регистрации Экспертиза ЛС ИМН и МТ (регистрация 7 мес перерегистрция 4
- 20. Государственная регистрация ЛС, ИМН, МТ После завершения экспертизы ЛС составляется заключение о безопасности, эффективности и качестве
- 21. Оценка производства и системы обеспечения качества при государственной регистрации В соответствии с приказом МЗРК от19 ноября2009
- 22. Использованные материалы: Материалы сайта WHO Collaborating Centre for Drug Statistics Methodology: http://www.whocc.no/atcddd/ Материалы сайта http://www.apteka.ua Астапенко
- 24. Скачать презентацию




















 ГОСТ 7.0-99 «Информационно-библиотечная деятельность, библиография. Термины и определения»
ГОСТ 7.0-99 «Информационно-библиотечная деятельность, библиография. Термины и определения» Дзюдо в детском саду. Учебная программа составлена с учётом возраста обучающихся (мальчики и девочки) – 5-7 лет
Дзюдо в детском саду. Учебная программа составлена с учётом возраста обучающихся (мальчики и девочки) – 5-7 лет Основы строительной стандартизации
Основы строительной стандартизации Комбинаторные задачи и начальные сведения из теории вероятностей в курсе алгебры 9 класса.
Комбинаторные задачи и начальные сведения из теории вероятностей в курсе алгебры 9 класса.  Сборка компьютера. (Глава 3)
Сборка компьютера. (Глава 3) Модули
Модули Кредитование внешнеторговых операций Выполнили: Жукова Юлия Жукова Зоя
Кредитование внешнеторговых операций Выполнили: Жукова Юлия Жукова Зоя Організація оповіщення про хімічні надзвичайні ситуації
Організація оповіщення про хімічні надзвичайні ситуації Общая характеристика системы физического воспитания
Общая характеристика системы физического воспитания Языкознание эпохи Возрождения
Языкознание эпохи Возрождения Ecowiki.ru Вики-портал – площадка для сбора единой базы актуальных знаний и ресурсов по различным эко-направлениям Рассылка: ecowiki@googlegrou
Ecowiki.ru Вики-портал – площадка для сбора единой базы актуальных знаний и ресурсов по различным эко-направлениям Рассылка: ecowiki@googlegrou Чрезвычайные ситуации
Чрезвычайные ситуации kishechnye_shvy
kishechnye_shvy Средства наблюдения
Средства наблюдения эко
эко Компонувальник. Патерни проектування
Компонувальник. Патерни проектування Коффердам
Коффердам Предпосылки модернизации системы подготовки спортивного резерва в Российской Федерации и ход ее реализации
Предпосылки модернизации системы подготовки спортивного резерва в Российской Федерации и ход ее реализации Значение массажа в системе устранения заикания
Значение массажа в системе устранения заикания История развития и современное состояние оздоровительной и адаптивной физической культуры
История развития и современное состояние оздоровительной и адаптивной физической культуры Обзор изменений и нововведений в законодательстве для субъектов малого предпринимательства в 2018-2019 годах
Обзор изменений и нововведений в законодательстве для субъектов малого предпринимательства в 2018-2019 годах Комбинационные цифровые схемы
Комбинационные цифровые схемы Презентация на тему "Инактивированные вакцины" - скачать презентации по Медицине
Презентация на тему "Инактивированные вакцины" - скачать презентации по Медицине Сканирующий тахеометр Trimble SX10
Сканирующий тахеометр Trimble SX10 Размещение в документе графики
Размещение в документе графики Соціальні норми в Об’єднаних Арабських Еміратах
Соціальні норми в Об’єднаних Арабських Еміратах Техническая защита информации
Техническая защита информации В каждой мимолётности вижу я миры.
В каждой мимолётности вижу я миры.