Содержание
- 2. Физические свойства SO2 (серистый ангидрид; сернистый газ) SO3 (серный ангидрид)
- 3. Физические свойства Окси́д се́ры(IV) (диокси́д се́ры, серни́стый газ, серни́стый ангидри́д) — SO2. В нормальных условиях представляет
- 4. Пространственная модель молекулы-SO3 Окисление серы и реакция с водой
- 5. Применение SO2 обесцвечивает органические красителя и применяется для отбеливания шелка, шерсти и соломы. Этим газом окуривают
- 6. Главные источники Оксид серы (IV) поступает в воздух в результате сжигания топлива и плавки руд, содержащих
- 7. Поступления в организм Вещества могут поступать в организм различными путями: через рот, дыхательные пути, кожу, слизистые
- 8. Общий характер действия Раздражает дыхательные пути, вызывая спазм бронхов и увеличение сопротивления дыхательных путей. При воздействии
- 9. Острое отравление Кожный зуд, сыпи, фурункулез. Покраснение и опухание конъюнктивы. Появление мелких точечных дефектов на роговице.
- 10. Хроническое отравление SO2 токсичен. Симптомы - удушье, расстройство речи, затруднение глотания, рвота расстройство речи, затруднение глотания,
- 11. Кислотные дожди скульптура из известняка одного из двенадцати апостолов на фронтоне церкви Святых Петра и Павла
- 12. Кислотные дожди Кислотный дождь — все виды метеорологических осадков — дождь — все виды метеорологических осадков
- 13. Причины кислотных дождей Главной причиной кислотных дождей является присутствие в составе атмосферы Земли двуокиси серы SO2
- 14. Соединения серы влияют на климат различными путями. Это представлено на схеме.
- 15. Экологические и экономические последствия Скульптура, пострадавшая от кислотного дождя Последствия выпадения кислотных дождей наблюдаются в США,
- 16. Экологические и экономические последствия Выделяют три стадии воздействия кислотных дождей на водоемы. Первая стадия — начальная.
- 17. Экологические и экономические последствия Лес после кислотного дождя Кислотный дождь наносит вред не только водной флоре
- 18. Интересные факты. Сера КИНОВАРЬ. Если в лаборатории разлили ртуть (возникла опасность отравления ртутными парами!), её первым
- 20. Скачать презентацию
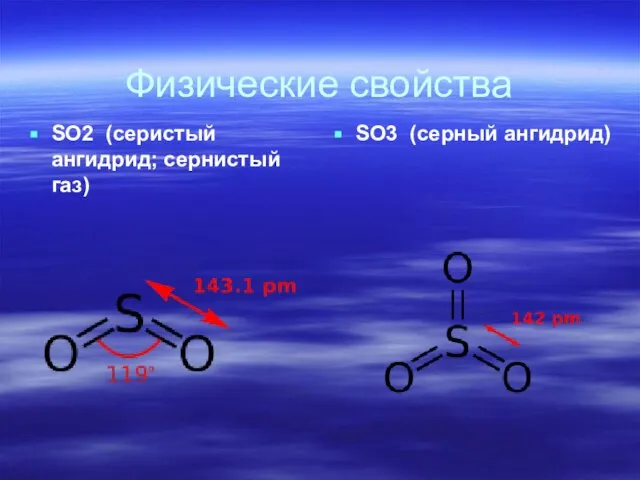
Физические свойства
SO2 (серистый ангидрид; сернистый газ)
SO3 (серный ангидрид)
Физические свойства
SO2 (серистый ангидрид; сернистый газ)
SO3 (серный ангидрид)
Физические свойства
Окси́д се́ры(IV) (диокси́д се́ры, серни́стый газ, серни́стый ангидри́д) — SO2. В
Физические свойства
Окси́д се́ры(IV) (диокси́д се́ры, серни́стый газ, серни́стый ангидри́д) — SO2. В
Окси́д се́ры(VI) (се́рный ангидри́д, трео́кись се́ры, се́рный га́з) SO3 - существует в двух аллотропных формах: жидкой и кристаллической. В природе не встречается, получается окислением диоксида серы. SO3 — высший оксид серы, тип химической связи: ковалентная полярная химическая связь. В обычных условиях легколетучая бесцветная жидкость с удушающим запахом. При температурах ниже 16,9 °C застывает с образованием смеси различных кристаллических модификаций твёрдого SO3.
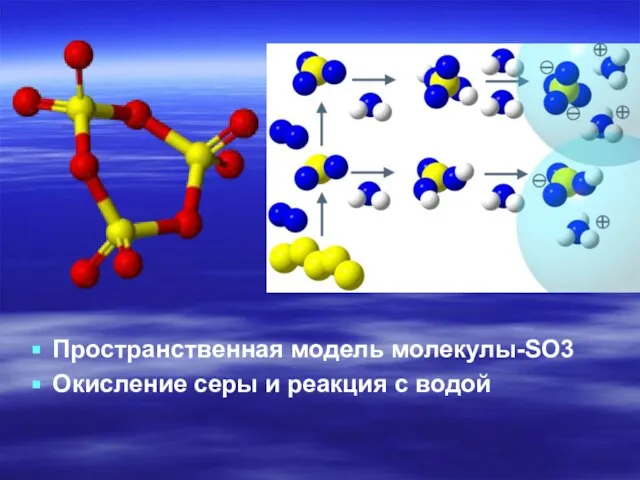
Пространственная модель молекулы-SO3
Окисление серы и реакция с водой
Пространственная модель молекулы-SO3
Окисление серы и реакция с водой
Применение
SO2 обесцвечивает органические красителя и применяется для отбеливания шелка, шерсти и
Применение
SO2 обесцвечивает органические красителя и применяется для отбеливания шелка, шерсти и
В пищевой промышленности диоксид серы используется как консервант и обозначается на упаковке под кодом Е220.
Применяется он также и в качестве растворителя в лабораториях. При таковом его применении следует помнить о возможном содержании в SO2 примесей в виде H2O и SO3. Их удаляют пропусканием через растворитель концентрированной H2SO4; это лучше делать под вакуумом или в другой закрытой аппаратуре
Серный ангидрид используют в основном в производстве серной кислоты.
Главные источники
Оксид серы (IV) поступает в воздух в результате сжигания
Главные источники
Оксид серы (IV) поступает в воздух в результате сжигания
Серный ангидрид SO3 выбрасываются в атмосферу при сжигании угольного топлива, нефти и природного газа, а также при выплавке цветных металлов и производстве серной кислоты.
Поступления в организм
Вещества могут поступать в организм различными путями: через
Поступления в организм
Вещества могут поступать в организм различными путями: через
Общий характер действия
Раздражает дыхательные пути, вызывая спазм бронхов и
Общий характер действия
Раздражает дыхательные пути, вызывая спазм бронхов и
Острое отравление
Кожный зуд, сыпи, фурункулез.
Покраснение и опухание конъюнктивы.
Появление мелких
Острое отравление
Кожный зуд, сыпи, фурункулез.
Покраснение и опухание конъюнктивы.
Появление мелких
Ломота в бровях и глазных яблоках, ощущением песка в глазах.
Светобоязнь, слезотечение.
Общая слабость, головные боли, головокружение, тошнота.
Ослабление слуха.
Расстройства пищеварения, поносы.
Судороги и потеря сознания (при острой интоксикации).
Психические нарушения, понижение интеллекта
Хроническое отравление
SO2 токсичен. Симптомы - удушье, расстройство речи, затруднение глотания, рвота
Хроническое отравление
SO2 токсичен. Симптомы - удушье, расстройство речи, затруднение глотания, рвота
При длительном воздействии диоксида серы увеличивается число заболеваний раком.
Сернистый ангидрид может вызывать общее отравление организма, проявляющееся в изменении состава крови, поражении органов дыхания, повышении восприимчивости к инфекционным заболеваниям. Развивается нарушение обмена веществ, повышение артериального давления у детей, ларингит, конъюнктивит, ринит, бронхопневмония, аллергические реакции, острые заболевания верхних дыхательных путей и системы кровообращения. При кратковременном воздействии – раздражение слизистой оболочки глаз, слезотечение, затруднение дыхания, тошнота, рвота, головные боли. Повышенная утомляемость, ослабление мышечной силы, снижение памяти. Замедление восприятия, ослабление функциональной способности сердца, изменение бактерицидности кожи.
Кислотные дожди
скульптура из известняка одного из двенадцати апостолов на фронтоне церкви
Кислотные дожди
скульптура из известняка одного из двенадцати апостолов на фронтоне церкви
копия поврежденной оригинальной скульптуры апостола.
Кислотные дожди
Кислотный дождь — все виды метеорологических осадков — дождь — все виды метеорологических
Кислотные дожди
Кислотный дождь — все виды метеорологических осадков — дождь — все виды метеорологических
Впервые термин «кислотный дождь» был введен в 1872 году английским исследователем Робертом Смитом. Его внимание привлек викторианский смог в Манчестере. И хотя ученые того времени отвергли теорию о существовании кислотных дождей, сегодня уже никто не сомневается, что кислотные дожди являются одной из причин гибели жизни в водоемах, лесов, урожаев, и растительности. Кроме того, кислотные дожди разрушают здания и памятники культуры, трубопроводы, приводят в негодность автомобили, понижают плодородие почв и могут приводить к просачиванию токсичных металлов в водоносные слои почвы.
Причины кислотных дождей
Главной причиной кислотных дождей является присутствие в составе
Причины кислотных дождей
Главной причиной кислотных дождей является присутствие в составе
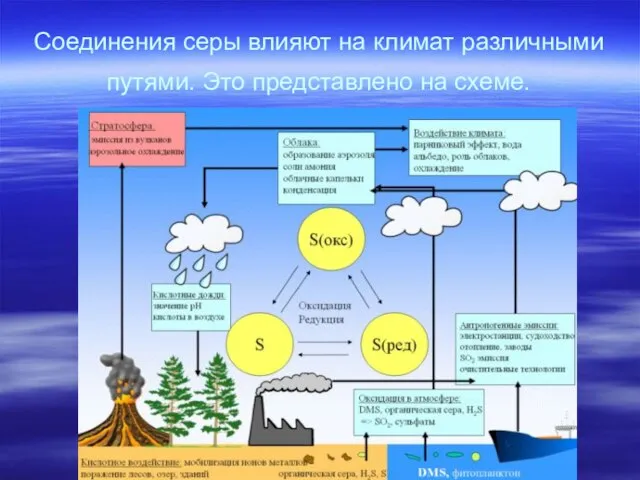
Соединения серы влияют на климат различными путями. Это представлено на схеме.
Соединения серы влияют на климат различными путями. Это представлено на схеме.
Экологические и экономические последствия
Скульптура, пострадавшая от кислотного дождя
Последствия выпадения кислотных дождей
Экологические и экономические последствия
Скульптура, пострадавшая от кислотного дождя
Последствия выпадения кислотных дождей
Экологические и экономические последствия
Выделяют три стадии воздействия кислотных дождей на
Экологические и экономические последствия
Выделяют три стадии воздействия кислотных дождей на
Экологические и экономические последствия
Лес после кислотного дождя
Кислотный дождь наносит
Экологические и экономические последствия
Лес после кислотного дождя
Кислотный дождь наносит
Интересные факты. Сера
КИНОВАРЬ. Если в лаборатории разлили ртуть (возникла опасность отравления
Интересные факты. Сера
КИНОВАРЬ. Если в лаборатории разлили ртуть (возникла опасность отравления
СЕРОБАКТЕРИИ. В природе постепенно происходит круговорот серы, подобный круговороту азота и углерода. Растения потребляют серу — ведь её атомы входят в состав белка. Растения берут серу из растворимых сульфатов, а гнилостные бактерии превращают серу белков в сероводород (отсюда — отвратительный запах гниения). Но есть так называемые серобактерии, которым вообще не нужна органическая пища. Они питаются сероводородом, и в их организмах в результате реакции между H2S, CO2 и O2 образуются углеводы и элементарная сера. Серобактерии нередко оказываются переполнены крупинками серы — почти всю их массу составляет сера с очень небольшой "добавкой" органических веществ.














 Курсовая работа «Религиозный радикализм: государственно-общественное регулирование»
Курсовая работа «Религиозный радикализм: государственно-общественное регулирование» Компьютерная графика
Компьютерная графика Органы мочевой системы
Органы мочевой системы  Benjamin Franklin (1706-1790)
Benjamin Franklin (1706-1790) Аудитория Уанета Январь 2011 г. gemiusAudience
Аудитория Уанета Январь 2011 г. gemiusAudience An american summer
An american summer Презентация "Театр и музыка Древней Греции (10 класс)" - скачать презентации по МХК
Презентация "Театр и музыка Древней Греции (10 класс)" - скачать презентации по МХК Введение в направление подготовки: местное самоуправление
Введение в направление подготовки: местное самоуправление Изобразительное искусство романтизма
Изобразительное искусство романтизма Основные особенности управленческой деятельности Планирование воспитательной деятельности в образовательном учреждении
Основные особенности управленческой деятельности Планирование воспитательной деятельности в образовательном учреждении Техническое обслуживание и ремонт газораспределительного механизма двигателя А-41
Техническое обслуживание и ремонт газораспределительного механизма двигателя А-41 150 культур Дона
150 культур Дона Религия. Иудаизм
Религия. Иудаизм Звіт про роботу в конкурсах - презентация для начальной школы_
Звіт про роботу в конкурсах - презентация для начальной школы_ запросы в БД
запросы в БД  Гимнастика. Виды гимнастики
Гимнастика. Виды гимнастики Понятие и признаки правоотношений
Понятие и признаки правоотношений Государственные символы России. Герб. Флаг. Гимн России
Государственные символы России. Герб. Флаг. Гимн России Экспериментальный сад «Лоулайн Лэб» (Lowline Lab)
Экспериментальный сад «Лоулайн Лэб» (Lowline Lab) Гимнастика, часть физической культуры
Гимнастика, часть физической культуры Негізгі және қосымша шағымдарын анықтау
Негізгі және қосымша шағымдарын анықтау Презентация по алгебре Линейные уравнения с одной переменной 7 класс
Презентация по алгебре Линейные уравнения с одной переменной 7 класс Dativ
Dativ Basics of software development O. Fedorova, associate professor of Department PMI
Basics of software development O. Fedorova, associate professor of Department PMI ПРЕЗЕНТАЦИЯ НА ТЕМУ: «СИСТЕМА ВЫСШЕГО ОБРАЗОВАНИЯ ВЕЛИКОБРИТАНИИ».
ПРЕЗЕНТАЦИЯ НА ТЕМУ: «СИСТЕМА ВЫСШЕГО ОБРАЗОВАНИЯ ВЕЛИКОБРИТАНИИ». Зачем нужен менеджер продукта при живом проектировщике интерфейсов? Денис Бесков / http://beskov.ru World Usability Day, Москва, 2011
Зачем нужен менеджер продукта при живом проектировщике интерфейсов? Денис Бесков / http://beskov.ru World Usability Day, Москва, 2011 Канализация электроэнергии на напряжении выше 1 кВ
Канализация электроэнергии на напряжении выше 1 кВ Презентация "Рембрандт ван Рейн (1606-1669)" - скачать презентации по МХК
Презентация "Рембрандт ван Рейн (1606-1669)" - скачать презентации по МХК