Содержание
- 2. Белками, или белковыми веществами, называют высокомолекулярные (молекулярная масса варьирует от 5-10 тыс. до 1 млн и
- 3. Антуан Франсуа де Фуркруа Белки были выведены в отдельный класс биологических молекул в XVIII веке в
- 4. Голландский химик Геррит Мульдер провёл анализ состава белков и выдвинул гипотезу, что практически все белки имеют
- 5. Термин «протеин» для обозначения подобных молекул был предложен в 1838 году шведским химиком Якобом Берцелиусом
- 6. В XXI веке исследование белков перешло на качественно новый уровень, когда исследуются не только индивидуальные очищенные
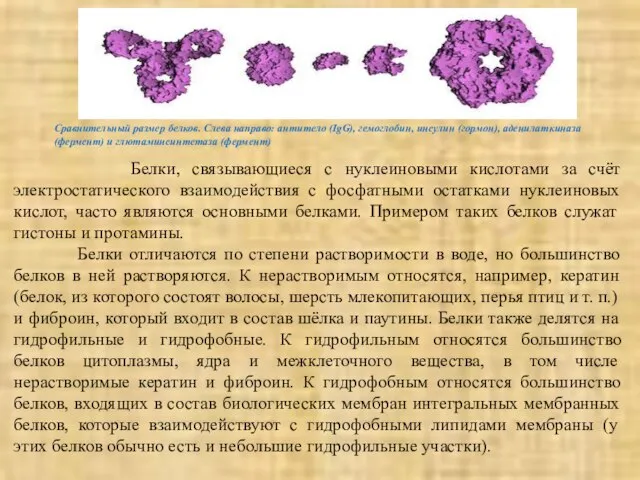
- 7. Сравнительный размер белков. Слева направо: антитело (IgG), гемоглобин, инсулин (гормон), аденилаткиназа (фермент) и глютаминсинтетаза (фермент) Белки,
- 8. каталитические (ферменты); регуляторные (гормоны); структурные (коллаген, фиброин); двигательные (миозин); транспортные (гемоглобин, миоглобин); защитные (иммуноглобулины, интерферон); запасные
- 9. Белки – основа биомембран, важнейшей составной части клетки и клеточных компонентов. Они играют ключевую роль в
- 10. Химический состав организма человека ВОДА – 65% ЖИРЫ – 10% БЕЛКИ – 18% УГЛЕВОДЫ – 5%
- 11. К концу XIX века было исследовано большинство аминокислот, которые входят в состав белков. В 1894 году
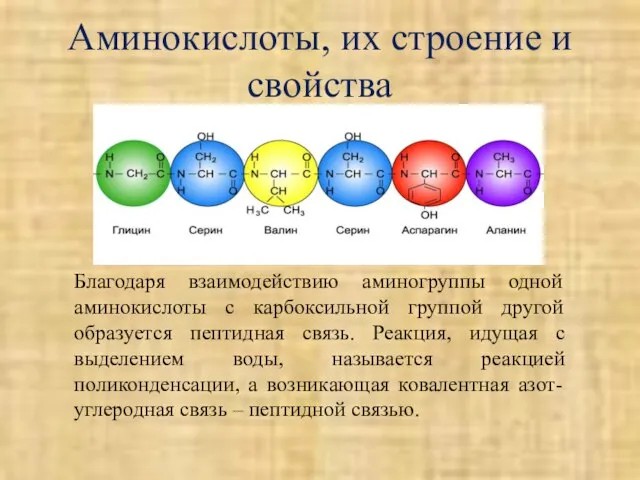
- 12. Аминокислоты, их строение и свойства В клетках и тканях встречается свыше 170 различных аминокислот. В составе
- 13. Аминокислоты, их строение и свойства Благодаря взаимодействию аминогруппы одной аминокислоты с карбоксильной группой другой образуется пептидная
- 14. Большую роль в создании структуры белков играют ионные (солевые) и водородные связи, а также гидрофобное взаимодействие
- 15. В начале XX века немецкий химик Эмиль Фишер экспериментально доказал, что белки состоят из аминокислотных остатков,
- 16. Однако центральная роль белков в организмах не была признана до 1926 года, когда американский химик Джеймс
- 17. Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру белков. Идея о том, что
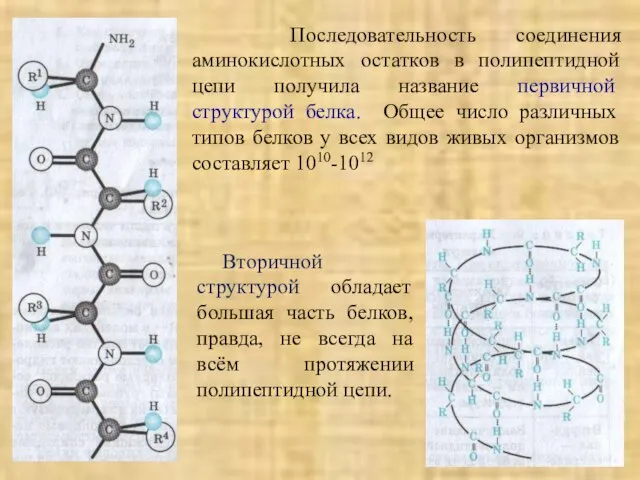
- 18. Последовательность соединения аминокислотных остатков в полипептидной цепи получила название первичной структурой белка. Общее число различных типов
- 19. Полипептидные цепочки с определённой вторичной структурой могут быть по-разному расположены в пространстве. Это пространственное расположение получило
- 20. В ряде случаев отдельные субъединицы белка с помощью водородных связей, электростатического и других взаимодействий образуют сложные
- 21. В 1949 году Фред Сенгер определил аминокислотную последовательность инсулина, продемонстрировав таким способом, что белки — это
- 22. Характеристика трёх структур белковых молекул Пептидная связь
- 23. Существует несколько классификаций белков. В их основе лежат разные признаки: Степень сложности (простые и сложные); Форма
- 24. Белки – амфотерные электролиты. При определённом значении рН среды (она называется изоэлектрической точкой) число положительных и
- 25. Процесс гидратации означает связывание белками воды, при этом они проявляют гидрофильные свойства: набухают, их масса и
- 26. При денатурации под влиянием внешних факторов (температуры, механического воздействия, действия химических агентов и ряда других факторов)
- 27. Под процессом пенообразования понимают способность белков образовывать высококонцентрированные системы «жидкость –газ», называемые пенами. Устойчивость пены, в
- 28. Реакцию гидролиза с образованием аминокислот в общем виде можно записать так: Гидролиз белков
- 29. Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается
- 30. Ход работы Добавляют к 5 каплям разбавленного раствора яичного белка 5 капель 0,5%-ного водного раствора нингидрина,
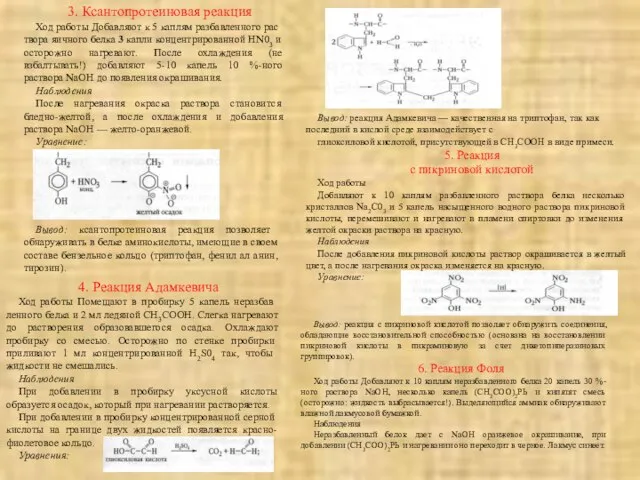
- 31. 3. Ксантопротеиновая реакция Ход работы Добавляют к 5 каплям разбавленного раствора яичного белка 3 капли концентрированной
- 32. Функции белков в организме Каталитическая Структурная Защитная Регуляторная Сигнальная Транспортная Запасная Рецепторная Моторная
- 33. Ноначастицы из белковых оболочек вируса
- 34. Гидрофобы (гидрофобные вещества) Вещества, плохо или вовсе нерастворимые в воде (от греч. phobos – страх). К
- 35. Макроэлементы Элементы, количество которых составляет до 0,001% от массы тела (кислород, углерод, азот, водород, фосфор, калий,
- 36. Буферность Способность поддерживать относительно постоянную концентрацию ионов водорода в растворе. Определяется ионами (фосфатная буферная система, бикарбонатная
- 37. Полисахариды Углеводы, являющиеся полимерами и состоящие из неопределенно большого (до нескольких сотен или тысяч) числа остатков
- 38. Липопротеиды Сложные соединения липидов с белками. Выполняют строительную функцию.
- 39. Проверь себя 1. Главным носителем жизни являются … 2. … - это сложные высокомолекулярные соединения, построенные
- 40. 5. Многие белки растворимы в …, почти все растворяются в … . 6. Нерастворимы белки, из
- 41. КРИТЕРИИ ОЦЕНКИ: «5» - все ответы правильные; «4» - 1-2 неверных ответа; «3» - 3 неверных
- 42. ОТВЕТЫ: 1. Белки. 2. Белки; остатков α – аминокислот. 3. С, Н, О, N, S. 4.
- 43. 6.Ткани живых организмов: кожа, сухожилия, мышцы, ногти, волосы. 7.Первичную, вторичную, третичную, четвертичную. 8.Строительная, каталитическая, двигательная, транспортная,
- 45. Скачать презентацию





































 Зоопарк в Линкольн парке Чикаго
Зоопарк в Линкольн парке Чикаго Autonomic Nervous System 2
Autonomic Nervous System 2 Biochemie nervového systému
Biochemie nervového systému Ароматерапия и стресс
Ароматерапия и стресс Кошки в жизни человека
Кошки в жизни человека Заттар мен энергия алмасуы. Энергетикалық алмасу
Заттар мен энергия алмасуы. Энергетикалық алмасу Тема: подраздел Вторичноротые (Deuterostomia) Тип Иглокожие (Echinodermata)
Тема: подраздел Вторичноротые (Deuterostomia) Тип Иглокожие (Echinodermata)  Строение клетки. Ткани
Строение клетки. Ткани Урок на тему: «Ткани» биология 8 класс. Автор урока учитель биологии высшей категории МОУ СОШ № 43 г. Пензы. Петрунина Т.П.
Урок на тему: «Ткани» биология 8 класс. Автор урока учитель биологии высшей категории МОУ СОШ № 43 г. Пензы. Петрунина Т.П.  Современные приматы
Современные приматы Уход за короткошерстными собаками
Уход за короткошерстными собаками Организм клеткасындағы S-фазаны анықтау
Организм клеткасындағы S-фазаны анықтау Введение в биологию
Введение в биологию Презентация на тему "Влияние человека на животных" - скачать презентации по Биологии
Презентация на тему "Влияние человека на животных" - скачать презентации по Биологии Майстерність маскування хамелеонів
Майстерність маскування хамелеонів Где зимуют птицы?
Где зимуют птицы?  Презентация на тему Кролики
Презентация на тему Кролики Применение реакций брожения в пищевой промышленности
Применение реакций брожения в пищевой промышленности Презентация Закон постоянства состава
Презентация Закон постоянства состава Государственное бюджетное образовательное учреждение Центр образования №153 Гормоны мозга.
Государственное бюджетное образовательное учреждение Центр образования №153 Гормоны мозга.  Урок - практикум Строение эукариотической клетки. Животная клетка
Урок - практикум Строение эукариотической клетки. Животная клетка Животная клетка
Животная клетка Регуляция углеводного обмена
Регуляция углеводного обмена Класс однодольные. Семейство злаки и лилейные
Класс однодольные. Семейство злаки и лилейные Движущие силы эволюции. Борьба за существование. 11 класс Тема урока:
Движущие силы эволюции. Борьба за существование. 11 класс Тема урока: Дощовий черв’як
Дощовий черв’як Развитие представлений о возникновении жизни
Развитие представлений о возникновении жизни Экология.Биоценозы
Экология.Биоценозы