Содержание
- 2. Биохимический моделист-конструктор. 1 этап Образуется «скелет» молекулы - "базовая" структура, на основе которой затем формируются многочисленные
- 3. Биохимический моделист-конструктор. 2 этап «Декорирование» скелета: метилирование, ацилирование, десатурация, гидроксилирование, гликозилирование. «Декорирование» может кардинально менять биологическую
- 4. Биохимический моделист-конструктор. 2 этап Ацилтрансферазы. У арабидопсиса – более 50 генов. Ацилтрансферазы вторичного метаболизма у разных
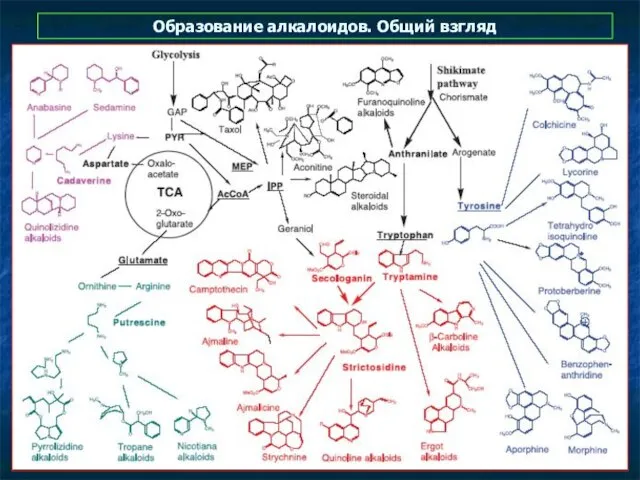
- 5. Образование алкалоидов. Общий взгляд
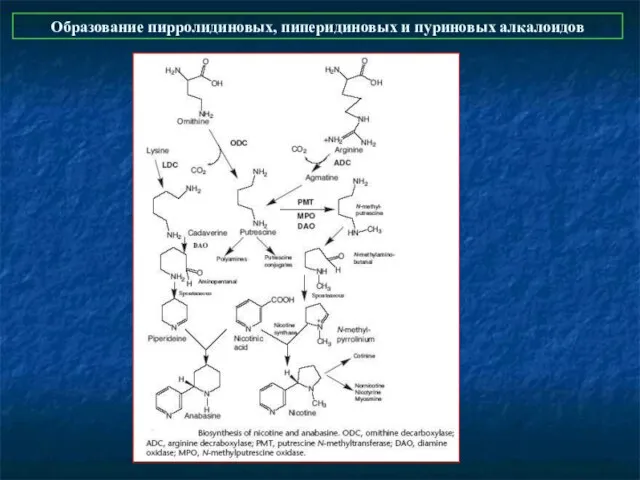
- 6. Образование пирролидиновых, пиперидиновых и пуриновых алкалоидов
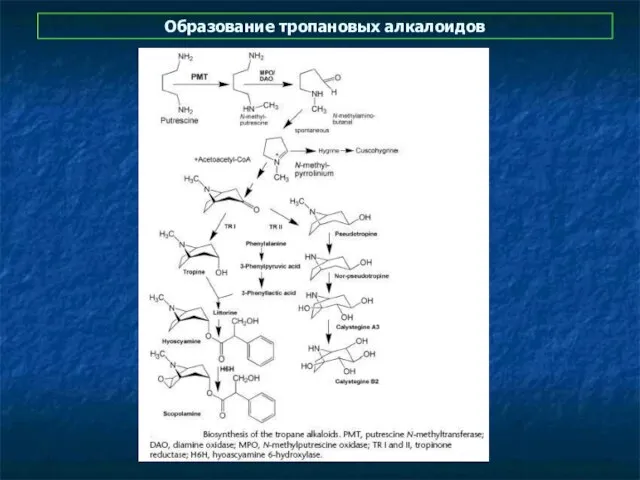
- 7. Образование тропановых алкалоидов
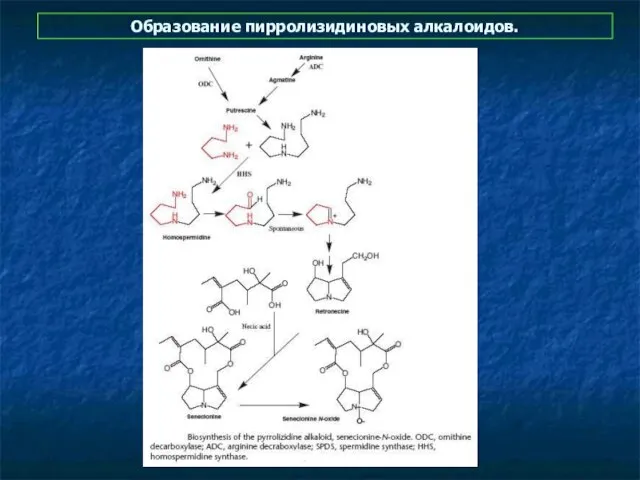
- 8. Образование пирролизидиновых алкалоидов.
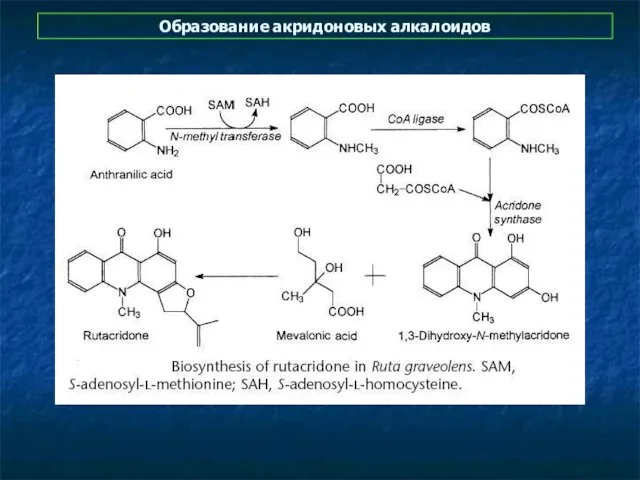
- 9. Образование акридоновых алкалоидов
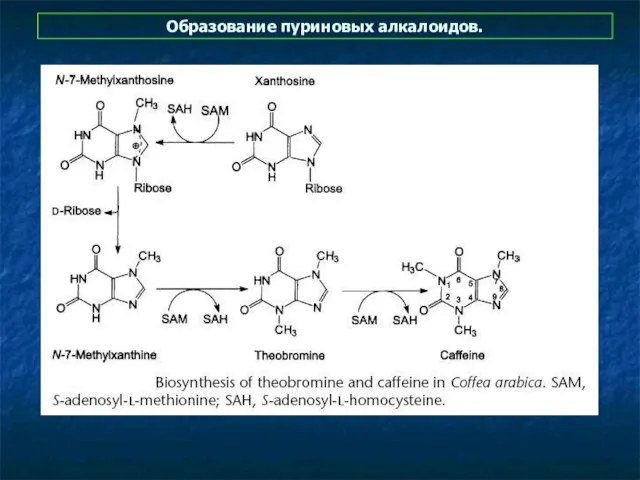
- 10. Образование пуриновых алкалоидов.
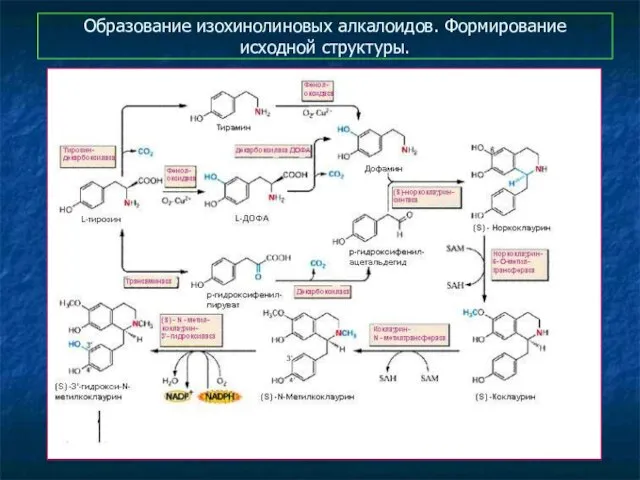
- 11. Образование изохинолиновых алкалоидов. Формирование исходной структуры.
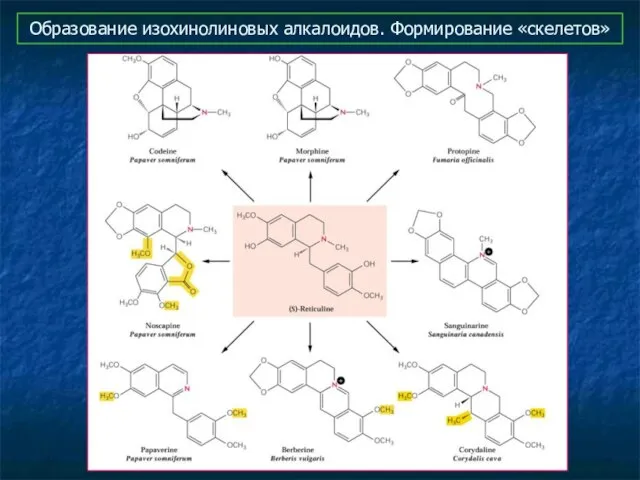
- 12. Образование изохинолиновых алкалоидов. Формирование «скелетов»
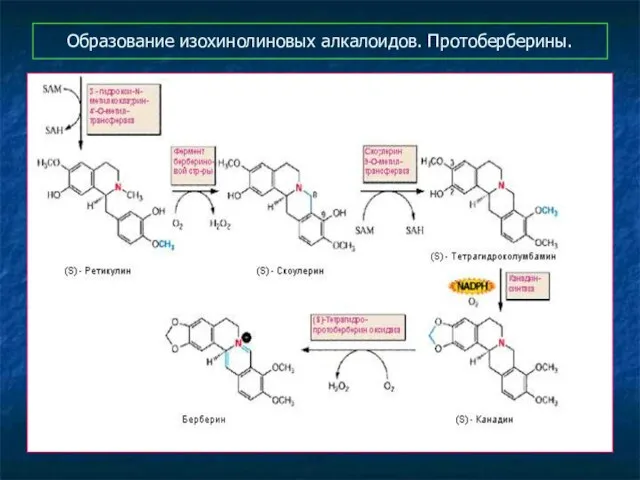
- 13. Образование изохинолиновых алкалоидов. Протоберберины.
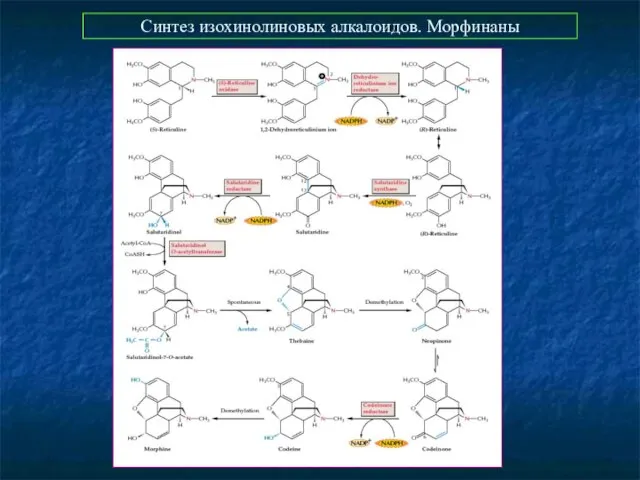
- 14. Синтез изохинолиновых алкалоидов. Морфинаны
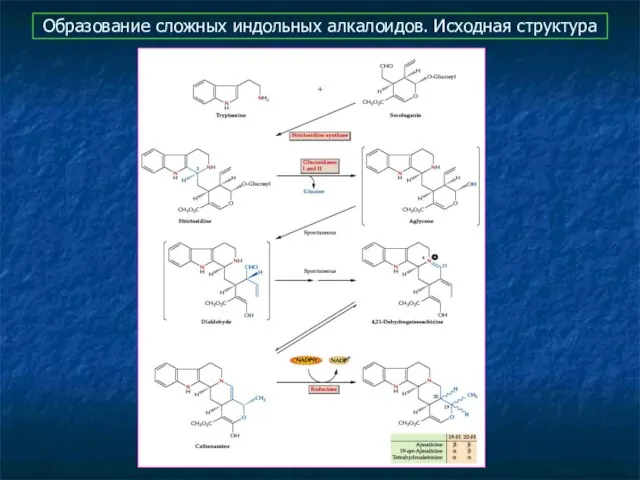
- 15. Образование сложных индольных алкалоидов. Исходная структура
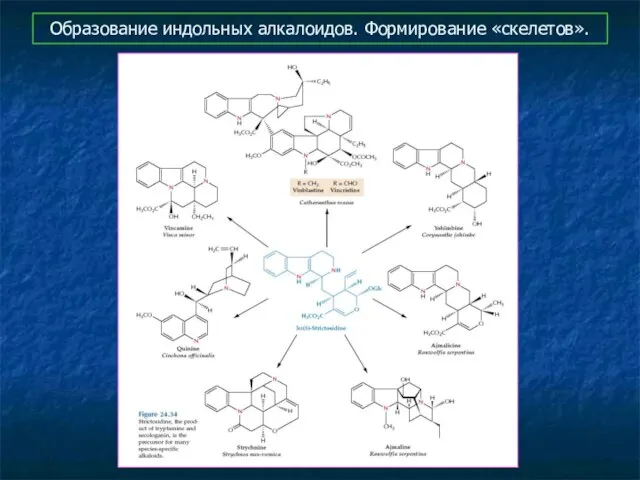
- 16. Образование индольных алкалоидов. Формирование «скелетов».
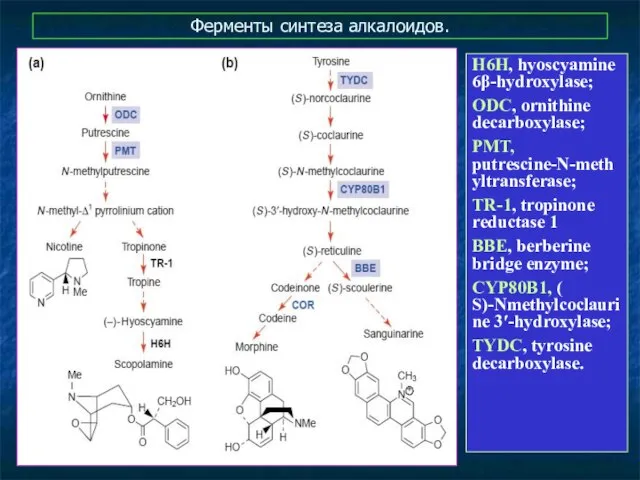
- 17. Ферменты синтеза алкалоидов. H6H, hyoscyamine 6β-hydroxylase; ODC, ornithine decarboxylase; PMT, putrescine-N-methyltransferase; TR-1, tropinone reductase 1 BBE,
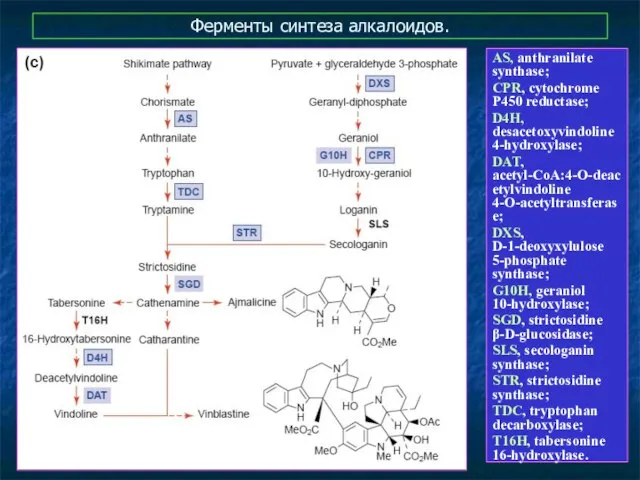
- 18. Ферменты синтеза алкалоидов. AS, anthranilate synthase; CPR, cytochrome P450 reductase; D4H, desacetoxyvindoline 4-hydroxylase; DAT, acetyl-CoA:4-O-deacetylvindoline 4-O-acetyltransferase;
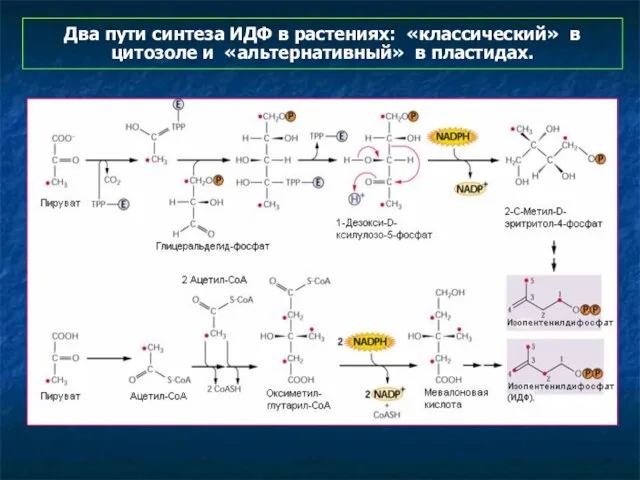
- 19. Два пути синтеза ИДФ в растениях: «классический» в цитозоле и «альтернативный» в пластидах.
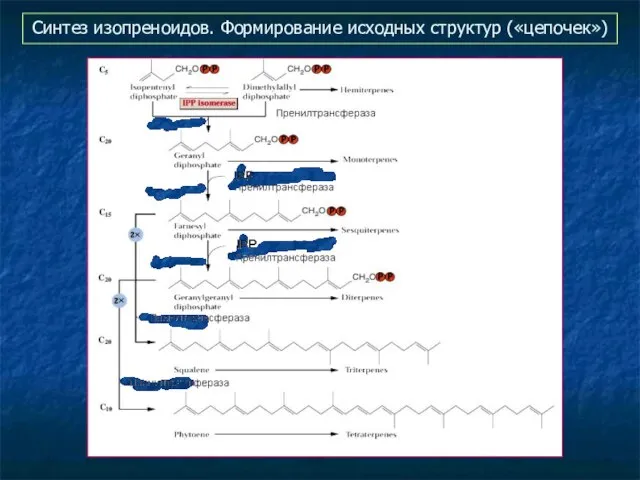
- 21. Синтез изопреноидов. Формирование исходных структур («цепочек»)
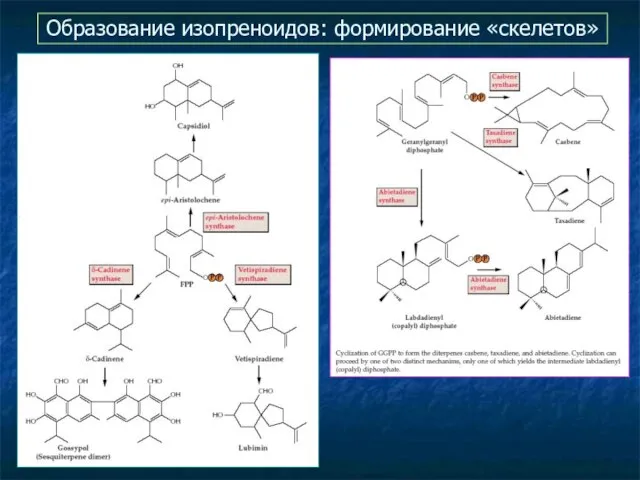
- 22. Образование изопреноидов: формирование «скелетов»
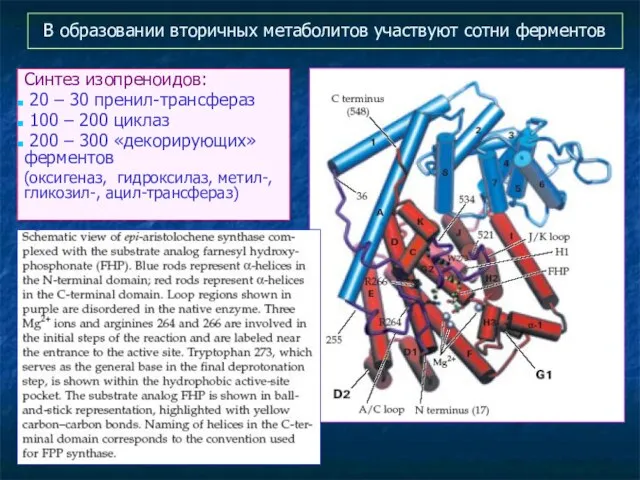
- 23. В образовании вторичных метаболитов участвуют сотни ферментов Синтез изопреноидов: 20 – 30 пренил-трансфераз 100 – 200
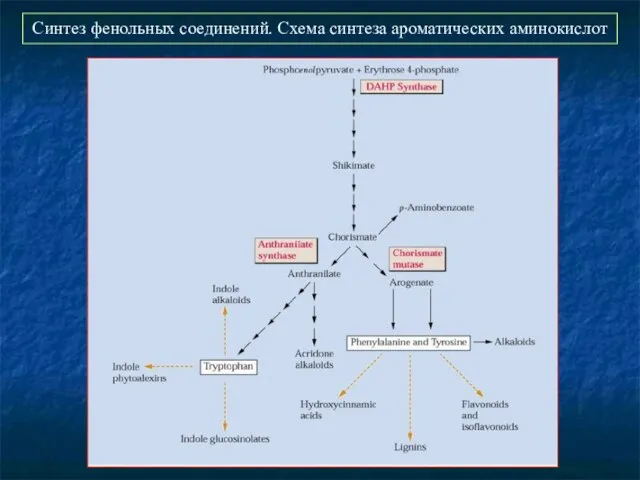
- 24. Синтез фенольных соединений. Схема синтеза ароматических аминокислот
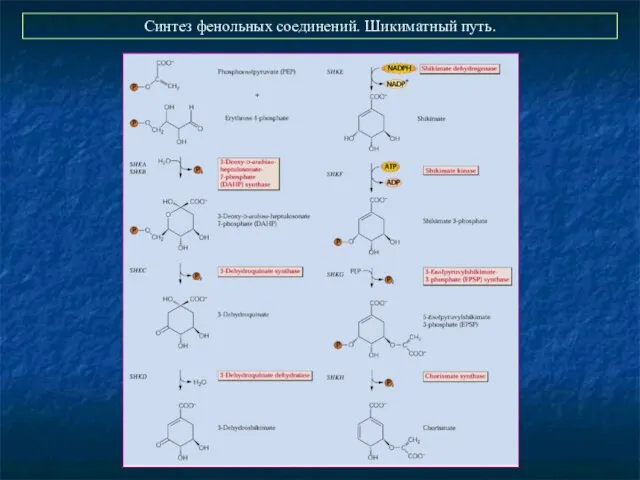
- 25. Синтез фенольных соединений. Шикиматный путь.
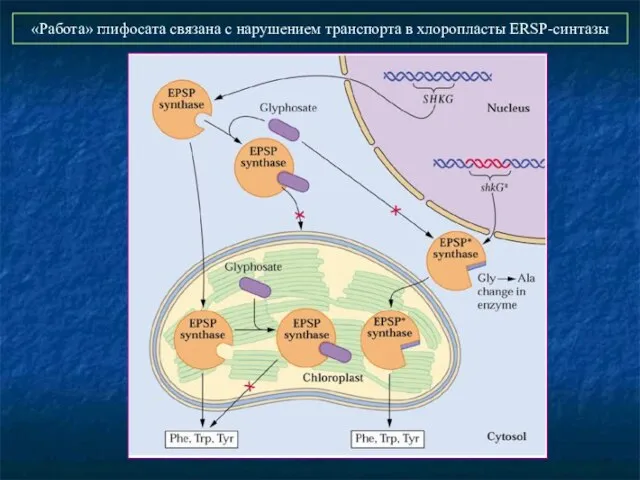
- 26. «Работа» глифосата связана с нарушением транспорта в хлоропласты ERSP-синтазы
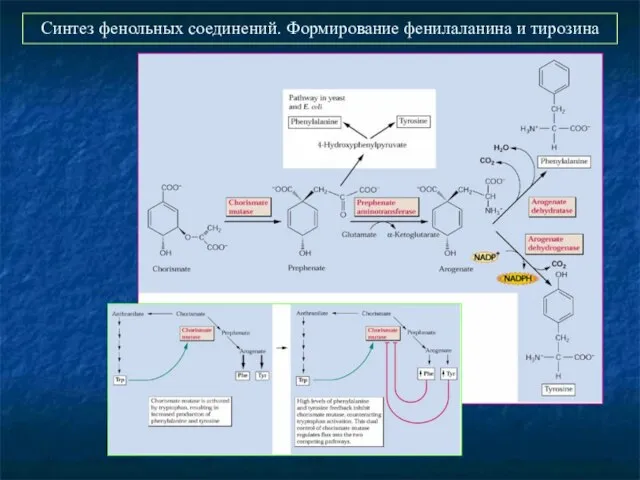
- 27. Синтез фенольных соединений. Формирование фенилаланина и тирозина
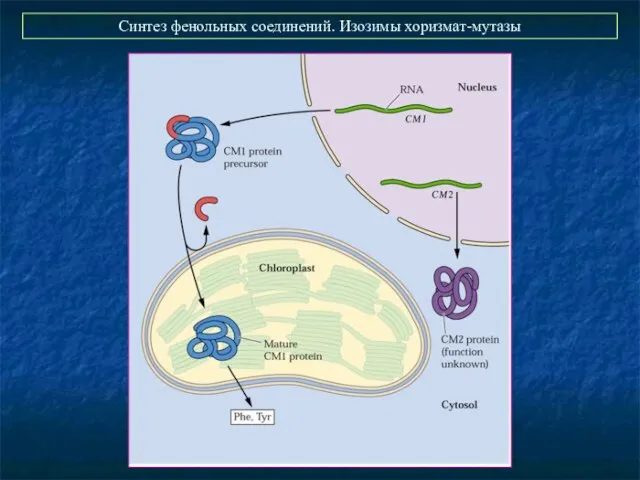
- 28. Синтез фенольных соединений. Изозимы хоризмат-мутазы
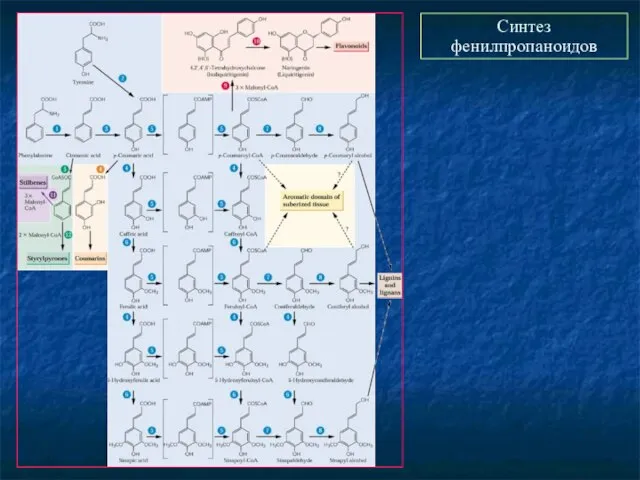
- 29. Синтез фенилпропаноидов
- 30. Синтез фенилпропаноидов.
- 31. Начальные ферменты синтеза фенилпропаноидов Фенилаланин–аммиак-лиаза (ФАЛ, PAL). Первое сообщение – 1961 год (юбилей!), из ячменя, МВ
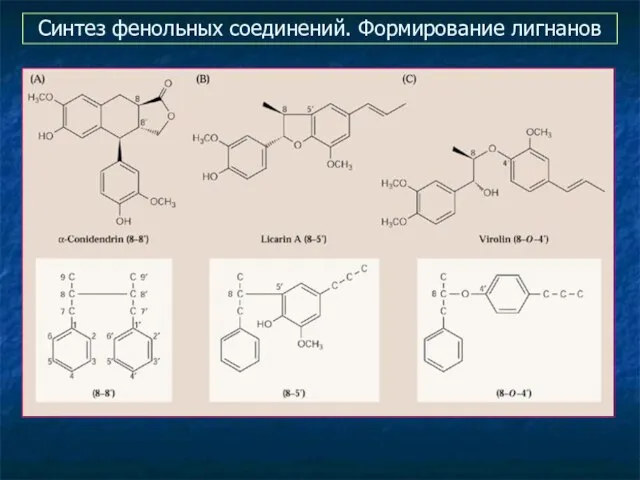
- 32. Синтез фенольных соединений. Формирование лигнанов
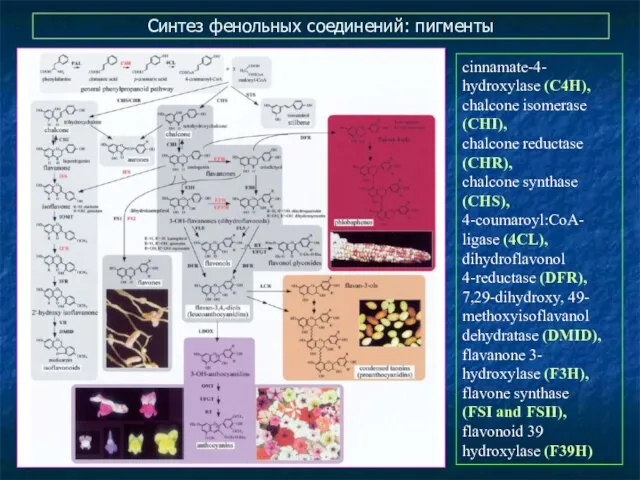
- 33. Синтез фенольных соединений: пигменты cinnamate-4- hydroxylase (C4H), chalcone isomerase (CHI), chalcone reductase (CHR), chalcone synthase (CHS),
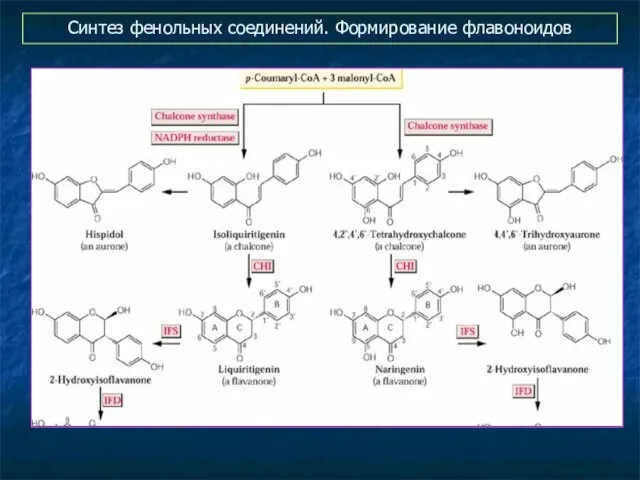
- 34. Формирование флавоноидов
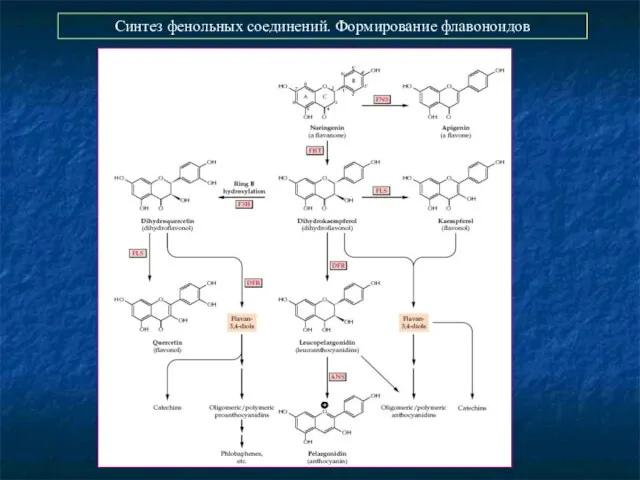
- 35. Синтез фенольных соединений. Формирование флавоноидов
- 36. Синтез фенольных соединений. Формирование флавоноидов
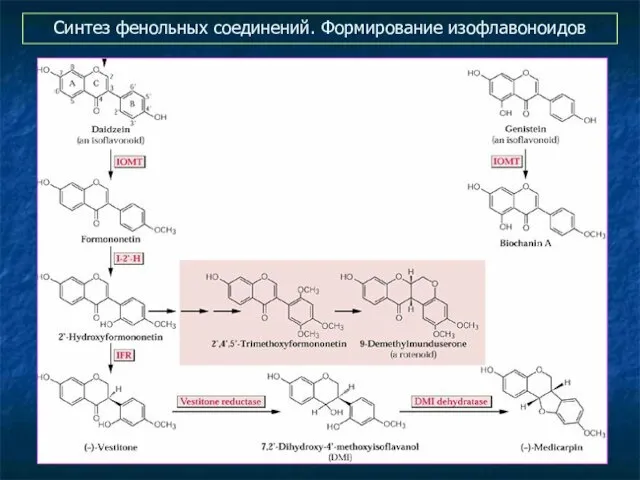
- 37. Синтез фенольных соединений. Формирование изофлавоноидов
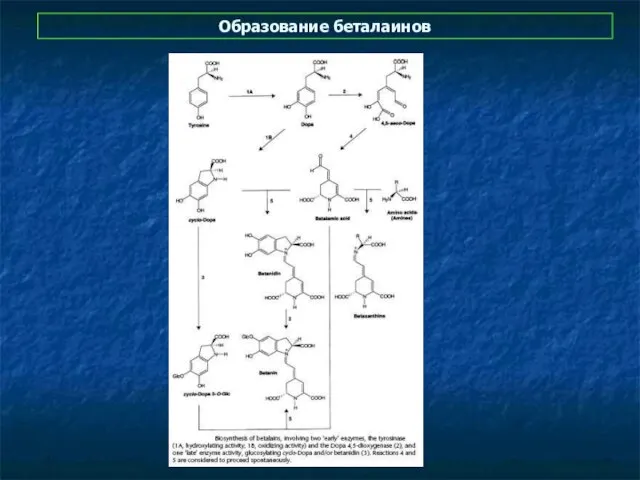
- 38. Образование беталаинов
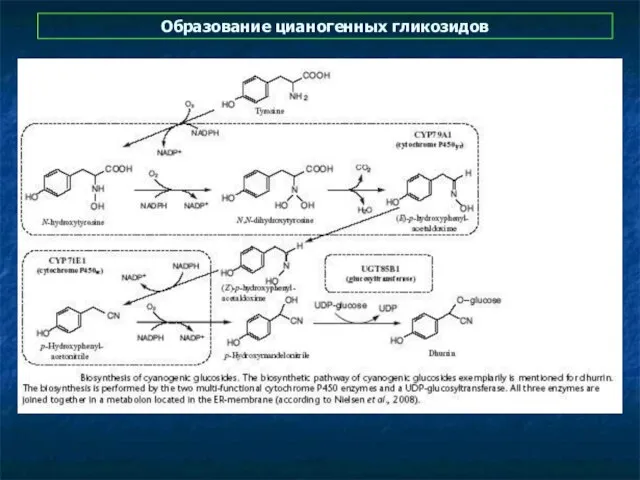
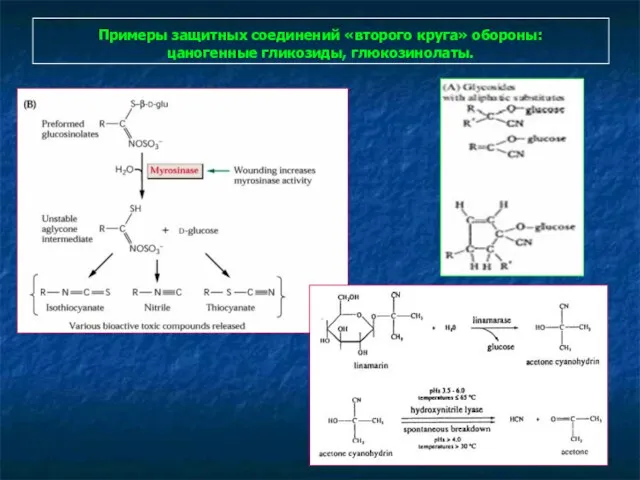
- 39. Синтез цианогенных гликозидов
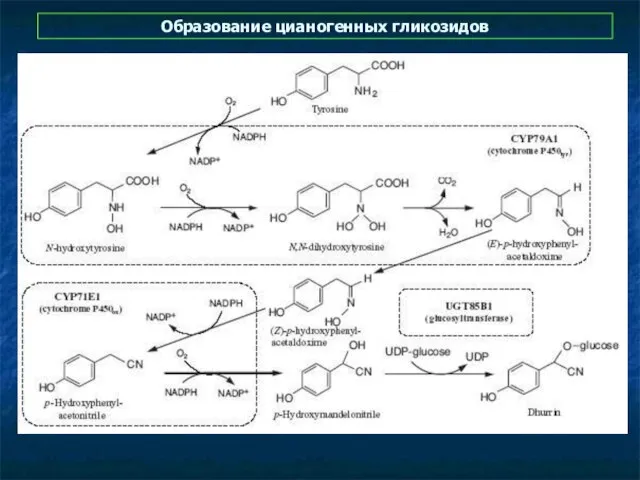
- 40. Образование цианогенных гликозидов
- 41. Образование цианогенных гликозидов
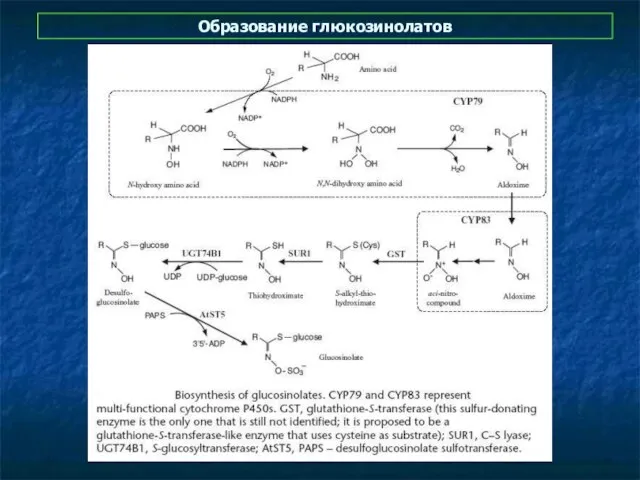
- 42. Образование глюкозинолатов
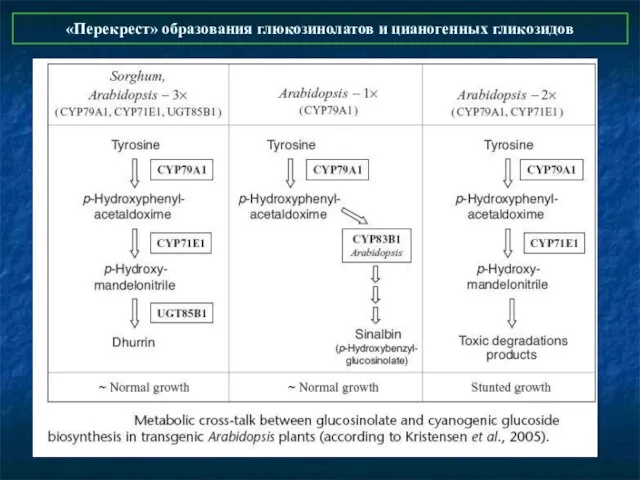
- 43. «Перекрест» образования глюкозинолатов и цианогенных гликозидов
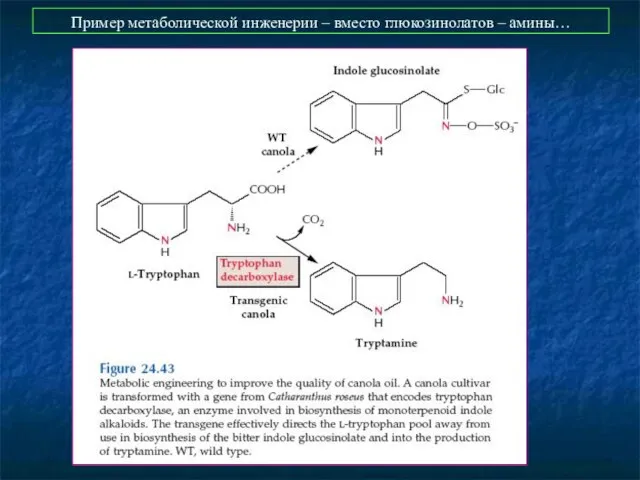
- 44. Пример метаболической инженерии – вместо глюкозинолатов – амины…
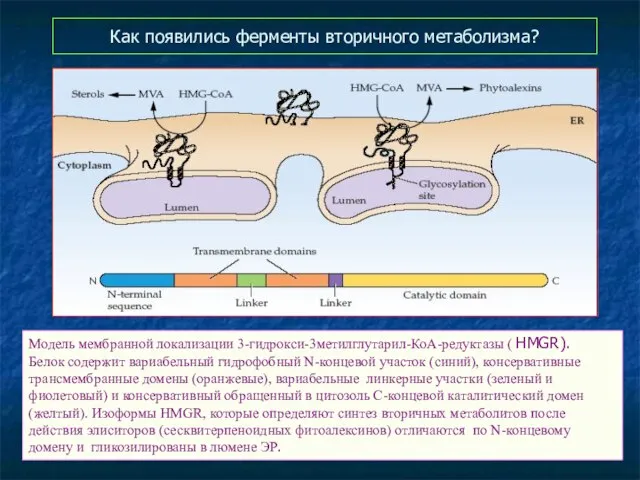
- 45. Как появились ферменты вторичного метаболизма? Модель мембранной локализации 3-гидрокси-3метилглутарил-КоА-редуктазы ( HMGR). Белок содержит вариабельный гидрофобный N-концевой
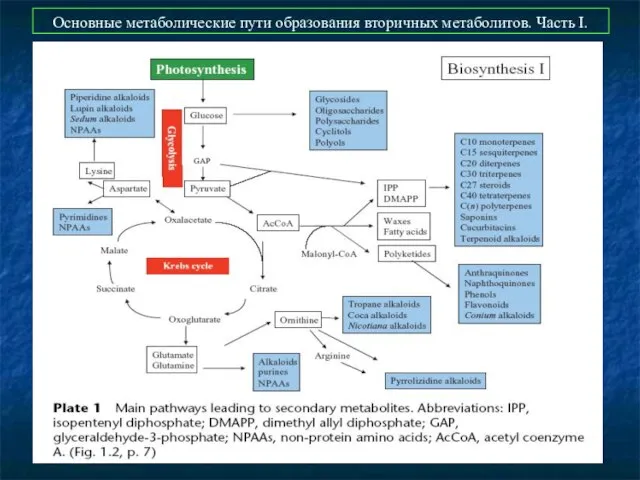
- 46. Основные метаболические пути образования вторичных метаболитов. Часть I.
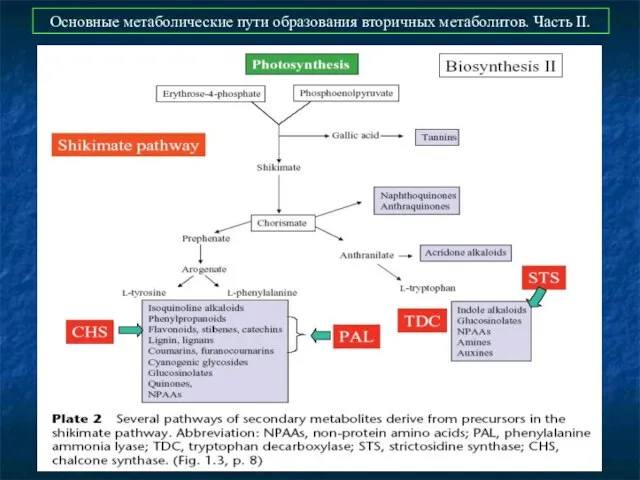
- 47. Основные метаболические пути образования вторичных метаболитов. Часть II.
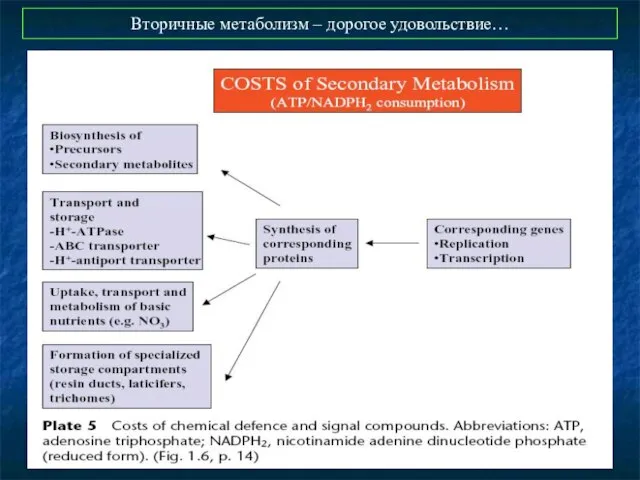
- 48. Вторичные метаболизм – дорогое удовольствие…
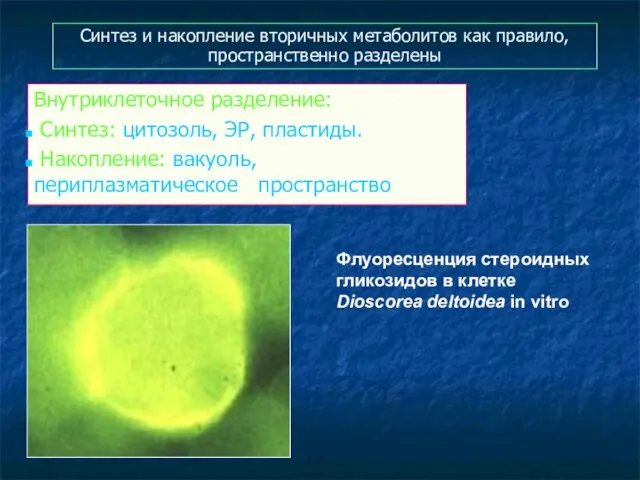
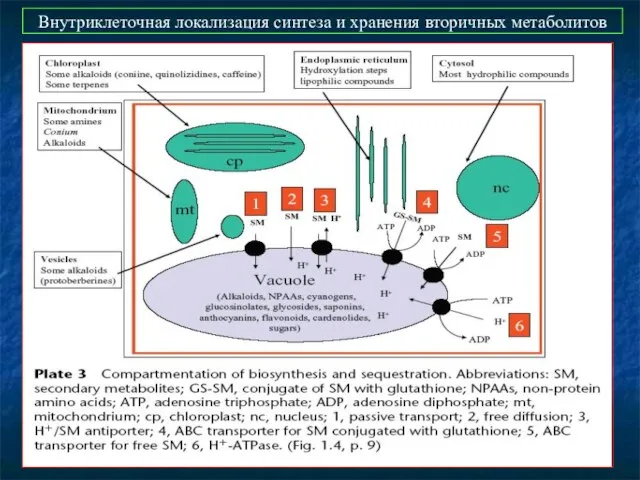
- 49. Синтез и накопление вторичных метаболитов как правило, пространственно разделены Внутриклеточное разделение: Синтез: цитозоль, ЭР, пластиды. Накопление:
- 50. Внутриклеточная локализация синтеза и хранения вторичных метаболитов
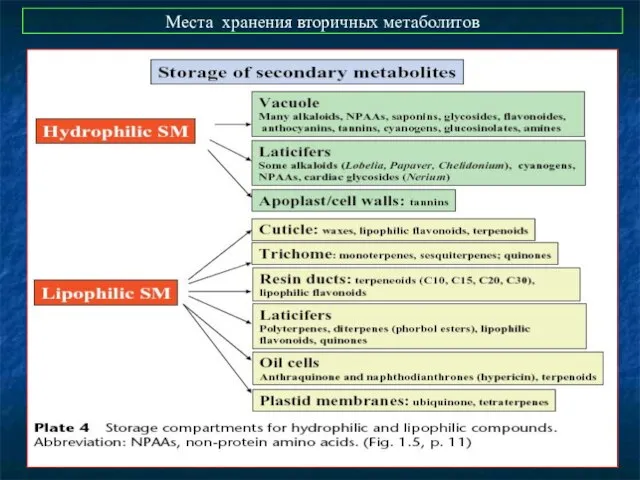
- 51. Места хранения вторичных метаболитов
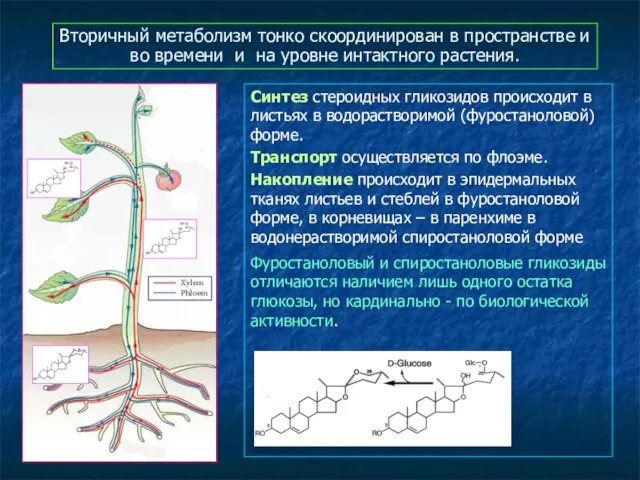
- 52. Вторичный метаболизм тонко скоординирован в пространстве и во времени и на уровне интактного растения. Синтез стероидных
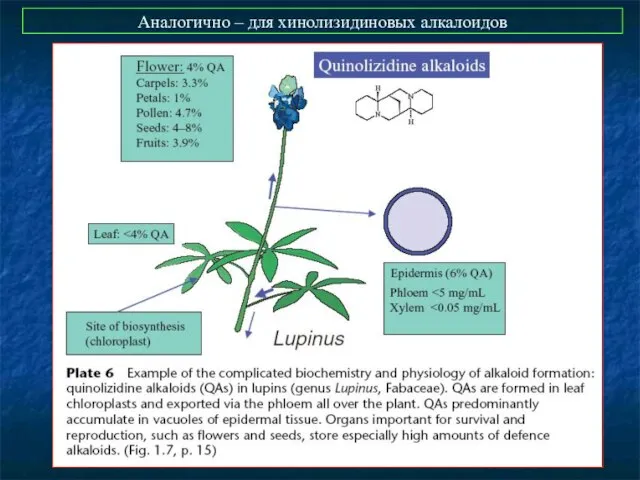
- 53. Аналогично – для хинолизидиновых алкалоидов
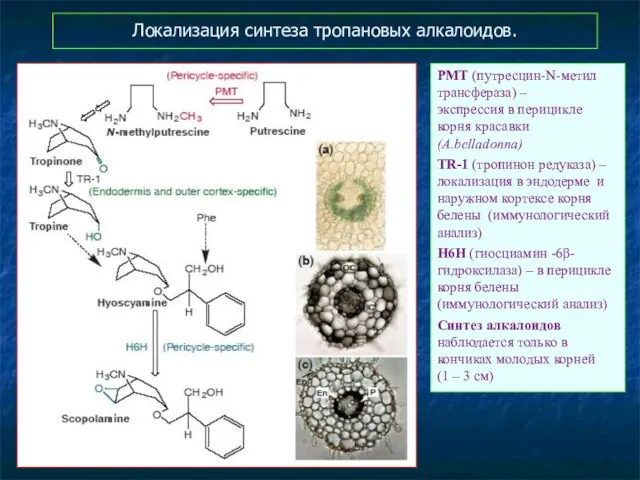
- 54. Локализация синтеза тропановых алкалоидов. PMT (путресцин-N-метил трансфераза) – экспрессия в перицикле корня красавки (A.belladonna) TR-1 (тропинон
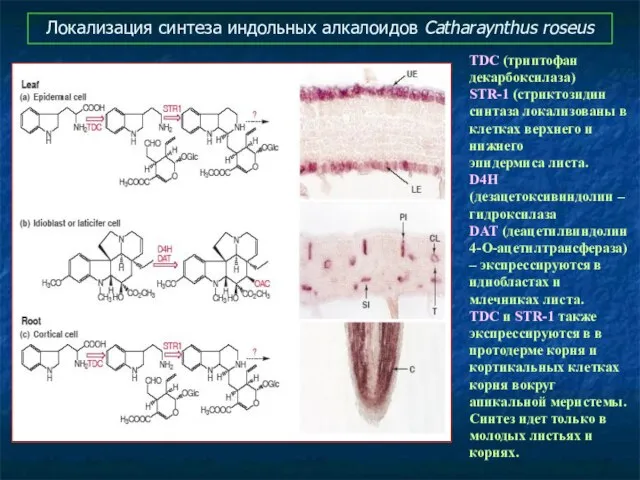
- 55. Локализация синтеза индольных алкалоидов Catharaynthus roseus TDC (триптофан декарбоксилаза) STR-1 (стриктозидин синтаза локализованы в клетках верхнего
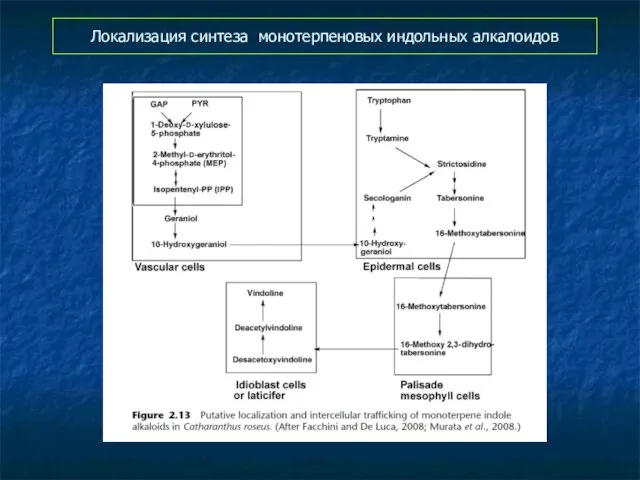
- 56. Локализация синтеза монотерпеновых индольных алкалоидов
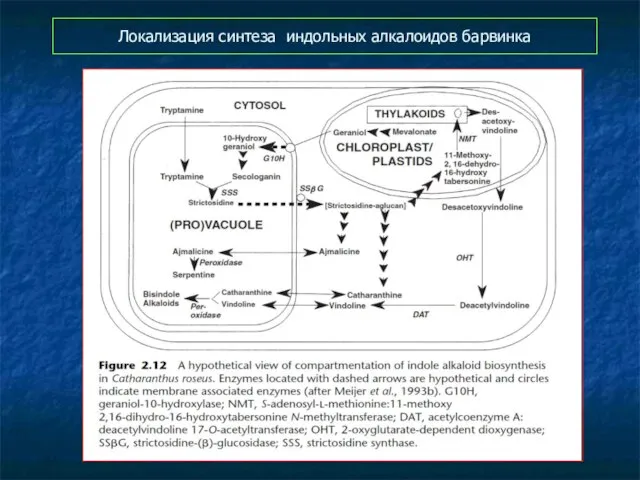
- 57. Локализация синтеза индольных алкалоидов барвинка
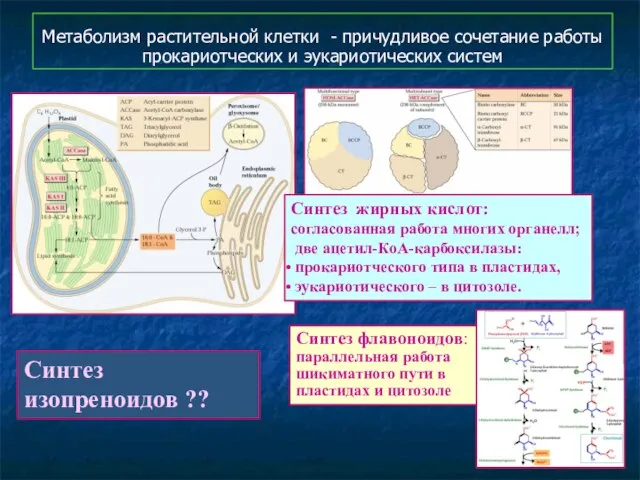
- 58. Метаболизм растительной клетки - причудливое сочетание работы прокариотческих и эукариотических систем Синтез жирных кислот: согласованная работа
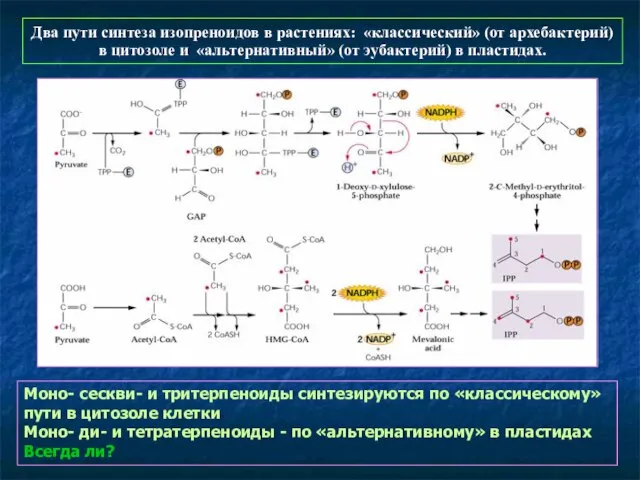
- 59. Два пути синтеза изопреноидов в растениях: «классический» (от архебактерий) в цитозоле и «альтернативный» (от эубактерий) в
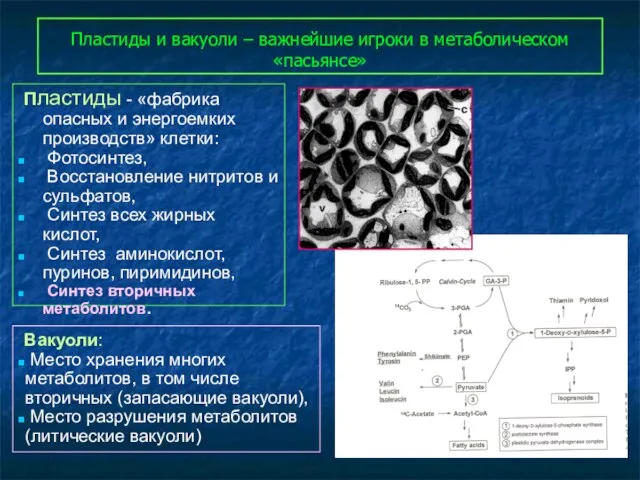
- 60. Пластиды и вакуоли – важнейшие игроки в метаболическом «пасьянсе» Пластиды - «фабрика опасных и энергоемких производств»
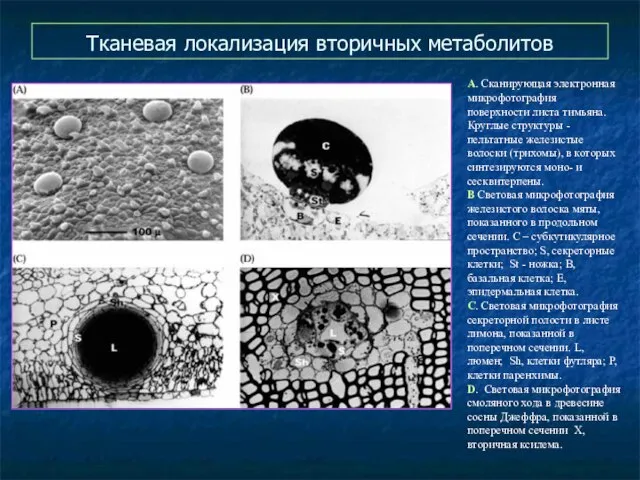
- 61. Тканевая локализация вторичных метаболитов А. Сканирующая электронная микрофотография поверхности листа тимьяна. Круглые структуры - пельтатные железистые
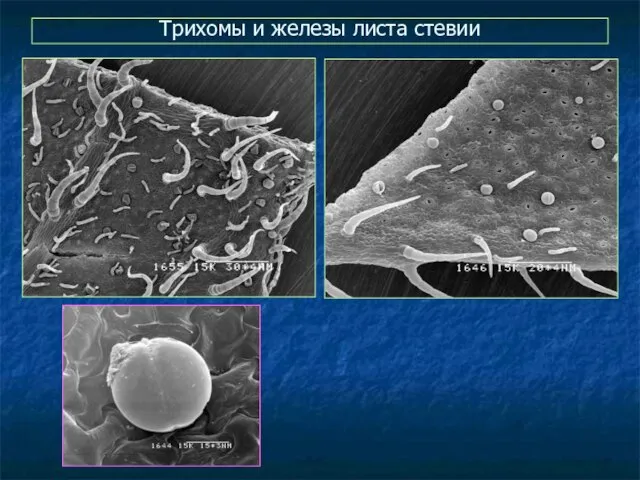
- 62. Трихомы и железы листа стевии
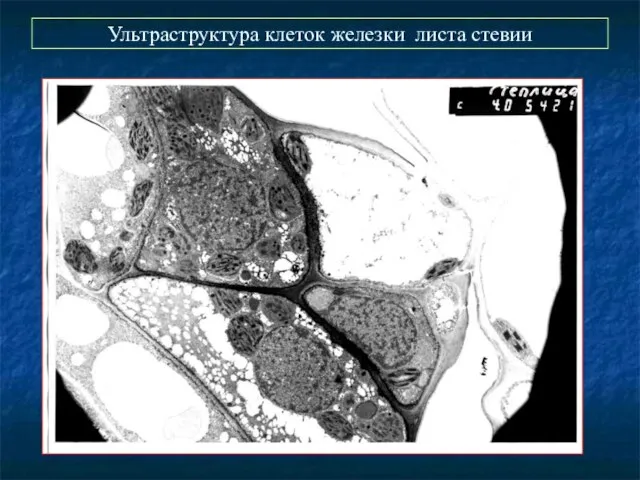
- 63. Ультраструктура клеток железки листа стевии
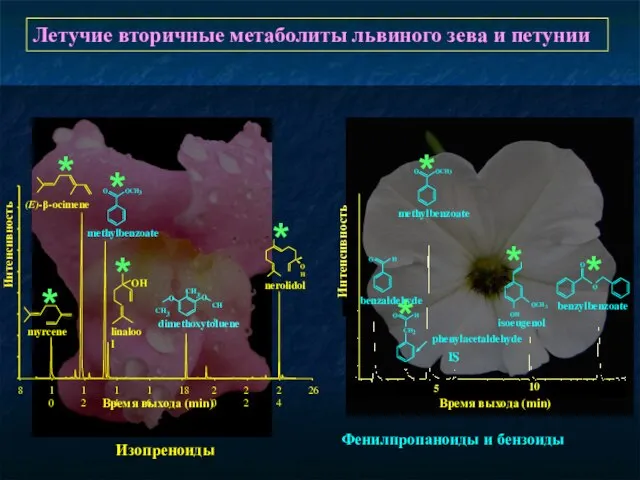
- 64. Летучие вторичные метаболиты львиного зева и петунии myrcene dimethoxytoluene Время выхода (min) Интенсивность (E)-β-ocimene linalool IS
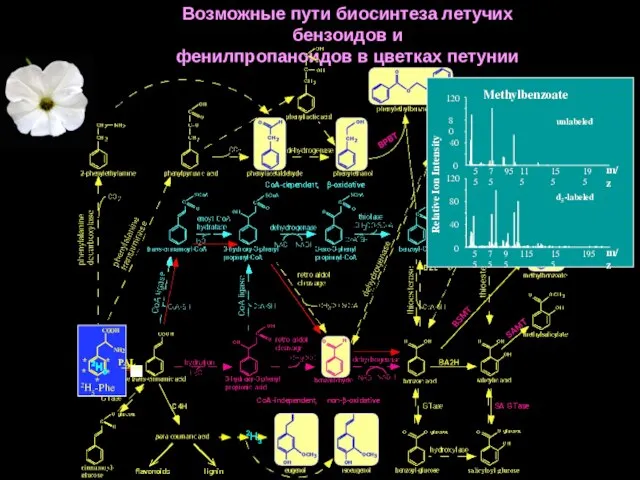
- 65. Возможные пути биосинтеза летучих бензоидов и фенилпропаноидов в цветках петунии 2H5 2H5 2H5 2H5 2H5 2H5
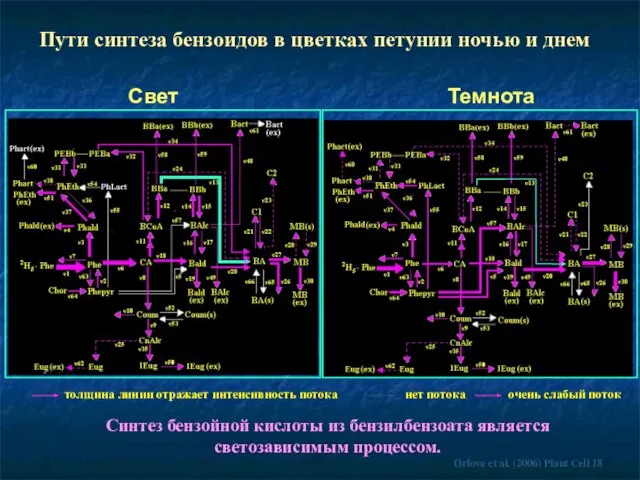
- 66. Свет Пути синтеза бензоидов в цветках петунии ночью и днем Темнота Синтез бензойной кислоты из бензилбензоата
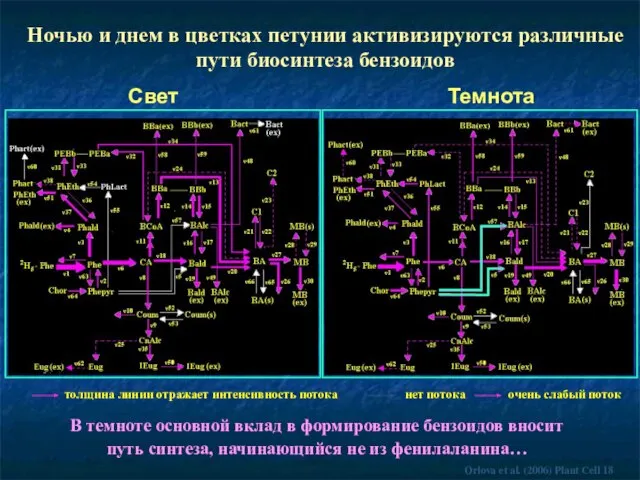
- 67. Свет Ночью и днем в цветках петунии активизируются различные пути биосинтеза бензоидов Темнота В темноте основной
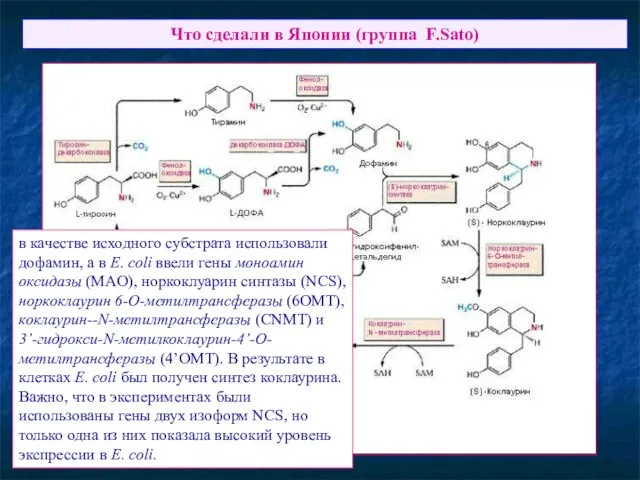
- 68. Что сделали в Японии (группа F.Sato) в качестве исходного субстрата использовали дофамин, а в E. coli
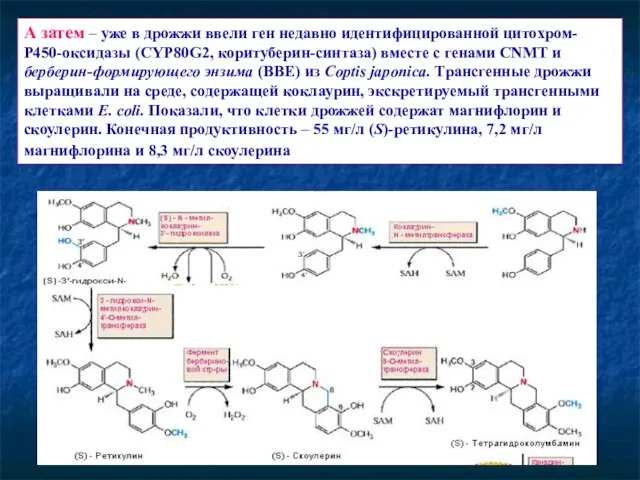
- 69. А затем – уже в дрожжи ввели ген недавно идентифицированной цитохром-Р450-оксидазы (CYP80G2, коритуберин-синтаза) вместе с генами
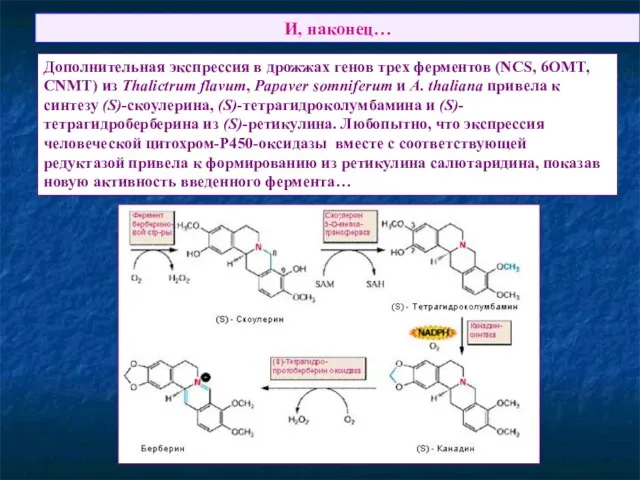
- 70. И, наконец… Дополнительная экспрессия в дрожжах генов трех ферментов (NCS, 6OMT, CNMT) из Thalictrum flavum, Papaver
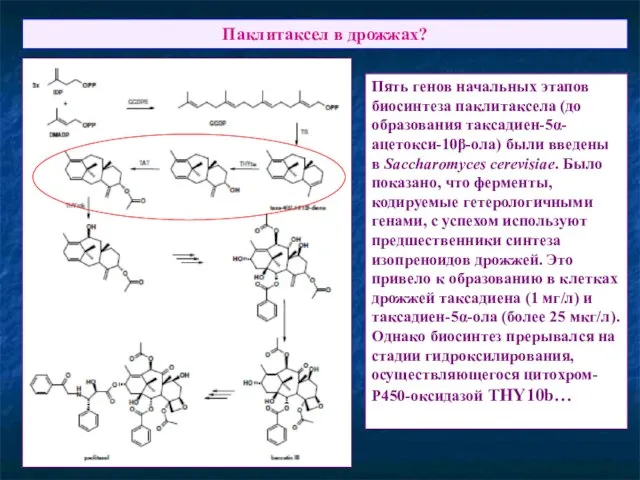
- 71. Паклитаксел в дрожжах? Пять генов начальных этапов биосинтеза паклитаксела (до образования таксадиен-5α-ацетокси-10β-ола) были введены в Saccharomyces
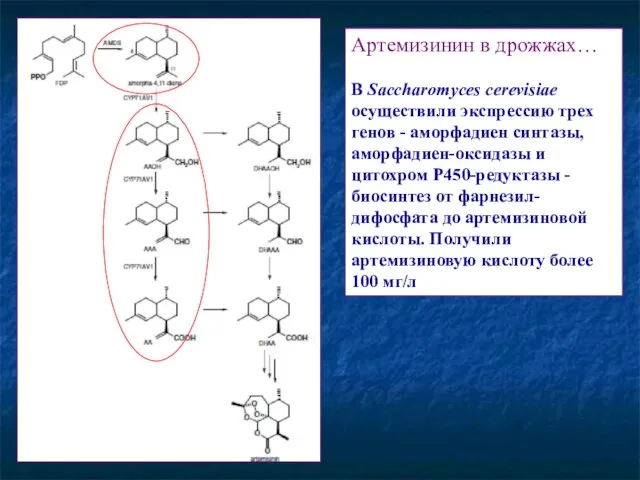
- 72. Артемизинин в дрожжах… В Saccharomyces cerevisiae осуществили экспрессию трех генов - аморфадиен синтазы, аморфадиен-оксидазы и цитохром
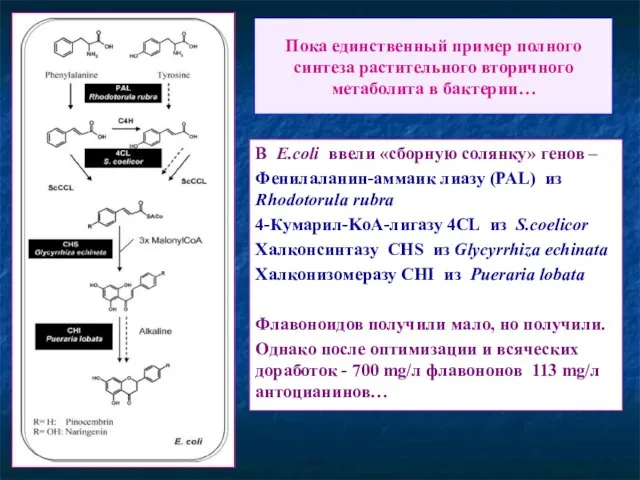
- 73. Пока единственный пример полного синтеза растительного вторичного метаболита в бактерии… В E.coli ввели «сборную солянку» генов
- 74. Зачем нужен вторичный метаболизм растению? Основные точки зрения: Совсем не нужен (вторичные метаболиты – «отходы производства»)
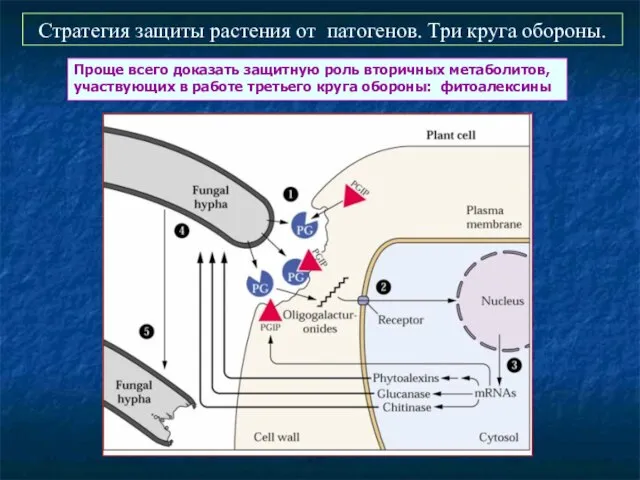
- 75. Стратегия защиты растения от патогенов. Три круга обороны. Проще всего доказать защитную роль вторичных метаболитов, участвующих
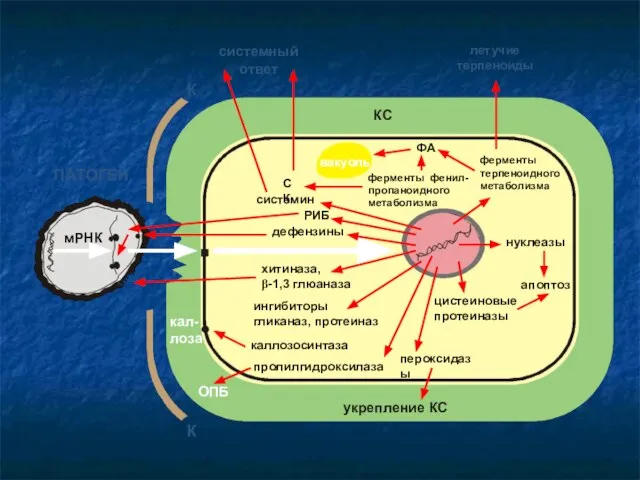
- 77. ПАТОГЕН системин ферменты терпеноидного метаболизма ФА СК ингибиторы гликаназ, протеиназ пролилгидроксилаза каллозосинтаза летучие терпеноиды цистеиновые протеиназы
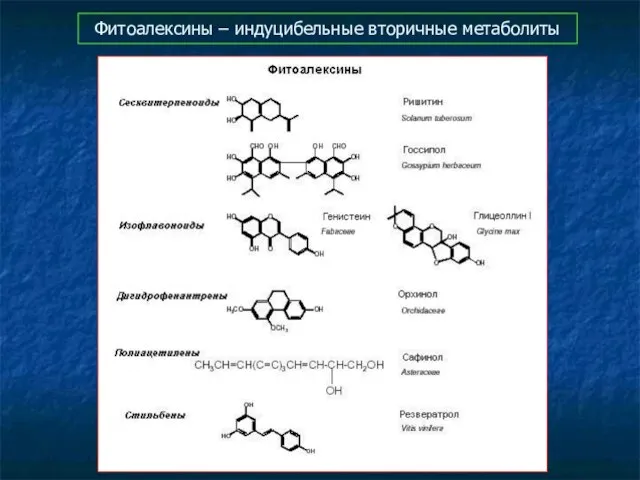
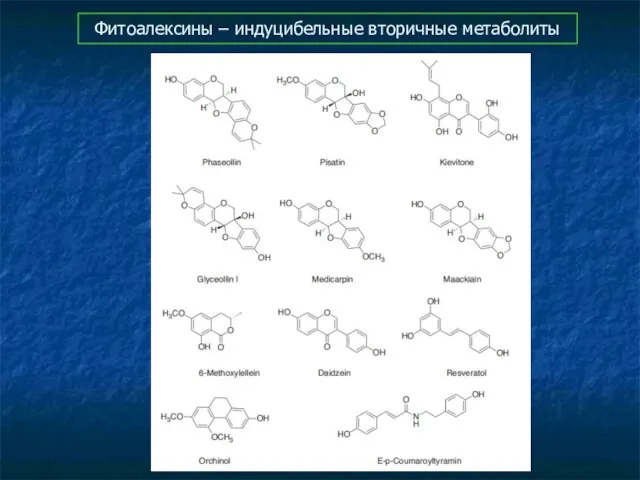
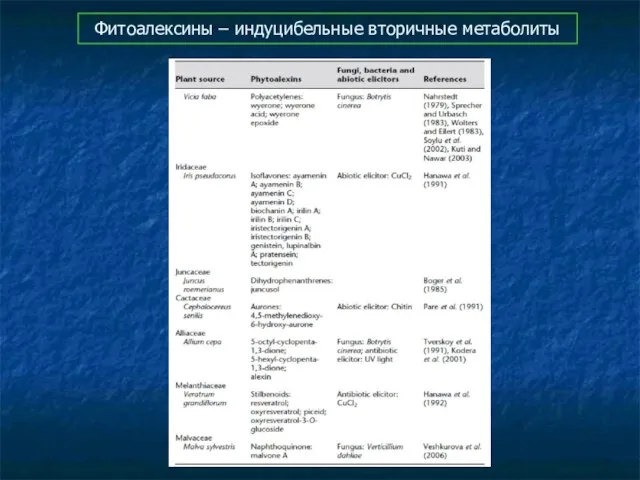
- 78. Фитоалексины – индуцибельные вторичные метаболиты
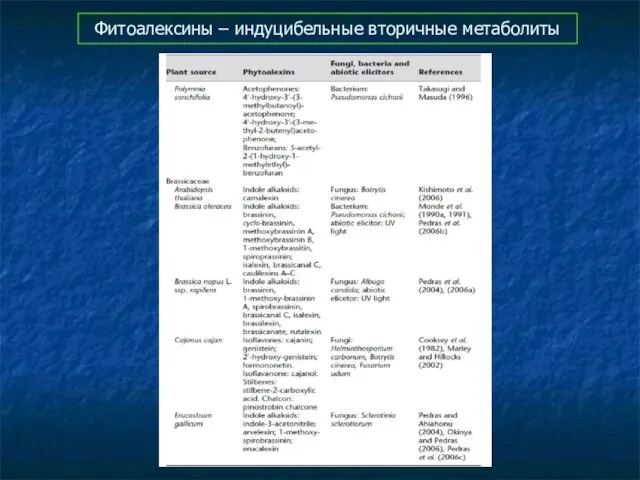
- 79. Фитоалексины – индуцибельные вторичные метаболиты
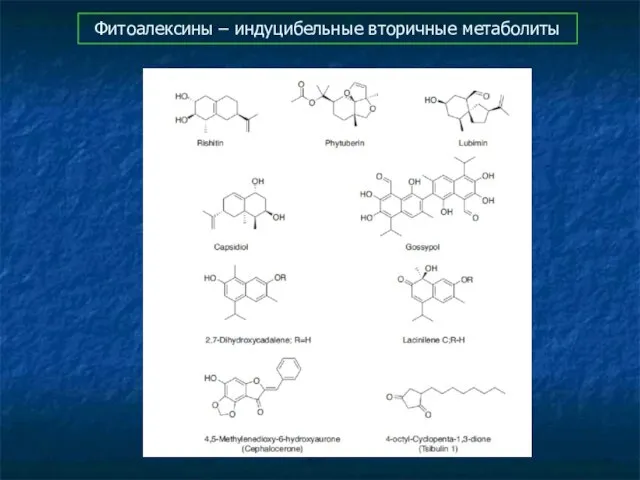
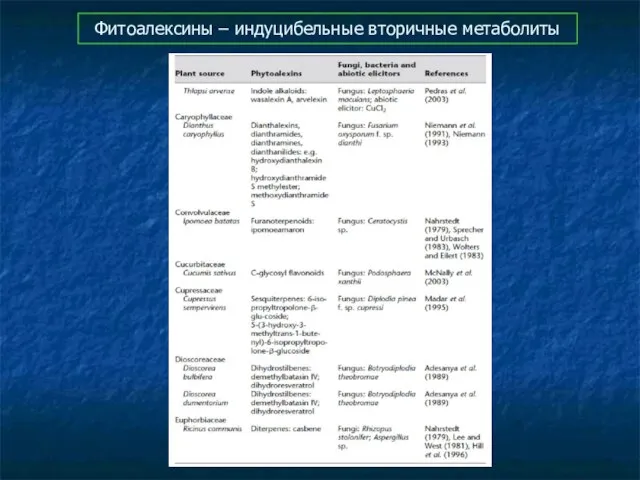
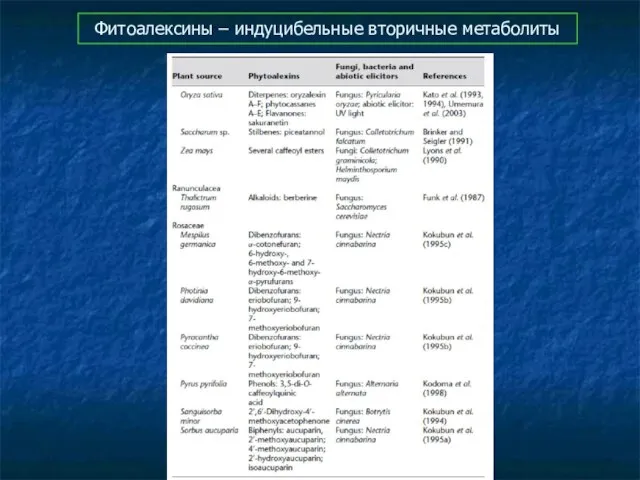
- 80. Фитоалексины – индуцибельные вторичные метаболиты
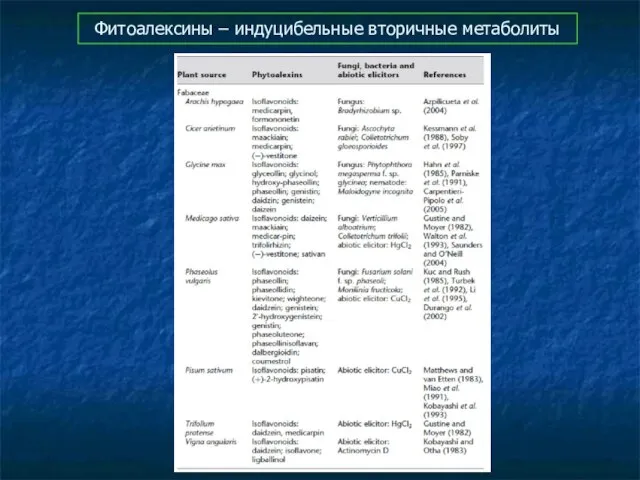
- 81. Фитоалексины – индуцибельные вторичные метаболиты
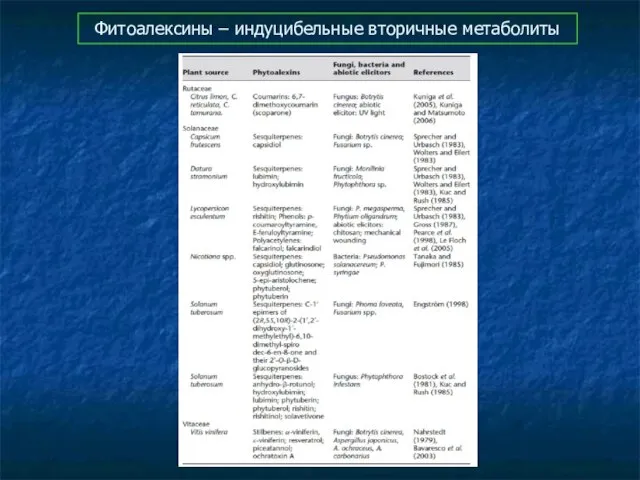
- 82. Фитоалексины – индуцибельные вторичные метаболиты
- 83. Фитоалексины – индуцибельные вторичные метаболиты
- 84. Фитоалексины – индуцибельные вторичные метаболиты
- 85. Фитоалексины – индуцибельные вторичные метаболиты
- 86. Фитоалексины – индуцибельные вторичные метаболиты
- 87. Фитоалексины – индуцибельные вторичные метаболиты
- 88. Фитоалексины – индуцибельные вторичные метаболиты
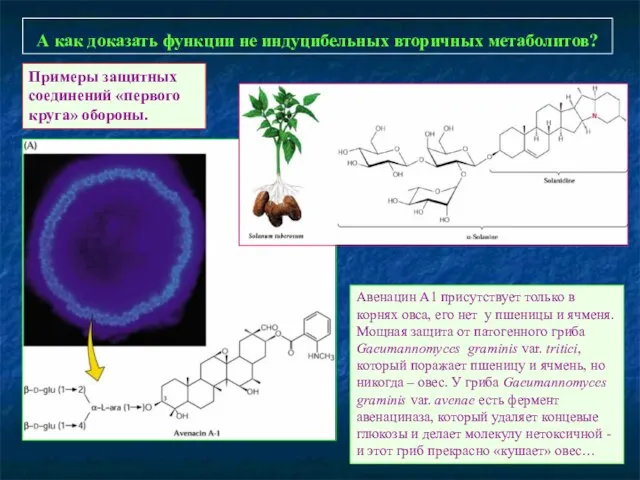
- 89. А как доказать функции не индуцибельных вторичных метаболитов? Авенацин А1 присутствует только в корнях овса, его
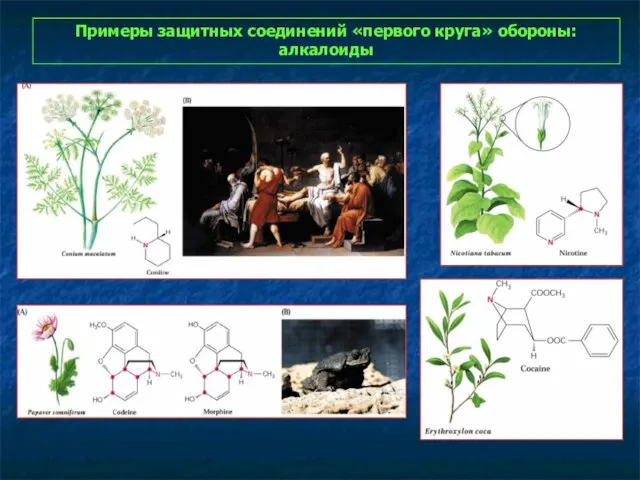
- 90. Примеры защитных соединений «первого круга» обороны: алкалоиды
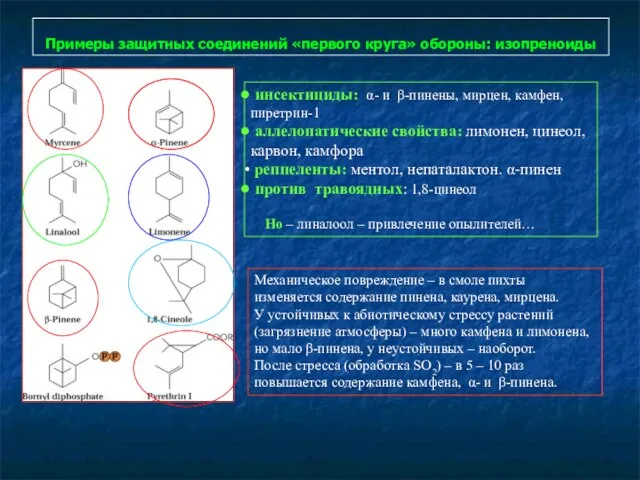
- 91. Примеры защитных соединений «первого круга» обороны: изопреноиды инсектициды: α- и β-пинены, мирцен, камфен, пиретрин-1 аллелопатические свойства:
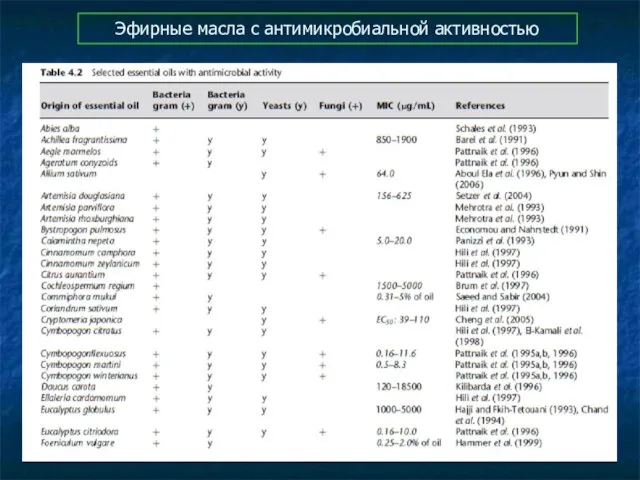
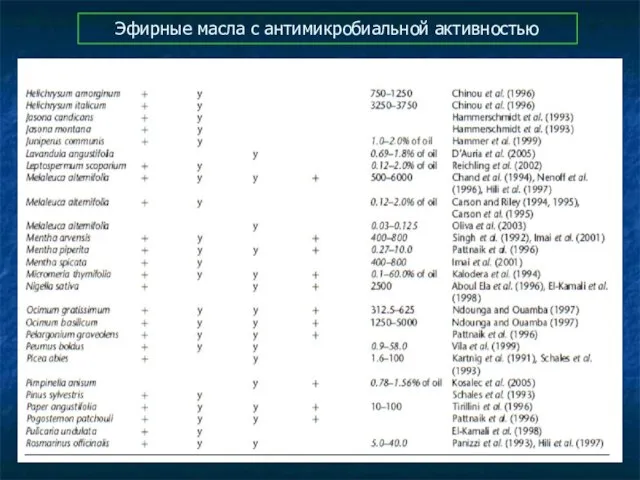
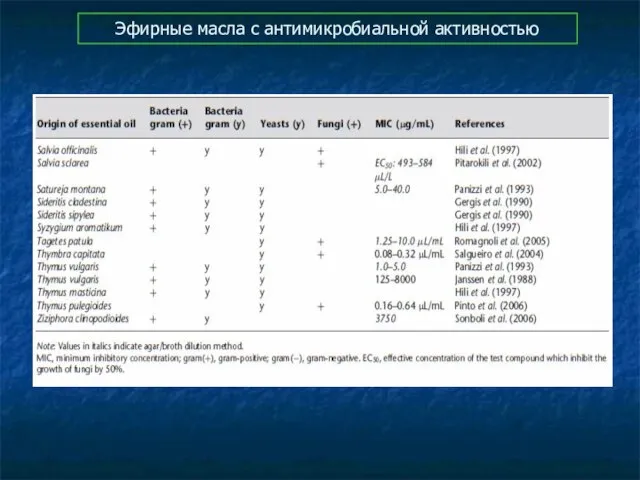
- 92. Эфирные масла с антимикробиальной активностью
- 93. Эфирные масла с антимикробиальной активностью
- 94. Эфирные масла с антимикробиальной активностью
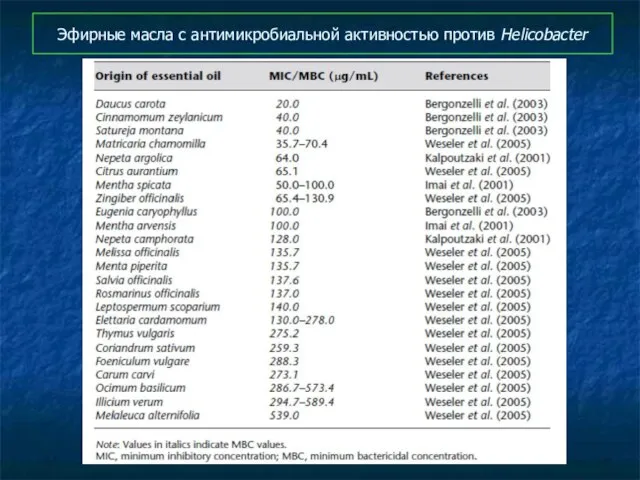
- 95. Эфирные масла с антимикробиальной активностью против Helicobacter
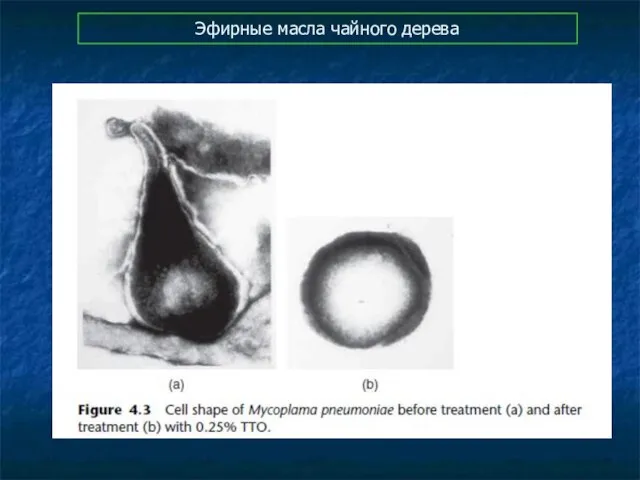
- 96. Эфирные масла чайного дерева
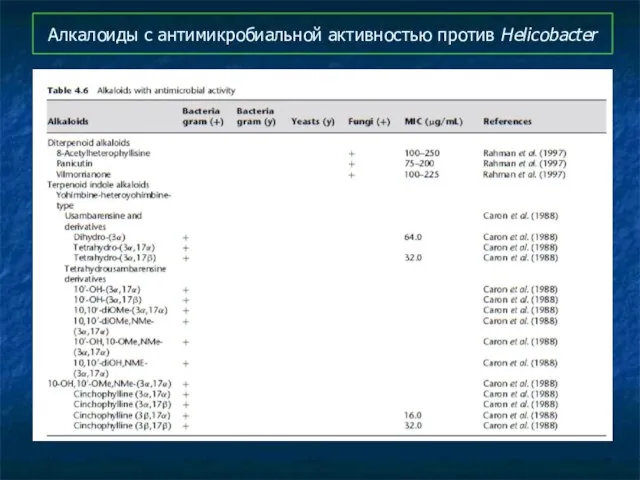
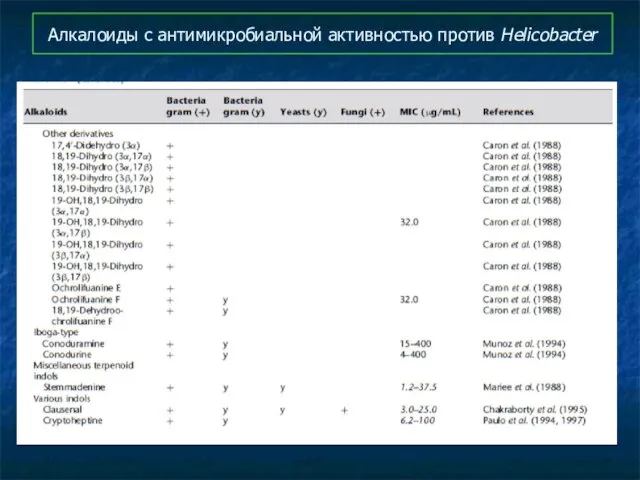
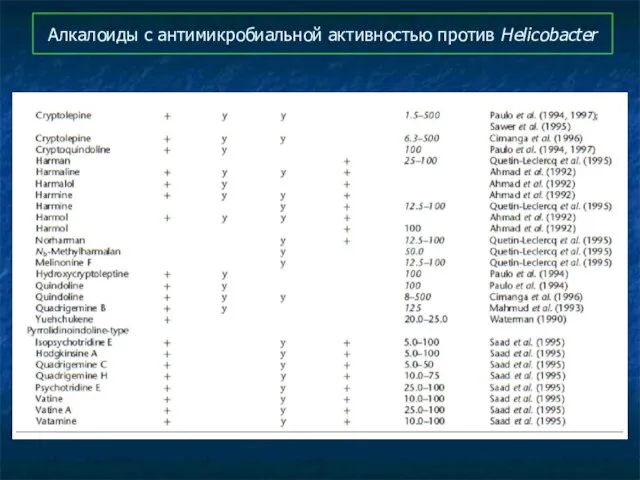
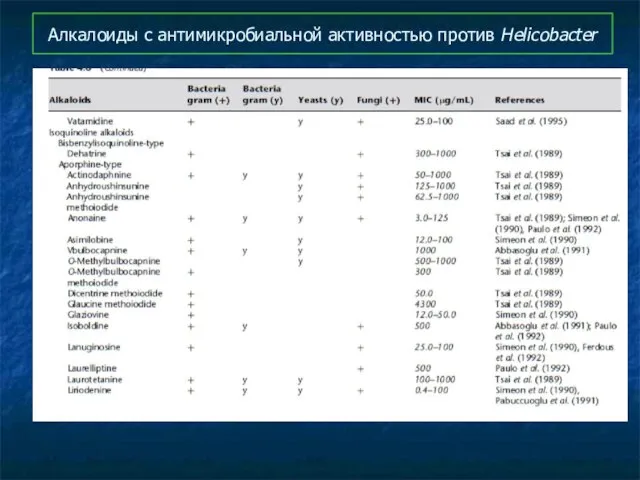
- 97. Алкалоиды с антимикробиальной активностью против Helicobacter
- 98. Алкалоиды с антимикробиальной активностью против Helicobacter
- 99. Алкалоиды с антимикробиальной активностью против Helicobacter
- 100. Алкалоиды с антимикробиальной активностью против Helicobacter
- 101. Антивирусная активность эфирных масел Plant source Viruses IC50 (%; ppm) References Herpes simplex virus ( HSV;
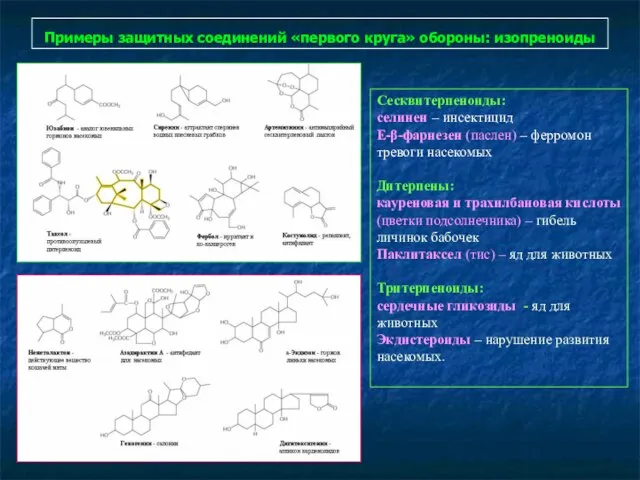
- 102. Примеры защитных соединений «первого круга» обороны: изопреноиды Сесквитерпеноиды: селинен – инсектицид Е-β-фарнезен (паслен) – ферромон тревоги
- 103. Защитное действие смол. Массовая атака короедов сосны на ствол Pinus contorta. Каждое белое пятно на стволе
- 104. Примеры защитных соединений «второго круга» обороны: цаногенные гликозиды, глюкозинолаты.
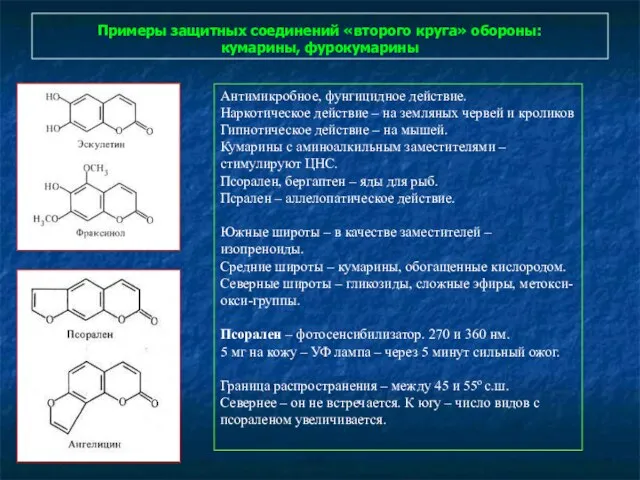
- 105. Примеры защитных соединений «второго круга» обороны: кумарины, фурокумарины Антимикробное, фунгицидное действие. Наркотическое действие – на земляных
- 106. Но: постоянное присутствие и биологическая активность не являются достаточным доказательством. Что делать? Один из возможных подходов
- 107. Но: постоянное присутствие и биологическая активность не являются достаточным доказательством. Что делать? Снятие организменного контроля развития
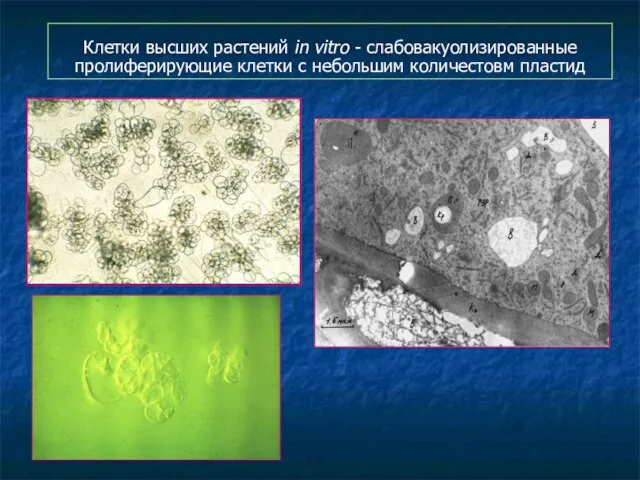
- 108. Клетки высших растений in vitro - слабовакуолизированные пролиферирующие клетки с небольшим количестовм пластид
- 109. Некоторые закономерности синтеза вторичных метаболитов в культуре клеток высших растений Избирательная возможность синтеза метаболитов не получен
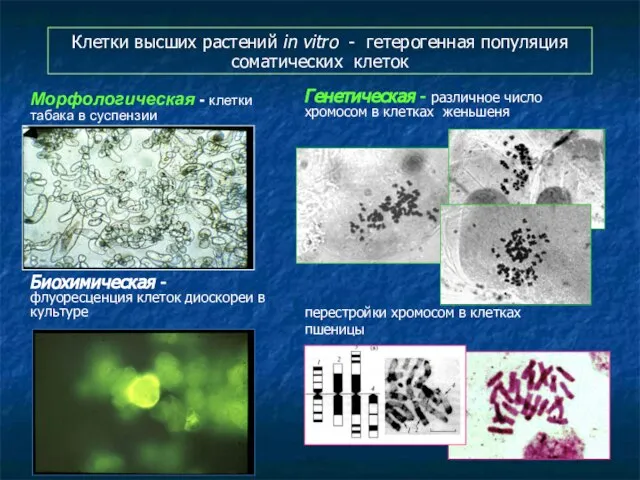
- 110. Клетки высших растений in vitro - гетерогенная популяция соматических клеток Морфологическая - клетки табака в суспензии
- 111. Вторичный метаболизм в клетках in vitro - синтез изопреноидов Dioscirea deltoidea стероидные гликозиды Panax ginseng, P.
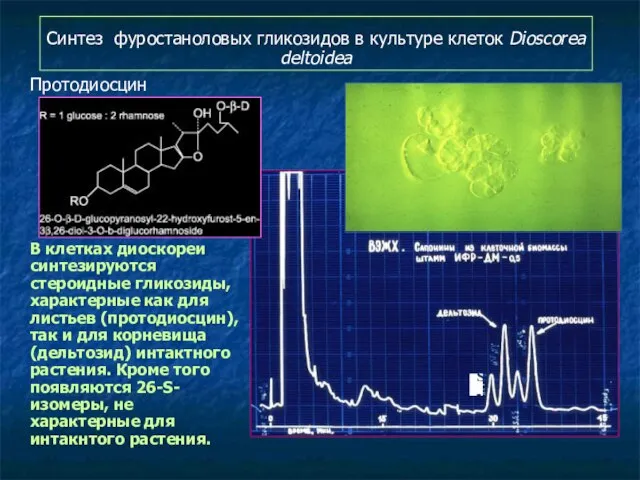
- 112. Синтез фуростаноловых гликозидов в культуре клеток Dioscorea deltoidea Протодиосцин В клетках диоскореи синтезируются стероидные гликозиды, характерные
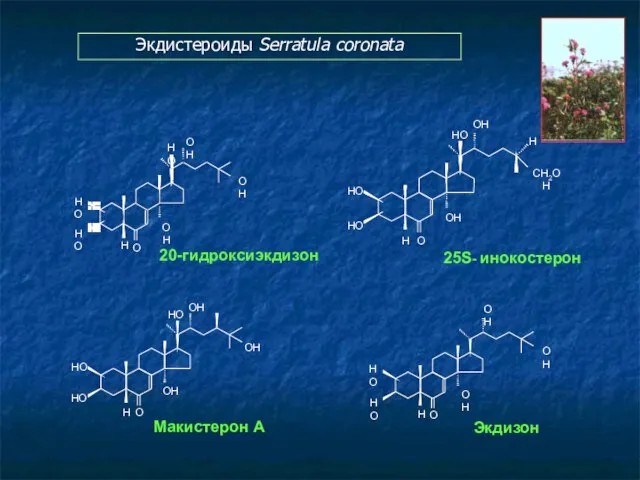
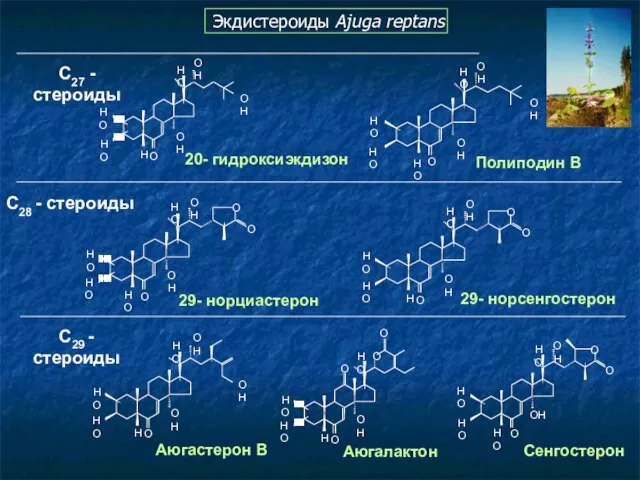
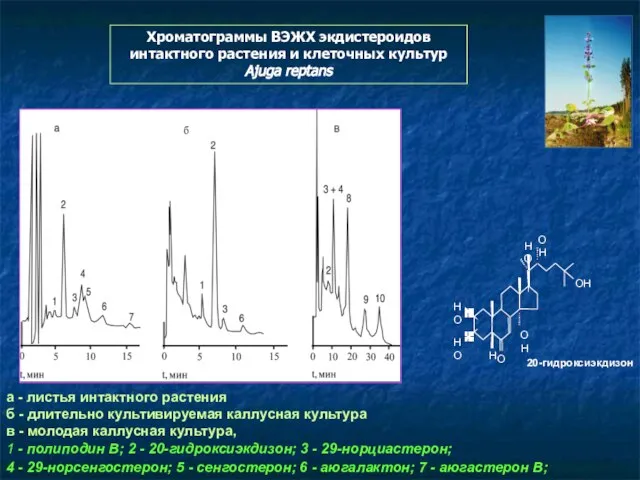
- 113. Экдистероиды Serratula coronata
- 114. C28 - стероиды
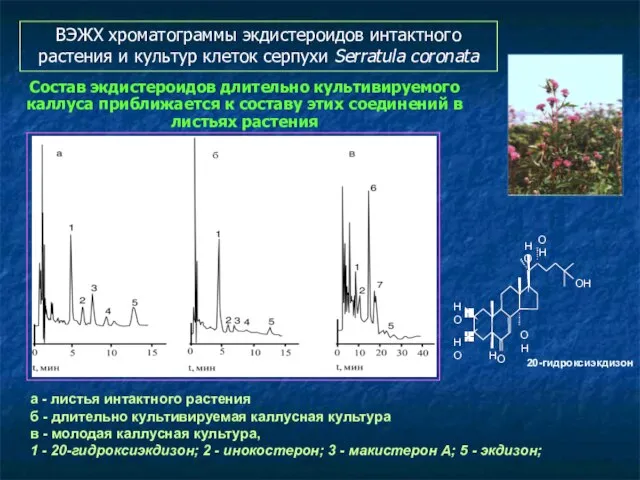
- 115. а - листья интактного растения б - длительно культивируемая каллусная культура в - молодая каллусная культура,
- 116. а - листья интактного растения б - длительно культивируемая каллусная культура в - молодая каллусная культура,
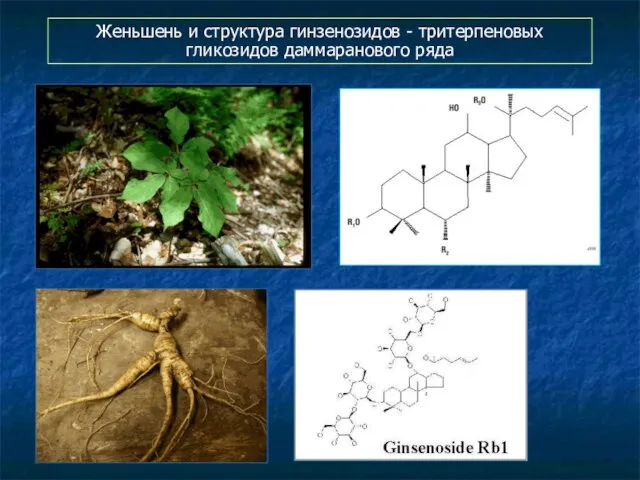
- 117. Женьшень и структура гинзенозидов - тритерпеновых гликозидов даммаранового ряда
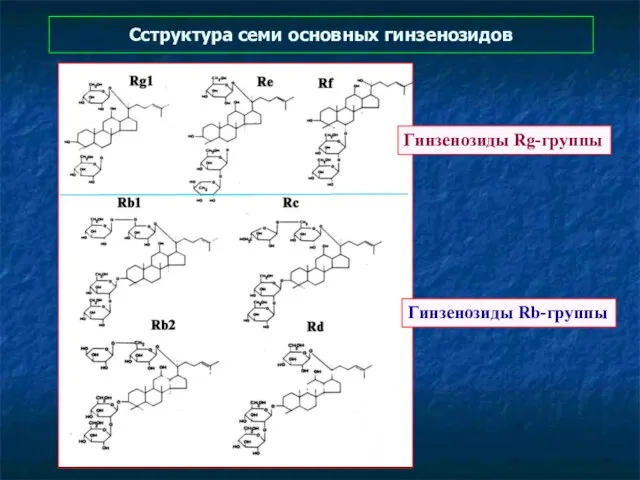
- 118. Cструктура семи основных гинзенозидов Гинзенозиды Rg-группы Гинзенозиды Rb-группы
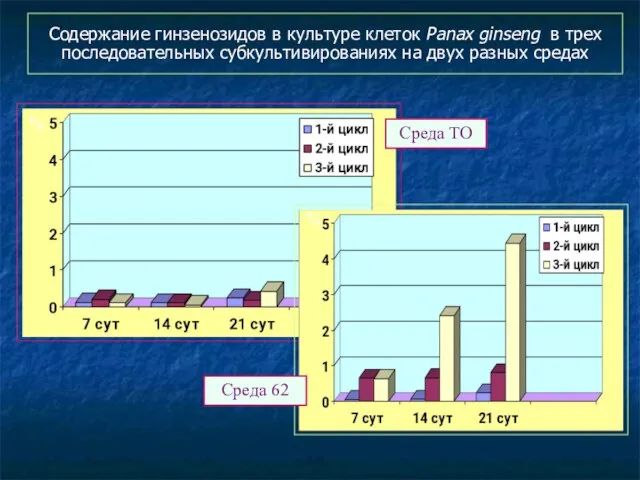
- 119. Содержание гинзенозидов в культуре клеток Panax ginseng в трех последовательных субкультивированиях на двух разных средах %
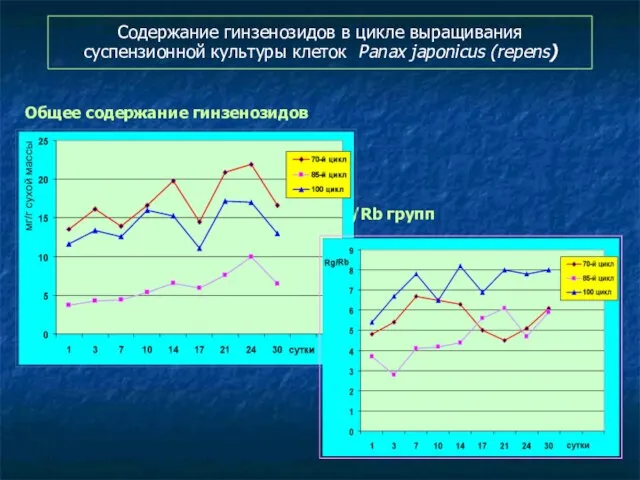
- 120. Содержание гинзенозидов в цикле выращивания суспензионной культуры клеток Panax japonicus (repens) Общее содержание гинзенозидов Соотношение Rg/Rb
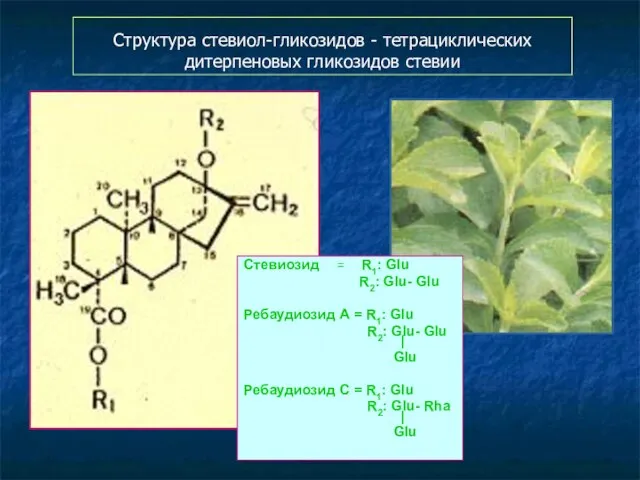
- 121. Структура стевиол-гликозидов - тетрациклических дитерпеновых гликозидов стевии Стевиозид = R1: Glu R2: Glu- Glu Ребаудиозид А
- 122. Содержание стевиол-гликозидов в интактных растениях Stevia rebaudiana и культурах in vitro (mg/g) 1. Intact plant 1.
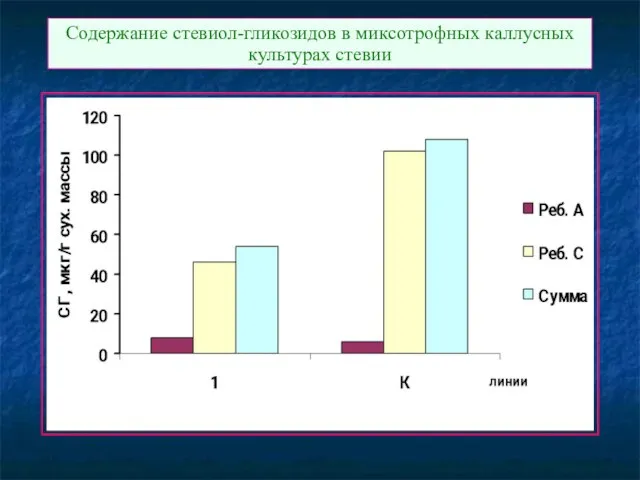
- 123. Содержание стевиол-гликозидов в миксотрофных каллусных культурах стевии
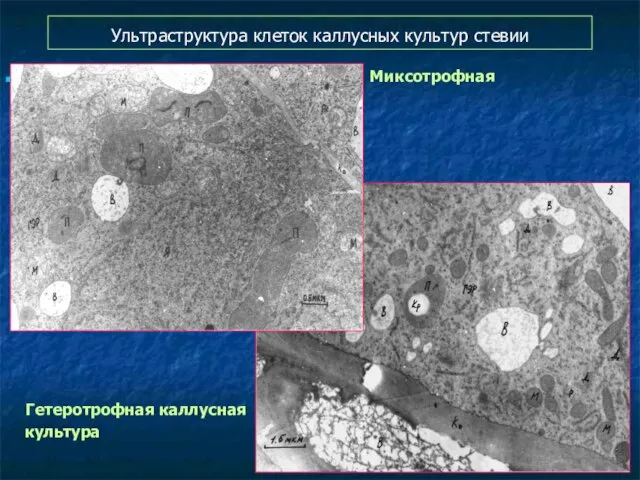
- 124. Ультраструктура клеток каллусных культур стевии Миксотрофная каллусная культура Гетеротрофная каллусная культура
- 126. Скачать презентацию



















 Животные. Пищеварительная система. Обмен веществ
Животные. Пищеварительная система. Обмен веществ Цестоды. Свиной цепень
Цестоды. Свиной цепень Пищевые ресурсы
Пищевые ресурсы Нетрадиционные способы посадки. Огород на окне
Нетрадиционные способы посадки. Огород на окне Кровь: состав и выполняемые функции
Кровь: состав и выполняемые функции Определение пола и наследование признаков, сцепленных с полом
Определение пола и наследование признаков, сцепленных с полом Кто кому помогает?
Кто кому помогает? Мифы и легенды о грибах
Мифы и легенды о грибах Ткани растений Урок биологии 6 класс
Ткани растений Урок биологии 6 класс Обмен веществ в организме человека
Обмен веществ в организме человека Витамины сырья и продуктов питания
Витамины сырья и продуктов питания Бесполое и половое размножение
Бесполое и половое размножение ЭНДОКРИННАЯ СИСТЕМА
ЭНДОКРИННАЯ СИСТЕМА  Развитие жизни на Земле
Развитие жизни на Земле Технология рекомбинантных ДНК. (Лекция 1)
Технология рекомбинантных ДНК. (Лекция 1) Презентация на тему "Царства" - скачать презентации по Биологии
Презентация на тему "Царства" - скачать презентации по Биологии Значение млекопитающих в природе и жизни человека.
Значение млекопитающих в природе и жизни человека. Анатомия репродуктивной системы
Анатомия репродуктивной системы ПАРАЗИТИЗМ Выполнила Кириллова Анастасия.
ПАРАЗИТИЗМ Выполнила Кириллова Анастасия. Амфибилер
Амфибилер Артерии и вены большого круга кровообращения
Артерии и вены большого круга кровообращения Общая характеристика голосеменных растений
Общая характеристика голосеменных растений Презентация на тему "Строение пищеварительной системы" - скачать бесплатно презентации по Биологии_
Презентация на тему "Строение пищеварительной системы" - скачать бесплатно презентации по Биологии_ Lemur. Animal world
Lemur. Animal world Интеллектуальная игра день птиц
Интеллектуальная игра день птиц Периодическая тимпания рубца у телят
Периодическая тимпания рубца у телят 2 Морфология микроорганизмов(прокариоты)
2 Морфология микроорганизмов(прокариоты) Презентация на тему "Виды вирусных заболеваний человека, животных и растений" - скачать презентации по Биологии
Презентация на тему "Виды вирусных заболеваний человека, животных и растений" - скачать презентации по Биологии