Содержание
- 2. Биохимия – наука, изучающая организмы методами химии и родственных дисциплин (Ю. А. Овчинников) Биохимия – наука
- 3. Молекулярная биология - Наука об атомно-молекулярной структуре и функциях биополимеров в клетках и более сложных системах
- 4. Элементный состав Земли, по убыванию массовых %
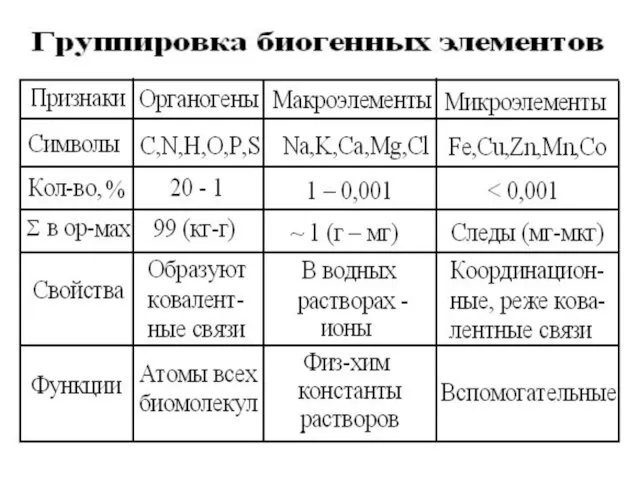
- 5. 16 важнейших биогенных элементов: Входят в состав всех типов клеток надцарств биоты. Легчайшие атомы 1-4 периодов.
- 7. Выводы: 1. Содержание биогенных элементов в организме зависит не от их доступности в окружающей среде, а
- 8. 3 важнейших элемента периодической системы для познания основ биохимии Углерод За счет 4 валентности создает объем
- 9. Азот Тройную связь в молекуле N2 разрушить крайне трудно. Поэтому его молекулы инертны и в состав
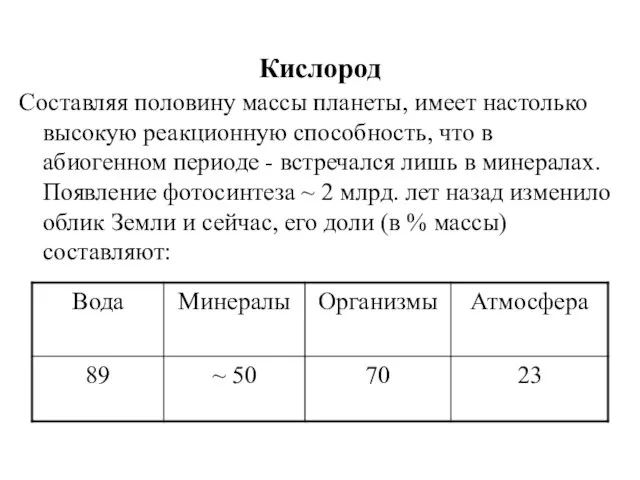
- 10. Кислород Составляя половину массы планеты, имеет настолько высокую реакционную способность, что в абиогенном периоде - встречался
- 11. Описательный этап = статическая биохимия занял ~100 лет
- 12. Причины этой длительности: Множество объектов исследования – все биоразнообразие. Сложность многоклеточных организ-мов, проявляющаяся в иерархии структур,
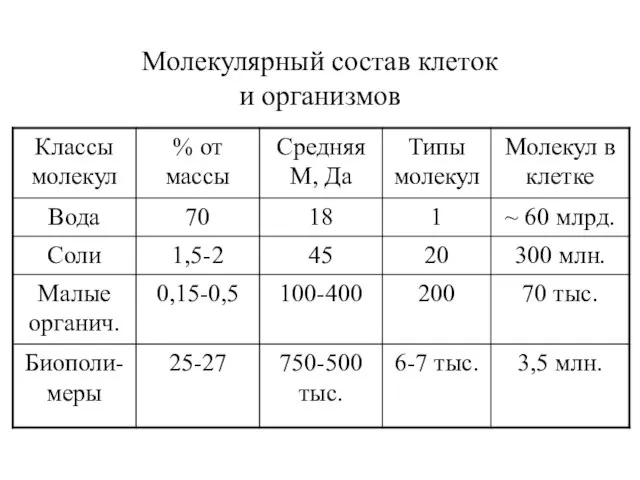
- 13. Молекулярный состав клеток и организмов
- 14. Вода – несжимаемый наполнитель всех клеток (~ 65 %); доступный универсальный растворитель ионов и молекул; среда
- 15. Малые биомолекулы: Существует 5-10 типов моноз, ~ 10 высших карбоновых = жирных к-т = ВЖК, >
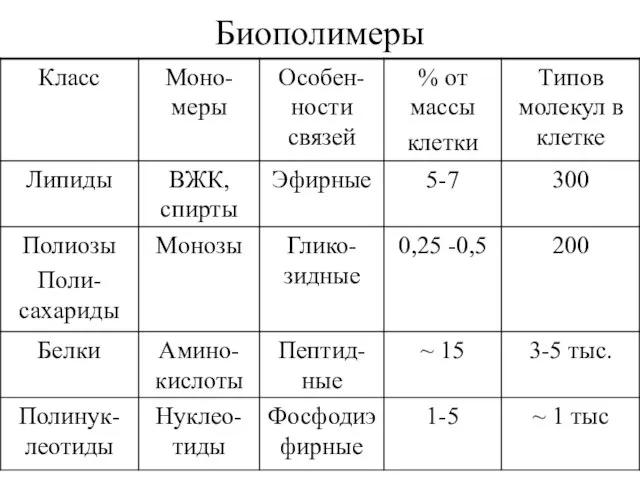
- 16. Биополимеры
- 17. Преимущества биополимеров: В их состав входят до 107 мономеров. Гибкие и объемные, имеют пространственные конформации D
- 18. Крик (Crick) Фрэнсис Харри Комптон (1916-2004) Английский биофизик. За расшифровку трех-мерной молекулярной структуры ДНК в 1962
- 19. Таким образом, начав с расшифровки механизмов хранения, воспроизведения, передачи и реализации наследственной информации, молекулярная биология параллельно
- 20. Аминокислоты - карбоновые кислоты, содержащие карбоксильную и аминную группы, которые находятся у одного и того же
- 21. Классифицировать аминокислоты можно по полярности их радикалов, о чем ниже. По функциональному значению аминокислоты условно можно
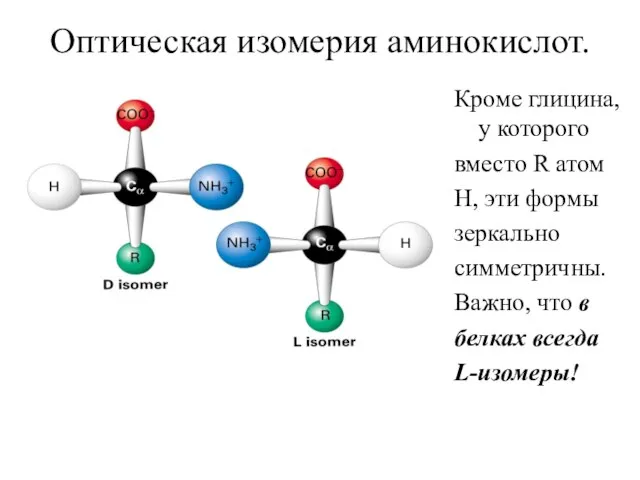
- 22. Оптическая изомерия аминокислот. Кроме глицина, у которого вместо R атом Н, эти формы зеркально симметричны. Важно,
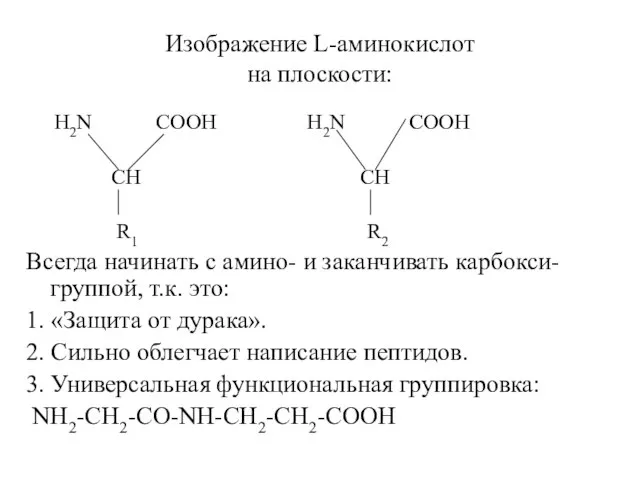
- 23. Изображение L-аминокислот на плоскости: H2N COOH H2N COOH CH CH R1 R2 Всегда начинать с амино-
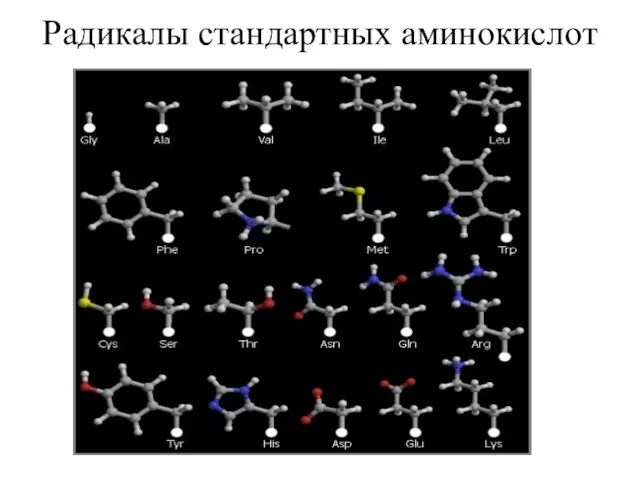
- 24. Радикалы стандартных аминокислот
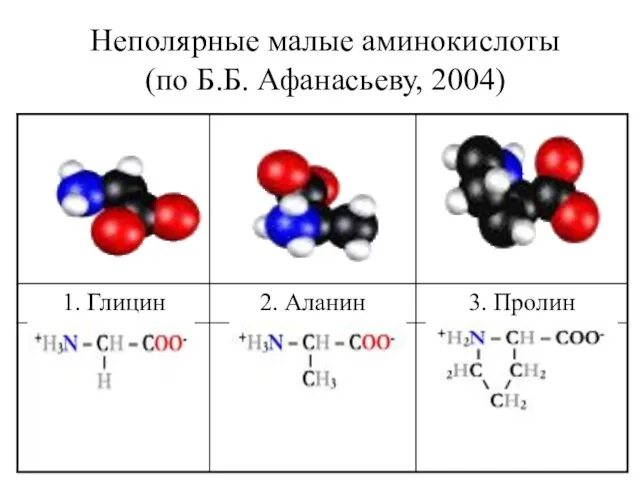
- 25. Неполярные малые аминокислоты (по Б.Б. Афанасьеву, 2004)
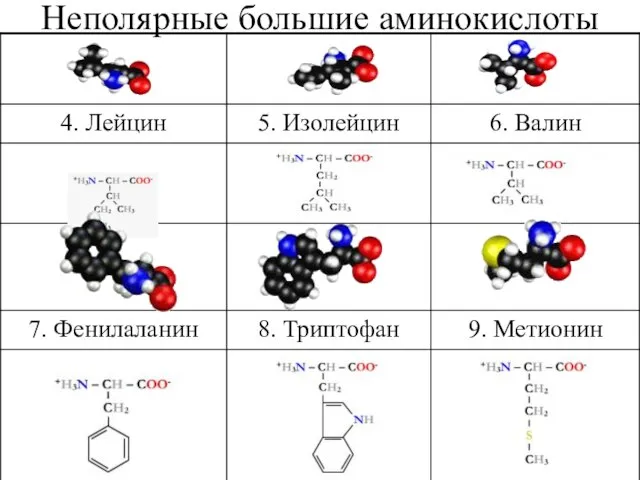
- 26. Неполярные большие аминокислоты
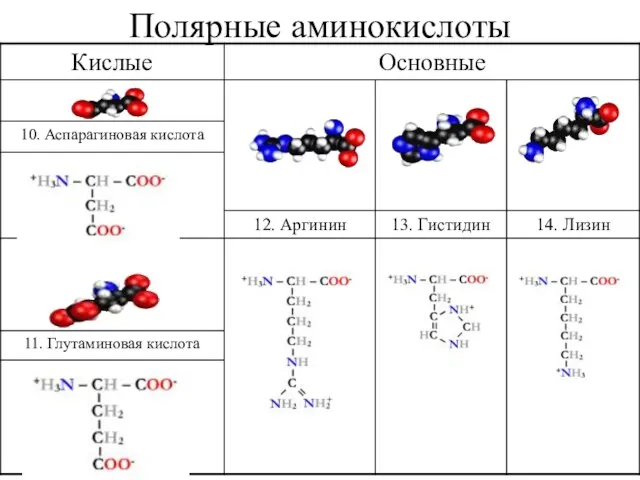
- 27. Полярные аминокислоты
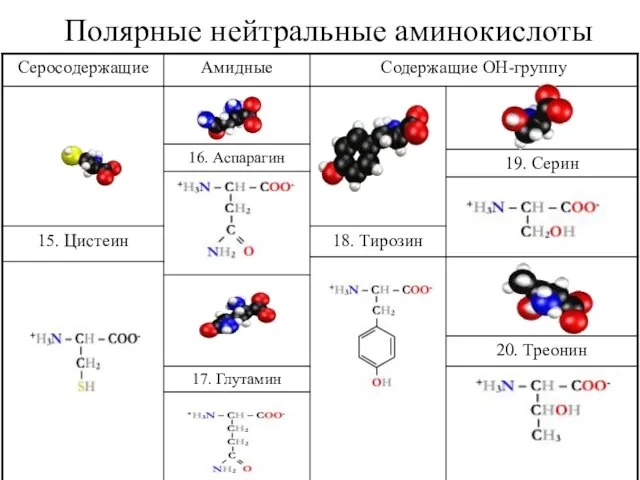
- 28. Полярные нейтральные аминокислоты
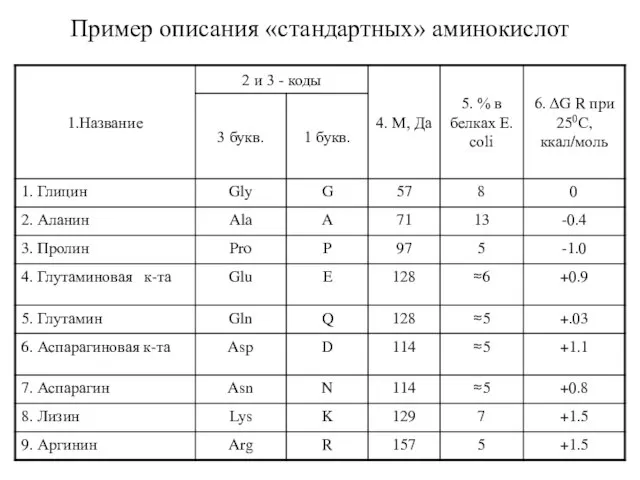
- 29. Пример описания «стандартных» аминокислот
- 30. В нейтральных растворах все аминокислоты ионизованы Термин «заряженные аминокислоты» относится исключительно к боковому радикалу аминокислоты и
- 31. В самом конце ХIХ в. немецкий химик-органик Э.Г. Фишер доказал, что α-аминокислоты могут реагировать между собой,
- 32. ФИШЕР ЭМИЛЬ ГЕРМАН (1852-1919) Основатель химии природных соединений = биоорганической химии. Изучил строение и син-тезировал ряд
- 33. Регулярный остов полипептида: Но это - понятие химии, его можно разместить на плоскости, а говоря о
- 34. По "жизненным условиям" и общему типу строения белки делят на 3 класса: 1. Высоко регулярную структуру
- 35. Белки классифицируют на простые и сложные: К простым белкам относят макромолекулы состоящие только из аминокислотных остатков.
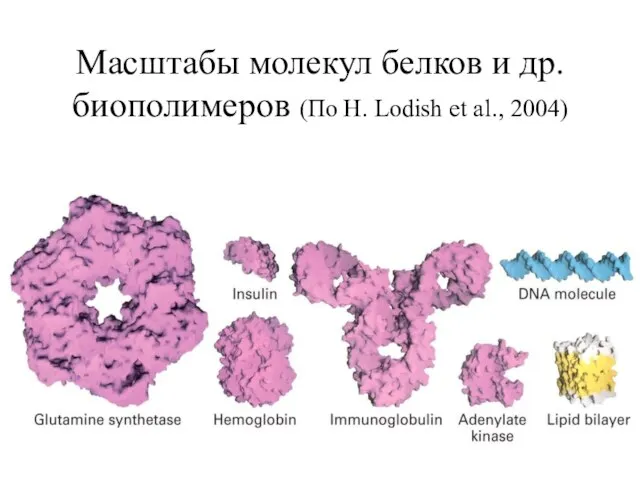
- 36. Масштабы молекул белков и др. биополимеров (По H. Lodish et al., 2004)
- 38. Скачать презентацию






















 Вымирающие животные России
Вымирающие животные России Вопросы ЕГЭ по биологии, вызывающие затруднения
Вопросы ЕГЭ по биологии, вызывающие затруднения Биология полорогих: горных баранов, овцебыка, зубра
Биология полорогих: горных баранов, овцебыка, зубра Витаминные лекарственные средства
Витаминные лекарственные средства Определить вид антибиоза
Определить вид антибиоза КРАСНАЯ КНИГА ТУЛЬСКОЙ ОБЛАСТИ РАСТЕНИЯ
КРАСНАЯ КНИГА ТУЛЬСКОЙ ОБЛАСТИ РАСТЕНИЯ  Рост пшеницы
Рост пшеницы Антибиотические отношения. Хищничество
Антибиотические отношения. Хищничество Презентация на тему "Голенастые или аистообразные" - скачать презентации по Биологии
Презентация на тему "Голенастые или аистообразные" - скачать презентации по Биологии Презентация на тему Яблочный спас познавательная игра по биологии, 6 класс
Презентация на тему Яблочный спас познавательная игра по биологии, 6 класс  Цветочный мир. Кроссворд
Цветочный мир. Кроссворд Основы гистологии. Эпителиальные, мышечные, соединительная и нервная ткани
Основы гистологии. Эпителиальные, мышечные, соединительная и нервная ткани Лишайники. Разнообразие лишайников
Лишайники. Разнообразие лишайников Ботаника. Царство растения
Ботаника. Царство растения Врожденные и приобретенные формы поведения Врожденные формы поведения отражают видовой опыт животных и человека. Приобретенные
Врожденные и приобретенные формы поведения Врожденные формы поведения отражают видовой опыт животных и человека. Приобретенные  Отдел Зеленые водоросли
Отдел Зеленые водоросли Назальный полип, гамартома
Назальный полип, гамартома Одноклеточные организмы Protista
Одноклеточные организмы Protista Витамины
Витамины Презентация на тему Рыжий муравей
Презентация на тему Рыжий муравей Кошачий сосальщик (Opisthorchis felineus), марита
Кошачий сосальщик (Opisthorchis felineus), марита Игра. 5-7 класс
Игра. 5-7 класс Растительный и животный мир России
Растительный и животный мир России Вегетативная нервная система
Вегетативная нервная система Регуляция активности ферментов
Регуляция активности ферментов Чередова Ольга Максимовна Учитель биологии, МКОУ «СОШ №2» п. Сывдарма
Чередова Ольга Максимовна Учитель биологии, МКОУ «СОШ №2» п. Сывдарма Дыхательная система человека
Дыхательная система человека ВИРУСЫ – НЕКЛЕТОЧНАЯ ФОРМА ЖИЗНИ…
ВИРУСЫ – НЕКЛЕТОЧНАЯ ФОРМА ЖИЗНИ…