Содержание
- 2. Функции крови Дыхательная (Hb переносит О2 от легких ко всем клеткам и тканям, этим обеспечивая процессы
- 3. Защитная (в крови существует целая система белков, вызывающих ее свертывание и защищающих тем самым организм от
- 4. Количество крови у разных видов животных по отношению к массе тела составляет от 4,5-5% (кролик, свинья)
- 6. РОЭ (СОЭ) мм/час Лошади – 64 Овцы – 0,8 Коровы – 0,58 Свиньи – 30 Кролики
- 7. Физико-химические показатели крови Плотность: 1,050 – 1,060. Вязкость: в 4,5 – 6 раз больше, чем воды.
- 8. Для обеспечения жизни необходимо динамическое постоянство состава и физико-химических свойств биологических жидкостей организма, особенно крови как
- 9. Почти полностью эта величина обусловлена содержащимися в крови хлоридом натрия и др. низкомолекулярными веществами, очень небольшая
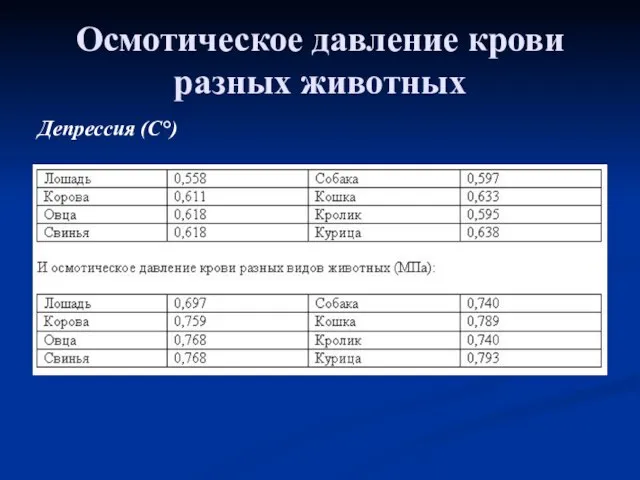
- 10. Осмотическое давление крови разных животных Депрессия (С°)
- 11. При различных заболеваниях, ожогах и кровопотерях широко применяют водные растворы электролитов – физиологические растворы. Чаще всего
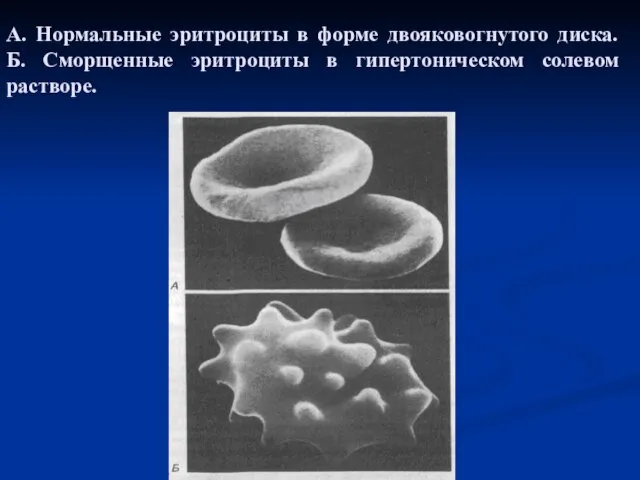
- 12. А. Нормальные эритроциты в форме двояковогнутого диска. Б. Сморщенные эритроциты в гипертоническом солевом растворе.
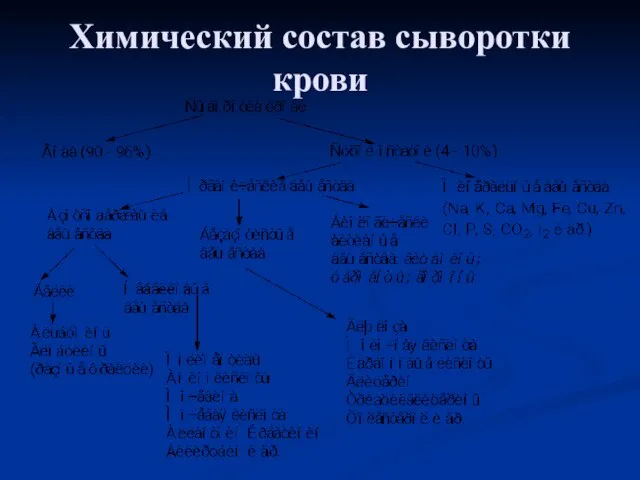
- 13. Химический состав сыворотки крови
- 14. Капиллярная система Наиболее полно обмен веществ между кровью и тканями протекает в капиллярной системе. Это обеспечивается
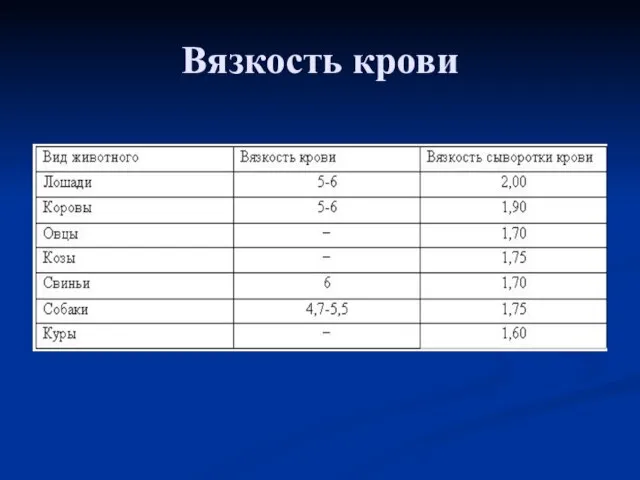
- 15. Вязкость крови
- 16. Зависимость вязкости от количества эритроцитов
- 17. Кислотность крови Все процессы в организме животных могут происходить при строго определенных концентрациях водородных ионов. Даже
- 18. Кислотность крови разных животных
- 19. Ацидоз Понижение щелочного резерва крови называют ацидозом, что наблюдается при кетозах, сердечной недостаточности, патологических изменениях в
- 20. Алкалоз При противоположном ацидозу состоянии – алкалозе – в крови повышается содержание гидрокарбонатов, избыток которых выделяется
- 21. Буферные системы крови Буферные системы обеспечивают динамическое постоянство рН крови
- 22. Гидрокарбонатная буферная система Составляет 7–9 % всей буферной емкости крови. Определение компонентов этой системы широко используется
- 23. Фосфатная буферная система Фосфатная буферная система представляет собой сопряженную кислотно-основную пару, состоящую из иона Н2РО4- (донор
- 24. Белковая буферная система Белковая буферная система образована белками плазмы крови. Имеет меньшее значение для поддержания кислотно-основного
- 25. Буферное действие белков Буферное действие белков плазмы невелико (10% буферной емкости крови ), тогда как гемоглобин
- 26. Гемоглобиновая буферная система Гемоглобиновая буферная система – самая мощная буферная система крови. Она в 9 раз
- 27. Буферные свойства гемоглобина Буферные свойства гемоглобина прежде всего обусловлены возможностью взаимодействия кислореагирующих соединений с калиевой солью
- 28. Гемоглобиновый буфер
- 29. В капиллярах альвеол гемоглобин (Н–Hb) превращается в оксигемоглобин (Н–HbO2). Оксигемоглобин, как относительно сильная органическая кислота реагирует
- 30. Белковый состав плазмы Белки неоднородные по своему составу, физико-химическим и биологическим свойствам. Методом электрофореза на бумаге
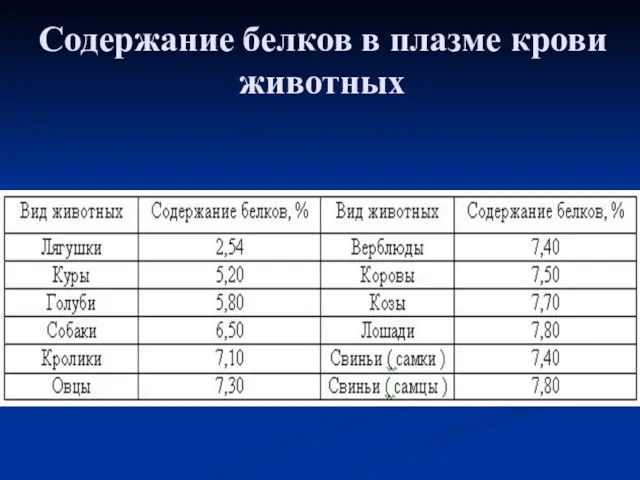
- 31. Содержание белков в плазме крови животных
- 32. Электрофолеграмма сыворотки крови человека. Схема прибора для электрофореза на бумаге.
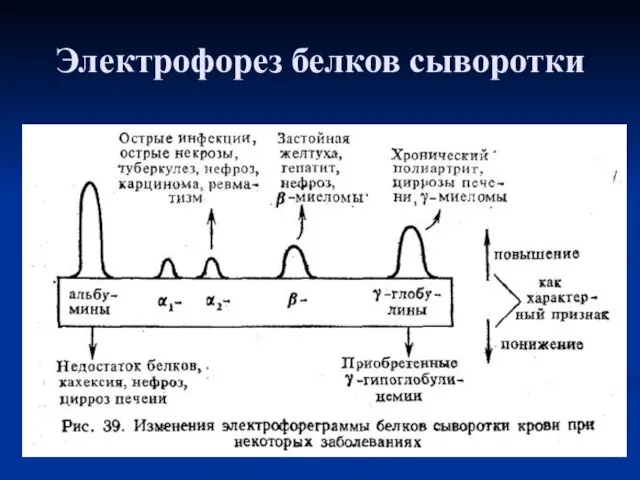
- 33. Электрофорез белков сыворотки
- 34. Роль белков крови Создают онкотическое давление. Участвуют в свертывании крови. Создают определенную вязкость крови, ответственны за
- 35. Специальные белки плазмы. Гаптоглобин. Гаптоглобин входит в состав α2-глобулиновой фракции. Этот белок обладает способностью соединяться с
- 36. Трансферрин Трансферрин относится к β-глобулинам и обладает способностью соединяться с железом. Концентрация трансферрина в сыворотке крови
- 37. Церулоплазмин Церулоплазмин имеет голубоватый цвет, обусловленный наличием в его составе 0,32% меди. Обладает слабой каталитической активностью,
- 38. С-реактивный белок С-реактивный белок получил свое название в результате способности вступать в реакцию преципитации с С-полисахаридом
- 39. Интерферон Интерферон – специфический белок, синтезируемый в клетках организма в результате воздействия вирусов. В свою очередь
- 40. Ферменты плазмы Ферменты, которые обнаруживаются в норме в плазме или сыворотке крови, условно можно разделить на
- 41. Секреторные ферменты синтезируются в печени, в норме выделяются в плазму крови, где играют определенную физиологическую роль
- 42. Индикаторные (клеточные) ферменты Попадают в кровь из тканей, где они выполняют определенные внутриклеточные функции. Большая часть
- 43. Индикаторные (клеточные) ферменты При инфаркте миокарда в крови увеличивается активность креатинкиназы (КК), лактатдегидрогеназы (ЛДГ-1), аспартатаминотрансферазы (АСТ).
- 44. Индикаторные (клеточные) ферменты При патологиях костной системы щелочная фосфатаза (ЩФ). При патологиях поджелудочной железы – амилаза.
- 45. Экскреторные ферменты Синтезируются главным образом в печени (аминопептидаза, щелочная фосфатаза и др.). Эти ферменты в физиологических
- 46. Нарушения содержания белков Гипопротеинемия – снижение концентрации белков в крови (при белковом голодании, приеме больших количеств
- 47. Нарушения содержания белков Диспротеинемия – нарушение соотношения концентраций отдельных фракций белков крови при неизменной общей концентрации
- 48. Содержание азотистых веществ в плазме крови животных, мг %
- 49. Мочевина Мочевина – главный компонент остаточного (небелкового) азота – составляет до 70-80% его количества. При нарушении
- 50. Мочевая кислота Мочевая кислота является главным конечным продуктом белкового обмена у птиц и её содержание в
- 51. Аминокислоты Аминокислоты в количественном отношении стоят на втором месте после мочевины среди составных частей остаточного азота.
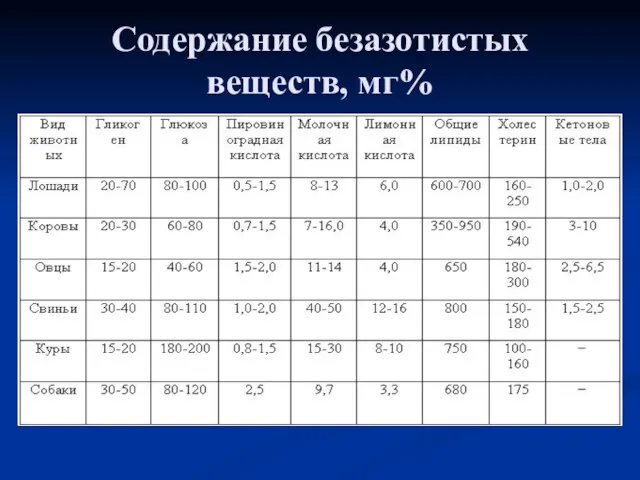
- 52. Содержание безазотистых веществ, мг%
- 53. Содержание глюкозы Содержание углеводов (глюкозы) в крови относительно постоянно для каждого вида животных. Постоянство поддерживается сложным
- 54. Содержание лактата и ПВК Постоянная составная часть крови – молочная кислота. Ее количество может увеличиваться в
- 55. Содержание липидов Липидов в крови содержится от 0,5 до 0,9 %, а в некоторых случаях достигает
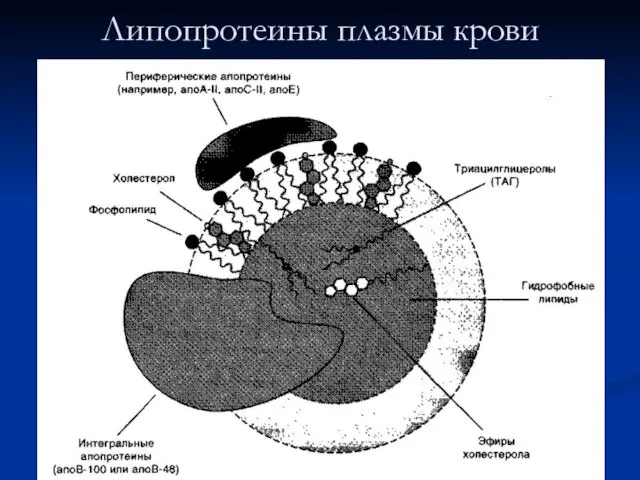
- 56. Липопротеины плазмы крови
- 57. Общая характеристика липопротеинов Липиды в водной среде (а значит, и в крови) нерастворимы, поэтому для транспорта
- 58. Липопротеины В организме синтезируются следующие типы липопротеинов: -хиломикроны (ХМ), -липопротеины очень низкой плотности (ЛПОНП), -липопротеины низкой
- 59. Свойства липопротеинов ЛП хорошо растворимы в крови, не опалесцируют, так как имеют небольшой размер и отрицательный
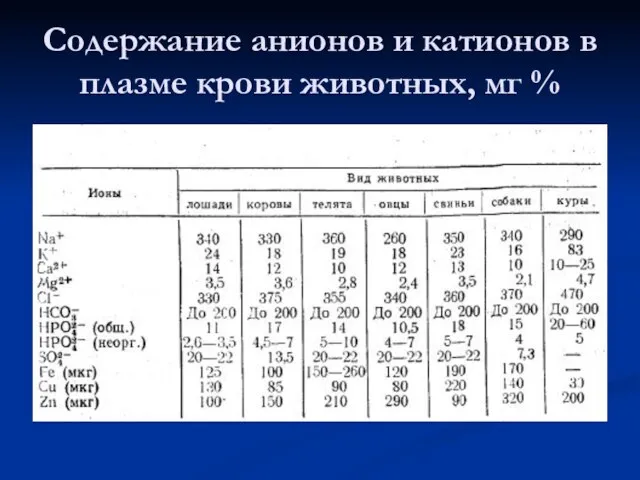
- 60. Содержание анионов и катионов в плазме крови животных, мг %
- 61. Нарушение обмена кальция Гипокальциемия – уменьшение содержания кальция в крови ниже 2 ммоль/л может быть результатом
- 62. Всасывание кальция затрудняется при значительном избытке в пище фосфора (оптимальное соотношение Са/Р составляет 1:1,3–1,5). Такое же
- 63. Гиперкальциемия – повышение уровня кальция в сыворотке крови выше 2,5–3 ммоль/л. Наиболее важным фактором, ведущим к
- 64. Относительная гиперкальциемия может возникать при ацидозе, когда кальций переходит из неактивной белковосвязанной формы в ионизированную –
- 65. Нарушение обмена магния Магний является вторым по концентрации катионом внутриклеточной среды (около 15 ммоль/л), а в
- 66. Нарушение в организме магний-кальциевого равновесия наблюдается при заболевании рахитом. При этом количество магния в крови уменьшается
- 68. Скачать презентацию























































 Функции биологических мембран
Функции биологических мембран Презентация на тему "Биоэтические проблемы медицинской генетики" - скачать презентации по Биологии
Презентация на тему "Биоэтические проблемы медицинской генетики" - скачать презентации по Биологии Животная и растительная клетки
Животная и растительная клетки Выполнила: Набиева Г.Р. учитель биологии, Нижнекамской специальной (коррекционной) общеобразовательной школы №23 VIII вида
Выполнила: Набиева Г.Р. учитель биологии, Нижнекамской специальной (коррекционной) общеобразовательной школы №23 VIII вида Морские обитатели контраст форм
Морские обитатели контраст форм Каракал
Каракал Florystyka komunijna
Florystyka komunijna Витамины и их функции
Витамины и их функции Семена огородных культур
Семена огородных культур Исследование цветочной пыльцы Дымился луг цветочною пыльцой, Цветочною пыльцой умылось солнце, Умылось солнце утренней росой И
Исследование цветочной пыльцы Дымился луг цветочною пыльцой, Цветочною пыльцой умылось солнце, Умылось солнце утренней росой И  Наследственная изменчивость. Мутационная изменчивость. Генные мутации
Наследственная изменчивость. Мутационная изменчивость. Генные мутации Выявление изменчивости у организмов
Выявление изменчивости у организмов Презентация к уроку биологии в 8 классе
Презентация к уроку биологии в 8 классе Отряд Гусеобразные Учитель биологии Косьянова Елена Юрьевна МБОУ «СОШ №3 с УИОП» г. Сорск Хакасия
Отряд Гусеобразные Учитель биологии Косьянова Елена Юрьевна МБОУ «СОШ №3 с УИОП» г. Сорск Хакасия Системы. Кровеносная, лимфатическая, нервная
Системы. Кровеносная, лимфатическая, нервная Электрохимический ряд напряжений металлов
Электрохимический ряд напряжений металлов Кто такие динозавры
Кто такие динозавры Что растёт на подоконнике?
Что растёт на подоконнике? Семейства цветковых растений (7 класс)
Семейства цветковых растений (7 класс) Родительское поведение у животных
Родительское поведение у животных БХиМБ. Катаболизм пищевых и тканевых липидов. Лекция 6
БХиМБ. Катаболизм пищевых и тканевых липидов. Лекция 6 Загадка человека (урок 2)
Загадка человека (урок 2) Внешнее строение листа Учитель биологии Дворядкина В.Н.
Внешнее строение листа Учитель биологии Дворядкина В.Н.  Host-parasite interactions
Host-parasite interactions Многообразие насекомых. Отряды
Многообразие насекомых. Отряды Тема урока: Живые царства. Грибы: строение и многообразие.
Тема урока: Живые царства. Грибы: строение и многообразие. Биотехнологические процессы в медицине и иммунологии. Стволовые клетки и их использование
Биотехнологические процессы в медицине и иммунологии. Стволовые клетки и их использование Животные Австралии animals of Australia
Животные Австралии animals of Australia