Содержание
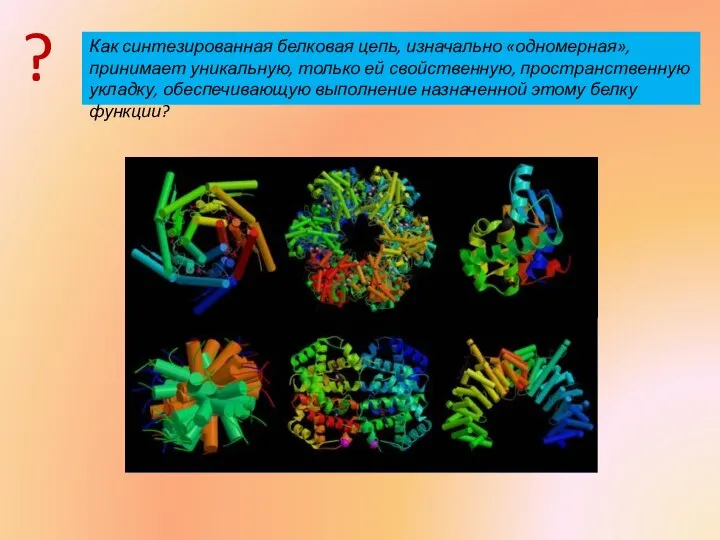
- 2. Как синтезированная белковая цепь, изначально «одномерная», принимает уникальную, только ей свойственную, пространственную укладку, обеспечивающую выполнение назначенной
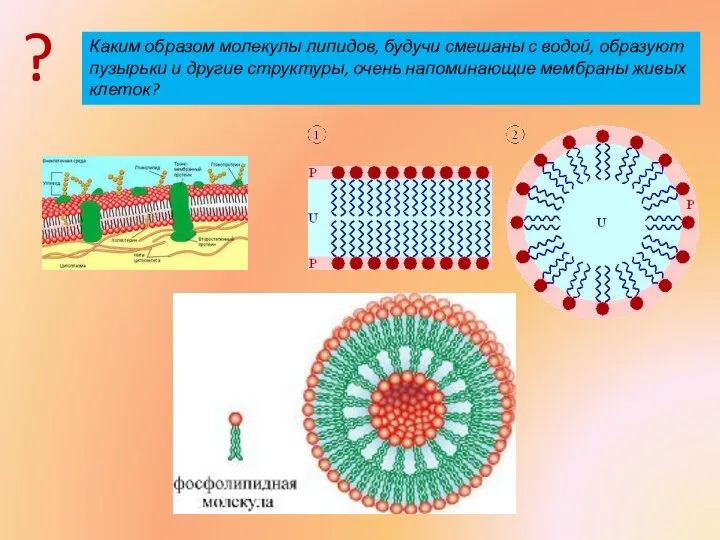
- 3. Каким образом молекулы липидов, будучи смешаны с водой, образуют пузырьки и другие структуры, очень напоминающие мембраны
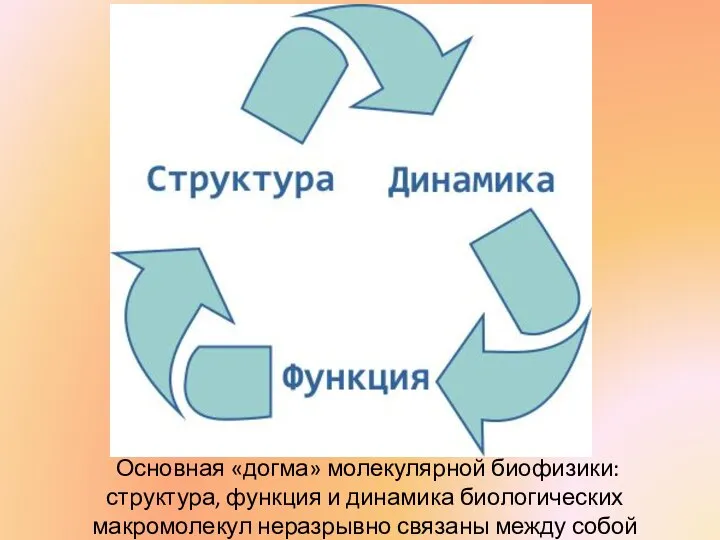
- 4. Основная «догма» молекулярной биофизики: структура, функция и динамика биологических макромолекул неразрывно связаны между собой
- 5. Одним из первых биофизических экспериментов может считаться знаменитый опыт Гальвани — во времена, когда не только
- 6. Одним из первых молекулярных биофизиков может считаться Эрвин Шрёдингер, чья книга «Что такое жизнь с точки
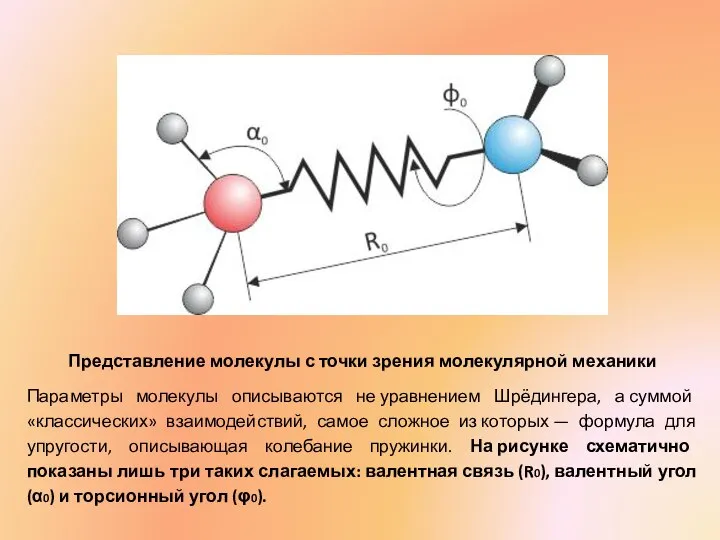
- 7. Представление молекулы с точки зрения молекулярной механики Параметры молекулы описываются не уравнением Шрёдингера, а суммой «классических»
- 17. Масс-спектроскопия (масс-спектроскопия, масс-спектрография, масс-спектральный анализ, масс-спектрометрический анализ) — метод исследования вещества, основанный на определении отношения массы
- 22. СПЕЦИФИКА БИОМАКРОМОЛЕКУЛ СТАТИСТИЧЕСКИЙ ХАРАКТЕР ПОВЕДЕНИЯ, Т.К. БИОМАКРОМОЛЕКУЛЫ СОСТОЯТ ИЗ БОЛЬШОГО ЧИСЛА ОДНОТИПНЫХ ЗВЕНЬЕВ – МОНОМЕРОВ. НАЛИЧИЕ
- 23. Теория Дебая-Хюккеля Теория сильных электролитов (1923 г.) Основные положения: Сильные электролиты в водных растворах практически полностью
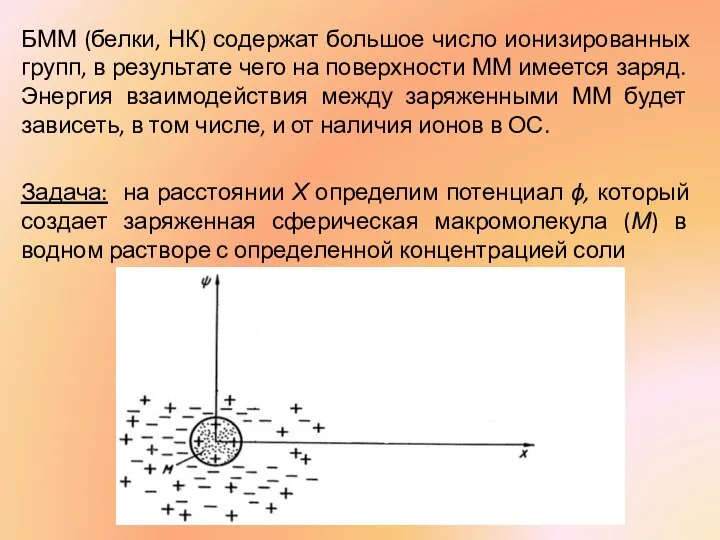
- 24. БММ (белки, НК) содержат большое число ионизированных групп, в результате чего на поверхности ММ имеется заряд.
- 25. Используем для решения уравнение Пуассона, которое связывает плотность заряда (ρ) в точке поля с его потенциалом
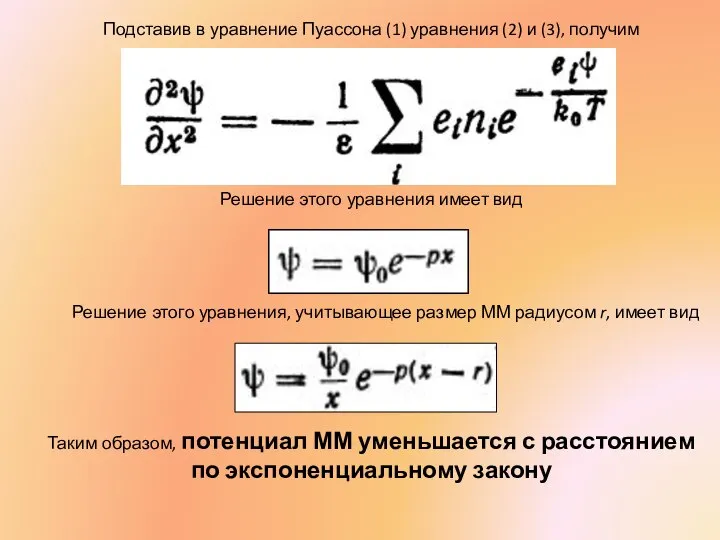
- 26. Подставив в уравнение Пуассона (1) уравнения (2) и (3), получим Решение этого уравнения имеет вид Таким
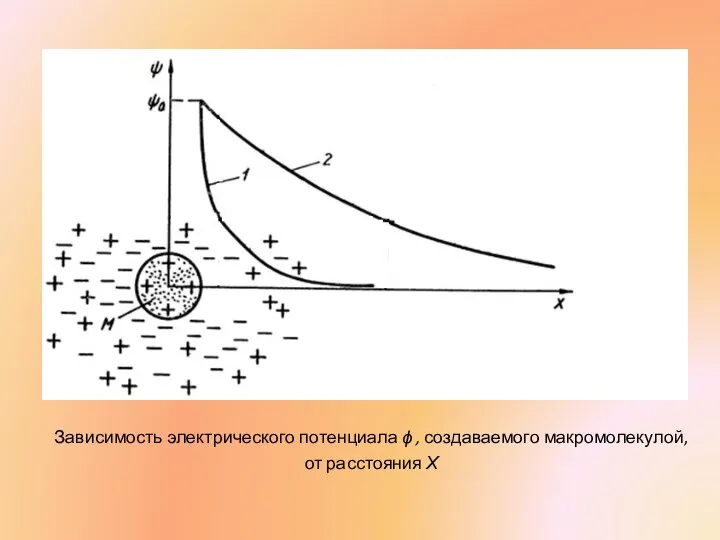
- 27. Зависимость электрического потенциала ϕ , создаваемого макромолекулой, от расстояния Х
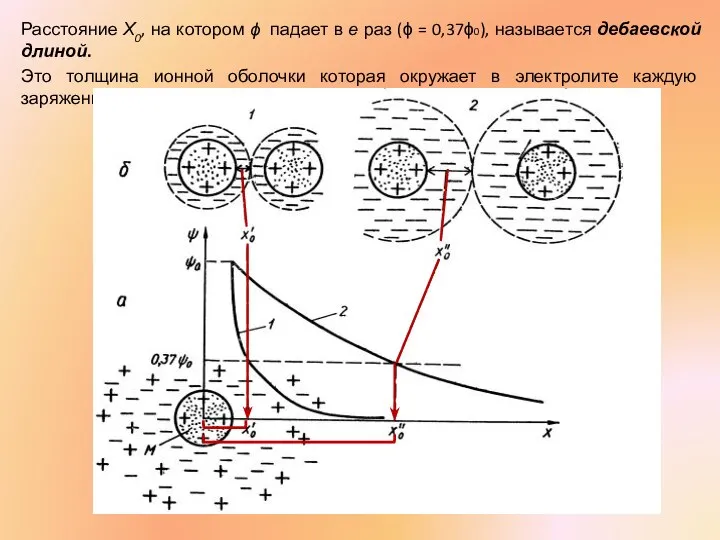
- 28. Расстояние Х0, на котором ϕ падает в е раз (ϕ = 0,37ϕ0), называется дебаевской длиной. Это
- 29. Влияние концентрации ионов на взаимодействие заряженных ММ определяется ионной силой раствора (μ): Тогда толщина ионной оболочки
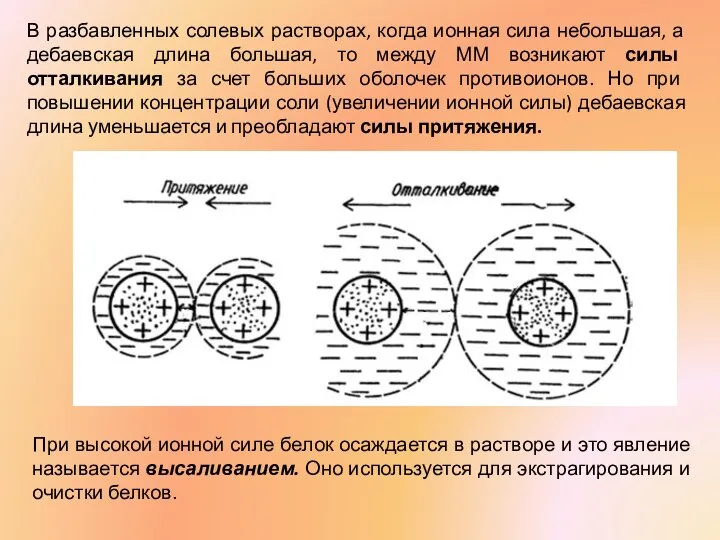
- 31. В разбавленных солевых растворах, когда ионная сила небольшая, а дебаевская длина большая, то между ММ возникают
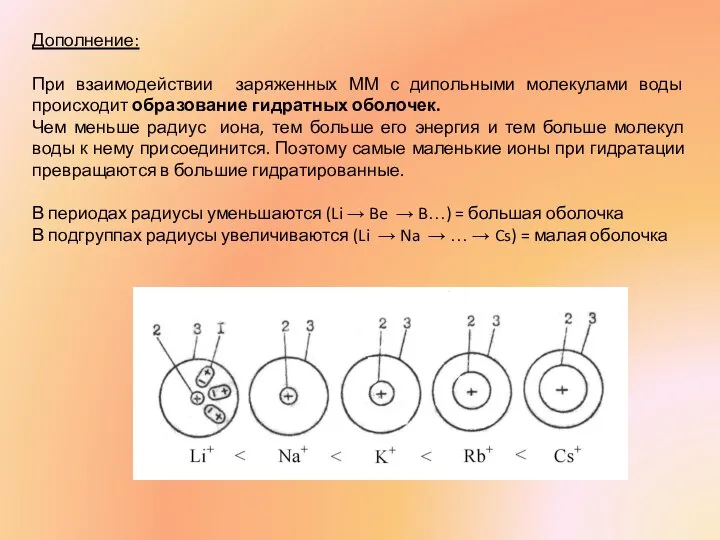
- 32. Дополнение: При взаимодействии заряженных ММ с дипольными молекулами воды происходит образование гидратных оболочек. Чем меньше радиус
- 33. Лекция №2 «Конформация макромолекул. Виды конформационных перестроек» 16 февраля 2017 г. ауд. 205 13.50
- 35. Скачать презентацию


















 Презентация на тему "Гаметогенез. Оплодотворение" - скачать презентации по Биологии
Презентация на тему "Гаметогенез. Оплодотворение" - скачать презентации по Биологии Семейство Крестоцветные
Семейство Крестоцветные Отдел Зеленые водоросли
Отдел Зеленые водоросли Строение работа сердца
Строение работа сердца Животный мир Северной Америки
Животный мир Северной Америки Нервная система
Нервная система Естественный отбор – направляющий фактор эволюции. Вершинина Валерия 10-А класс
Естественный отбор – направляющий фактор эволюции. Вершинина Валерия 10-А класс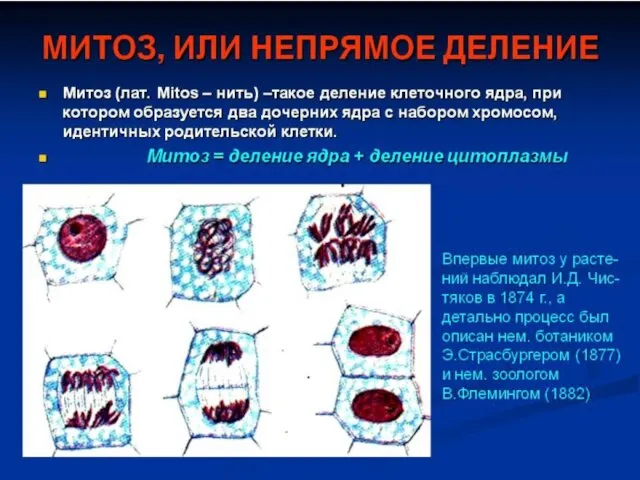 Жизненный цикл клетки. Митоз. Мейоз
Жизненный цикл клетки. Митоз. Мейоз Предмет и задачи микробиологии и иммунологии
Предмет и задачи микробиологии и иммунологии Близнецовый метод в генетике человека
Близнецовый метод в генетике человека Сущность процесса пищеварения. Пищеварение в ротовой полости
Сущность процесса пищеварения. Пищеварение в ротовой полости Ретротранспозоны и ДНК транспозоны
Ретротранспозоны и ДНК транспозоны Caracteristica morfo-funcţională a organismului la pasăre
Caracteristica morfo-funcţională a organismului la pasăre Теория эволюции Откуда берутся новые формы живых систем?
Теория эволюции Откуда берутся новые формы живых систем? Молекулярно-генетические методы исследований генома. Современные методы диагностики и профилактики наследственных болезней
Молекулярно-генетические методы исследований генома. Современные методы диагностики и профилактики наследственных болезней Тестирование биологической активности ксенобиотиков
Тестирование биологической активности ксенобиотиков Бактерії – найменші одноклітинні організми
Бактерії – найменші одноклітинні організми Презентация на тему "Строение пищеварительной системы" - скачать бесплатно презентации по Биологии_
Презентация на тему "Строение пищеварительной системы" - скачать бесплатно презентации по Биологии_ Эфирные масла и их биологическое действие
Эфирные масла и их биологическое действие Биологические особенности роста и плодоношения малины и ежевики
Биологические особенности роста и плодоношения малины и ежевики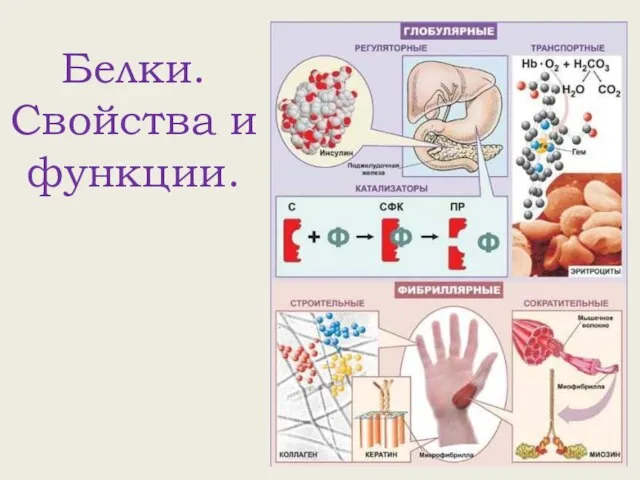 Белки. Свойства и функции.
Белки. Свойства и функции. Методы изучения насследственности человека.
Методы изучения насследственности человека.  Презентация на тему Antibiotic (Антибиотики)
Презентация на тему Antibiotic (Антибиотики)  Функции белков
Функции белков Использование комнатных растений для активизации познавательной деятельности учащихся на уроках биологии
Использование комнатных растений для активизации познавательной деятельности учащихся на уроках биологии Класс Двудольных
Класс Двудольных Глотка, пищевод, желудок
Глотка, пищевод, желудок Класс Ракообразные Учитель химии и биологии государственного учреждения образования «Брагинская средняя школа» г.п. Брагин
Класс Ракообразные Учитель химии и биологии государственного учреждения образования «Брагинская средняя школа» г.п. Брагин