Содержание
- 2. Миелинизированное волокно Для понимания механизмов проведения по нервным волокнам возбуждения необходимо учитывать как электрические, так и
- 3. Рис. 1-83. Схема строения миелинизированного нервного волокна (А), шванновской клетки (Б) и структура перехвата Ранвье (В)
- 4. Шванновская клетка Миелин представляет собой упаковку листков специфических плазматических мембран, продуцируемых глиальными клетками, которые обертываются вокруг
- 5. Рис. 1-84. Рост мембраны шванновской клетки и формирование миелиновой оболочки аксона. А - рост мембраны шванновской
- 6. Распространение по аксону пассивного электротонического потенциала Пассивный электротонический потенциал распространяется по нервному волокну на небольшие расстояния,
- 7. Рис. 1-85. Распространение пассивного электротонического потенциала на примере немиелинизированного волокна. А - аксон в состоянии покоя.
- 8. Распространение потенциала действия Распространение возбуждения в форме потенциала действия принципиально отличается от распространения пассивного электротонического потенциала.
- 9. Рис. 1-86. Распространение потенциала действия на примере немиелинизированного волокна. А - аксон в состоянии покоя. Потенциалуправляемые
- 10. Механизм распространения потенциала действия по немиелинизированному волокну Рис. 1-87. Механизм проведения потенциала действия в немиелинизированном волокне.
- 11. В зонах (2), находящихся в состоянии покоя, локальные круговые токи электротонически сдвигают потенциал покоя в сторону
- 12. Механизм распространения потенциала действия по миелинизированному волокну Рис. 1-88. Механизм проведения потенциала действия в миелинизированном волокне.
- 13. Раздражение перехвата Ранвье (0) нервного волокна приводит к открытию потенциалуправляемых Na+-ионных каналов, что ведет к возникновению
- 14. Проведение возбуждения по двум типам волокон Распространение возбуждения в немиелинизированном и миелинизированном нервном волокне суммарно и
- 15. Рис. 1-89. Сравнение общих принципов проведения возбуждения по немиелинизированному и миелинизированному нервному волокну
- 16. Внеклеточные потенциалы В качестве предварительного усилителя обычно применяют усилитель постоянного тока с дифференциальным входом (рис. 1-90
- 17. Рис. 1-90. Потенциалы нервного волокна и их регистрация. А - дифференциальный усилитель для внеклеточной регистрации потенциалов
- 18. Законы проведения возбуждения Существует несколько необходимых условий проведения возбуждения по нерву, названных «законами» проведения возбуждения по
- 20. Скачать презентацию
Миелинизированное волокно
Для понимания механизмов проведения по нервным волокнам возбуждения необходимо учитывать
Миелинизированное волокно
Для понимания механизмов проведения по нервным волокнам возбуждения необходимо учитывать
Миелинизация нервного волокна играет огромную роль в нервной системе, а нарушение миелиновой оболочки приводит к фатальным патологическим процессам, механизм которых до настоящего времени подвергается интенсивному изучению, поэтому мы рассмотрим подробно миелиновую оболочку и ее формирование.
На рисунке 1.83 А представлен фрагмент миелинизированного аксона и выделен перехват Ранвье. Миелиновая оболочка создается в результате того, что шванновская клетка (или иначе миелоцит) многократно обертывает аксон. При этом образуются слипающиеся слои и тем самым формируется миелиновая оболочка. Далее представлены структуры шванновской клетки (рис. 1-83 Б).
Миелин в периферической нервной системе конструируется другими уникальными протеинами мембраны. Миелин, окружающий каждый миелинизированный аксон, формируется из многих глиальных клеток. Каждый регион миелина формируется одиночной глиальной клеткой и отделен от следующего региона немиелинизированным участком, названным перехватом Ранвье. Только в этом участке аксональная мембрана напрямую контактирует с экстрацеллюлярной жидкостью (рис. 1-83 В).
Миелиновая оболочка может быть достаточно толстой и состоять из 50-100 мембран, играющих роль электрического изолятора аксона, т.е. предотвращающего перенос ионов между цитозолем аксона и экстрацеллюлярной жидкостью. Как следствие электрическая активность в аксоне ограничена только зоной мембраны перехвата Ранвье, именно того места, где ионы могут проходить через мембрану. Этот участок мембраны имеет большую плотность потенциалуправляемых Na+-каналов, около 10 000 на 1 μм2 аксональной плазматической мембраны, тогда как участки аксональной мембраны между перехватами Ранвье имеют очень незначительное количество ионных каналов.
Суммарный диаметр аксона, покрытого миелиновой оболочкой, обычно составляет около 20 μм. Длина перехвата Ранвье достигает 2 μм, а миелинизированный промежуток между двумя перехватами Ранвье составляет около 2000 μм.
Рис. 1-83. Схема строения миелинизированного нервного волокна (А), шванновской клетки (Б)
Рис. 1-83. Схема строения миелинизированного нервного волокна (А), шванновской клетки (Б)
Шванновская клетка
Миелин представляет собой упаковку листков специфических плазматических мембран, продуцируемых глиальными
Шванновская клетка
Миелин представляет собой упаковку листков специфических плазматических мембран, продуцируемых глиальными
На рисунке 1-84 А показано, как в процессе развития нервной системы большая шванновская клетка обертывает аксон нейрона. Дальнейший рост мембраны шванновской клетки вместе с ее вращением вокруг аксона образует слоистую спираль с двойной плазматической мембраной вокруг аксона. Таким образом, миелин представляет собой слой относительно богатых фосфолипидами плазматических мембран шванновской клетки. Далее (рис. 1-84 Б) показаны схема аксона, окруженного шванновской клеткой, и профиль слоев мембраны, образующий миелин.
Часто несколько аксонов окружены глиальной клеткой (рис. 1-84 В). Как у позвоночных, так и у некоторых беспозвоночных животных глиальные клетки сопровождают аксоны по всей длине. Но специализация этих глиальных клеток в форме миелина преобладающе встречается у позвоночных. Глиальные клетки позвоночных, позднее формирующие миелин, имеют на своей поверхности миелинассоциированный гликопротеин и другие протеины, связывающиеся с соседними аксонами и вызывающими формирование миелина. Миелиновая мембрана, подобно всем мембранам, содержит бислой фосфолипидов, но миелин содержит только несколько типов протеинов. Основной протеин миелина и протеолипид обнаружили только в миелине в центральной нервной системе, и их наличие позволяет плазматическим мембранам плотно упаковываться вместе.
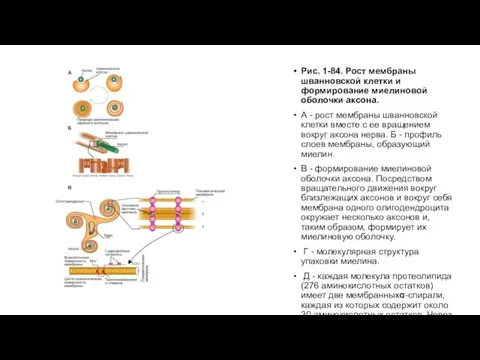
Рис. 1-84. Рост мембраны шванновской клетки и формирование миелиновой оболочки аксона.
А
Рис. 1-84. Рост мембраны шванновской клетки и формирование миелиновой оболочки аксона.
А
В - формирование миелиновой оболочки аксона. Посредством вращательного движения вокруг близлежащих аксонов и вокруг себя мембрана одного олигодендроцита окружает несколько аксонов и, таким образом, формирует их миелиновую оболочку.
Г - молекулярная структура упаковки миелина.
Д - каждая молекула протеолипида (276 аминокислотных остатков) имеет две мембранныхα-спирали, каждая из которых содержит около 30 аминокислотных остатков. Через них осуществляется протеолипид-протеолипид взаимодействия
Распространение по аксону пассивного электротонического потенциала
Пассивный электротонический потенциал распространяется по нервному
Распространение по аксону пассивного электротонического потенциала
Пассивный электротонический потенциал распространяется по нервному
Сопротивление аксоплазмы (rin) и наружной среды (rout) очень мало, и ими можно в определенном смысле пренебречь. Обычно рассматривают лишь один элемент мембраны, включающий ее емкость (Сm) и сопротивление (Rm), но надо помнить, что мембрана аксона состоит из огромного количества подобных элементов, связанных между собой и образующих непрерывный кабель (см. рис. 1-85 Б). Можно заметить, что реально каждый такой элемент имеет, помимо емкости мембраны (Сm), сопротивление потенциалуправляемого Na+-канала (RNa), натриевую батарею (VNa), сопротивление потенциалуправляемого К+-канала (RК), калиевую батарею (VK),сопротивление канала утечки - К2Р-канала (Rl), батарею канала утечки (Vl). Однако в покоящемся аксоне большинством этих элементов можно пренебречь, оставив лишь емкость мембраны (Сm) и сопротивление мембраны (Rm), которые будут определяться прежде всего сопротивлением открытых каналов утечки (Rl), как наиболее меньшим. Сопротивление канала утечки (Rl) можно оставить для демонстрации движения ионов по круговым локальным токам через эти каналы в невозбужденных участках мембраны аксона.
Аксоплазма и наружная среда клетки, будучи электролитами, оказываются хорошими проводниками. В покоящемся аксоне они становятся эквипотенциальными, т.е. разность потенциалов на мембране будет одинакова во всех фрагментах (точках) волокна (например, -65 мВ). Если в зону (точку 0) аксона ввести микроэлектрод и изменить разность потенциалов на мембране в этой зоне (рис. 1-85 В), тогда соседние зоны (1) и более удаленные зоны (2, 3, 4 и так далее) окажутся неэквипотенциальными, и между ними потечет ток. Этот ток станет уменьшать возникшую разность потенциалов и одновременно менять потенциал в соседних и близлежащих областях. Влияние тока будет уменьшаться по мере удаления от зоны (0).
Поскольку внутриклеточная среда служит проводником, входящий в зону 0 небольшой ток (смещающий потенциал покоя от -65 до -55 мВ, т.е. в подпороговой области) распространяется в обе стороны от этого участка. Так как мембрана нервного волокна не идеальный изолятор, распространяющиеся токи начнут покидать волокно через единственно открытые каналы утечки, т.е. возникнут выходящие токи. Если этот локальный, входящий в данном случае через микроэлектрод, ток подпороговый, он вызывает возникновение пассивного электротонического потенциала и распространяется с затуханием. Линии на рис. 1-85 В показывают части локальных кругов тока, текущего между слегка деполяризованной и недеполяризованной областями внутри и снаружи аксона и через зоны мембраны, находящиеся в покое (зоны 1), а также на большем удалении (зоны 2, 3, 4 и т.д.). Как будут замыкаться эти линии? Поскольку внешняя среда соединена так или иначе с минусом входа усилителя, то локальные круги тока замкнутся через электронно-измерительную схему на микроэлектроде.
Изменения мембранного потенциала (рис. 1-85 Г) измеряются регистрирующими электродами у основания аксона (V1) и в различных точках вдоль него (V2, V3, V4, V5, V6), а график этих изменений представлен на рис. 1-85 Д.
Рис. 1-85. Распространение пассивного электротонического потенциала на примере немиелинизированного волокна.
А -
Рис. 1-85. Распространение пассивного электротонического потенциала на примере немиелинизированного волокна.
А -
Распространение потенциала действия
Распространение возбуждения в форме потенциала действия принципиально отличается от
Распространение потенциала действия
Распространение возбуждения в форме потенциала действия принципиально отличается от
На рисунке 1-86 А представлена схема немиелинизированного волокна, для удобства обсуждения механизма распространения потенциала действия разбитая на фрагменты, каждый из которых включает один потенциалуправляемый Na+-канал (показан розовым цветом), находящийся в состоянии покоя, один потенциалуправляемый К+-канал (показан желтым цветом), находящийся в состоянии инактивации, и один канал утечки (показан коричневым цветом), через который осуществляется выход ионов К+ во внешнюю среду.
Для понимания механизмов распространения потенциала действия необходимо учитывать как пассивные (емкость и сопротивление), так и активные (активация потенциалупраляемых каналов) свойства мембраны нервного волокна. Рассмотрим эквивалентную электрическую схему (рис. 1-86 Б), представляющую собой электрическую модель нервного волокна, удобную для рассматривания проведения потенциала действия. Сопротивлением аксоплазмы и наружной среды можно в определенном смысле пренебречь. На этой схеме представлен лишь один элемент мембраны.
Каждый элемент имеет емкость мембраны Сm (рис. 1-86 Б), сопротивление потенциалуправляемого Na+-канала (RNa), натриевую батарею VNa, сопротивление потенциалуправляемого К+-канала (RK, калиевую батарею сопротивление канала утечки, К2Р-канала (Rl), батарею канала утечки Vl. Сопротивление канала утечки и его батарея приведены для демонстрации движения ионов по круговым локальным токам через эти каналы в невозбужденных участках мембраны аксона, соседствующих с возбужденным.
Пространственное распределение потенциала по мембране определяется токами, протекающими через нее. Однако при распространении потенциала действия по аксону ток зависит от координаты (эта пространственная неоднородность зависит, например, от наличия открытых потенциалуправляемых каналов). Именно поэтому локальное изменение потенциала (его первая производная) определяется локальными токами (т.е. ток как функция координаты). В свою очередь, локальный ток через мембрану определяется локальным потенциалом, и изменение тока (его первая производная) зависит как от пространственного изменения потенциала (резистивный компонент), так и от временного изменения потенциала (емкостной компонент).
На рисунке 1-86 В показан аксон с введенным в него стимулирующим электродом и группой регистрирующих микроэлектродов. Потенциалы действия в каждой регистрируемой точке показаны на рис. 1-86 Г и измеряются регистрирующими электродами у основания аксона (V1), а также в различных точках вдоль него (V2, V3, V4, V5, V6); график этих изменений представлен на рис. 1-86 Д. Уже из этих последних рисунков видно, что при распространении потенциала действия по аксону ни его амплитуда, ни его форма не меняются. Механизм явления представлен на следующем рисунке.
Рис. 1-86. Распространение потенциала действия на примере немиелинизированного волокна.
А - аксон
Рис. 1-86. Распространение потенциала действия на примере немиелинизированного волокна.
А - аксон
Механизм распространения потенциала действия по немиелинизированному волокну
Рис. 1-87. Механизм проведения потенциала
Механизм распространения потенциала действия по немиелинизированному волокну
Рис. 1-87. Механизм проведения потенциала
А - схема немиелинизированного нервного волокна в покое. Для описания механизма проведения возбуждения по немиелинизированному нервному волокну аксон разбит на условные фрагменты 0, 1, 2, 3...n, каждый из которых содержит потенциалуправляемые Na+- и К+-каналы и каналы утечки. Зеленый цвет всех фрагментов аксона соответствует состоянию покоя (рис. 1-86 А).
А - раздражение фрагмента (0) нервного волокна приводит к открытию потенциалуправляемых Na+-ионных каналов, что ведет к возникновению входящего Na+-тока (фрагмент волокна окрашен красным цветом) и генерации фазы деполяризации потенциала действия на этом участке аксона. Поскольку внутриклеточная среда служит проводником, входящий в зону (0) ток распространяется в обе стороны от возбужденного участка. Так как мембрана нервного волокна не идеальный изолятор, распространяющиеся токи будут покидать волокно через единственно открытые каналы утечки, т.е. возникнут выходящие токи, протекающие через соседние участки мембраны (зоны 1, а также зоны 2, 3 и т.д.).
Таким образом, локальный входящий ток всегда вызывает выходящие токи в прилегающих невозбужденных участках, т.е. возникают локальные круговые токи между возбужденным и прилегающими невозбужденными участками. Линии показывают локальные круги тока, текущего между деполяризованной и недеполяризованной областями внутри и снаружи аксона и через зоны мембраны, находящиеся в покое (зоны 1), а также на большем удалении.
Б - токи, протекающие через зоны (1), электротонически изменяют их потенциал, приводя к разряду мембранной емкости и, следовательно, к деполяризации. Важно отметить, что эта фаза распространения потенциала действия опосредована пассивными свойствами мембраны нервного волокна (аналогично распространению пассивного электротонического потенциала). Однако в отличие от пассивного электротонического потенциала, деполяризация, возникающая в зонах (1), при распространении потенциала действия достигает порога открывания потенциалуправляемых Na+-каналов. Это приводит к лавинообразному открытию всех Na+-каналов в зонах (1), что сопровождается возникновением фазы деполяризации потенциала действия в этих зонах волокна.
Входящий Na+-ток вызывает локальные круговые токи между возбужденными зонами (1) и прилегающими участками - невозбужденными зонами (2), а также зоной 0. Несмотря на то что в результате этого процесса зона (0) также частично деполяризуется, потенциалуправляемые Na+-каналы в ней находятся в состоянии инактивации, а вся зона - в состоянии рефрактерности (голубой цвет на рисунке). Именно поэтому здесь потенциал действия вновь не возникнет.
В зонах (2), находящихся в состоянии покоя, локальные круговые токи электротонически
В зонах (2), находящихся в состоянии покоя, локальные круговые токи электротонически
Механизм распространения потенциала действия по миелинизированному волокну
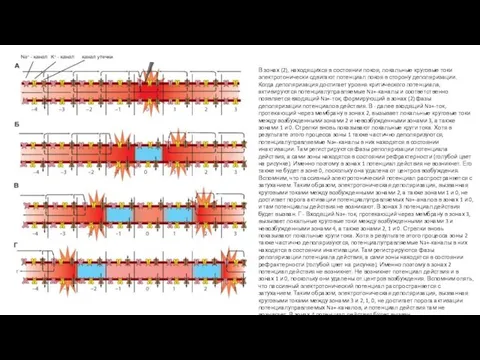
Рис. 1-88. Механизм проведения потенциала
Механизм распространения потенциала действия по миелинизированному волокну
Рис. 1-88. Механизм проведения потенциала
А - для описания механизма проведения возбуждения по миелинизированному нервному волокну аксон разбит на условные фрагменты 1, 2, 3...n, каждый из которых содержит 1 перехват Ранвье с потенциалуправляемыми Na+- и К+-каналами и каналами утечки. Внешняя поверхность мембраны перехватов Ранвье заряжена положительно, а внутренняя поверхность их мембраны заряжена отрицательно.
Остальные области мембраны покрыты миелином. Зеленый цвет всех фрагментов аксона соответствует состоянию покоя. Электрическая активность в миелинизированном аксоне возможна только в области перехватов Ранвье, где ионы могут проходить через мембрану. Эти регионы мембраны имеют большую плотность потенциалуправляемых Na+-каналов. Участки нервного волокна, которые покрыты миелином, имеют значительно более высокое сопротивление, чем обычная плазматическая мембрана.
Таким образом, локальные круговые токи, которые необходимы для генерации потенциала действия, на миелинизированных участках не возникают. Потенциалы действия возникают только в перехватах Ранвье. Миелинизированное волокно представляет собой значительно более качественный кабель по сравнению с немиелинизированным аксоном. Как следствие, электрические сигналы будут распространяться электротонически на большие расстояния.
Б - схема состояния миелинизированного нервного волокна при действии на перехват Ранвье (0) порогового раздражителя. Вспомним, что у миелинизированных нервных волокон, вследствие высокой концентрации свободных ионов внутри и снаружи нервного волокна, внутри- и внеклеточная среды являются хорошими проводниками. Кроме того, ток может протекать через мембрану только в районах перехватов Ранвье.
Раздражение перехвата Ранвье (0) нервного волокна приводит к открытию потенциалуправляемых Na+-ионных
Раздражение перехвата Ранвье (0) нервного волокна приводит к открытию потенциалуправляемых Na+-ионных
Проведение возбуждения по двум типам волокон
Распространение возбуждения в немиелинизированном и миелинизированном
Проведение возбуждения по двум типам волокон
Распространение возбуждения в немиелинизированном и миелинизированном
Сальтаторное проведение ценно по двум причинам. Во-первых, вызывая деполяризацию только перехватов Ранвье, возбуждение «прыгает» вдоль длинных участков оси нервного волокна, и этот механизм увеличивает скорость проведения возбуждения примерно в 5-50 раз. Во-вторых, сальтаторное проведение консервирует энергию у аксона, потому что деполяризуются только перехваты, позволяя при генерации потенциалов действия терять в 100 раз меньше ионов и, таким образом, требуя минимального метаболизма для восстановления натриевой и калиевой разностей концентраций относительно мембраны после серии нервных импульсов.
Другая любопытная черта сальтаторного проведения в больших миелиновых волокнах заключается в следующем. В конце потенциала действия, когда потенциалуправляемые Na+-каналы инактивируются, реполяризация развивается так быстро, что многие из К+-каналов даже не успевают открыться. Таким образом, проведение нервного импульса в миелинизированных волокнах опосредовано в основном ионной проводимостью через потенциалуправляемые Na+-каналы и каналы утечки. Вклад потенциалуправляемых К+-каналов незначителен. Этим объясняется тот факт, что потенциалы действия миелинизированных нервных волокон часто не имеют фазы следовой гиперполяризации.
Рис. 1-89. Сравнение общих принципов проведения возбуждения по немиелинизированному и миелинизированному
Рис. 1-89. Сравнение общих принципов проведения возбуждения по немиелинизированному и миелинизированному
Внеклеточные потенциалы
В качестве предварительного усилителя обычно применяют усилитель постоянного тока с
Внеклеточные потенциалы
В качестве предварительного усилителя обычно применяют усилитель постоянного тока с
Далее (рис. 1-90 Б) показаны записи внеклеточного потенциала нервного волокна на примере ответов седалищного нерва лягушки. Потенциал действия нерва во многом отличается от потенциала действия отдельных волокон. Он не подчиняется закону «все или ничего», поскольку при увеличении силы раздражающего импульса увеличивается число возбужденных аксонов и, следовательно, растет суммарная амплитуда самого потенциала действия. Сложный потенциал действия нерва отличается также своими порогом, формой и рядом других характеристик.
По скорости проведения возбуждения, длительности различных фаз потенциала действия и строению нервные волокна принято выделять три основных типа, обозначаемых буквами А, В и С (рис. 1-90 В).
Волокна типа А делятся на четыре подгруппы. Это α, β, γ и δ. Все они покрыты миелиновой оболочкой. Наиболее толстые из них, так называемые альфа-волокна (аА), у теплокровных животных и человека имеют диаметр 12-22 μм и характеризуются значительной скоростью проведения возбуждения: 70-120 м/с. Такие волокна проводят возбуждение от моторных нервных центров спинного мозга к скелетным мышцам и от рецепторов мышц к соответствующим нервным центрам. Пик потенциала действия аА волокон у теплокровных длится 0,4-0,5 мс. После его окончания развивается следовая деполяризация, которая продолжается 15-20 мс и переходит в следовую гиперполяризацию длительностью около 40-60 мс.
Три другие группы волокон типа А (β, γ и δ) имеют меньший диаметр, меньшую скорость проведения и более длительный потенциал действия. Это преимущественно чувствительные волокна, проводящие возбуждение от различных рецепторов в центральную нервную систему. Исключение составляют γА-волокна, значительная часть которых проводит возбуждение от клеток спинного мозга к так называемым интрафузальным мышечным волокнам, входящим в состав рецепторов мышц - мышечных веретен (см. раздел «Мышцы»).
К волокнам типа В относят миелинизированные, преимущественно преганглионарные, волокна автономной нервной системы. Скорость проведения возбуждения в этих волокнах у теплокровных животных составляет 3-18 м/с. Продолжительность потенциала действия волокон типа В примерно в 3 раза превышает длительность потенциала действия волокон типа А (она составляет 1-2 мс). Отличительная особенность этих волокон состоит в том, что в них не обнаруживается фаза следовой деполяризации, - нисходящее колено пика непосредственно переходит в следовую гиперполяризацию, которая в ряде случаев продолжается свыше 100 мс.
К волокнам типа С относят немиелинизированные нервные волокна очень малого диаметра (порядка 1 μм). Скорость проведения возбуждения в этих волокнах не более 3 м/с. Большинство С-волокон относится к постганглионарным волокнам симпатической нервной системы. К С-волокнам относят также нервные волокна, участвующие в проведении возбуждения от болевых рецепторов и некоторых рецепторов холода, тепла и давления. Потенциалы действия С-волокон характеризуются наибольшей продолжительностью (2 мс у теплокровных животных). Они имеют длительную фазу следовой деполяризации (50-80 мс), сопровождающуюся еще более продолжительной (300-1000 мс) следовой гиперполяризацией.
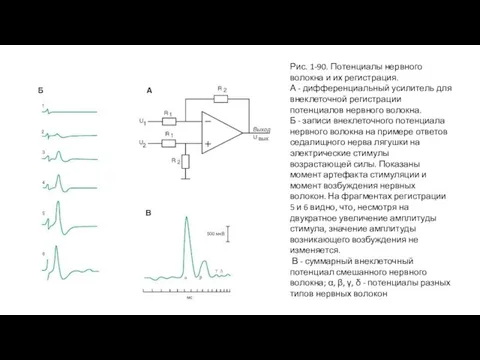
Рис. 1-90. Потенциалы нервного волокна и их регистрация.
А - дифференциальный усилитель
Рис. 1-90. Потенциалы нервного волокна и их регистрация.
А - дифференциальный усилитель
Б - записи внеклеточного потенциала нервного волокна на примере ответов седалищного нерва лягушки на электрические стимулы возрастающей силы. Показаны момент артефакта стимуляции и момент возбуждения нервных волокон. На фрагментах регистрации 5 и 6 видно, что, несмотря на двукратное увеличение амплитуды стимула, значение амплитуды возникающего возбуждения не изменяется.
В - суммарный внеклеточный потенциал смешанного нервного волокна; α, β, γ, δ - потенциалы разных типов нервных волокон
Законы проведения возбуждения
Существует несколько необходимых условий проведения возбуждения по нерву, названных
Законы проведения возбуждения
Существует несколько необходимых условий проведения возбуждения по нерву, названных
Первый закон заключается в том, что при раздражении нервного волокна возбуждение по нерву распространяется в обе стороны. Для доказательства этого на разные концы нервного волокна накладывают две пары электродов, связанных с двумя дифференциальными усилителями, как это показано на рис. 1-91 А. Раздражение наносят в центре, между этими электродами. В результате двустороннего проведения возбуждения регистрирующая аппаратура, связанная с усилителями, зарегистрирует прохождение импульса как под электродами усилителя (1), так и под электродами усилителя (2).
Второй закон заключается в том, что распространение возбуждения в обе стороны происходит с одинаковой скоростью. Если расстояние между электродами усилителя (1) и раздражающими электродами равно расстоянию между электродами усилителя (2) и раздражающими электродами (рис. 1-91 А), то регистрирующая аппаратура зарегистрирует прохождение импульса как под электродами усилителя (1), так и под электродами усилителя (2) одновременно.
Третий закон заключается в том, что возбуждение по нерву распространяется без затухания или без «декремента». Для доказательства на одну сторону нервного волокна накладывают пару электродов, посредством которых наносят раздражение, а две пары электродов, связанных с двумя дифференциальными усилителями, располагают на удалении, как это показано на рис. 1-91 Б. В этом случае регистрирующая аппаратура, связанная с усилителями (1) и (2), продемонстрирует одинаковую амплитуду потенциала действия нервного волокна.
Четвертый закон заключается в том, что для проведения возбуждения по нервному стволу необходима анатомическая и физиологическая целостность нервного волокна. Проведение импульсов возможно лишь при условии анатомической целостности волокна, поэтому любая травма поверхности волокна нарушают его проводимость. Отсутствие проводимости наблюдается также при нарушении физиологической целостности волокна. В эксперименте на одну сторону нервного волокна накладывают пару электродов, посредством которых наносят раздражение, а пару электродов, связанных с дифференциальным усилителем, располагают на удалении, как это показано на рис. 1-91 В. В этом случае регистрирующая аппаратура, связанная с усилителями (1), продемонстрирует в контрольных условиях потенциал действия нервного волокна. Достичь нарушения физиологической целостности нервного волокна можно, накладывая между раздражающими и регистрирующими электродами ватку, смоченную спиртом. Если перевязать лигатурой нервный ствол, проведение возбуждения по нему наблюдаться не будет из-за нарушения его анатомической целостности.














 Опорно-двигательная система. Значение опорно-двигательной системы. Строение костей
Опорно-двигательная система. Значение опорно-двигательной системы. Строение костей Влияние распорядка учебного дня на работоспособность и концентрацию и оптимизация временных затрат на учебный процесс
Влияние распорядка учебного дня на работоспособность и концентрацию и оптимизация временных затрат на учебный процесс Мухи: польза и вред. Исследовательский проект
Мухи: польза и вред. Исследовательский проект Презентация на тему Организм побеждает болезни
Презентация на тему Организм побеждает болезни Органическое вещество почвы
Органическое вещество почвы Птицы из красной книги Башкортостана. Региональный компонент на уроках математики в начальной школе
Птицы из красной книги Башкортостана. Региональный компонент на уроках математики в начальной школе Биосинтез заменимых аминокислот. Деградация нуклеиновых кислот. (Лекция 4)
Биосинтез заменимых аминокислот. Деградация нуклеиновых кислот. (Лекция 4) Наследственность, изменчивость
Наследственность, изменчивость Импринтинг. Нарушения импринтинга как причина наследственной патологии. Семинар 7
Импринтинг. Нарушения импринтинга как причина наследственной патологии. Семинар 7 Интеллектуалды ойын
Интеллектуалды ойын Где живут микробы
Где живут микробы Кольчатые черви
Кольчатые черви ВІЛ та СНІД
ВІЛ та СНІД  Как помочь птицам
Как помочь птицам Регуляция дыхания. Транспорт О2 кровью
Регуляция дыхания. Транспорт О2 кровью Заттардың тасымалдануы. Гуморальді және жасушалық иммунитетті салыстыру
Заттардың тасымалдануы. Гуморальді және жасушалық иммунитетті салыстыру Растение подорожник
Растение подорожник Фотосинтез Презентация для 6 класса Проценко Л.В._
Фотосинтез Презентация для 6 класса Проценко Л.В._ Клетка как биологическая система
Клетка как биологическая система Строение головного мозга. Продолговатый мозг. Задний мозг. Лекция № 23
Строение головного мозга. Продолговатый мозг. Задний мозг. Лекция № 23 Гордость и чудо Астраханского края - лотос
Гордость и чудо Астраханского края - лотос Прокариотическая клетка
Прокариотическая клетка Физиология кровообращения
Физиология кровообращения Мускулатура рыб. Физиологические основы движения. Лекция 4
Мускулатура рыб. Физиологические основы движения. Лекция 4 Основные эволюционные преобразования в кровеносной системе хордовых
Основные эволюционные преобразования в кровеносной системе хордовых Презентация на тему Значение, строение и функционирование нервной системы
Презентация на тему Значение, строение и функционирование нервной системы Живая природа - прототип человеческих изобретений
Живая природа - прототип человеческих изобретений Птица удод
Птица удод