Раздел «Структурные уровни и системная организация материи» Мальцев Алексей Владимирович, Доцент кафедры общей психологии
Содержание
- 2. Тема «Микро-, макро-, мегамиры» Изучается самостоятельно на семинарских занятиях в виде деловой игры
- 3. Тема «Системные уровни организации материи»
- 4. Свойства материи (природы) Целостность Системность Аддитивность Интегративность
- 5. Целостность природы Природное тело (объект) сочетает в себе много свойств (физических, химических, биологических) т.е. обладает целостностью
- 6. Целостность природы
- 7. Системность природы Природа рассматривается как совокупность взаимосвязанных элементов, которая образует целостный объект, имеющий новые качества, не
- 8. Примеры систем совокупность звезд нашей Галактики буквы, составляющие текст звезды, входящие в состав шарового скопления двойные
- 9. Системность природы
- 10. Аддитивные свойства систем Свойство системы, состоящее в том, что значение, соответствующее целому объекту, равно сумме значений,
- 11. Примеры аддитивных величин: Энергия; Импульс; Энтропия; Мощность; Давление, плотность (в случае смеси идеальных газов); Электрический заряд;
- 12. Аддитивные свойства систем Мало распространены при химических явлениях. Например количество вещества (в случае смеси не взаимодействующих
- 13. Интегративные свойства систем Такие свойства, которые присущи системе в целом, но не свойственны ни одному из
- 14. Примеры интегративности Экологические системы (биогеоценозы) Живой организм – особенно организм человека не сводится к сумме составляющих
- 15. Интегративность живых систем
- 16. Иерархичность природных систем порядок подчинённости низших звеньев высшим, организация их в структуру типа «дерево»;
- 17. Иерархичность физических систем Фундаментальные частицы (кварки) Составные элементарные частицы (протон) Атомные ядра Атомы Молекулы Макроскопические тела
- 18. Иерархичность астрономических систем звёзды с их планетными системами галактики скопления галактик сверхскопления галактик метагалактика
- 19. Иерархичность химических систем атом простая молекула (молекула из одного вида химического элемента) сложная молекула (молекула из
- 20. Иерархичность биологических систем Рассмотреть самостоятельно в рамках темы Особенности биологического уровня организации материи
- 21. Тема «Структуры микромира»
- 22. Элементарные частицы Это частицы, входящие в состав атома. Электрон был открыт Томсоном в 1867 году Протон
- 23. Фундаментальные частицы микрочастицы, внутреннюю структуру которой нельзя представить в виде объединения других свободных частиц.
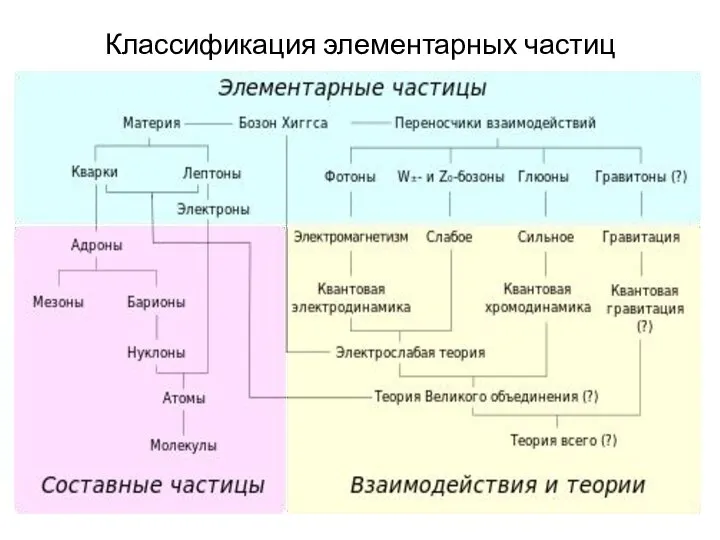
- 24. Классификация элементарных частиц
- 25. Частицы, образующие вещество Адроны – составные частицы, состоят из кварков, участвуют в сильных взаимодействиях (например протон
- 26. Частицы, образующие поле Фотон – переносчик электромагнитного взаимодействия Глюон – переносчик сильного взаимодействия Бозон – переносчик
- 27. По продолжительности жизни стабильные (протон, электрон, нейтрино, фотон), остальные не стабильные! нестабильные (свободный нейтрон) и резонансы,
- 28. Античасти́ца Частица-двойник некоторой другой элементарной частицы, обладающая той же массой, но отличающаяся от неё знаком заряда.
- 29. Взаимопревращения элементарных частиц 1.Распад нейтрона (Бета распад ): (нейтрон) n = p+ (протон) + e- (электрон)
- 30. β − распад превращение нейтрона в протон, при этом испускаются электрон и антинейтрино:
- 31. Вещество как совокупность корпускулярных структур кварки нуклоны (протоны и нейтроны) атомные ядра атомы с их электронными
- 32. Строение атома Атом состоит из ядра атома и электронной оболочки В ядре атома сосредоточена практически вся
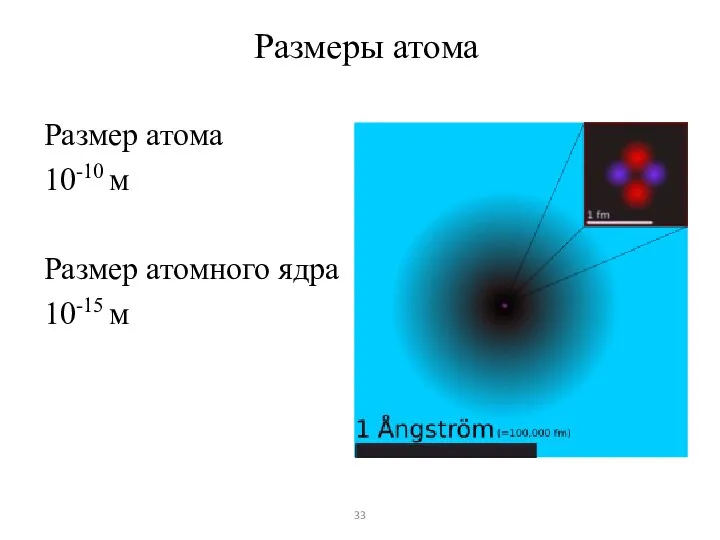
- 33. Размеры атома Размер атома 10-10 м Размер атомного ядра 10-15 м
- 34. Строение атома Число электронов в атоме равно порядковому номеру Z элемента в таблице Менделеева Число протонов
- 35. Тема «Химические системы»
- 36. Химический элемент Для обозначения химических элементов применяется запись - ZXA где Х – символ химического элемента
- 38. Изотопы химических элементов Ядра с одинаковыми Z, но разными А называются изотопами. изотопы кальция: 20Са40(20p20n) 20Са42(20p22n)
- 39. Организация электронных состояний атома в электронные оболочки Электронная оболочка атома — область пространства вероятного местонахождения электронов,
- 40. Организация электронных состояний атома в электронные оболочки n – главное квантовое число (энергетический уровень оболочки) l
- 41. Число электронов в оболочке на уровнях (n) и подуровнях (l )
- 42. Электронные конфигурации основного состояния элементов
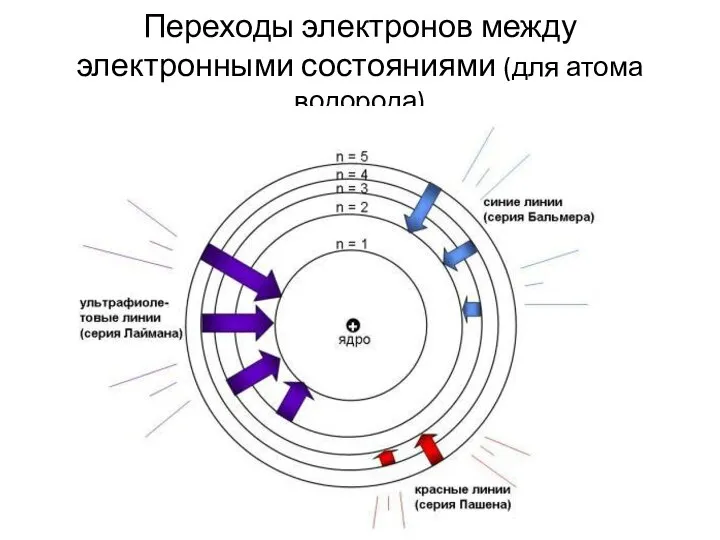
- 43. Переходы электронов между электронными состояниями Квантовое состояние с наименьшей энергией атома называют основным. Остальные квантовые состояния
- 44. Переходы электронов между электронными состояниями (для атома водорода)
- 45. Вещества простые и сложные Простые – химические вещества, образованные атомами одного рода. О2 Вещества сложные (соединения)
- 46. Полимеры и мономеры Полимеры – молекулы сложного строения, образованные последовательно связанными повторяющимися мономерными звеньями. Полимер –
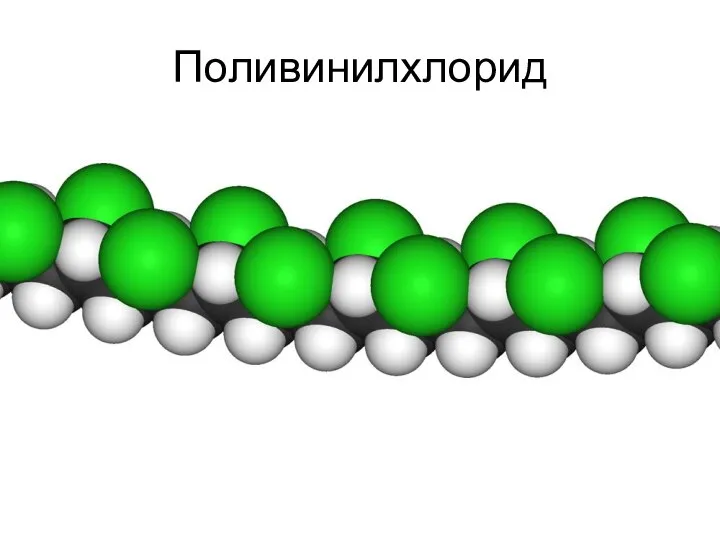
- 47. Поливинилхлорид
- 48. Катализаторы Химические вещества, ускоряющие скорость химических реакций, но не входящие в состав продуктов реакции. Биокатализаторы (ферменты
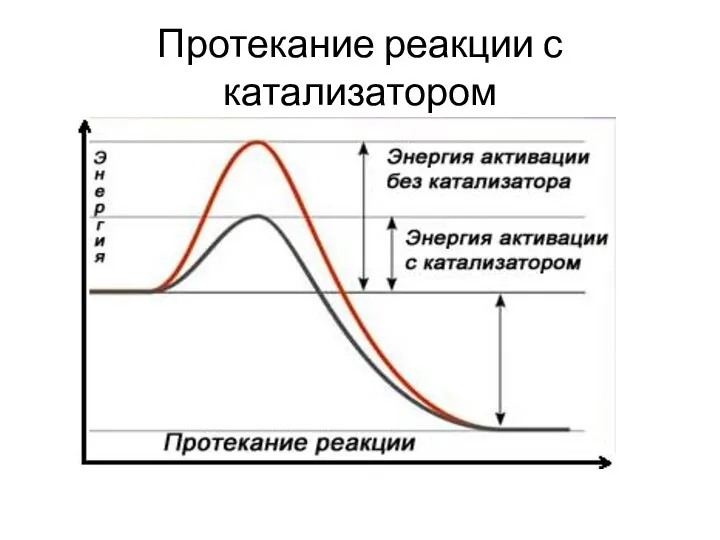
- 49. Протекание реакции с катализатором
- 50. Ферменты Отличительной особенностью ферментов по сравнению с небелковыми катализаторами является их высокая специфичность. При этом эффективность
- 51. Ферменты
- 53. Скачать презентацию












































 Одномембранные органоиды
Одномембранные органоиды Еволюція міжклітинного сигналінгу
Еволюція міжклітинного сигналінгу Презентация на тему "Жизнь без боли в пояснице" - скачать презентации по Биологии
Презентация на тему "Жизнь без боли в пояснице" - скачать презентации по Биологии Вред и польза сорняков
Вред и польза сорняков Тварини дбають про своє потомство
Тварини дбають про своє потомство Джунгарский хомяк
Джунгарский хомяк Презентация на тему Биополимеры. Нуклеиновые кислоты._
Презентация на тему Биополимеры. Нуклеиновые кислоты._ Общая эмбриология
Общая эмбриология Презентация по биологии Органы цветковых растений.
Презентация по биологии Органы цветковых растений.  Урок на тему: «Вода – растворитель» (Лабораторная работа с элементами игровой технологии). Цели : Образовательная – в ходе лаб
Урок на тему: «Вода – растворитель» (Лабораторная работа с элементами игровой технологии). Цели : Образовательная – в ходе лаб Половое размножение
Половое размножение Әйел жыныс мүшелерінің анатомиясы және физиологиясы
Әйел жыныс мүшелерінің анатомиясы және физиологиясы Презентация Угольная кислота
Презентация Угольная кислота Регуляция работы сердца и сосудов. Автоматизм сердечной деятельности
Регуляция работы сердца и сосудов. Автоматизм сердечной деятельности Жизнь природы летом
Жизнь природы летом Катаболизм жирных кислот. Метаболизм кетоновых тел. (Лекция 8)
Катаболизм жирных кислот. Метаболизм кетоновых тел. (Лекция 8) Хворостухина Олеся МОУ «Лицей №10», г. Пермь
Хворостухина Олеся МОУ «Лицей №10», г. Пермь Аттестационная работа. программа внеурочной деятельности Я - исследователь. (5-6 класс)
Аттестационная работа. программа внеурочной деятельности Я - исследователь. (5-6 класс) Презентация на тему "МЛЕКОПИТАЮЩИЕ, или ЗВЕРИ" - скачать бесплатно презентации по Биологии
Презентация на тему "МЛЕКОПИТАЮЩИЕ, или ЗВЕРИ" - скачать бесплатно презентации по Биологии Окружающий мир 3 класс Тема: Кровь и кровообращение
Окружающий мир 3 класс Тема: Кровь и кровообращение Использование интерактивных дидактических ресурсов при изучении темы «Цитология» Автор работы: Назарова Эльвира Александровна,
Использование интерактивных дидактических ресурсов при изучении темы «Цитология» Автор работы: Назарова Эльвира Александровна, ← Картинка 3 из 166 190 → Вернуться к результатам поиска
← Картинка 3 из 166 190 → Вернуться к результатам поиска  Строение и значение нервной системы
Строение и значение нервной системы Уголок природы дошкольников. Цветы
Уголок природы дошкольников. Цветы Физиология прокариот. Лекция 2
Физиология прокариот. Лекция 2 Презентация на тему "Отряды насекомых: Бабочки, Равнокрылые, Блохи, Двукрылые" - скачать презентации по Биологии
Презентация на тему "Отряды насекомых: Бабочки, Равнокрылые, Блохи, Двукрылые" - скачать презентации по Биологии Животные маленькие и большие
Животные маленькие и большие Презентация по экологии Экосистемы
Презентация по экологии Экосистемы