Содержание
- 2. Витамины – низкомолекулярные органические соединения, не синтезирующиеся в организме человека и животных, обладающие высокой биологической активностью
- 3. Общебиологические признаки витаминов Не синтезируются в организме человека; Не являются ни пластическим, ни энергетическим материалом, но
- 4. Название витамина: Буквенное Химическое Клиническое
- 5. Классификация витаминов Жирорастворимые А (ретинол) Д (холекальциферол, эргокальциферол) Е (токоферолы) К (филлохинон, нафтохинон) Водорастворимые В1 (тиамин)
- 6. Витаминоподобные соединения: Синтезируются в организме человека, но синтез не покрывает потребностей; Более низкая биологическая активность по
- 7. Витаминоподобные соединения Жирорастворимые F (полиненасы- щенные жирные кислоты) Q (убихинон) Водорастворимые Липоевая кислота Пангамовая кислота Оротовая
- 8. Антивитамины – соединения, близкие к витаминам по химическому строению, но обладающие противоположным биологическим действием. При попадании
- 9. Источники витаминов для человека Пища животного и растительного происхождения; Провитамины – соединения, содержащие в своей структуре
- 10. Нарушения обмена витаминов Гипо(а)витаминозы – заболевания, возникающие вследствие недостатка или отсутствия витаминов в организме. Гипервитаминозы –
- 11. Гипо(а)витаминозы витаминов с пищей резервирования витаминов Нарушение усвоения витаминов на клеточном уровне Поступление антивитаминов
- 12. Типы гипо(а)витаминозов Витаминдефицитные состояния – заболевания, обусловленные дефицитом в пище того или иного витамина. Это экзогенные
- 13. Типы гипо(а)витаминозов Витаминзависимые состояния – заболевания, в основе которых лежит дефект ферментов, обеспечивающих превращение витамина в
- 14. Типы гипо(а)витаминозов Витаминрезистентные состояния — генетически обусловленные заболевания, характеризующиеся неспособностью организма усваивать витамин на клеточном уровне
- 15. Общая характеристика жирорастворимых витаминов: Растворяются в жирах; Легко всасываются, но для их всасывания необходимы жиры (как
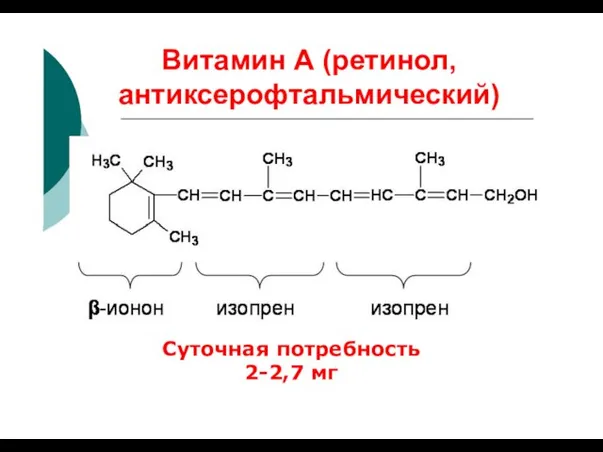
- 16. Витамин А (ретинол, антиксерофтальмический) Суточная потребность 2-2,7 мг
- 17. Источники витамина А Печень крупного рогатого скота и свиней; Яичный желток; Молочные продукты; Рыбий жир; В
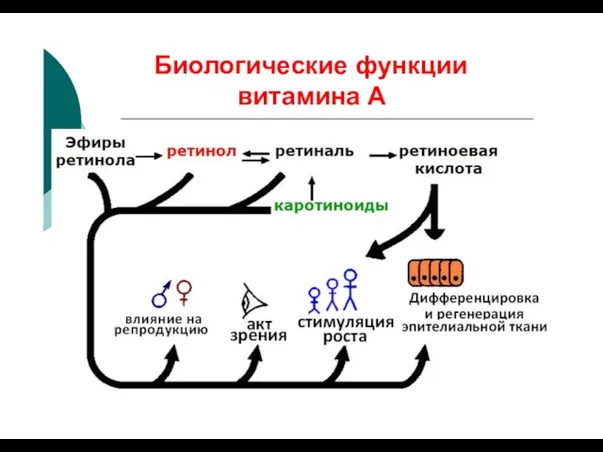
- 18. Биологические функции витамина А
- 19. Клинические проявления гиповитаминоза Нарушение сумеречного зрения - «куриная слепота» или гемералопия; Сухость роговицы – ксерофтальмия; Размягчение
- 20. Гипервитаминоз витамина А кожные высыпания, шелушение кожи, гиперкератоз выпадение волос общее истощение организма тошнота и рвота
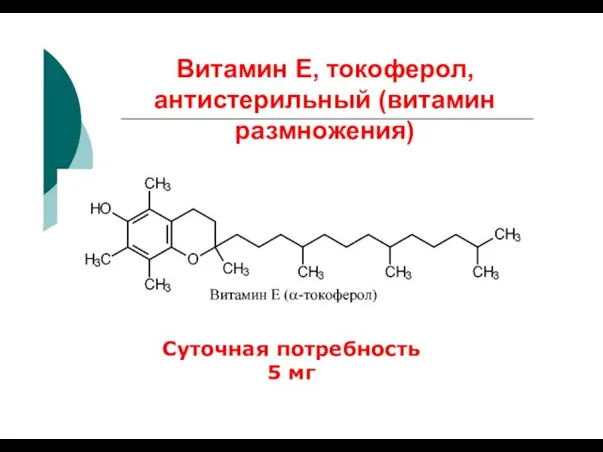
- 21. Витамин Е, токоферол, антистерильный (витамин размножения) Суточная потребность 5 мг
- 22. Источники витамина Е Растительные масла; Салат; Капуста; Семена злаков; Сливочное масло; Яичный желток.
- 23. Биологическая роль витамина Е Природный антиоксидант: Предотвращает повреждение липидов мембран и ДНК; Повышает биологическую активность витамина
- 24. Клинические проявления гиповитаминоза: Бесплодие; Поражение нервной системы, атаксия, мышечная дистрофия
- 25. Гипервитаминоз витамина Е головная боль повышенная утомляемость расстройства работы желудочно-кишечного тракта
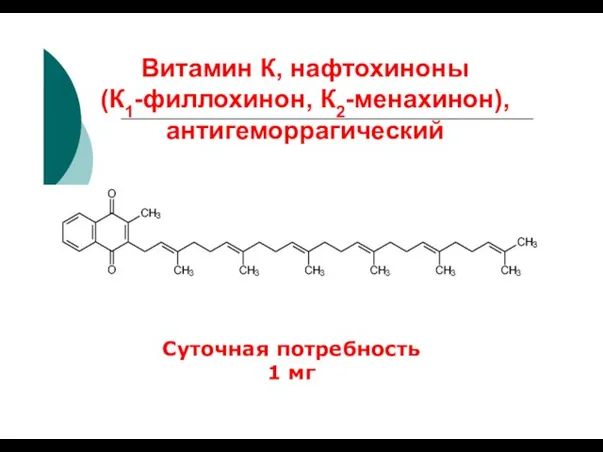
- 26. Витамин К, нафтохиноны (К1-филлохинон, К2-менахинон), антигеморрагический Суточная потребность 1 мг
- 27. Источники витамина К Капуста; Шпинат; Корнеплоды; Фрукты; Печень; Микрофлора толстого кишечника.
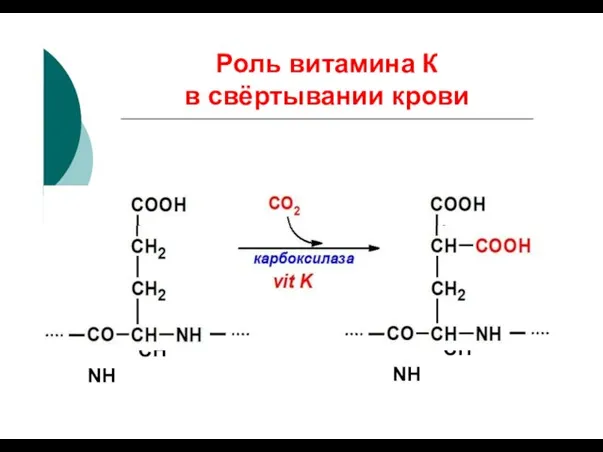
- 28. Роль витамина К в свёртывании крови Стимулирует синтез II, VII, IX и X факторов свёртывания крови
- 29. COOH СО2 COOH Роль витамина К в свёртывании крови СН2 СН2 CO СН NН СН2 CO
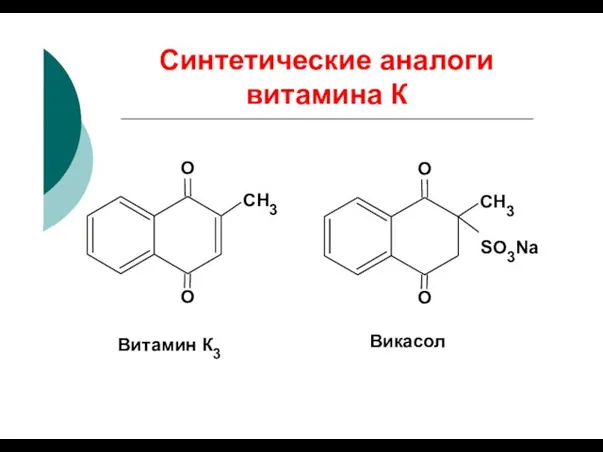
- 30. Синтетические аналоги витамина К O CH3 O O O CH3 SO3Na Витамин К3 Викасол
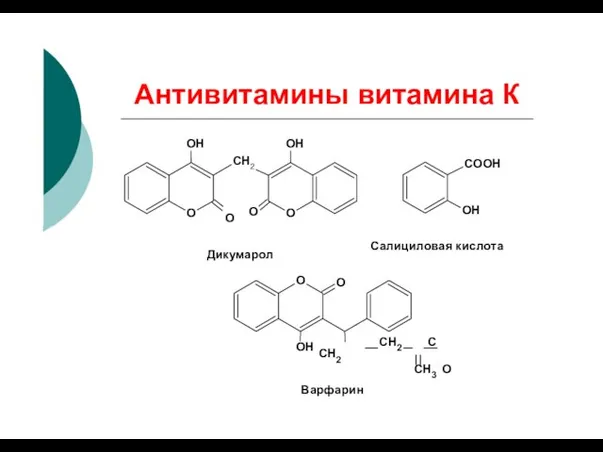
- 31. Антивитамины витамина К O СН2 O OH OH O O Дикумарол COOH OH Салициловая кислота O
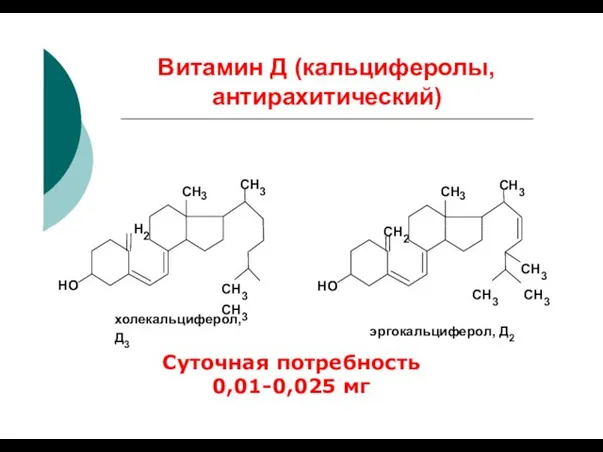
- 32. Витамин Д (кальциферолы, антирахитический) CH3 CH 3 CH3 CH 3 CH3 CH3 H2 HO холекальциферол, Д3
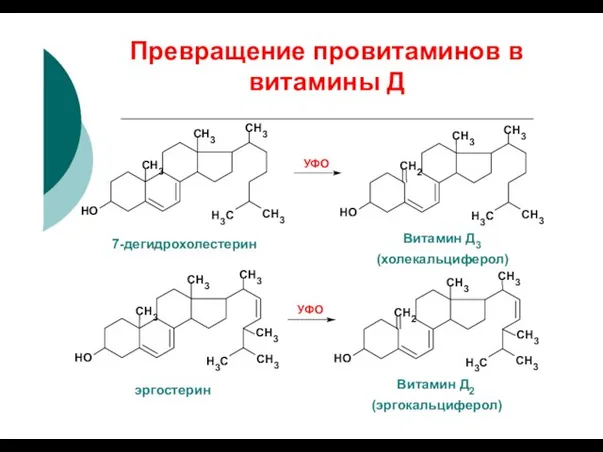
- 33. Источники витамина Д Сливочное масло; Желток яиц; Рыбий жир; Синтез в организме из 7-дегидрохолестерина.
- 34. Превращение провитаминов в витамины Д CH3 H3C CH3 CH3 CH3 HO CH3 CH3 CH2 CH3 HO
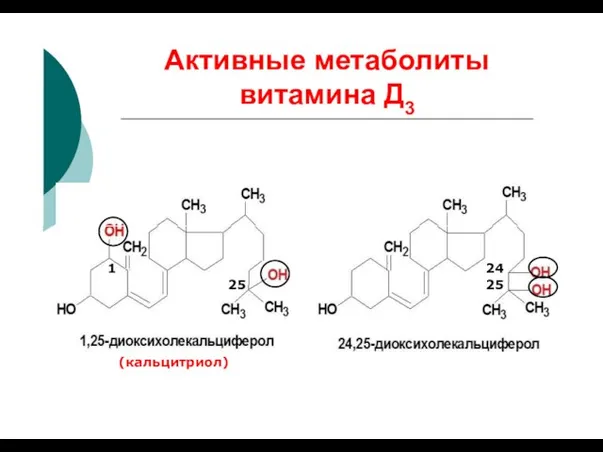
- 35. Активные метаболиты витамина Д3 (кальцитриол) 1 24 25 25
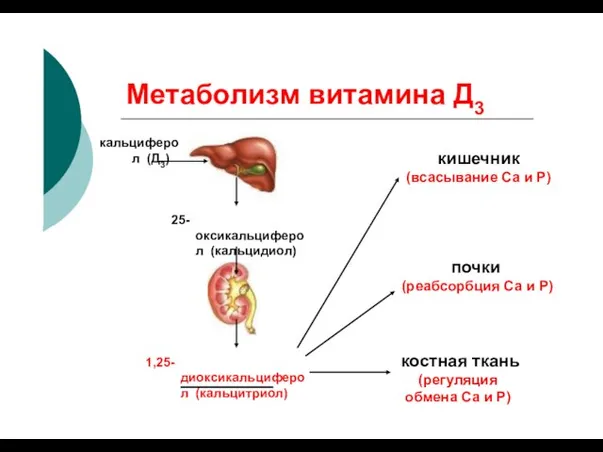
- 36. Метаболизм витамина Д3 кальциферол (Д3) кишечник (всасывание Са и Р) 25-оксикальциферол (кальцидиол) 1,25-диоксикальциферол (кальцитриол) почки (реабсорбция
- 37. Гипервитаминоз витамина Д кальцификация крупных артерий, почек, сердца и легких в костях – остеопороз с отложениями
- 38. Общебиологические свойства водорастворимых витаминов Не накапливаются в организме человека; Для них более характерны гипо(а)витаминозы; Являются составной
- 39. Общая схема действия водорастворимых витаминов Витамин Кофермент (активная форма) Фермент Биохими- ческая реакция
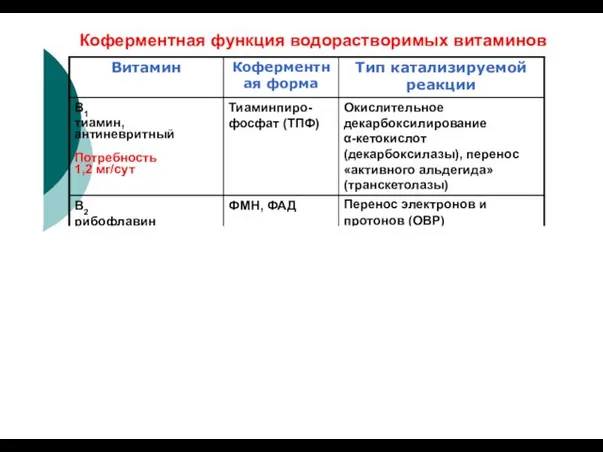
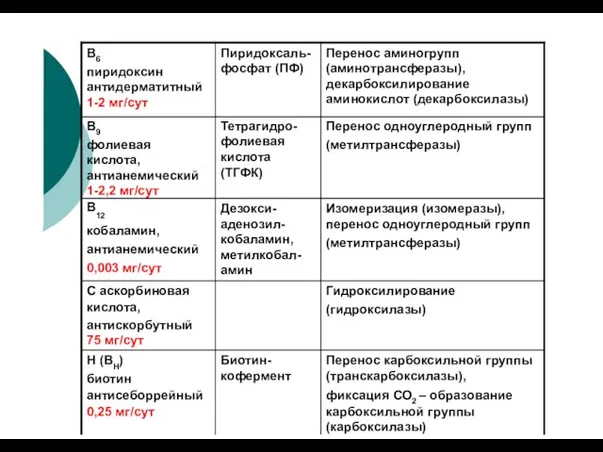
- 40. Коферментная функция водорастворимых витаминов
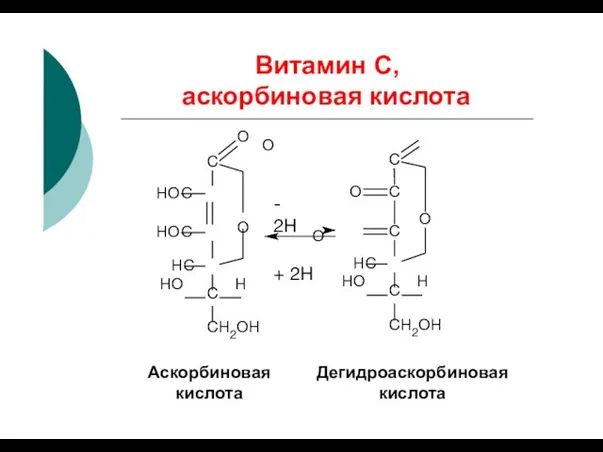
- 42. Витамин С, аскорбиновая кислота С HO С С С O O O O - 2Н Аскорбиновая
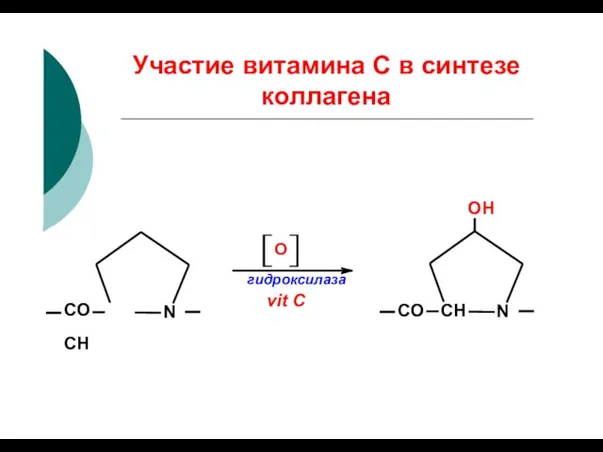
- 43. Участие витамина С в синтезе коллагена OH CO СН N О гидроксилаза vit С СН CO
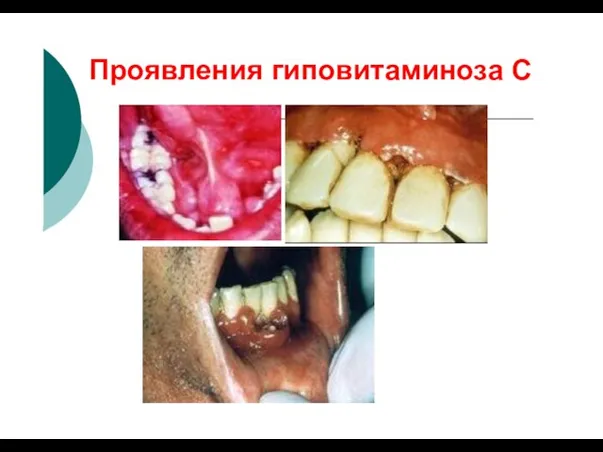
- 44. Проявления гиповитаминоза С
- 45. КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ ЛЕКЦИЯ по теме: ФЕРМЕНТЫ – 1 КРАСНОДАР
- 46. Ферменты – это биокатализаторы белковой природы, изменяющие скорость химических реакций в живых клетках
- 47. Свойства ферментов как белков Имеют высокую молекулярную массу Образуют коллоидные растворы Термолабильны Обладают высокой вязкостью, оптическими
- 48. Свойства ферментов как катализаторов Катализируют только термодинамически возможные реакции Не потребляются в ходе реакции и не
- 49. Собственные свойства ферментов Высокая биологическая активность Ферментная специфичность действия субстратная Иная зависимость от факторов, влияющих на
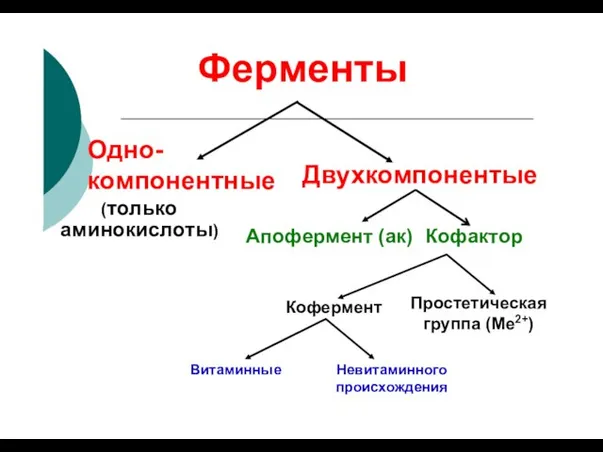
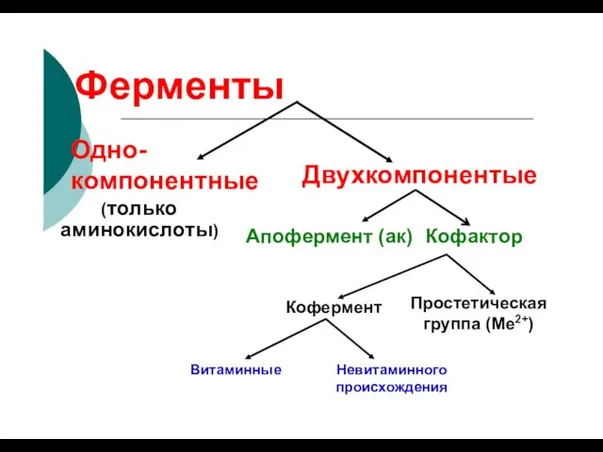
- 51. Ферменты Одно- компонентные (только Двухкомпонентые аминокислоты) Апофермент (ак) Кофактор Простетическая группа (Ме2+) Кофермент Витаминные Невитаминного происхождения
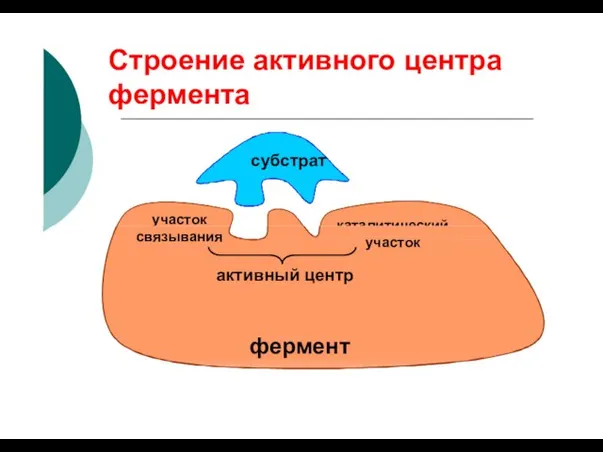
- 52. Строение активного центра фермента субстрат участок каталитический связывания участок активный центр фермент
- 53. Активный центр – участок молекулы фермента, в котором происходит узнавание, связывание и химическое превращение молекулы субстрата.
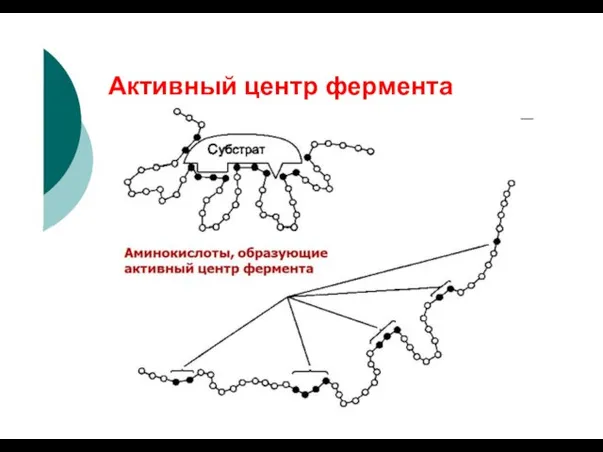
- 54. Активный центр фермента
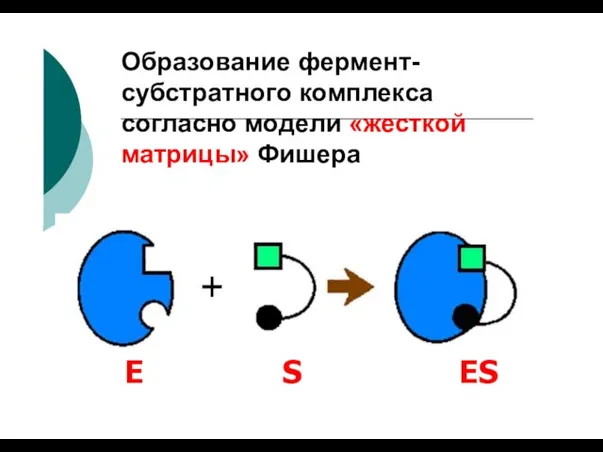
- 55. Образование фермент- субстратного комплекса согласно модели «жесткой матрицы» Фишера E S ES
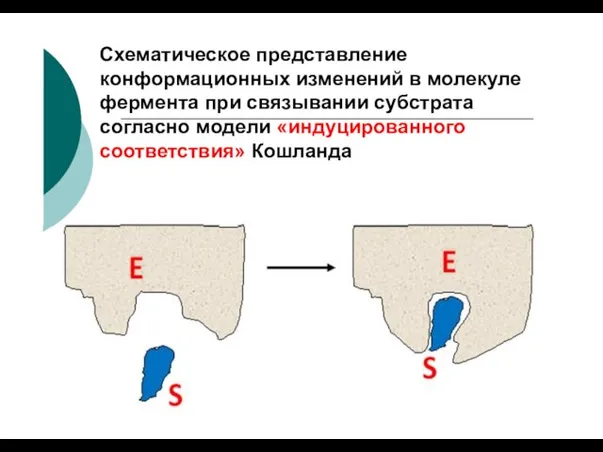
- 56. Схематическое представление конформационных изменений в молекуле фермента при связывании субстрата согласно модели «индуцированного соответствия» Кошланда
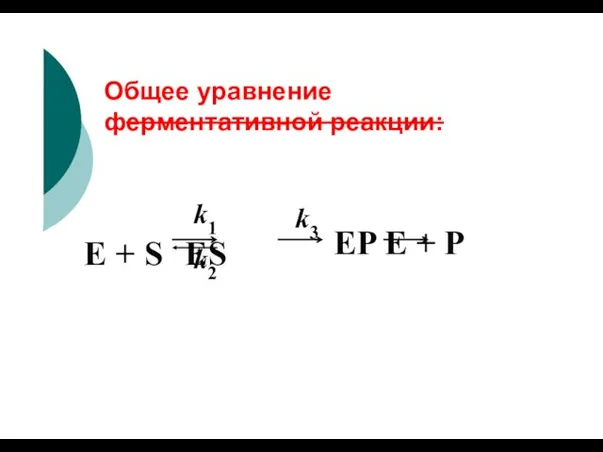
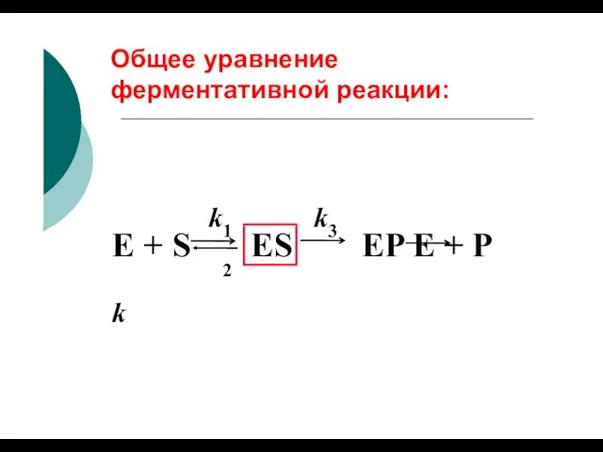
- 57. Общее уравнение ферментативной реакции: k1 E + S ES EP E + P k2 k3
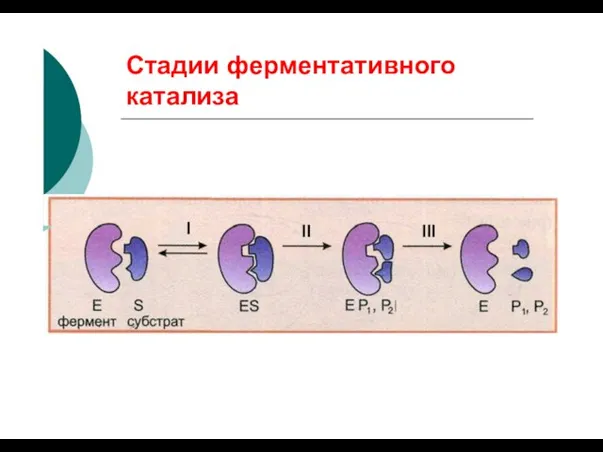
- 58. Стадии ферментативного катализа I III II
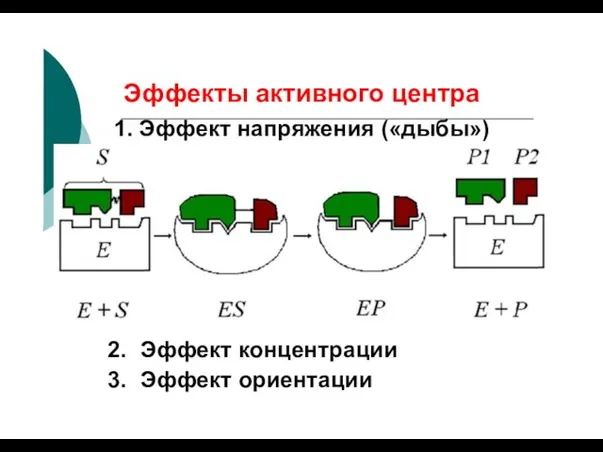
- 59. Эффекты активного центра 1. Эффект напряжения («дыбы») Эффект концентрации Эффект ориентации
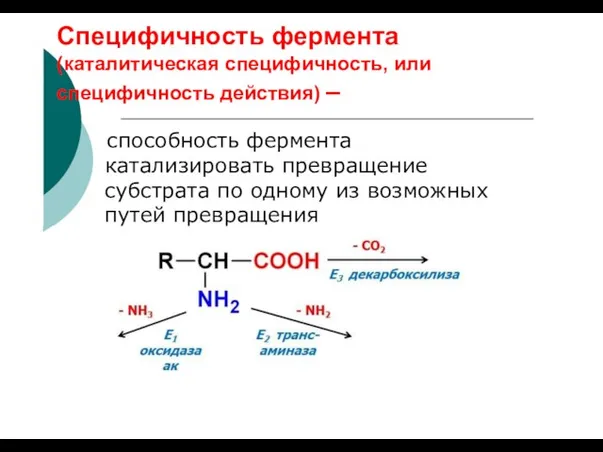
- 60. Специфичность фермента (каталитическая специфичность, или специфичность действия) – способность фермента катализировать превращение субстрата по одному из
- 61. Специфичность фермента (субстратная специфичность) – способность фермента узнавать, связывать и катализировать превращение только определённых субстратов, м.б.
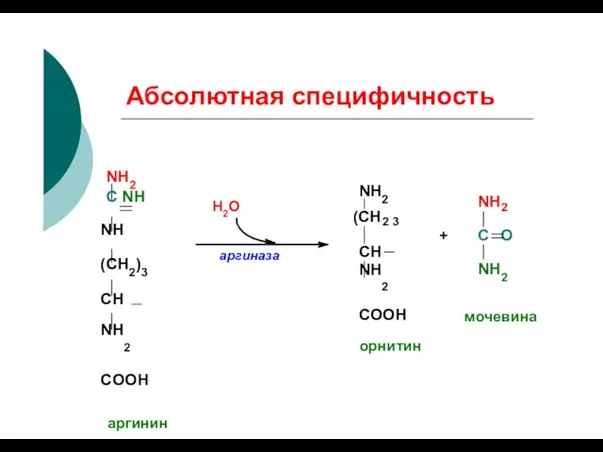
- 62. Абсолютная специфичность Н2О NH2 (СН ) 2 3 NH 2 аргиназа + С O NH2 NH2
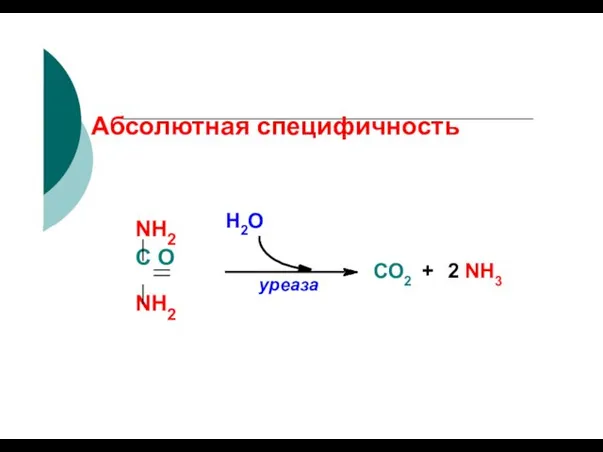
- 63. Абсолютная специфичность уреаза Н2О NH2 С O NH2 СО2 + 2 NH3
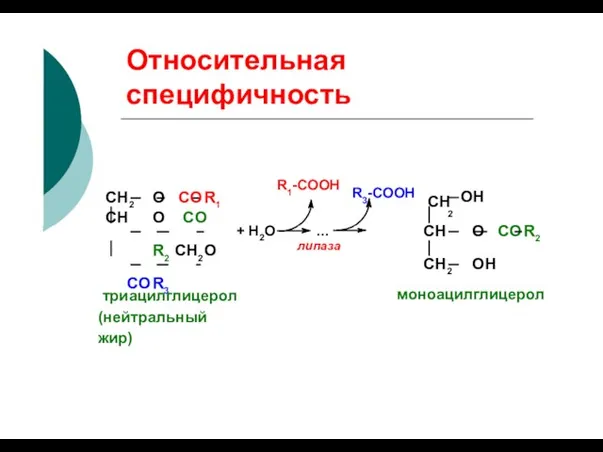
- 64. Относительная специфичность R1-COOH R3-COOH СН 2 OH + Н2О ... липаза СН2 O CО R1 СН
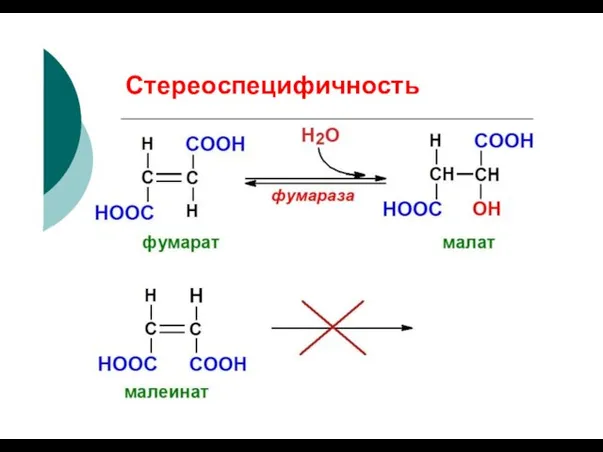
- 65. Стереоспецифичность
- 66. Общее уравнение ферментативной реакции: ES EP E + P E + S k 2 k3 k1
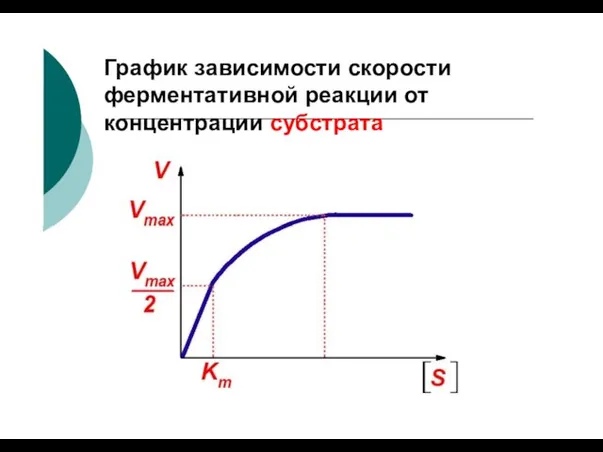
- 67. Константа Михаэлиса
- 68. Зависимость скорости ферментативной реакции от концентрации субстрата
- 70. График зависимости скорости ферментативной реакции от концентрации субстрата
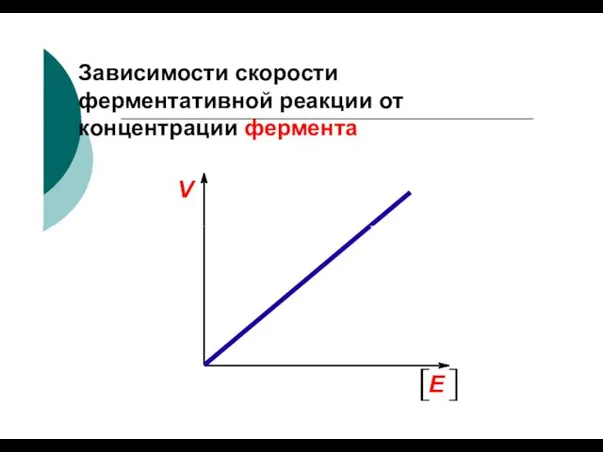
- 71. Зависимости скорости ферментативной реакции от концентрации фермента V E
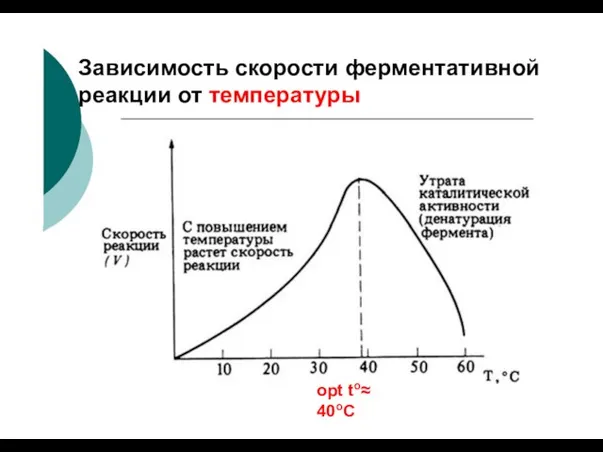
- 72. Зависимость скорости ферментативной реакции от температуры opt to≈ 40oC
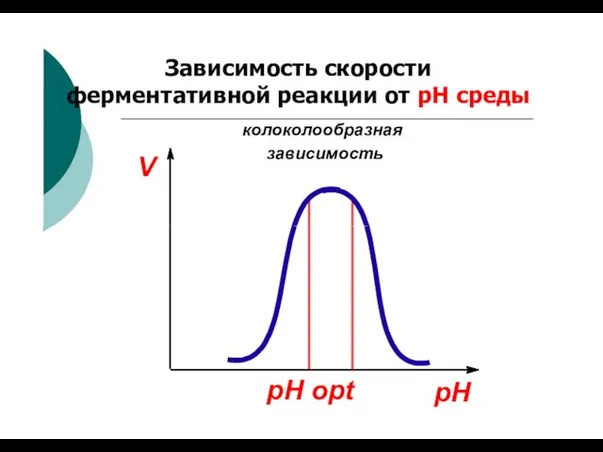
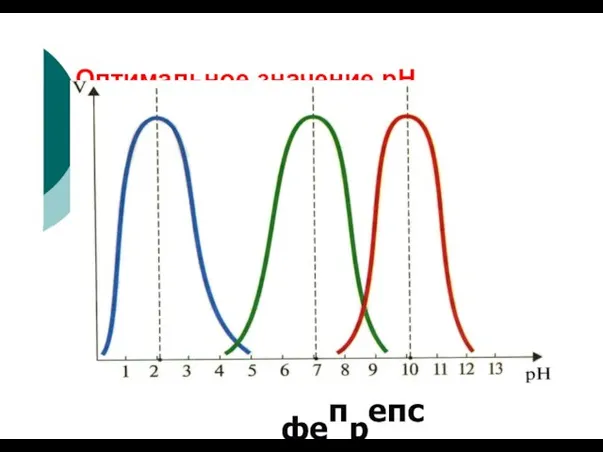
- 73. V колоколообразная зависимость Зависимость скорости ферментативной реакции от рН среды pH pH opt
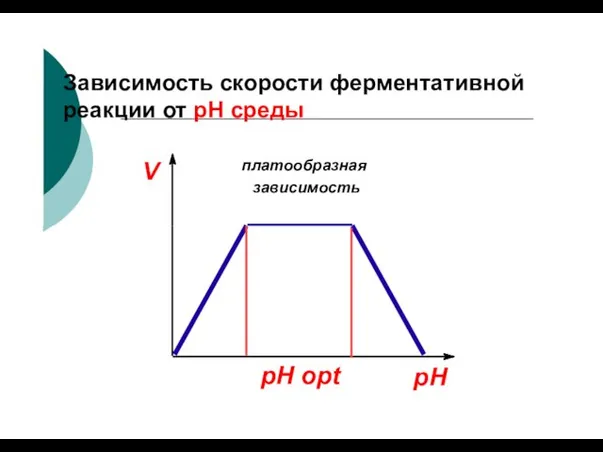
- 74. Зависимость скорости ферментативной реакции от рН среды V платообразная зависимость pH pH opt
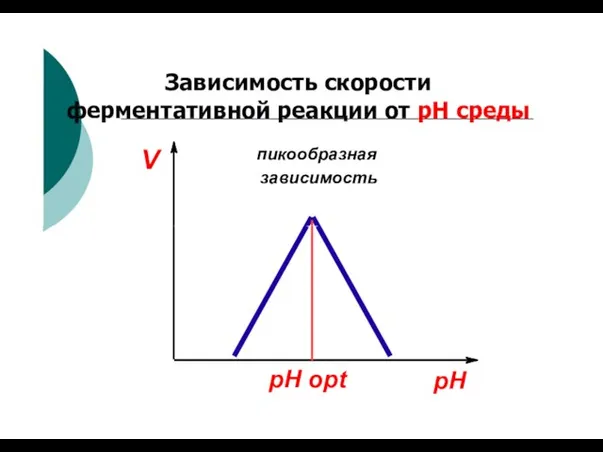
- 75. V пикообразная зависимость Зависимость скорости ферментативной реакции от рН среды pH pH opt
- 76. Оптимальное значение рН фепрепсин
- 77. активаторы ингибиторы обратимые необратимые
- 78. Неорганические вещества Низкомолекулярны е органические вещества Белки
- 79. Основные механизмы действия активаторов Площадка для взаимодействия фермента и субстрата Повышение сродства фермента и субстрата Отщепление
- 80. Механизмы ингибирования Конкурентное Неконкурентное Бесконкурентно е Субстратное Аллостерическо
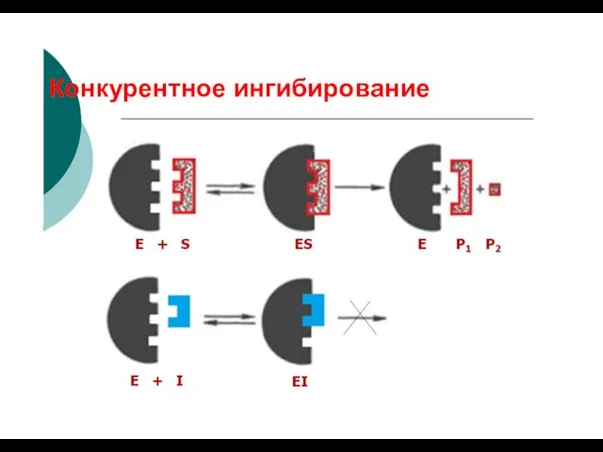
- 81. Конкурентное ингибирование
- 82. Конкурентное ингибирование E + S ES EP E + P E + I EI
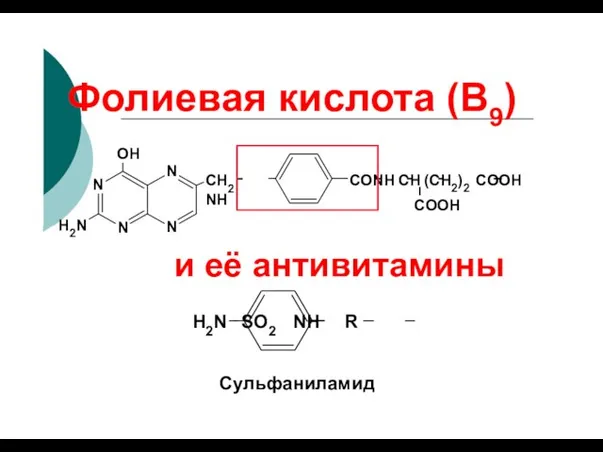
- 83. Фолиевая кислота (В9) N N OH СН2 NH СО NH СН (СН2)2 COOH COOH N H2N
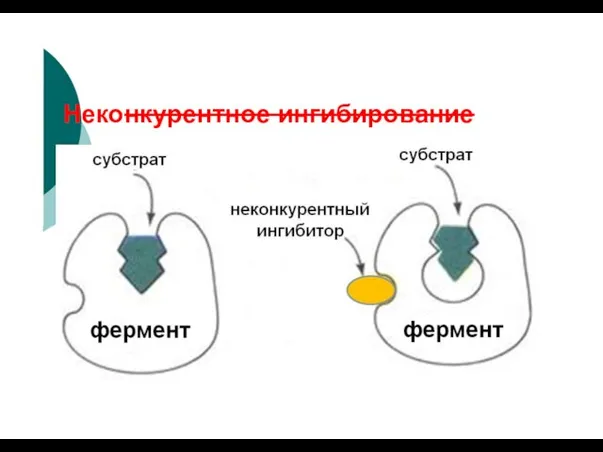
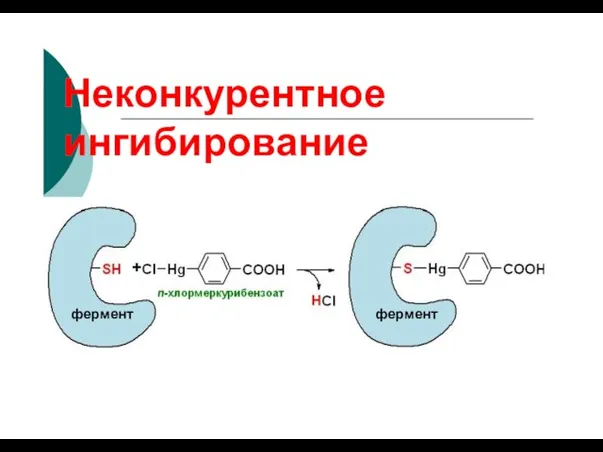
- 84. Неконкурентное ингибирование
- 85. Неконкурентное ингибирование фермент фермент +
- 86. Неконкурентное ингибирование E + S ES EP E + P E + I EI
- 87. Бесконкурентное ингибирование E + S ES EP E + P ES + I ESI
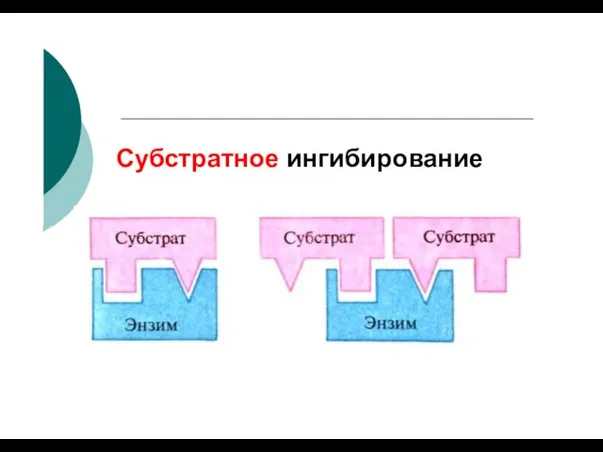
- 88. Субстратное ингибирование
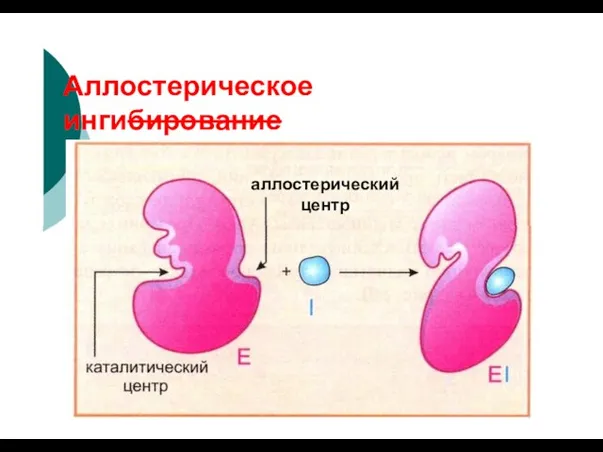
- 89. Аллостерическое ингибирование аллостерический центр
- 90. Ферменты Одно- компонентные (только Двухкомпонентые аминокислоты) Апофермент (ак) Кофактор Простетическая группа (Ме2+) Кофермент Витаминные Невитаминного происхождения
- 91. Металлы, содержащиеся в ферментах
- 92. Классификация коферментов По химическому строению Алифатические (липоевая кислота); Ароматические (коэнзим Q); Гетероциклические (ТПФ, ПФ); Нуклеотиды (НАД,
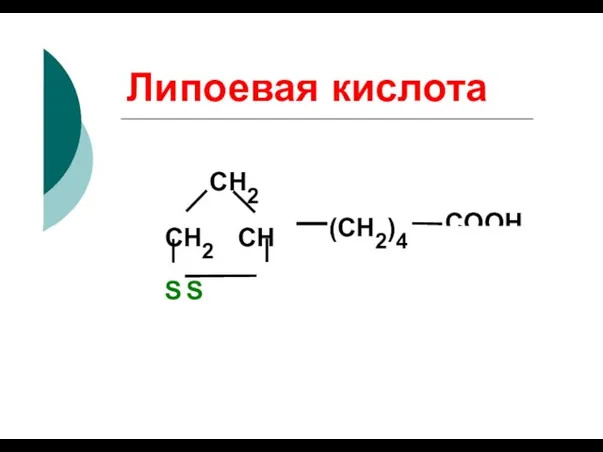
- 93. Липоевая кислота COOH (СН2)4 CH2 СН2 СН S S
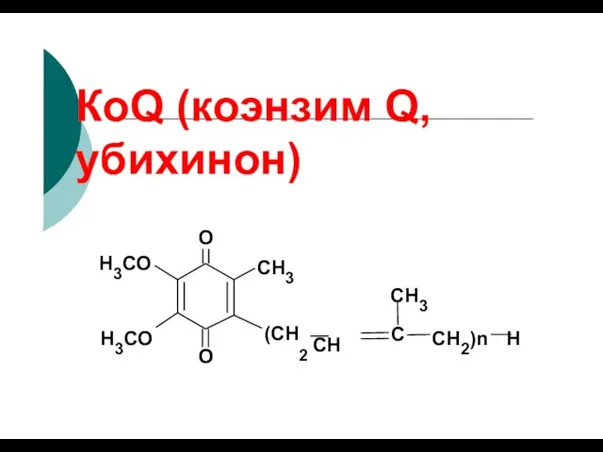
- 94. КоQ (коэнзим Q, убихинон) O O (СН2 СН С СН2)n Н CH3 CH3 Н3СО Н3СО
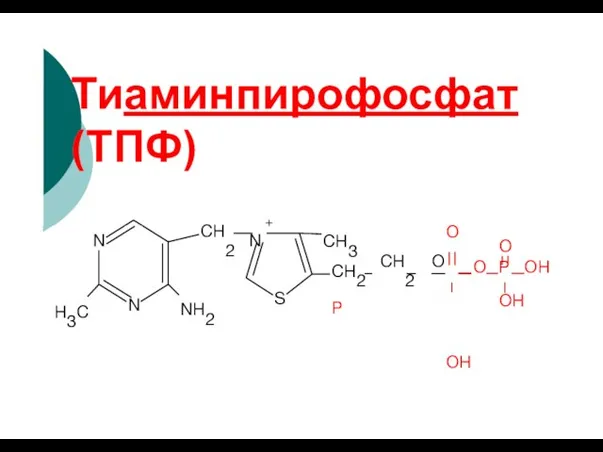
- 95. Тиаминпирофосфат (ТПФ) + N N H3C NH2 S CH2 N CH3 O CH2 CH2 O P
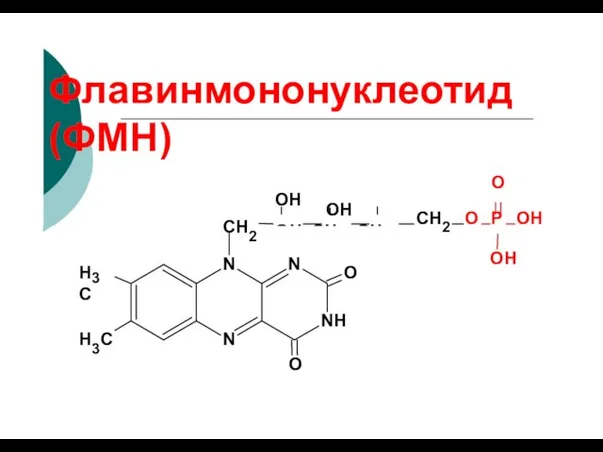
- 96. Флавинмононуклеотид (ФМН) OH OH OH CH CH CH N N NH N H C 3 H3C
- 97. По выполняемым функциям Переносчики протонов и электронов (НАД, ФАД, Ко Q); Переносчики групп (ТПФ, ПФ, КоА);
- 98. По механизму действия Коферменты с высоким потенциалом переноса энергии (переносчики энергии); Коферменты, участвующие в окислительно-восстановительных реакциях;
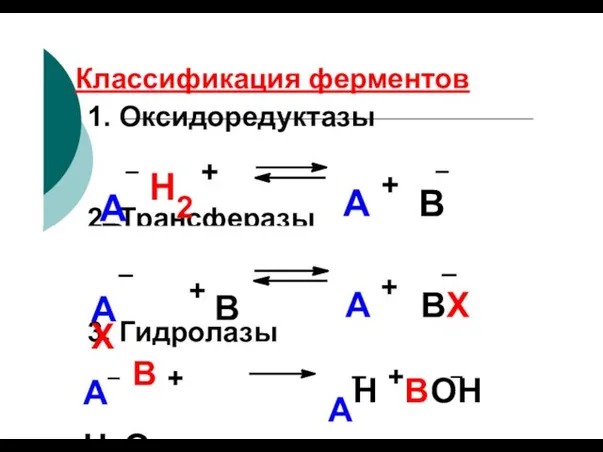
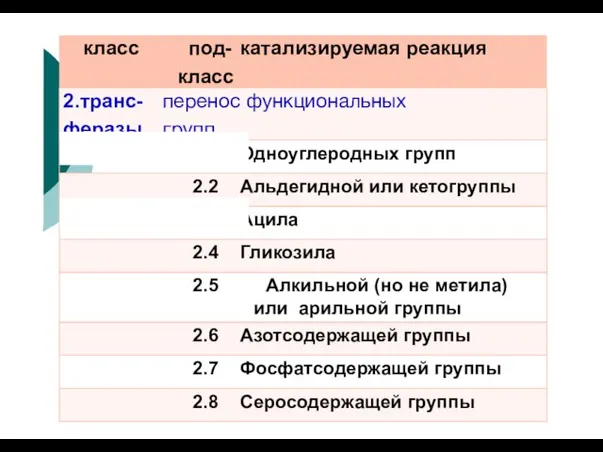
- 99. Классификация ферментов 1. Оксидоредуктазы 2. Трансферазы А Н2 + В А + В Н2 3. Гидролазы
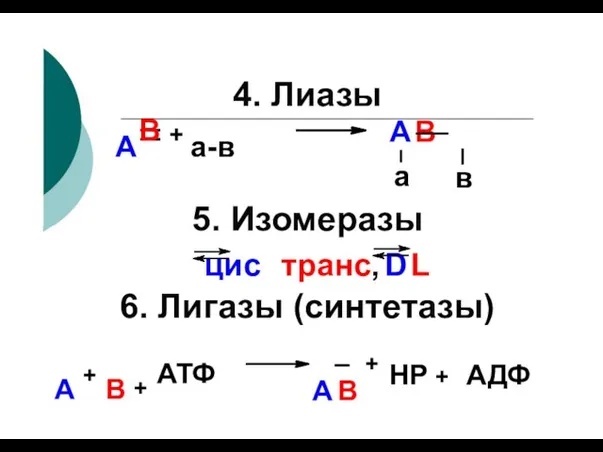
- 100. 4. Лиазы А В в А В + а-в 6. Лигазы (синтетазы) а 5. Изомеразы цис
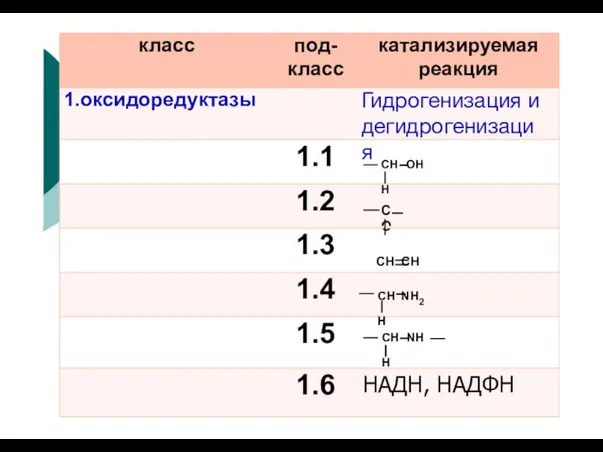
- 101. класс под- класс катализируемая реакция 1.оксидоредуктазы Гидрогенизация и дегидрогенизация 1.1 1.2 СН OH H С O
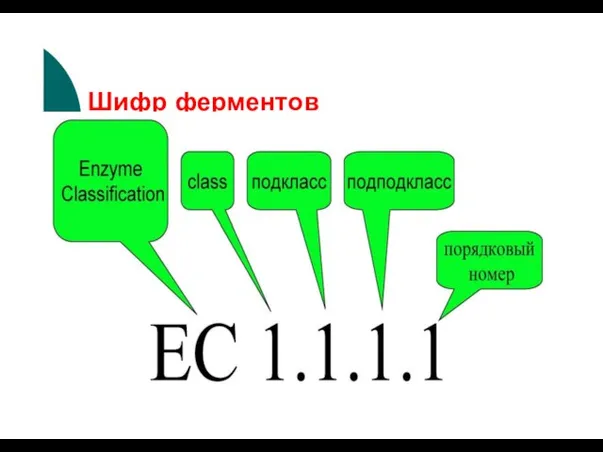
- 104. Шифр ферментов
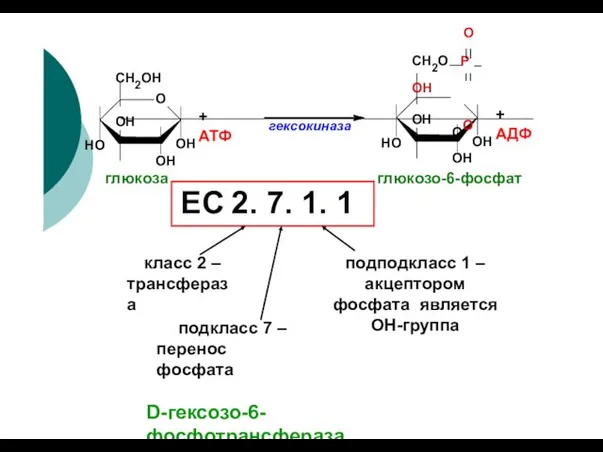
- 105. O СН2ОН HO OH OH OH + АТФ гексокиназа HO OH OH OH + АДФ O
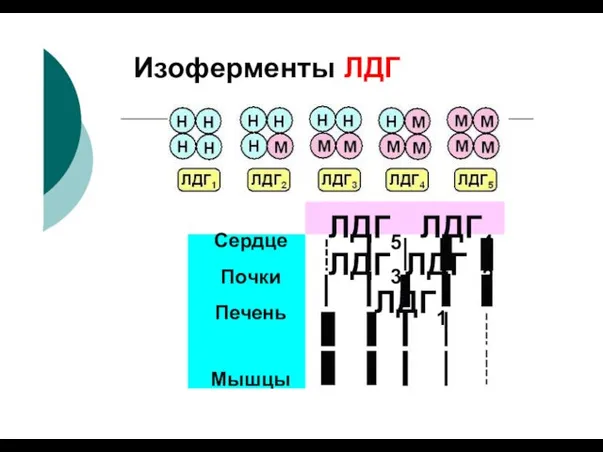
- 106. Изоферменты ЛДГ Сердце Почки Печень Мышцы ЛДГ5 ЛДГ4 3 ЛДГ ЛДГ 2 ЛДГ1
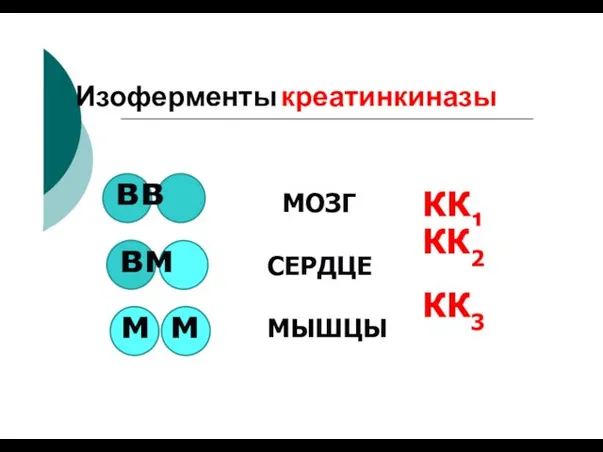
- 107. Изоферменты креатинкиназы в в МОЗГ КК1 в м м м СЕРДЦЕ МЫШЦЫ КК2 КК3
- 108. Единицы измерения количества и активности фермента 1 мкмоль превращенного S 1 мин 1МЕ =
- 109. nМЕ – количество единиц активности Кол-во превращенного S (мкмоль) nМЕ = Время (мин)
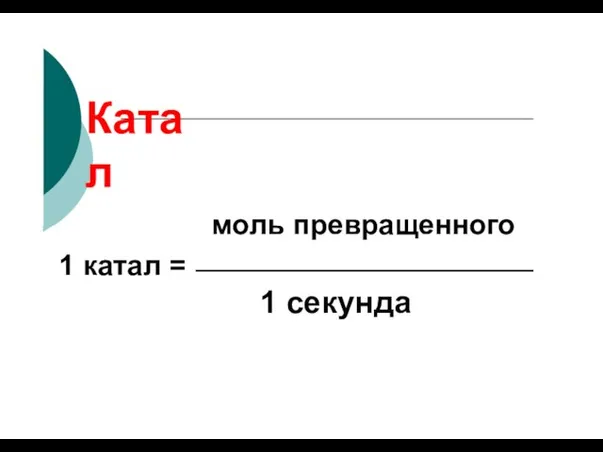
- 110. Катал моль превращенного 1 катал = 1 секунда
- 112. Скачать презентацию




















































 Мегатест покрытосеменные
Мегатест покрытосеменные Презентация на тему Положение человека в системе животного мира
Презентация на тему Положение человека в системе животного мира Класс Пресмыкающиеся (Рептилии)
Класс Пресмыкающиеся (Рептилии) Презентация на тему Враги кровообращения
Презентация на тему Враги кровообращения  Уход за короткошерстными собаками
Уход за короткошерстными собаками Жизнь на разных материках
Жизнь на разных материках Всё о чёрном море
Всё о чёрном море Выхухоль. Вид, русская выхухоль
Выхухоль. Вид, русская выхухоль День зустрічі птахів
День зустрічі птахів Организм – единое целое
Организм – единое целое Презентация на тему "Кое-что о приспособлениях Рыбы Защита" - скачать презентации по Биологии
Презентация на тему "Кое-что о приспособлениях Рыбы Защита" - скачать презентации по Биологии Выдающиеся биологи России Работа ученика 11класса Досова Ярослава
Выдающиеся биологи России Работа ученика 11класса Досова Ярослава Класс Птицы. Особенности внутреннего строения Птиц.
Класс Птицы. Особенности внутреннего строения Птиц. Биология человека: содержание. Предмет молекулярной биологии
Биология человека: содержание. Предмет молекулярной биологии Презентация на тему "Акулы " - скачать презентации по Биологии
Презентация на тему "Акулы " - скачать презентации по Биологии Значение покрытосеменных растений в жизни природы и человека
Значение покрытосеменных растений в жизни природы и человека Презентация на тему "Что такое донорство?" - скачать презентации по Биологии
Презентация на тему "Что такое донорство?" - скачать презентации по Биологии В мире птиц. Своя игра
В мире птиц. Своя игра Газированные напитки
Газированные напитки МОУ «Куровская средняя общеобразовательная школа № 6» МОУ «Куровская средняя общеобразовательная школа № 6»
МОУ «Куровская средняя общеобразовательная школа № 6» МОУ «Куровская средняя общеобразовательная школа № 6» Презентация для класса Происхождение человека
Презентация для класса Происхождение человека  Виды ресурсоведческих исследований
Виды ресурсоведческих исследований Наша малая Родина. Любимый город Нижнеудинск, которому 360 лет. Много лет стоит наш город на реке Уде. Краше в мире города не
Наша малая Родина. Любимый город Нижнеудинск, которому 360 лет. Много лет стоит наш город на реке Уде. Краше в мире города не  Урок биологии в 7 классе. Простейшие
Урок биологии в 7 классе. Простейшие LONDON THE CAPITAL AND THE HEART OF GREAT BRITAIN.
LONDON THE CAPITAL AND THE HEART OF GREAT BRITAIN.  Bones
Bones Изменчивость, наследственность
Изменчивость, наследственность Презентация на тему "Положение человека в системе животного мира" - скачать бесплатно презентации по Биологии
Презентация на тему "Положение человека в системе животного мира" - скачать бесплатно презентации по Биологии