Содержание
- 2. 1. Рід Influenzavirus A - віруси грипу типу А 2. Рід Influenzavirus B - віруси грипу
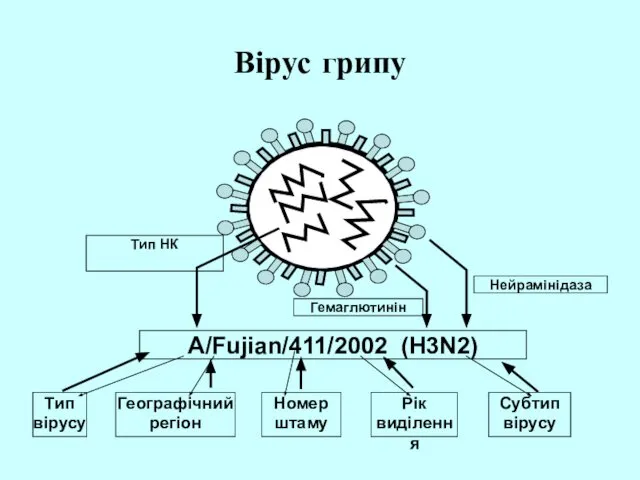
- 3. Вірус грипу
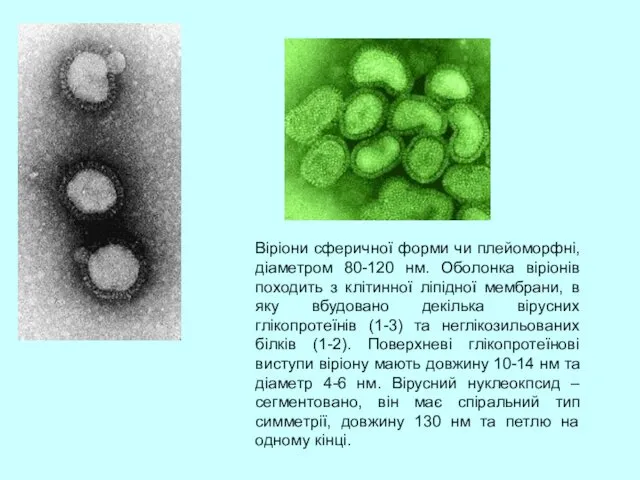
- 4. Віріони сферичної форми чи плейоморфні, діаметром 80-120 нм. Оболонка віріонів походить з клітинної ліпідної мембрани, в
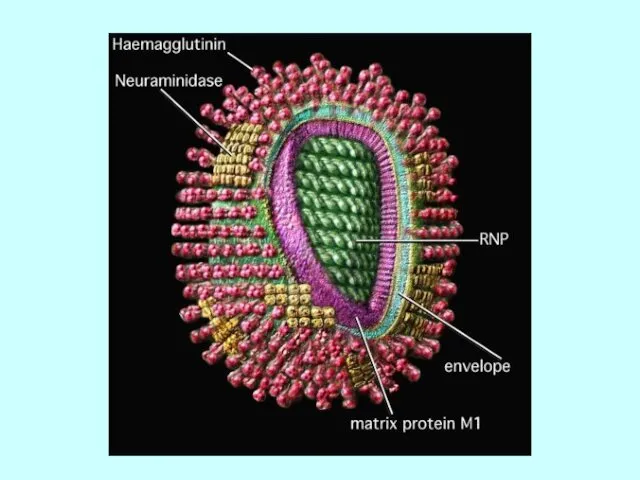
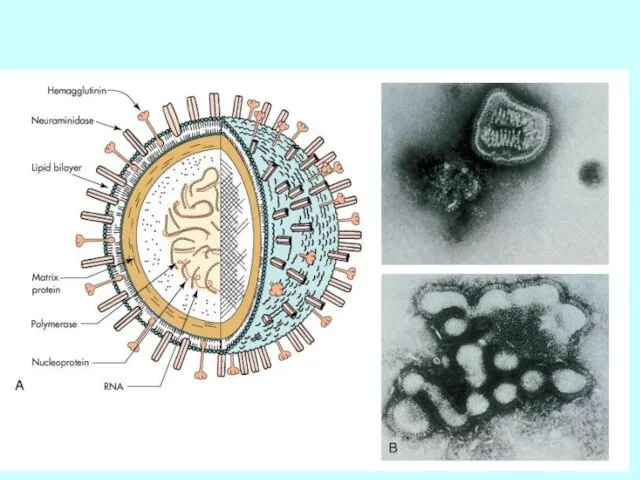
- 7. Антигенні властивості внутрішніх білків віріону (M1 и NP) визначають належність віруса грипу до роду А, В
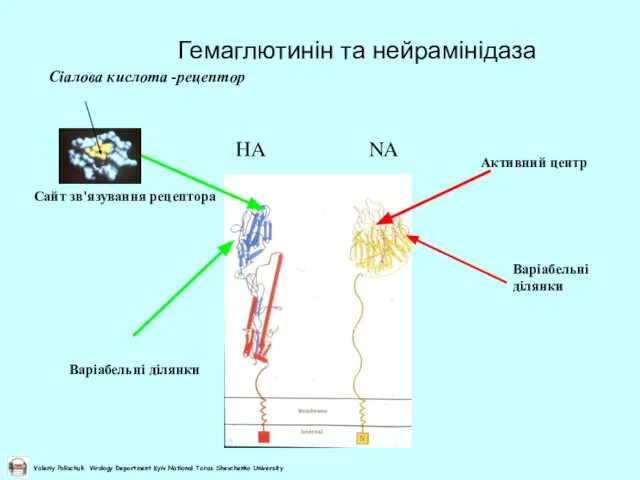
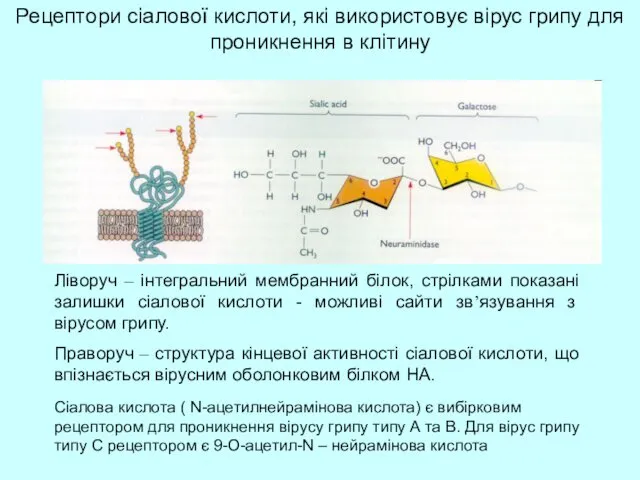
- 8. Гемаглютинін та нейрамінідаза Сайт зв'язування рецептора Активний центр Варіабельні ділянки Варіабельні ділянки HA NA Сіалова кислота
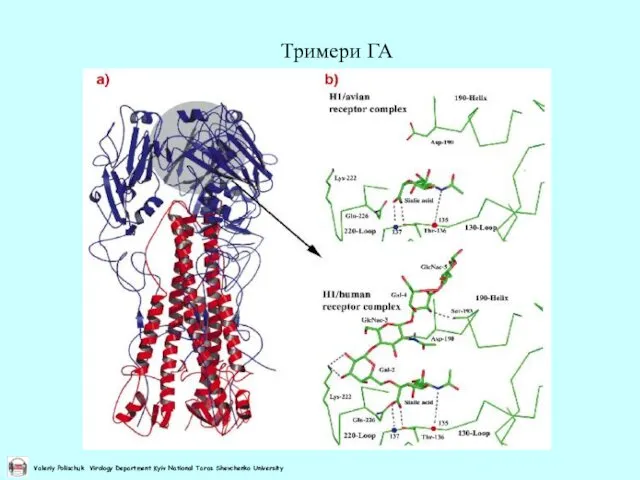
- 9. Тримери ГА
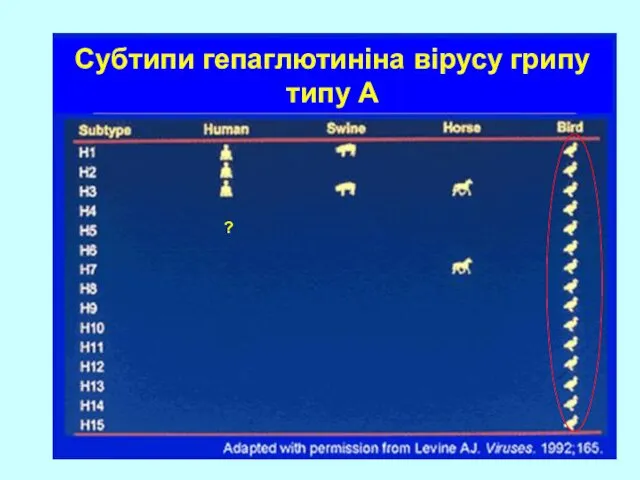
- 10. Субтипи гепаглютиніна вірусу грипу типу А ?
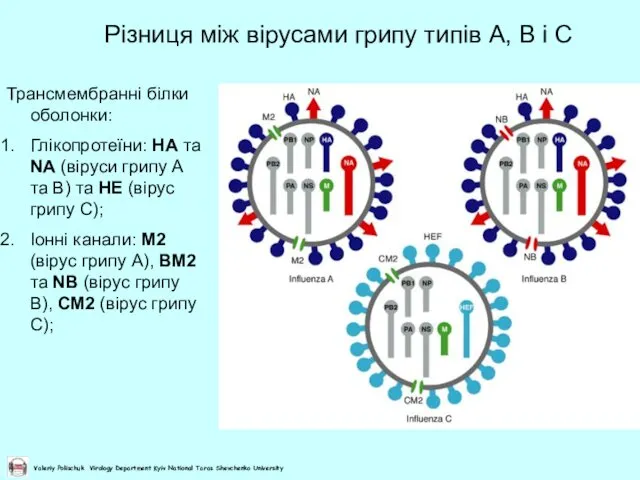
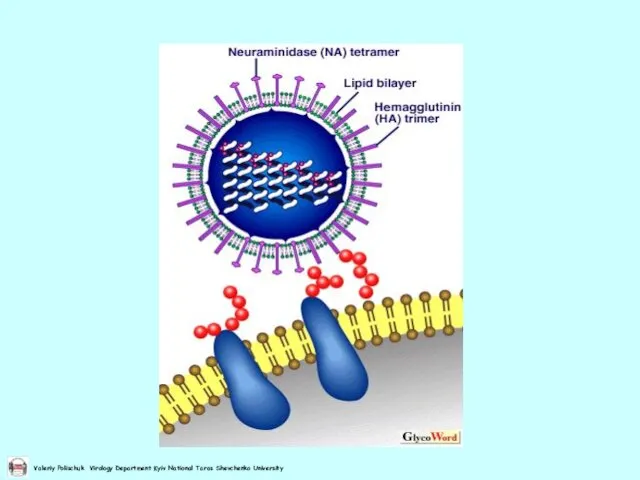
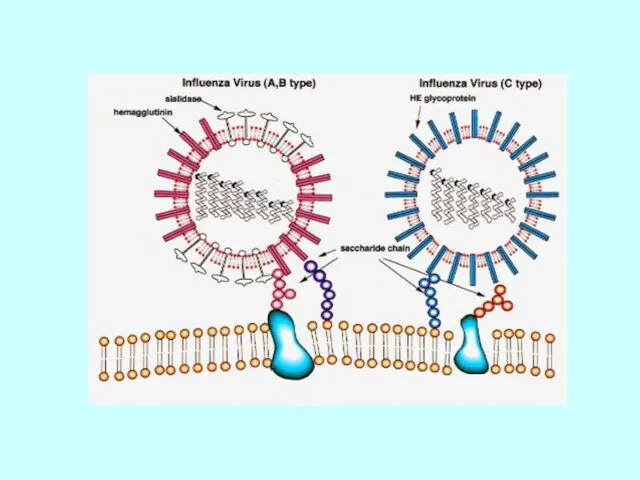
- 11. Різниця між вірусами грипу типів А, В і С Трансмембранні білки оболонки: Глікопротеїни: НА та NA
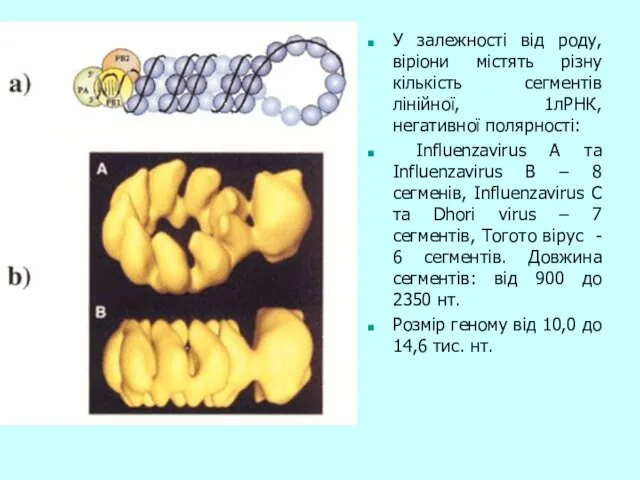
- 12. У залежності від роду, віріони містять різну кількість сегментів лінійної, 1лРНК, негативної полярності: Influenzavirus A та
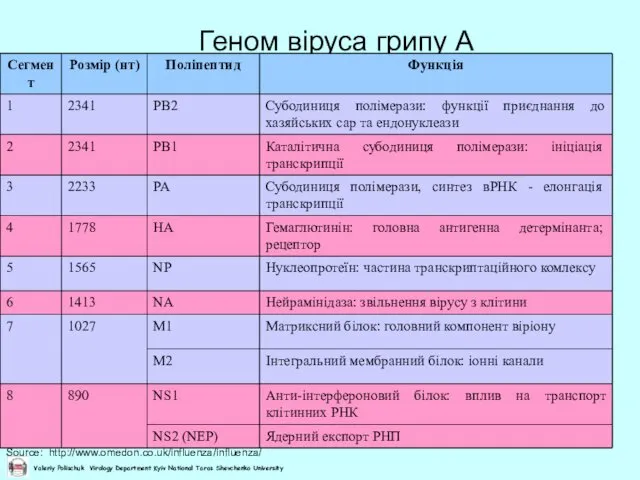
- 13. Геном віруса грипу А Source: http://www.omedon.co.uk/influenza/influenza/
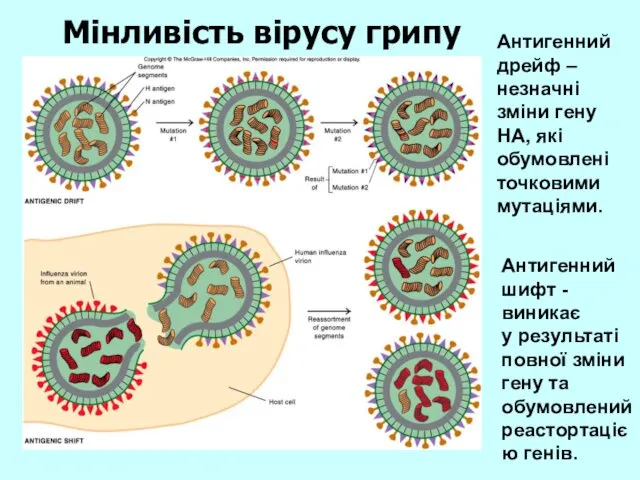
- 14. Антигенний дрейф – незначні зміни гену НА, які обумовлені точковими мутаціями. Антигенний шифт - виникає у
- 16. Фізико-хімічні та фізичні властивості Маса віріону 250 х 103 кДа. Плавуча густина у градієнті цукрози 1,19г/см3.
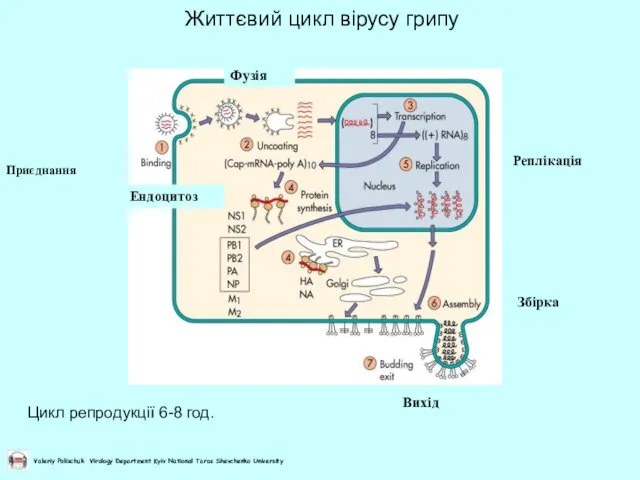
- 17. Життєвий цикл вірусу грипу Приєднання Вихід Збірка Реплікація Фузія Ендоцитоз Цикл репродукції 6-8 год.
- 18. Рецептори сіалової кислоти, які використовує вірус грипу для проникнення в клітину Ліворуч – інтегральний мембранний білок,
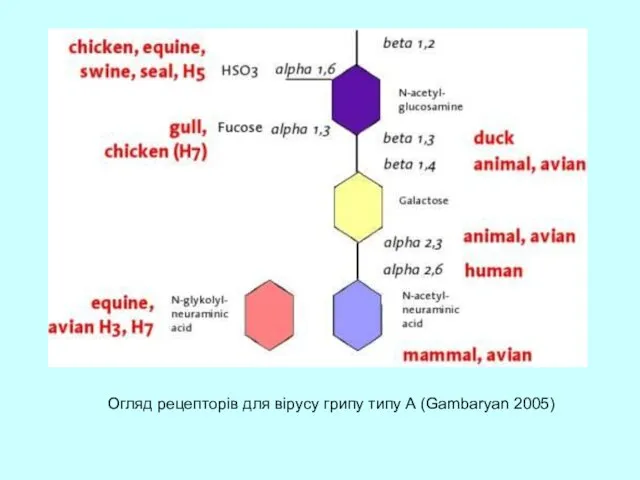
- 20. Огляд рецепторів для вірусу грипу типу А (Gambaryan 2005)
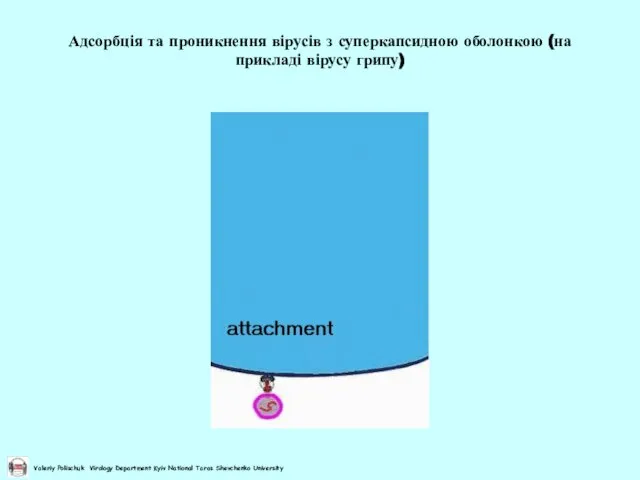
- 22. Адсорбція та проникнення вірусів з суперкапсидною оболонкою (на прикладі вірусу грипу)
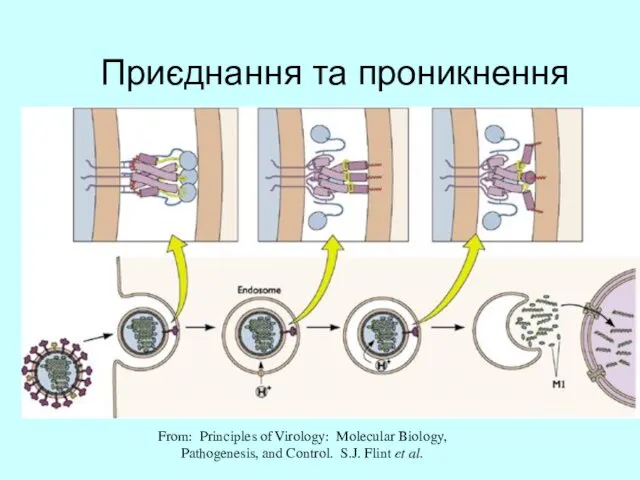
- 23. Приєднання та проникнення From: Principles of Virology: Molecular Biology, Pathogenesis, and Control. S.J. Flint et al.
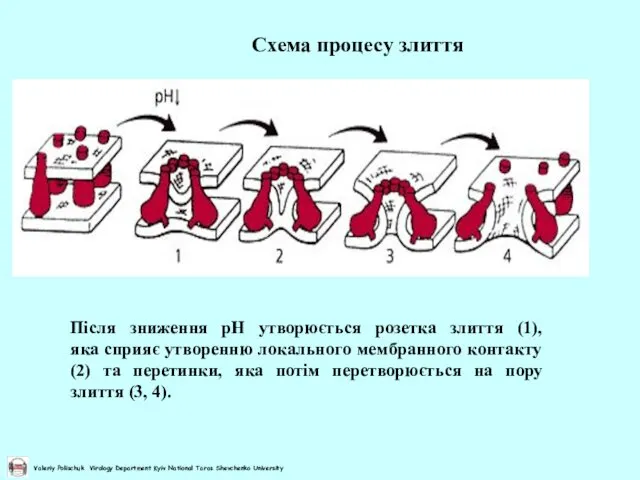
- 24. Після зниження рН утворюється розетка злиття (1), яка сприяє утворенню локального мембранного контакту (2) та перетинки,
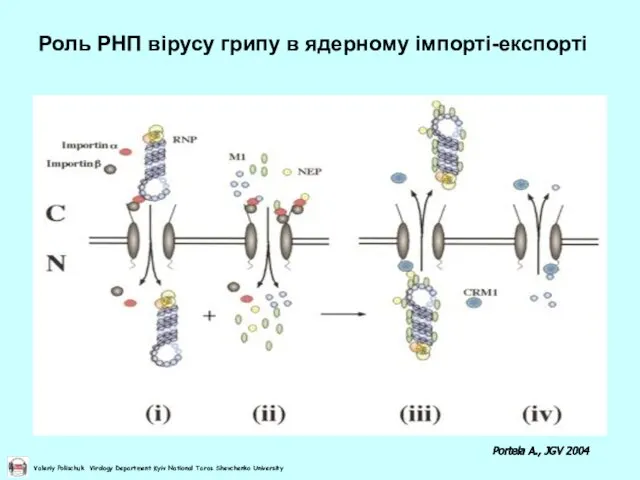
- 25. Роль РНП вірусу грипу в ядерному імпорті-експорті Portela A., JGV 2004
- 26. Реплікація вірусу грипу Унікальна стратегія “відбирання cap – структури у клітинних мРНК” Експресія генів та реплікація
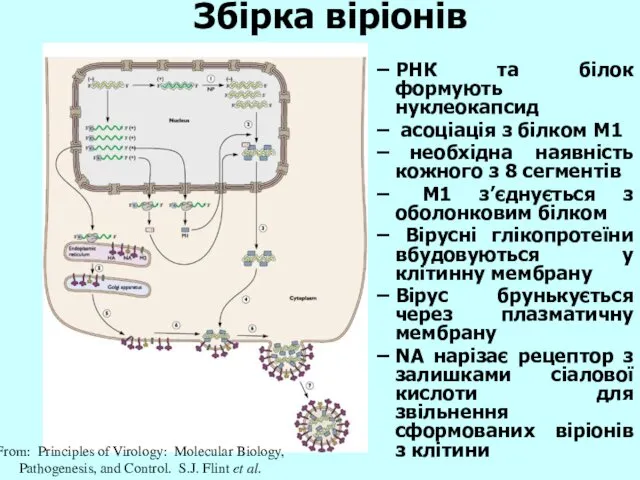
- 27. Збірка віріонів From: Principles of Virology: Molecular Biology, Pathogenesis, and Control. S.J. Flint et al. РНК
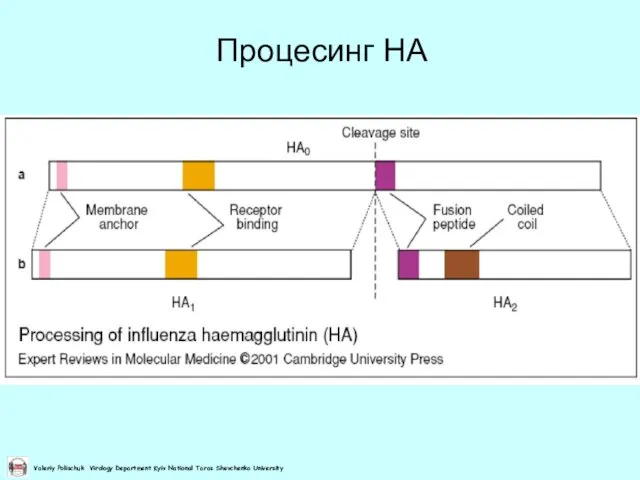
- 28. Процесинг НА
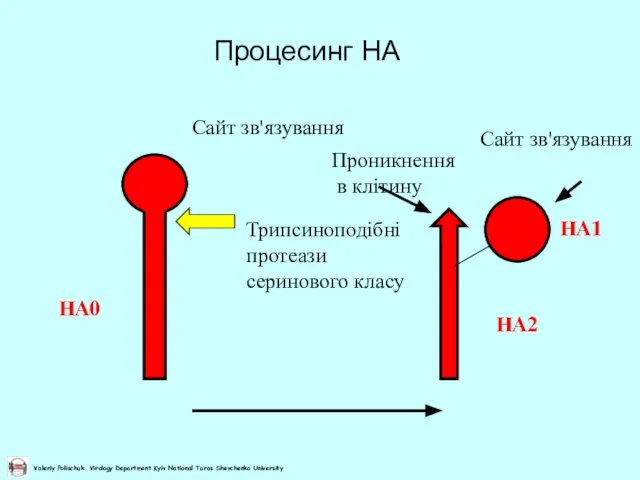
- 29. Процесинг НА Трипсиноподібні протеази серинового класу HA0 HA1 HA2 Сайт зв'язування Сайт зв'язування Проникнення в клітину
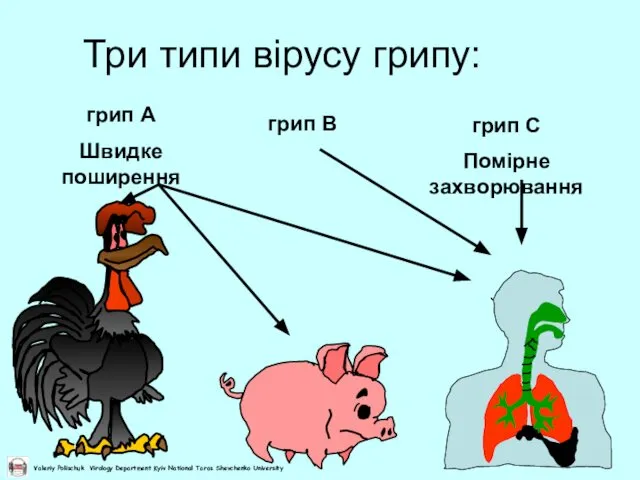
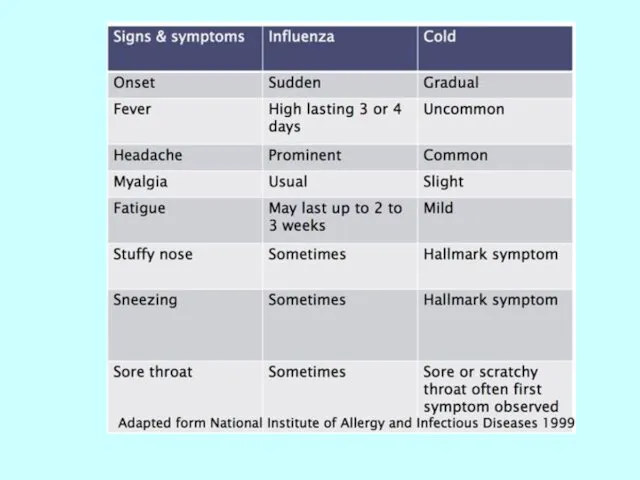
- 30. Три типи вірусу грипу: грип A Швидке поширення грип B грип C Помірне захворювання
- 31. Епідеміологія Сезонні епідемії щорічно в осінньо-зимовий період (в Північній півкулі), спорадична захворюваність виявляється і в інші
- 32. Актуальні штами вірусу грипу на сезон 2014-2015рр. для країн Північної півкулі (рекомендації ВООЗ) А(Н3N2), подібного до
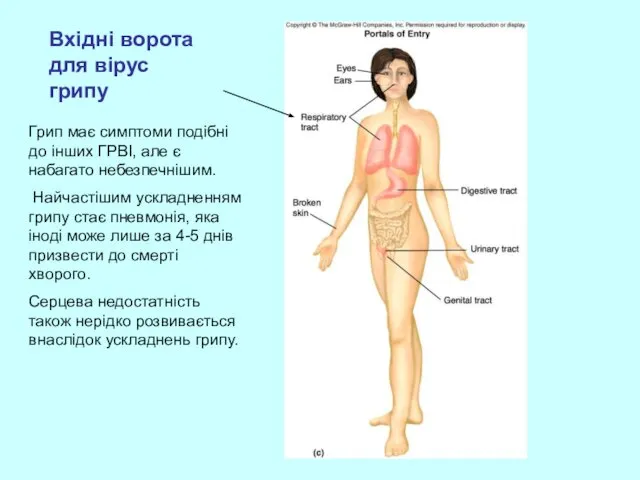
- 33. Вхідні ворота для вірус грипу Грип має симптоми подібні до інших ГРВІ, але є набагато небезпечнішим.
- 35. Патогенез Після проникнення у верхні дихальні шляхи, вірус грипу уражає слизову оболонку, розмножуючись в епітеліальних клітинах.
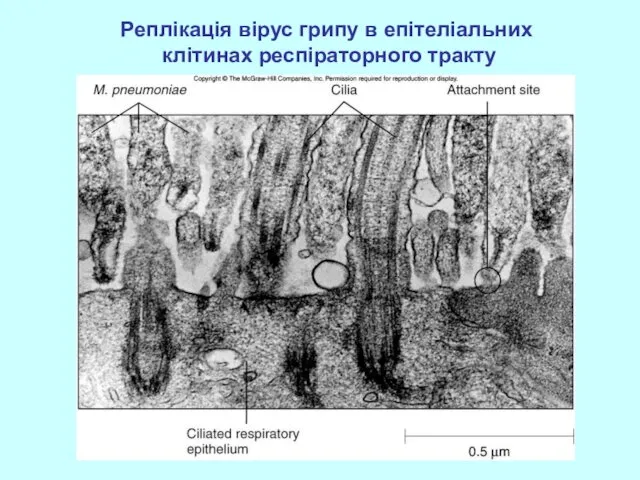
- 36. Реплікація вірус грипу в епітеліальних клітинах респіраторного тракту
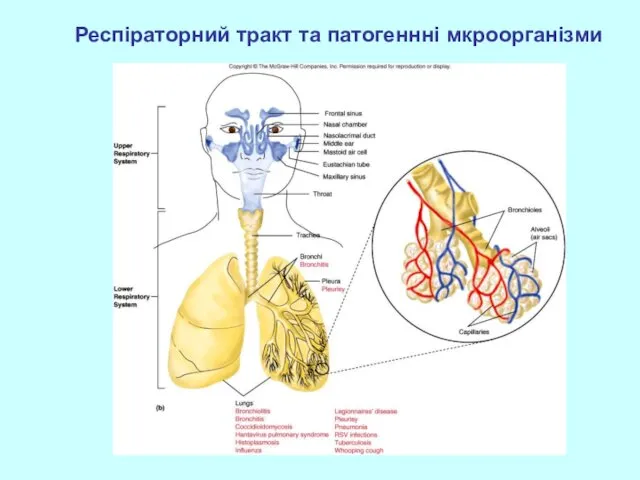
- 37. Респіраторний тракт та патогеннні мкроорганізми
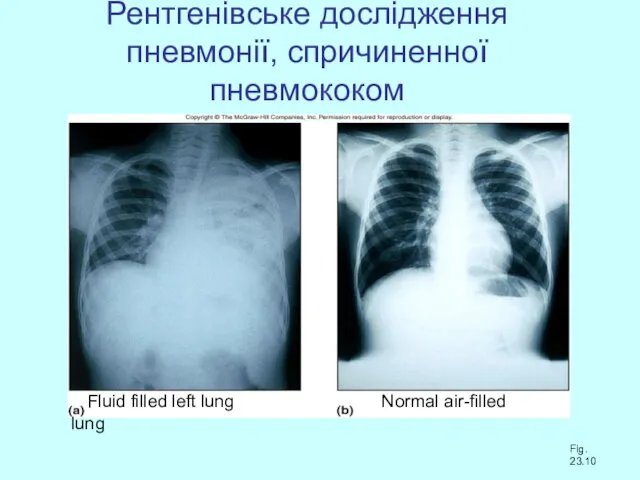
- 38. Рентгенівське дослідження пневмонії, спричиненної пневмококом Fluid filled left lung Normal air-filled lung Fig. 23.10
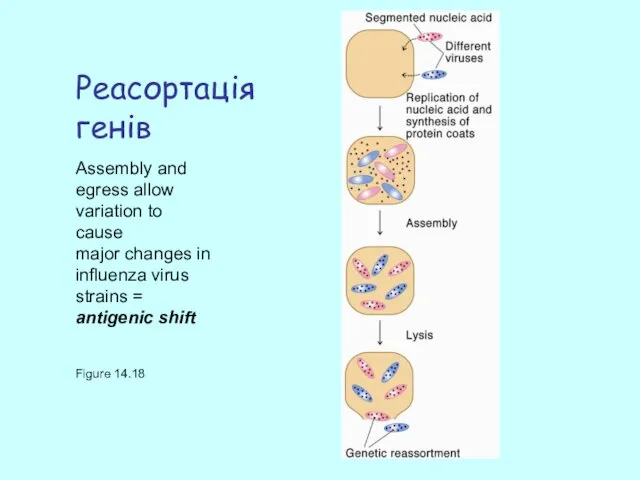
- 40. Реасортація генів Figure 14.18 Assembly and egress allow variation to cause major changes in influenza virus
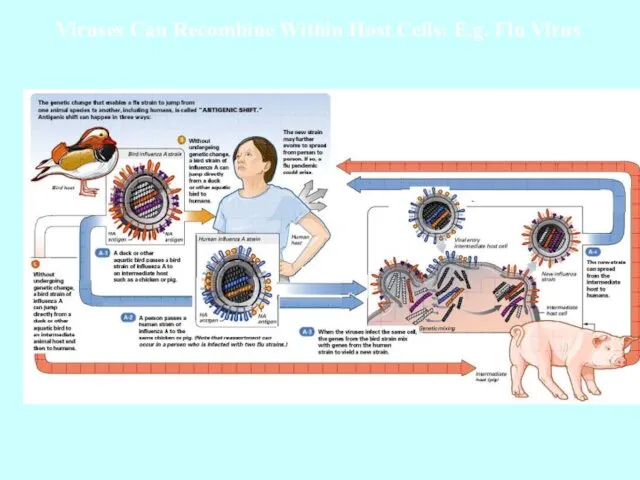
- 41. Viruses Can Recombine Within Host Cells: E.g. Flu Virus
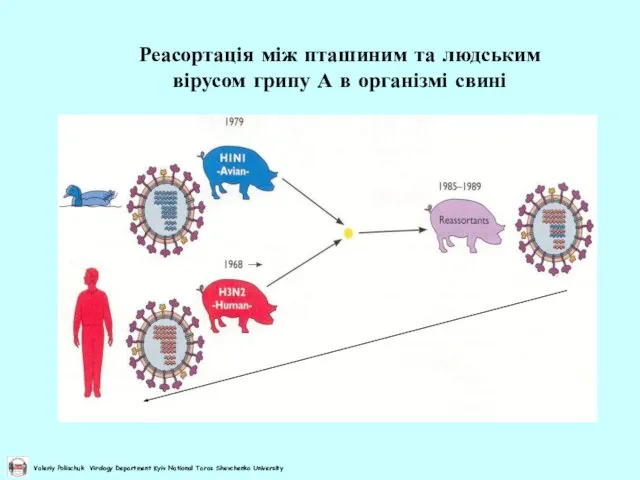
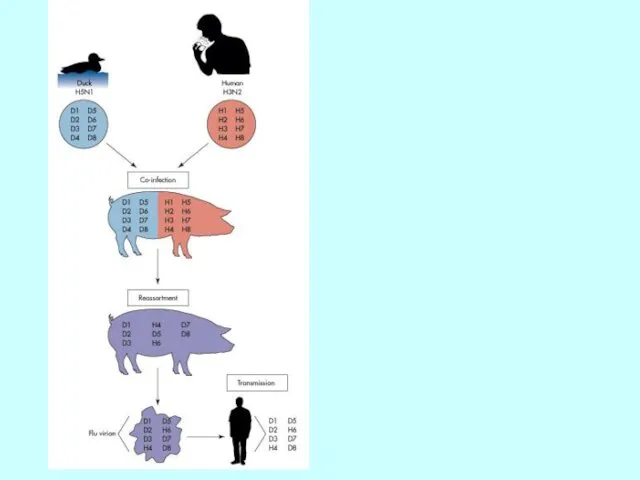
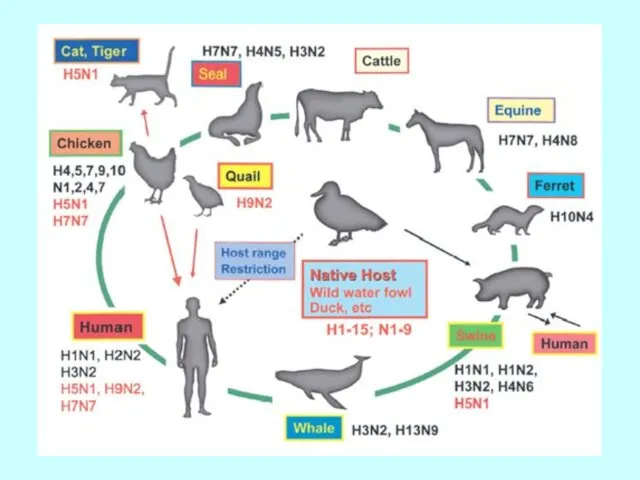
- 42. Реасортація між пташиним та людським вірусом грипу А в організмі свині
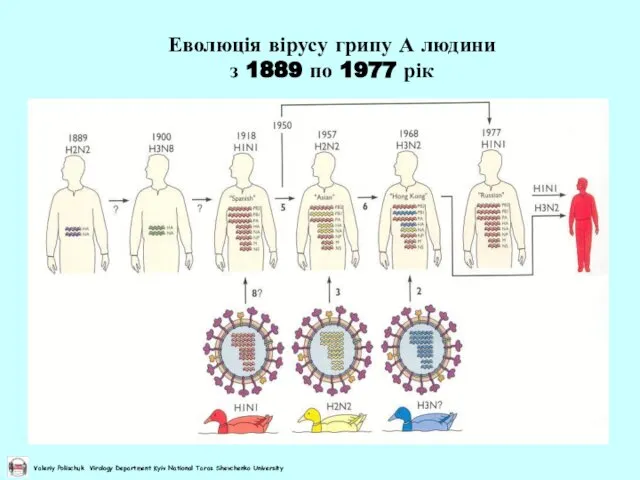
- 46. Еволюція вірусу грипу А людини з 1889 по 1977 рік
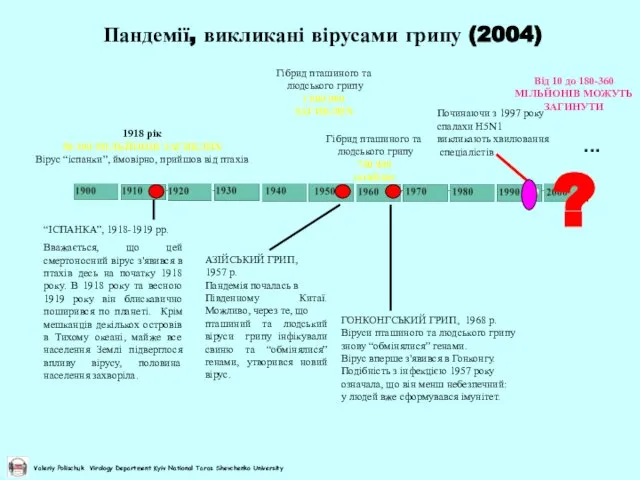
- 47. ... Від 10 до 180-360 МІЛЬЙОНІВ МОЖУТЬ ЗАГИНУТИ Пандемії, викликані вірусами грипу (2004) ?
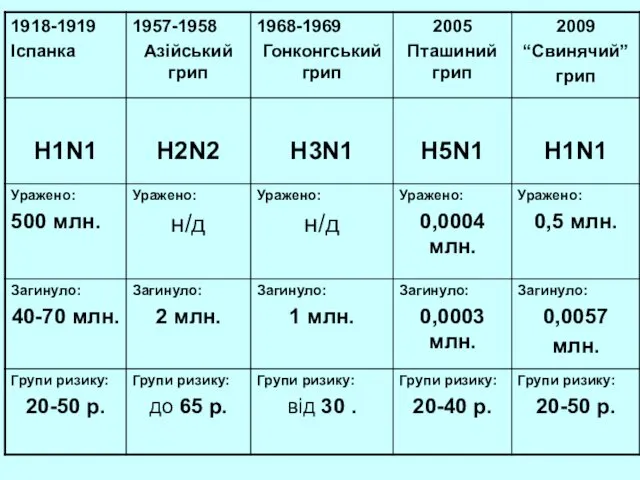
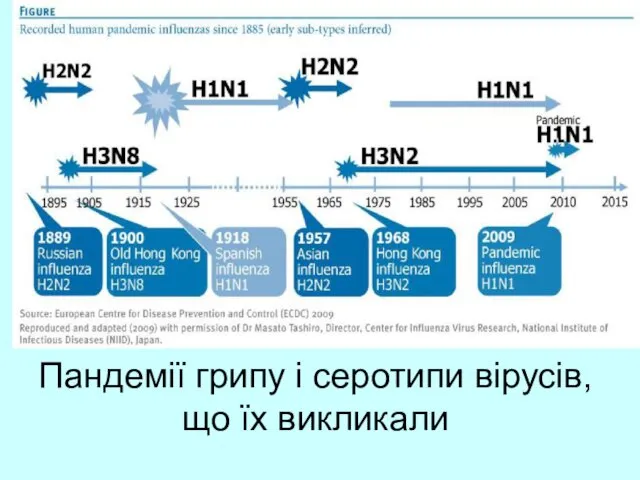
- 49. Пандемії грипу і серотипи вірусів, що їх викликали
- 52. Пандемія грипу, 1918 р. Public Health – Seattle & King County
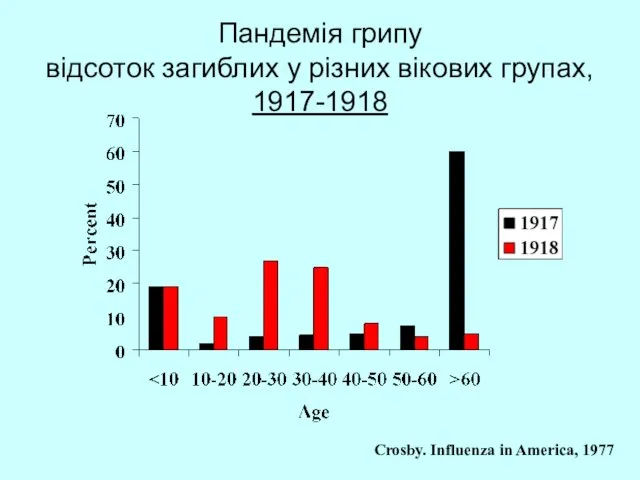
- 53. Пандемія грипу відсоток загиблих у різних вікових групах, 1917-1918 Crosby. Influenza in America, 1977
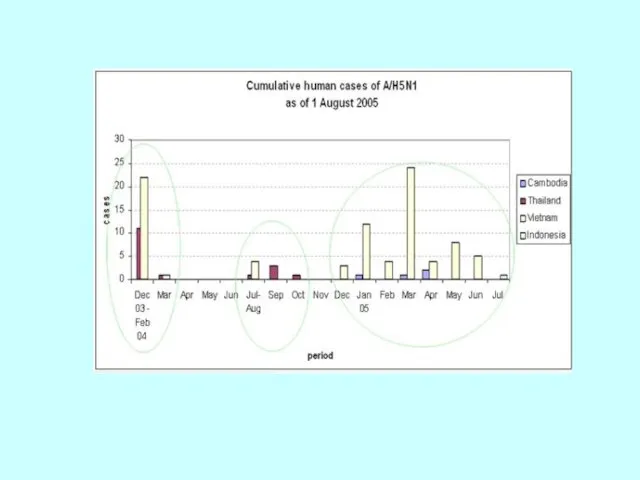
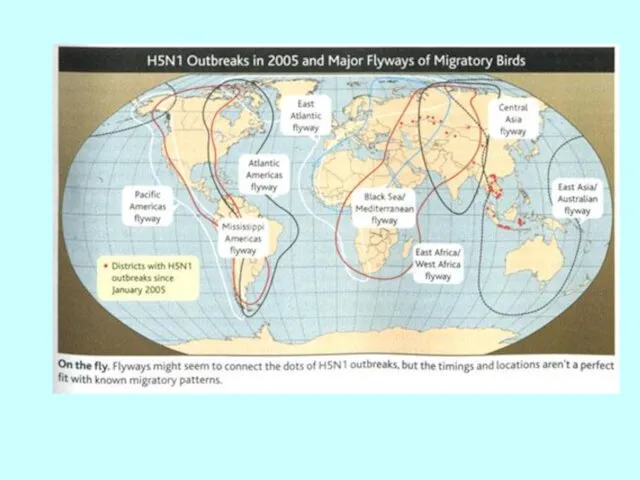
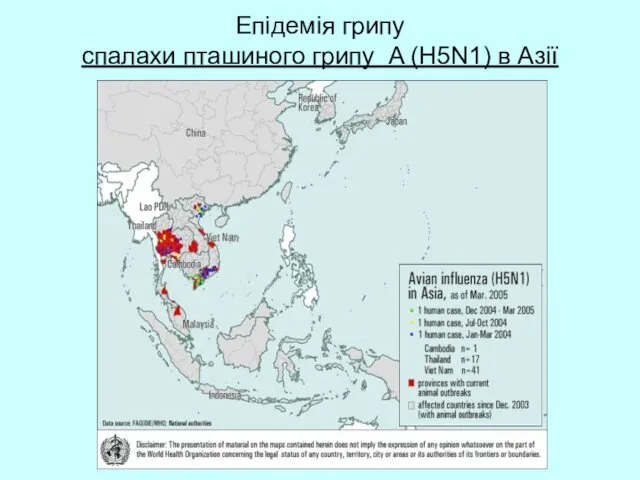
- 56. Епідемія грипу спалахи пташиного грипу A (H5N1) в Азії
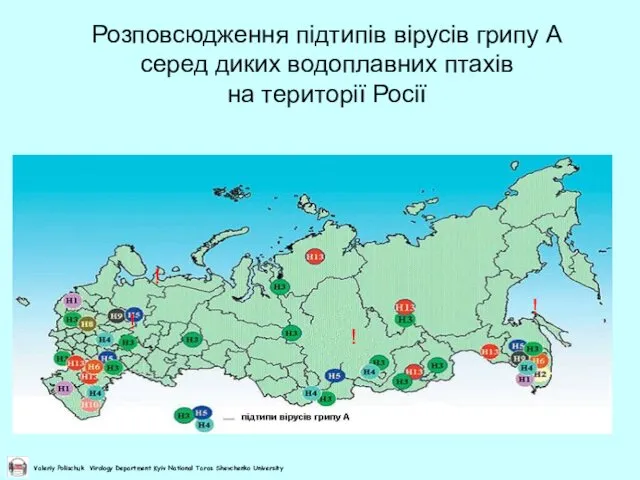
- 57. Розповсюдження підтипів вірусів грипу А серед диких водоплавних птахів на території Росії ! ! ! !
- 58. Грип птахів (класична чума птахів) H5N1, H9N2 – Азія Н7N7 – Європа Н5N1 – сіаліл(2-3) галактозна
- 59. Грип птахів Патогенність базується на генетичних характеристиках та/чи тяжкості захворювання у свійських птахів Низькопатогенний ГП (LPAI)
- 61. Клінічні симптоми Incubation period: 3-14 days Birds found dead Drop in egg production Neurological signs Depression,
- 62. Ознаки після загибелі Lesions may be absent with sudden death Severe congestion of the musculature Dehydration
- 63. Клінічно хвора на грип птиця
- 64. Історія 1878 р.- вперше ідентифіковано в Італії 1924-25 рр.- перші випадки у США Низькопатогенні варіанти вірусу
- 66. Первинний клінічний діагноз пташиного грипу базується на клінічній, епідеміологічній та лабораторній діагностиці за наступними критеріями: Висока
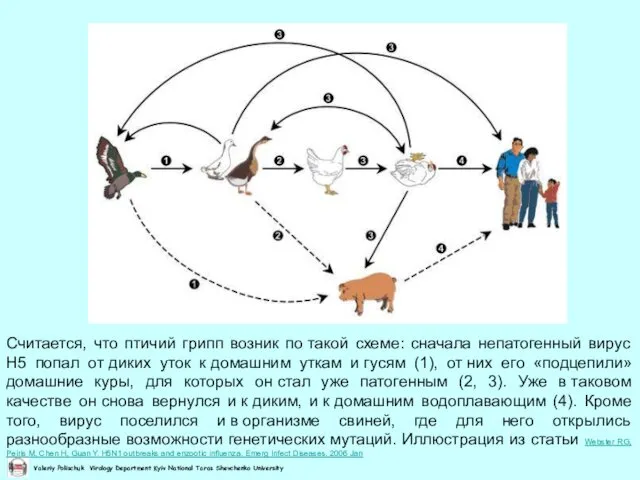
- 67. Считается, что птичий грипп возник по такой схеме: сначала непатогенный вирус H5 попал от диких уток
- 68. 02.12.2012 На Кубани - вспышка птичьего гриппа. От вируса уже погибли более двух тысяч пернатых. В
- 69. Грип свиней Грип свиней (англ. Swine influenza) - умовна назва захворювання людей та тварин, яке викликається
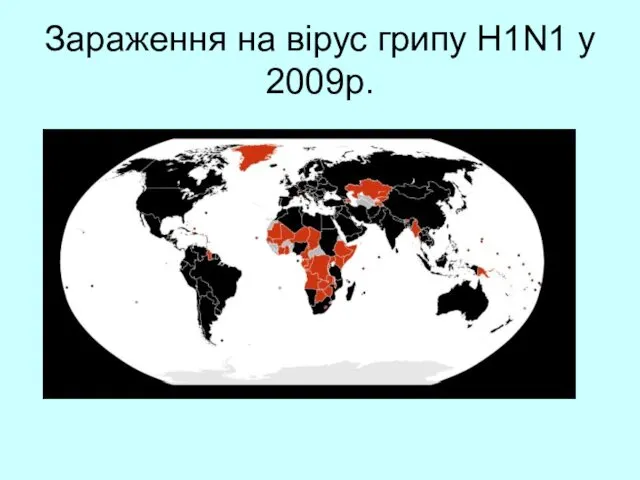
- 70. Зараження на вірус грипу H1N1 у 2009р.
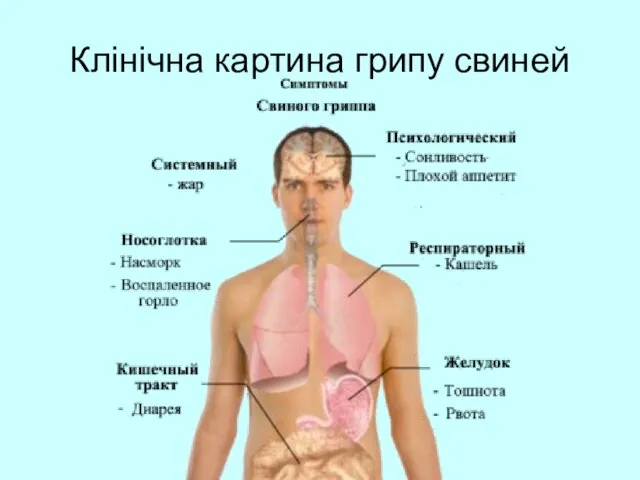
- 71. Клінічна картина грипу свиней
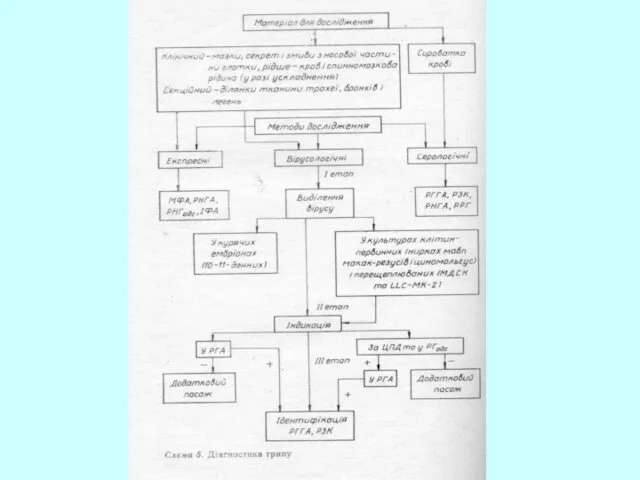
- 72. Діагностика грипу Експрес методи -імунохроматографічний тест (10-15 хв.), ПЛР, МФА,РНГА, ІФА, РНГадс. Вірусологічні методи - дозволяють
- 73. Профілактика та лікування 1. вакцини a. Інактивовані 1.повноцінні віріони 2.субодиничні b. Живі антенуйовані nasal spray available
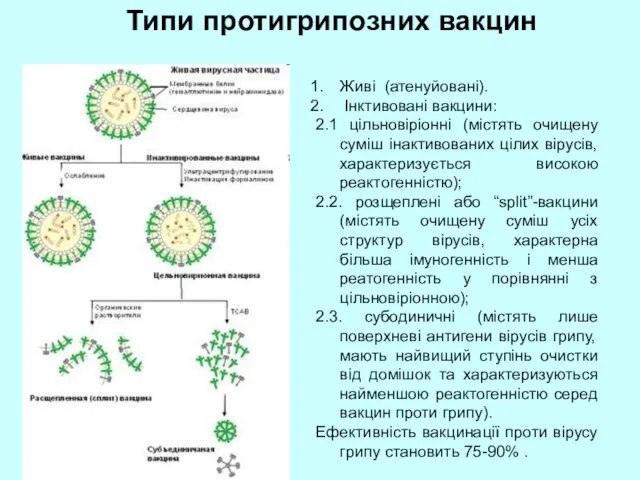
- 75. Типи протигрипозних вакцин Живі (атенуйовані). Інктивовані вакцини: 2.1 цільновіріонні (містять очищену суміш інактивованих цілих вірусів, характеризується
- 76. Вакцинація груп ризику : хворі на серцево-судинну патологію; хворі з патологіями дихальної, ендокринної систем; хворі з
- 77. Профілактика та лікування 1. вакцини a. Інактивовані 1.повноцінні віріони 2.субодиничні b. Живі антенуйовані nasal spray available
- 79. Скачать презентацию

























 Презентация по экологии Охрана и рациональное использование животного мира
Презентация по экологии Охрана и рациональное использование животного мира  РЕШЕНИЕ БИОЛОГИЧЕСКИХ ЗАДАЧ Электив по разделу «Организм»
РЕШЕНИЕ БИОЛОГИЧЕСКИХ ЗАДАЧ Электив по разделу «Организм» Размножение и развитие птиц. Строение куриного яйца
Размножение и развитие птиц. Строение куриного яйца ЗНАЧЕНИЕ ЭКОЛОГИЧЕСКИ ЧИСТЫХ ПРОДУКТОВ В ПИТАНИИ ЧЕЛОВЕКА Выполнила: ученица 9 класса «Г» МБОУ «СОШ№33 им.Н.А.Мордови
ЗНАЧЕНИЕ ЭКОЛОГИЧЕСКИ ЧИСТЫХ ПРОДУКТОВ В ПИТАНИИ ЧЕЛОВЕКА Выполнила: ученица 9 класса «Г» МБОУ «СОШ№33 им.Н.А.Мордови Пищевые ресурсы
Пищевые ресурсы Жгутиковые. Простейшие организмы
Жгутиковые. Простейшие организмы Семена Выполнила ученица 3 «А» класса МБОУ гимназии №26 Кипчакбаева Динара
Семена Выполнила ученица 3 «А» класса МБОУ гимназии №26 Кипчакбаева Динара  Виділення, його значення для організму. Форми виділення у тварин. Органи виділення тварин
Виділення, його значення для організму. Форми виділення у тварин. Органи виділення тварин Витамины. Классификация. Группы витаминов
Витамины. Классификация. Группы витаминов Презентація на тему: «Тютюн» підготувала учениця 11 класу СЗШ № 9
Презентація на тему: «Тютюн» підготувала учениця 11 класу СЗШ № 9  Презентация Биология наука о живом мире
Презентация Биология наука о живом мире Многообразие кишечнополостных
Многообразие кишечнополостных  Перелетные птицы
Перелетные птицы Снегири (лат. Pyrrhula) Канашевич Марии 5 «Д» класс
Снегири (лат. Pyrrhula) Канашевич Марии 5 «Д» класс  Кто такие насекомые
Кто такие насекомые Грибы
Грибы Основной механизм накопления водорода в клетке
Основной механизм накопления водорода в клетке Условия необходимые для развития растений. Урок 18
Условия необходимые для развития растений. Урок 18 Презентация на тему "Кровеносная и дыхательная система" - скачать презентации по Биологии
Презентация на тему "Кровеносная и дыхательная система" - скачать презентации по Биологии Органы и системы органов Автор: учитель биологии ГБОУ ЦО №1456 Водопьянова Марина Александровна
Органы и системы органов Автор: учитель биологии ГБОУ ЦО №1456 Водопьянова Марина Александровна Thoroughbred horse
Thoroughbred horse Обитатели водоёмов
Обитатели водоёмов Многообразие, значение и охрана земноводных
Многообразие, значение и охрана земноводных Органический мир океана
Органический мир океана Схема вегетативной рефлекторной дуги
Схема вегетативной рефлекторной дуги Способы размножения животных. Оплодотворение
Способы размножения животных. Оплодотворение РЫБЫ ПОПОВА В.В. УЧИТЕЛЬ НАЧАЛЬНЫХ КЛАССОВ МОУ СОШ № 29
РЫБЫ ПОПОВА В.В. УЧИТЕЛЬ НАЧАЛЬНЫХ КЛАССОВ МОУ СОШ № 29 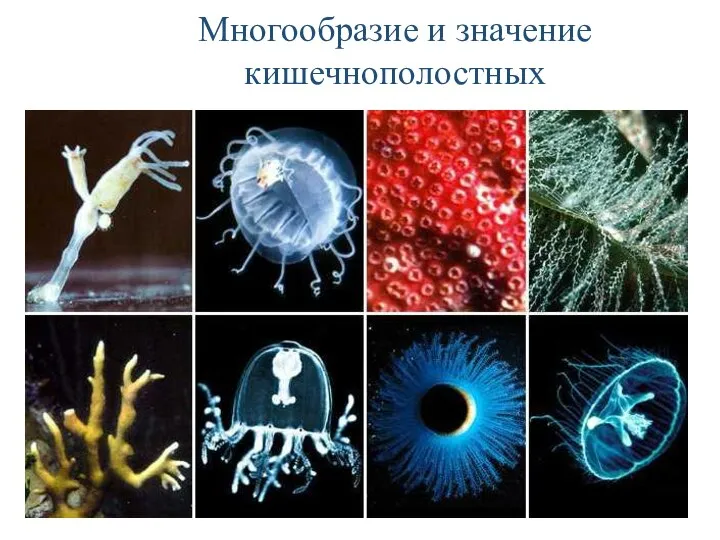 Многообразие кишечнополостных
Многообразие кишечнополостных