Содержание
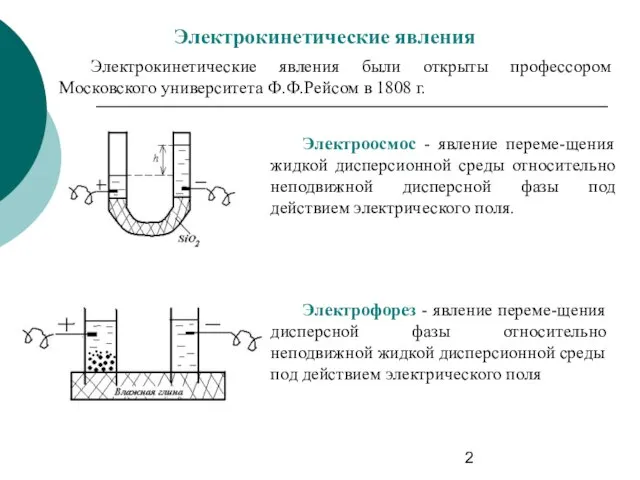
- 2. Электрокинетические явления Электрокинетические явления были открыты профессором Московского университета Ф.Ф.Рейсом в 1808 г. Электроосмос - явление
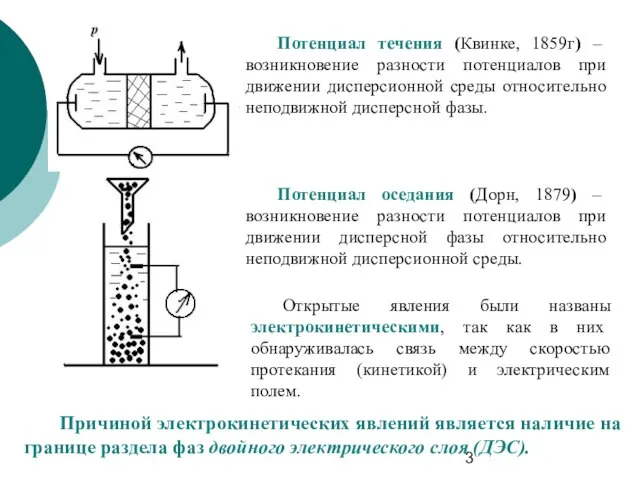
- 3. Потенциал течения (Квинке, 1859г) – возникновение разности потенциалов при движении дисперсионной среды относительно неподвижной дисперсной фазы.
- 4. Причины возникновения ДЭС I. Неравенство электрохимических потенциалов ионов в кристаллической решетке тв. тела и ионов в
- 5. В. Механизм поверхностной диссоциации Если , то иодид – ионы с поверхности будут переходить в раствор
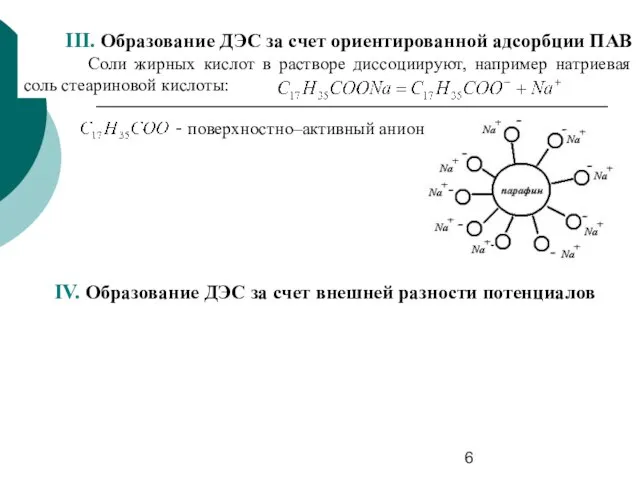
- 6. III. Образование ДЭС за счет ориентированной адсорбции ПАВ Соли жирных кислот в растворе диссоциируют, например натриевая
- 7. Строение коллоидных мицелл Мицелла (Дюкло 1908г.) – частица дисперсной фазы вместе с ДЭС. Внутреннюю часть мицеллы
- 8. Агрегат вместе с ПОИ составляет ядро мицеллы. Заряженное ядро мицеллы, притягивает ПИ из раствора. Часть ПИ
- 9. Пример 1: AgNO3 – электролит-стабилизатор, ионы которого образуют ДЭС: По правилу Фаянса - Пескова, ионы Ag+
- 10. Теории строения ДЭС Экспериментальные факты, послужившие основой для создания теорий строения ДЭС Существует электрический (термодинамический) потенциал
- 11. 1. ДЭС плоский (δ 2. ДЭС состоит из относительно прочно связанных с поверхностью дисперсной фазы ПОИ
- 12. Теория строения ДЭС Гельмгольца – Перрена (1879г) ДЭС – плоский конденсатор: внутренняя обкладка состоит из ПОИ,
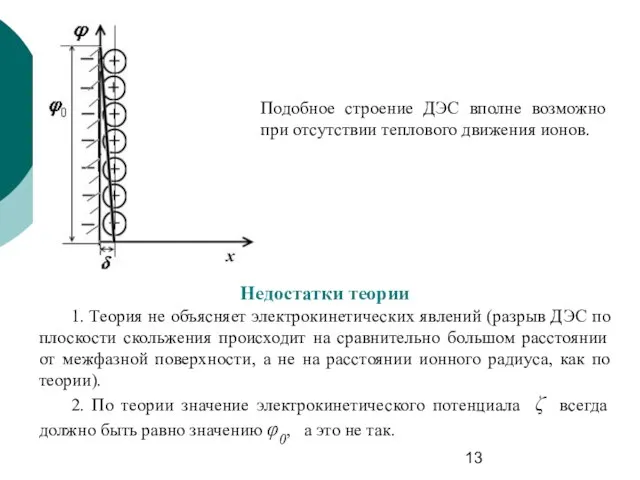
- 13. Подобное строение ДЭС вполне возможно при отсутствии теплового движения ионов. Недостатки теории 1. Теория не объясняет
- 14. Теория строения ДЭС Гуи – Чепмена (1910-1913 гг.) Основные положения 1. ПИ вблизи заряженной стенки находятся
- 15. 4. По мере удаления ПИ от поверхности, кулоновские силы ослабевают, а силы теплового движения возрастают. Это
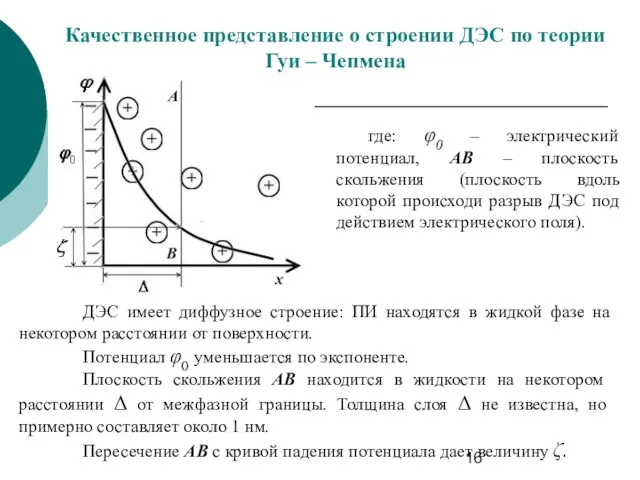
- 16. Качественное представление о строении ДЭС по теории Гуи – Чепмена где: φ0 – электрический потенциал, АВ
- 17. Количественная теория Гуи – Чэпмена Цель теории: найти закон изменения φ в ДЭС с расстоянием: φ=f(х),
- 18. Уравнение (2) дает возможность оценить значение δ при заданной концентрации электролита, учитывая, что z+ = z–,
- 19. 2. При больших значениях φ0 (φ0 > 100 мВ) электрический потенциал поверхности φ0 не влияет на
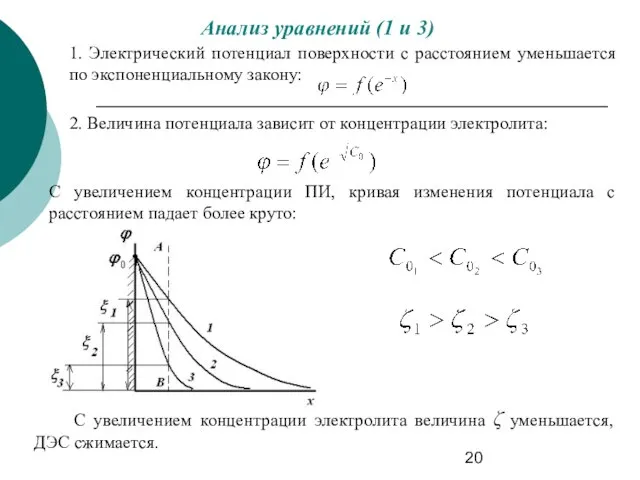
- 20. Анализ уравнений (1 и 3) 1. Электрический потенциал поверхности с расстоянием уменьшается по экспоненциальному закону: 2.
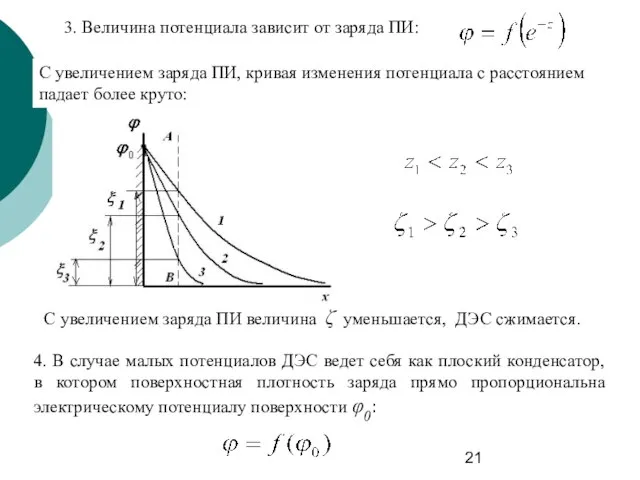
- 21. 3. Величина потенциала зависит от заряда ПИ: С увеличением заряда ПИ, кривая изменения потенциала с расстоянием
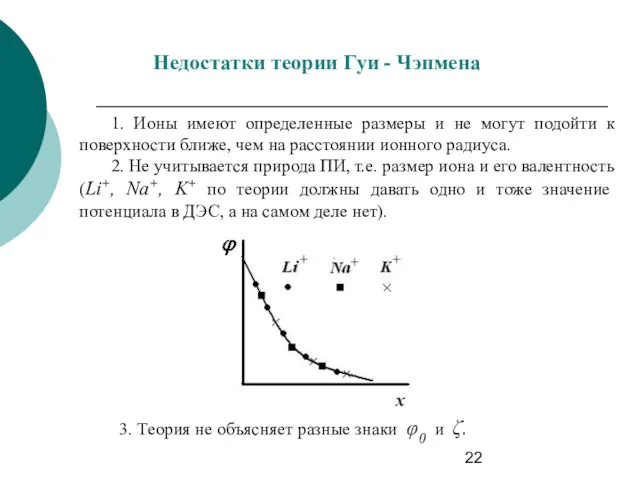
- 22. Недостатки теории Гуи - Чэпмена 1. Ионы имеют определенные размеры и не могут подойти к поверхности
- 23. В 1924 г. Штерн предложил схему строения ДЭС, в которой объединил теории Гельмгольца – Перрена и
- 24. Основные положения теории Штерна 1. Ионы имеют определенные размеры и не могут подходить к заряженной поверхности
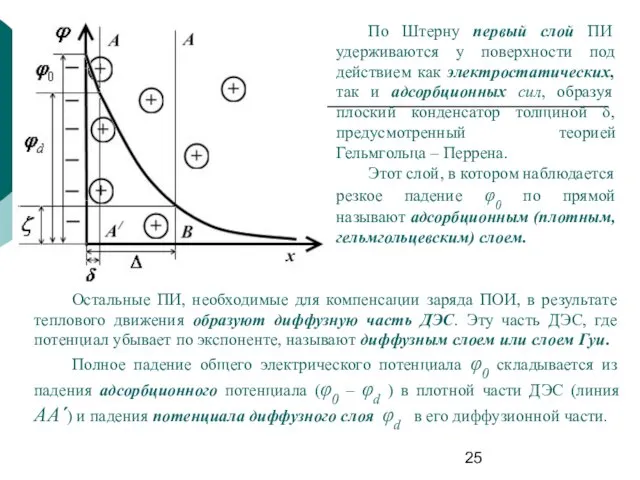
- 25. По Штерну первый слой ПИ удерживаются у поверхности под действием как электростатических, так и адсорбционных сил,
- 26. Влияние электролитов на ДЭС Влияние индифферентных электролитов Индифферентный электролит – электролит, ионы которого не могут достраивать
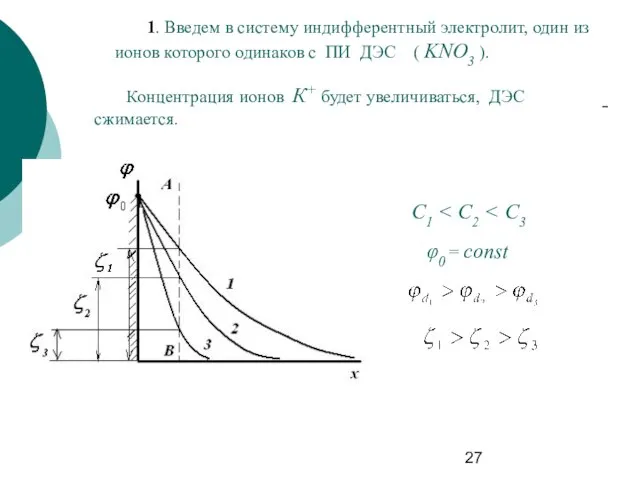
- 27. 1. Введем в систему индифферентный электролит, один из ионов которого одинаков с ПИ ДЭС ( KNO3
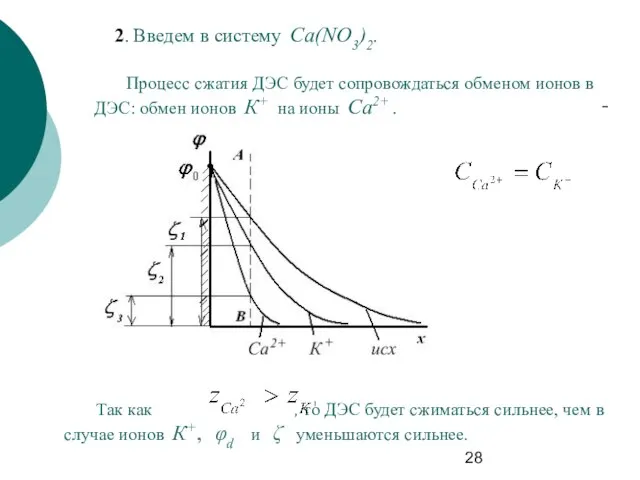
- 28. 2. Введем в систему Ca(NO3)2. Процесс сжатия ДЭС будет сопровождаться обменом ионов в ДЭС: обмен ионов
- 29. 3. Введем в систему Al(NO3)3. Перезарядка по Штерну Ионы Al3+, благодаря высокой адсорбционной способности, могут подходить
- 30. Многовалентные ионы (Al3+, Th4+) часто применяют для перезарядки дисперсных частиц, имеющих отрицательный дзета- потенциал. Также перезарядку
- 31. Влияние неиндифферентных электролитов Неидифферентный электролит – электролит, ионы которого способны достраивать кристаллическую решетку дисперсной фазы, изменяя
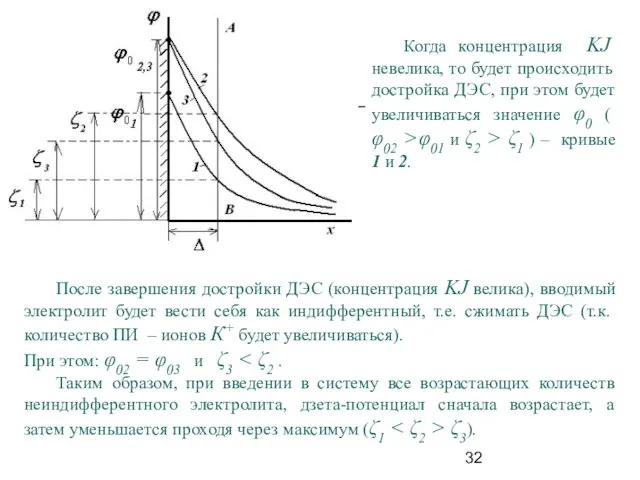
- 32. Когда концентрация KJ невелика, то будет происходить достройка ДЭС, при этом будет увеличиваться значение φ0 (
- 33. 2. Введение неиндифферентного электролита, содержащего ион, знак заряда которого противоположен по знаку ПОИ коллоидной частицы. В
- 34. При дальнейшем увеличении концентрации AgNO3 будет происходить полная перестройка мицеллы: ПОИ – Ag+, ПИ – NO3-
- 35. Измерение электрокинетического потенциала из явлений электрофореза и электроосмоса Электрокинетический потенциал – потенциал, возникающий на границе скольжения
- 36. Электрокинетический потенциал связан с электрофоретической подвижностью, уравнением Гельмгольца – Смолуховского: где: h – смещение границы золь
- 37. Электроосмос Для расчета дзета-потенциала при электроосмосе заменяют линейную скорость (U) движения частицы на объемную (v): где:
- 39. Скачать презентацию
























 Ход лучей в линзах и сферических зеркалах
Ход лучей в линзах и сферических зеркалах Коробка передач. Основное устройство и принцип работы
Коробка передач. Основное устройство и принцип работы Гипотеза де Бройля. Комптоновская длина волны и длина волны де Бройля
Гипотеза де Бройля. Комптоновская длина волны и длина волны де Бройля Динамика. Инерциальные системы отсчета. Первый закон Ньютона
Динамика. Инерциальные системы отсчета. Первый закон Ньютона Пара сил. Основная теорема статики
Пара сил. Основная теорема статики Енергозбереження в побуті
Енергозбереження в побуті Радиоактивные излучения. Радиоактивность. Закон радиоактивного распада
Радиоактивные излучения. Радиоактивность. Закон радиоактивного распада Количество теплоты. Удельная теплоёмкость
Количество теплоты. Удельная теплоёмкость Виды самоходной техники в АПК
Виды самоходной техники в АПК Термический каротаж. Внешние источники тепла. Излучение Солнца, звезд и галактик
Термический каротаж. Внешние источники тепла. Излучение Солнца, звезд и галактик Источники звука. Характеристики звука
Источники звука. Характеристики звука Момент силы относительно центра (точки)
Момент силы относительно центра (точки) Термометры и их виды
Термометры и их виды Выполнили:11 «А» Шафоростова Ольга Пирожкова Вероника. Руководитель: Бредгауэр Вера Александровна
Выполнили:11 «А» Шафоростова Ольга Пирожкова Вероника. Руководитель: Бредгауэр Вера Александровна Разработка ЖРД третьей ступени с дожиганием генераторного газа
Разработка ЖРД третьей ступени с дожиганием генераторного газа Теорема о циркуляции вектора магнитной индукции. (Лекция 14)
Теорема о циркуляции вектора магнитной индукции. (Лекция 14) Термодинаміка. Внутрішня енергія
Термодинаміка. Внутрішня енергія Электроемкость
Электроемкость МОУ «СОШ № 30 г.Белово»
МОУ «СОШ № 30 г.Белово» Механика материалов
Механика материалов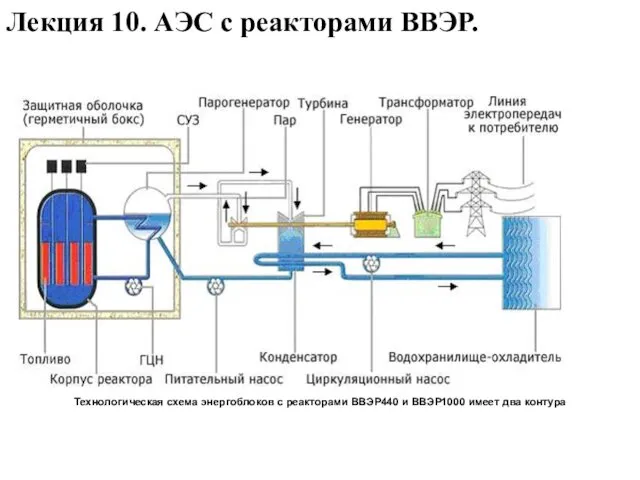 АЭС с реакторами ВВЭР
АЭС с реакторами ВВЭР Автоматизация процесса регулировки манометров
Автоматизация процесса регулировки манометров Презентация по физике "Свойства электромагнитных волн" - скачать бесплатно
Презентация по физике "Свойства электромагнитных волн" - скачать бесплатно Номинация «Научные исследования в области энергосберегающих технологий» ИССЛЕДОВАНИЕ ЗАВИСИМОСТИ ЭФФЕКТИВНОСТИ РАБОТЫ ГОРЕ
Номинация «Научные исследования в области энергосберегающих технологий» ИССЛЕДОВАНИЕ ЗАВИСИМОСТИ ЭФФЕКТИВНОСТИ РАБОТЫ ГОРЕ Воздействие электрического тока на человека
Воздействие электрического тока на человека Основы биореологии и гемодинамики. (Лекция 4)
Основы биореологии и гемодинамики. (Лекция 4) Свойство и принцип действия генератора переменного тока
Свойство и принцип действия генератора переменного тока Решение задач. Силы тяжести, упругости
Решение задач. Силы тяжести, упругости