Содержание
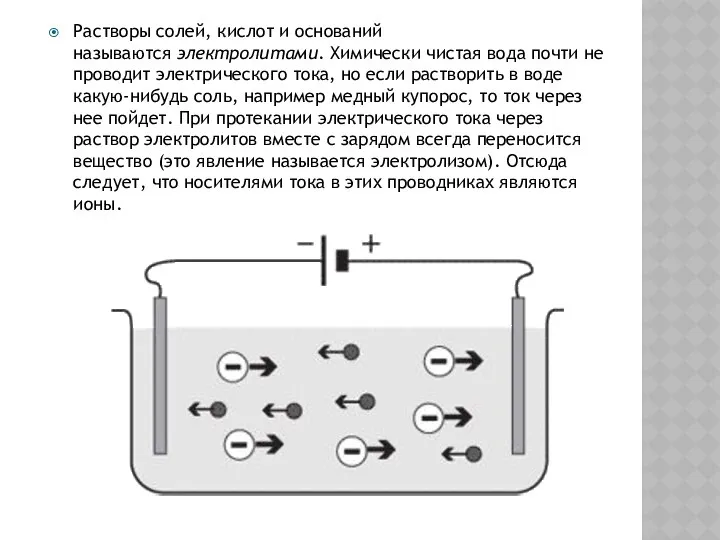
- 2. Растворы солей, кислот и оснований называются электролитами. Химически чистая вода почти не проводит электрического тока, но
- 3. Электрической диссоциацией называется расщепление в воде солей, кислот и щелочей на положительные и отрицательные ионы. Растворы
- 4. Электронная теория позволяет рассчитать массу вещества, выделившегося на электродах при электролизе. Она равна массе одного иона
- 5. Величины NA и е являются универсальными постоянными, а М и z постоянны для данного вещества. Поэтому
- 7. Скачать презентацию
Растворы солей, кислот и оснований называются электролитами. Химически чистая вода почти не
Растворы солей, кислот и оснований называются электролитами. Химически чистая вода почти не
Электрической диссоциацией называется расщепление в воде солей, кислот и щелочей на положительные
Электрической диссоциацией называется расщепление в воде солей, кислот и щелочей на положительные
Электрический ток в растворах (или расплавах) электролитов представляет собой перемещение ионов обоих знаков в противоположных направлениях. Опыт показывает, что сила тока при постоянном сопротивлении электролитов линейно зависит от напряжения, т. е. для растворов электролитов справедлив закон Ома.
Электронная теория позволяет рассчитать массу вещества, выделившегося на электродах при электролизе.
Электронная теория позволяет рассчитать массу вещества, выделившегося на электродах при электролизе.
Величины NA и е являются универсальными постоянными, а М и z постоянны
Величины NA и е являются универсальными постоянными, а М и z постоянны
Поэтому выражение
- величина, постоянная для данного вещества.
Масса вещества, выделившегося на электроде, пропорциональна заряду, прошедшему через раствор (или пропорциональна силе тока и времени). Эта зависимость носит название закона Фарадея.
Коэффициент k называется электрохимическим эквивалентом данного вещества. Он выражается в килограммах на кулон (кг/Кл).
Закон Фарадея позволяет определить заряд одновалентного иона:



 Физика в детских игрушках Автор работы: Казаченкова Анна ученица 8 класса МОУ «Хохловская СОШ»
Физика в детских игрушках Автор работы: Казаченкова Анна ученица 8 класса МОУ «Хохловская СОШ» Тепловой расчет полупроводников
Тепловой расчет полупроводников Прохождение излучения через границу раздела двух сред
Прохождение излучения через границу раздела двух сред Столкновения Абсолютно упругий удар
Столкновения Абсолютно упругий удар 8.5. ЦИКЛЫ ГАЗОТУРБИННЫХ УСТАНОВОК. Газотурбинные установки (ГТУ) имеют многие важные преимущества по сравнению с поршневыми д
8.5. ЦИКЛЫ ГАЗОТУРБИННЫХ УСТАНОВОК. Газотурбинные установки (ГТУ) имеют многие важные преимущества по сравнению с поршневыми д Тюнинг и доработка рулевого управления
Тюнинг и доработка рулевого управления Общие сведения об элементах систем
Общие сведения об элементах систем Динамика материальной точки и поступательного движения твердого тела
Динамика материальной точки и поступательного движения твердого тела Поперечные и продольные волны
Поперечные и продольные волны Различные подходы в определении информации
Различные подходы в определении информации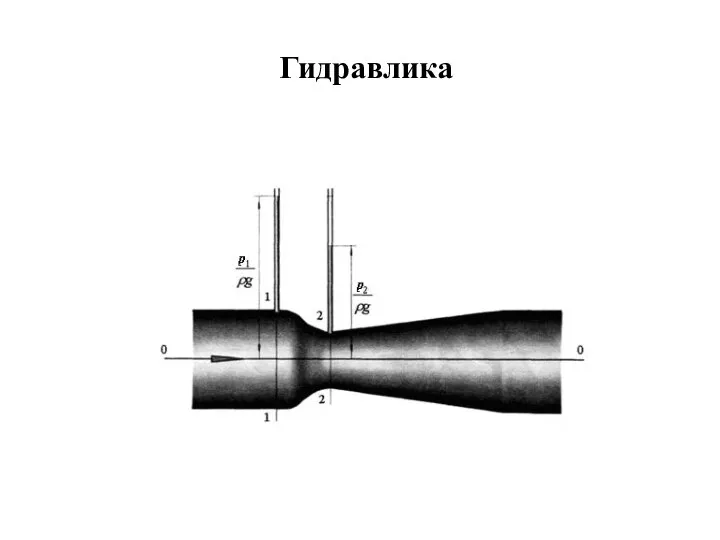 Гидравлика. Поверхностные силы. Насосы
Гидравлика. Поверхностные силы. Насосы Возникновение атомистической гипотезы строения вещества и ее экспериментальные доказательства. Идеальный газ
Возникновение атомистической гипотезы строения вещества и ее экспериментальные доказательства. Идеальный газ Проводниковые материалы
Проводниковые материалы Законы трения скольжения
Законы трения скольжения Пневматические приводы и средства автоматизации
Пневматические приводы и средства автоматизации Взаимные превращения жидкости, пара и твёрдого тела
Взаимные превращения жидкости, пара и твёрдого тела ИК и КР-спектроскопия
ИК и КР-спектроскопия Уравнение Шредингера
Уравнение Шредингера Действия электрического тока
Действия электрического тока Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №2. Научно-исследовательская работа по физике
Муниципальное общеобразовательное учреждение средняя общеобразовательная школа №2. Научно-исследовательская работа по физике  Магнитное поле и его графическое изображение. (Урок 39)
Магнитное поле и его графическое изображение. (Урок 39) Динамика материальной точки. (Лекция 1)
Динамика материальной точки. (Лекция 1)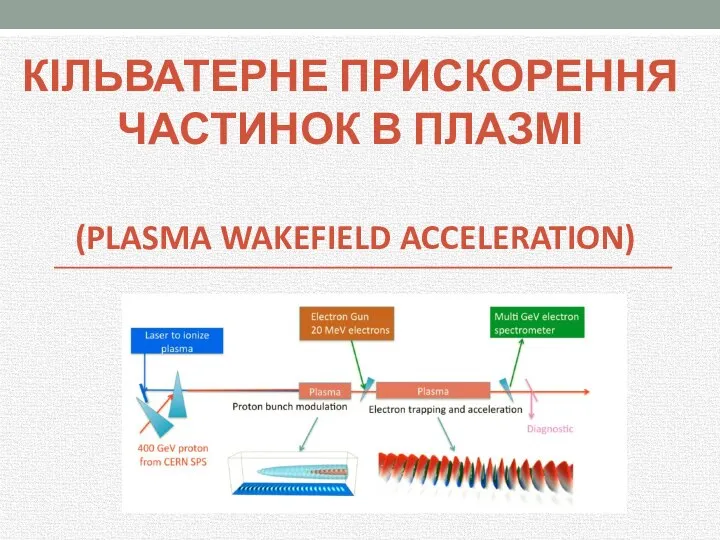 Кільватерне прискорення частинок в плазмі (plasma wakefield acceleration)
Кільватерне прискорення частинок в плазмі (plasma wakefield acceleration) Динамика твердого тела
Динамика твердого тела Презентация по физике "Электроизмерительные приборы" - скачать
Презентация по физике "Электроизмерительные приборы" - скачать  Оборудование и технология получения наноматериалов из газовой фазы
Оборудование и технология получения наноматериалов из газовой фазы Сверхпроводимость материалов
Сверхпроводимость материалов Диэлектрические материалы. Классификация диэлектриков
Диэлектрические материалы. Классификация диэлектриков