Содержание
- 2. План лекции Общие понятия Классификация дисперсных систем Методы получения коллоидов Методы очистки коллоидных растворов Молекулярно-кинетические свойства
- 3. Коллоидная химия Раздел физической химии, изучающий физико-химические свойства гетерогенных высокодисперсных систем, растворов и высокомолекулярных соединений
- 4. Немного истории… До начала XX века наука о коллоидах содержала описание свойств отдельных высокодисперсных систем и
- 5. По Т. Грэму Кристаллоиды – вещества быстро диффундирующие и проходящие через растительные и животные мембраны, легко
- 6. По И.Г. Борщеву В зависимости от условий одно и то же вещество может проявлять свойства кристаллической
- 7. Коллоидное состояние вещества Степень его раздробленности (дисперсности) и нахождение коллоидных частиц во взвешенном состоянии в растворителе
- 8. Удельная поверхность фазы S Sуд = ----- V S – суммарная поверхность всех частиц V –
- 9. Дисперсная система Дисперсионная среда – растворитель, в котором распределено вещество в раздробленном состоянии Дисперсная фаза –
- 10. Гетерогенные (неоднородные) системы Дисперсные системы, в которых одно вещество распределено в другом в виде частиц различных
- 11. Классификация дисперсных систем По величине частиц дисперсной фазы Грубодисперсные (больше 10-7м). Быстро оседают, видимы в микроскоп,
- 12. По агрегатному состоянию
- 13. Классификация коллоидных растворов По интенсивности взаимодействия частиц на поверхности раздела фаз: Лиофильные – сильное взаимодействие; устойчивы,
- 14. По текучести растворов: Золи – коллоидные растворы, имеющие текучесть (свободнодисперсные) Гели – коллоидные растворы, утратившие текучесть
- 15. Условия получения коллоидов Дисперсная фаза должна обладать плохой растворимостью Размеры диспергируемого вещества должны быть доведены до
- 16. Методы получения коллоидных растворов Дисперсионные методы – дробление вещества до коллоидной степени дисперсности Конденсационные методы –
- 17. Дисперсионные методы Механические (шаровые и коллоидные мельницы, ступка) – диспергирование с добавлением стабилизаторов Ультразвуковые – диспергирование
- 18. Пептизация – процесс перехода вещества из осадка в золь при добавлении диспергирующих веществ (Al(OH)3, Fe(OH)3 +
- 19. Конденсационные методы Окисление 2H2S + O2 → 2H2O + 2S↓ Восстановление Ag2O + H2 → 2Ag0
- 20. Нейтрализация Ca(OH)2 + H2SO4 → CaSO4 + 2H2O Замена растворителя При вливании спиртовых растворов серы, канифоли,
- 21. Методы очистки коллоидных растворов Диализ – основан на способности животных и растительных мембран пропускать ионы и
- 22. Молекулярно-кинетические свойства коллоидных растворов Седиментационное равновесие Броуновское движение Диффузия Осмотическое давление
- 23. Седиментационное равновесие 2 (d – d0) υ = ---- · r2g · ----------, см/с 9 η
- 24. h – высота, на которую нужно подняться, чтобы давление упало вдвое Изменение концентрации с высотой будет
- 25. Применение седиментационного анализа Определение размера и фракционного состава частиц (число частиц разного размера) Определение молекулярного веса
- 26. Броуновское движение Присуще частицам с размерами не более 10-6м Не зависит от природы вещества Обусловлено тепловым
- 27. Уравнение Эйнштейна-Смолуховского Описывает броуновское движение Δх = √2Дτ τ – время Δх – среднее смещение (среднее
- 28. Диффузия ΔC Δm = -Д · ----- · Δτ ΔX Скорость диффузии в случае коллоидных растворов
- 29. Осмотическое давление Осмотическое давление коллоидных растворов подчиняется закону Вант-Гоффа πосм = КБ · СV · T
- 30. πосм (1% золь золота) = 0,00045 атм πосм (1% раствор сахарозы) = 0,725 атм Осмотическое давление
- 32. Скачать презентацию





























 Активізація пізнавальної діяльності учнів на уроках фізики шляхом використання проблемних ситуацій
Активізація пізнавальної діяльності учнів на уроках фізики шляхом використання проблемних ситуацій Вольтамперометрия. Электрохимические методы
Вольтамперометрия. Электрохимические методы Роль силы трения в быту
Роль силы трения в быту Презентация по физике Статика
Презентация по физике Статика  Нагревание воздуха и его температура
Нагревание воздуха и его температура Электротехника и электроника. Трехфазные электрические цепи. (Лекция 8)
Электротехника и электроника. Трехфазные электрические цепи. (Лекция 8) Поле системы элементарных излучателей
Поле системы элементарных излучателей Исследование силы трения скольжения. Измерение коэффициента трения скольжения
Исследование силы трения скольжения. Измерение коэффициента трения скольжения Биологиялық жүйелер
Биологиялық жүйелер Топологические изоляторы
Топологические изоляторы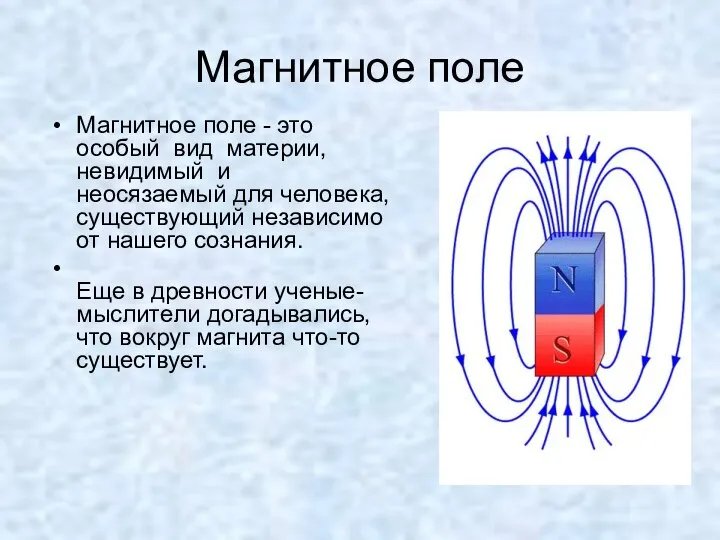 Магнитное поле Магнитное поле - это особый вид материи, невидимый и неосязаемый для человека, существующий н
Магнитное поле Магнитное поле - это особый вид материи, невидимый и неосязаемый для человека, существующий н Феромагнетики. Феромагнітне тіло
Феромагнетики. Феромагнітне тіло Твердотельные лазеры
Твердотельные лазеры Газотурбинные установки
Газотурбинные установки Оптические методы анализа
Оптические методы анализа Применение игровых технологий на уроках физики
Применение игровых технологий на уроках физики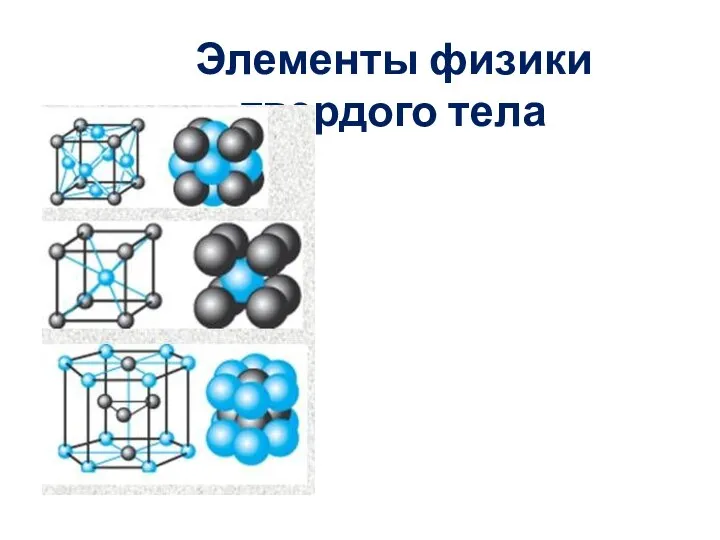 Элементы физики твердого тела
Элементы физики твердого тела Кинематика роботов. Кинематические схемы. (Лекция 2.1)
Кинематика роботов. Кинематические схемы. (Лекция 2.1) Разряды в жидких и твердых диэлектриках. Электрические характеристики внутренней изоляции. (Лекция 6)
Разряды в жидких и твердых диэлектриках. Электрические характеристики внутренней изоляции. (Лекция 6) Формирование колесной пары электровоза ВЛ11
Формирование колесной пары электровоза ВЛ11 Электростатика. (Лекция 11)
Электростатика. (Лекция 11) Механика. Работа и энергия
Механика. Работа и энергия Изобретения Леонардо да Винчи
Изобретения Леонардо да Винчи Основы специальной теории относительности
Основы специальной теории относительности Учебный курс
Учебный курс  Силы в природе, законы Ньютона. Решение задач
Силы в природе, законы Ньютона. Решение задач Тема урока: «Инерция» 15.11.2013г.
Тема урока: «Инерция» 15.11.2013г. Олимпиада в Сочи 2014 Физические задачи по теме «Механика» 9-10 класс на спортивную тематику
Олимпиада в Сочи 2014 Физические задачи по теме «Механика» 9-10 класс на спортивную тематику