Содержание
- 2. Движение электронов в атоме Все окружающие нас тела состоят из элементарных частиц (атомов) или из групп
- 3. 30.08.1871, Спринг Грув - 19.10.1937, Кембридж) – британский физик новозеландского происхождения. Известен как «отец» ядерной физикиИзвестен
- 4. 1911 г. Планетарная модель атома Проблема: электрон движется с ускорением следовательно, излучает, следовательно, теряет энергию следовательно,
- 5. Спектр излучения атома водорода
- 6. Каждый атом или молекула может находиться в том или другом энергетическом состоянии. Иначе говоря, их внутренняя
- 7. Взаимодействие частиц в квантовой механике характеризуют потенциальной энергией, формула которой заимствуется из классической механики. Например, потенциальная
- 8. Постулаты Бора Нильс Хе́нрик Дави́д Бор (дат. Niels Henrik David Bohr; 7.10; 7.10 1885; 7.10 1885,
- 9. Постулаты Бора 1. Электрон в атоме может двигаться только по определенным стационарным орбитам, каждой из которых
- 10. Постулаты Бора
- 11. Постулаты Бора 2. Разрешенными стационарными орбитами являются только те, для которых угловой момент импульса L электрона
- 12. Постулаты Бора 3. Излучение или поглощение кванта излучения происходит при переходе атома из одного стационарного состояния
- 13. Постулаты Бора Распределение электронной плотности показывает, в каких областях вокруг атома электрон пребывает преимущественно, то есть
- 14. Квантование энергии атома Запишем условие вращения электрона массы по круговой орбите радиуса r под действием кулоновской
- 15. Квантование энергии атома Решая эту систему уравнений, находим для радиусов стационарных орбит электрона в атоме водорода
- 16. Квантование энергии атома Вводя в качестве универсальной константы теории боровский радиус =0,529∙10-10 м как радиус первой
- 17. Квантование энергии атома Для скорости электрона на n-ой стационарной орбите получаем значение Полная энергия электрона, движущегося
- 18. Квантование энергии атома и потенциальной энергии кулоновского взаимодействия электрона с ядром эВ
- 19. Квантование энергии атома Полная энергия электрона в атоме оказалась отрицательной, так как отрицательна потенциальная электростатическая энергия
- 20. Квантование энергии атома Для описания атома используют квантовые числа – энергетические параметры, определяющие состояние электрона и
- 21. Главное квантовое число n может принимать любые целые положительные значения от 1 до ∞. Оно определяет
- 22. С увеличением n расстояние между энергетическими уровнями и энергия связи электронов с ядрами уменьшается, значение энергетического
- 23. Спектр излучения атома водорода
- 24. Орбитальное квантовое число l определяет форму орбитали. Значение орбитального числа l=(n-1)=0,1,2,3...(n-1). Также вводят буквенные обозначения: 0-s,
- 26. Число орбиталей на энергетических подуровнях Орбитали с l = 0 называются s-орбиталями, l = 1 –
- 27. Каждому уровню энергии соответствует стоячая электронная волна, электрон колеблется вокруг и возле атомов и образует как
- 28. Условное изображение облаков электронной плотности для разных состояний электрона в атоме водорода
- 29. Магнитное квантовое число характеризует величину магнитного поля, создаваемого при вращении электрона вокруг ядра. Поэтому значение магнитного
- 30. Магнитное квантовое число характеризует величину магнитного поля, создаваемого при вращении электрона вокруг ядра. Поэтому значение магнитного
- 31. Спиновое квантовое число s Электрон помимо координат и импульса характеризуется вектором спина, спин, подобно заряду, –
- 32. В том же 1925 г. голландец Ральф Кронинг и независимо Джордж Уленбек и Самюэль Гаудсмит предположили,
- 33. Спин – это одно из проявлений принципа тождественности частиц, который применительно к электронам звучит так: все
- 35. Скачать презентацию
































 Теодолиттер. Оптикалық теодолиттер
Теодолиттер. Оптикалық теодолиттер Сила Лоренца. (Лекции 15-16)
Сила Лоренца. (Лекции 15-16) Лекция №3
Лекция №3  Постоянный ток. Электрический ток в различных средах
Постоянный ток. Электрический ток в различных средах Решение задачи изгиба многослойной упругопластической пластины
Решение задачи изгиба многослойной упругопластической пластины Переходные процессы в линейных электрических цепях
Переходные процессы в линейных электрических цепях Гідростатичний парадокс Автор: Загородня Катерина, учениця 8 класу Новогуйвинської гімназії Житомирського району Житомирськ
Гідростатичний парадокс Автор: Загородня Катерина, учениця 8 класу Новогуйвинської гімназії Житомирського району Житомирськ Простая физика сложных явлений
Простая физика сложных явлений Системы единиц физических величин
Системы единиц физических величин Нерозгалужене коло з активним опором та індуктивністю
Нерозгалужене коло з активним опором та індуктивністю Электролиз меди, цинка, алюминия
Электролиз меди, цинка, алюминия Лучше Северного Сияния, только Северное Сияние…
Лучше Северного Сияния, только Северное Сияние… Определение расстояния до недоступной точки
Определение расстояния до недоступной точки Момент пары сил
Момент пары сил Презентация по физике "Производство и передача электроэнергии" - скачать бесплатно
Презентация по физике "Производство и передача электроэнергии" - скачать бесплатно Характеристики электростатического поля
Характеристики электростатического поля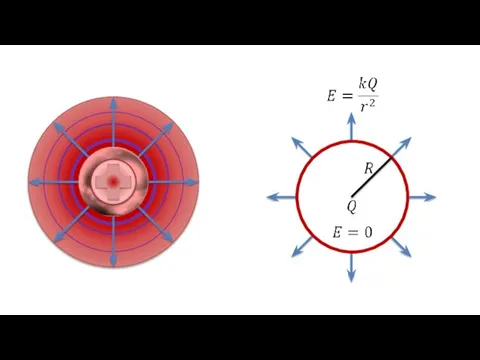 Напряженность заряженного шара
Напряженность заряженного шара Michael Faraday
Michael Faraday Свойства твердых тел
Свойства твердых тел Дарсонвалізація. Змінний характер струму
Дарсонвалізація. Змінний характер струму Свойства твёрдых тел, жидкостей и газов
Свойства твёрдых тел, жидкостей и газов Может ли магнит потерять свою силу
Может ли магнит потерять свою силу Магниты на основе современных массивных высокотемпературных сверхпроводников
Магниты на основе современных массивных высокотемпературных сверхпроводников Линейные электрические цепи. Постоянный ток
Линейные электрические цепи. Постоянный ток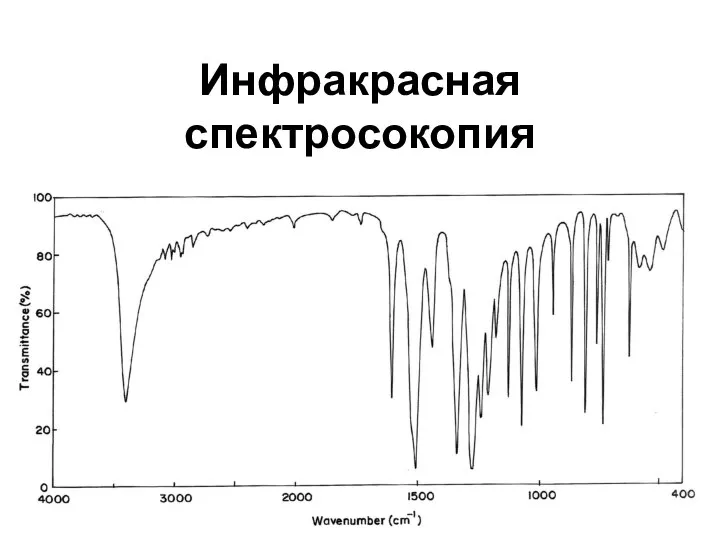 Инфракрасная спектросокопия
Инфракрасная спектросокопия Основное уравнение молекулярно-кинетической теории газов
Основное уравнение молекулярно-кинетической теории газов Измерительные приборы
Измерительные приборы Магнитное поле
Магнитное поле