Содержание
- 2. Горение — один из сложных физико-химических процессов, с которым встречался человек еще на пороге развития цивилизации.
- 3. Процесс горения как физическое явление изучен достаточно полно, но дать ему единое определение трудно. Все зависит
- 4. Российским физикам (Семенов Н.Н., Зельдович Я.Б. и др.) в первую очередь принадлежит разработка основных вопросов теории
- 5. Для специалистов, занимающихся прекращением горения на пожаре, инженерно-технической экспертизой по расследованию возникновения, распространения горения и взрыва,
- 6. Горение — сложный физико-химический процесс, при котором горючие вещества и материалы под воздействием высоких температур вступают
- 7. Химической составляющей данного процесса является окислительно-восстановительная реакция, протекающая между горючим и окислителем: Г + O→ПГ +
- 8. Горючие вещества и материалы являются восстановителями. Атомы, входящие в их состав, отдают электроны при протекании окислительно-восстановительного
- 9. Восстановителями являются: металлы, Η2, С, Si, бескислородные кислоты (НСl, HBr, HJ, H2S) и их соли, ΝΗ3
- 10. При расчете процесса горения (расчет массы сгоревшего горючего, объема окислителя на горение, объема и состава выделившихся
- 11. При горении в воздухе на один моль кислорода, участвующего в реакциях окисления, приходится примерно 3,76 моля
- 12. Во-первых, на его нагревание в зоне горения затрачивается большое количество теплоты, выделяемой при горении, чем в
- 13. Уравнение реакции горения в воздухе следует записывать, прибавляя в левую и правую части этих уравнении по
- 14. Для осуществления процесса горения по этому уравнению необходимо, чтобы в зоне горения на 1 м3 горючего
- 15. Для количественного описания горения недостаточно рассматривать этот процесс только в виде конечного уравнения реакции горения, отражающего
- 16. Горение углеводородов является чрезвычайно сложным процессом, протекающим через ряд последовательных стадий. В составе продуктов окисления содержатся
- 17. Для объяснения сложных процессов окисления различных видов топлива в 1897г. А.Н. Бах предложил пероксидную теорию. В
- 18. Согласно этой теории молекулы кислорода перед вступлением в реакцию должны активироваться. Они либо распадаются на отдельные
- 19. При замещении двух атомов водорода в перекиси водорода органическими радикалами образуются органические перекиси, при замещении одного
- 20. Перекиси и гидроперекиси, образующиеся из различных классов органических соединений, в большинстве случаев легко разлагаются с вспышкой
- 21. Образующиеся при распаде перекисей радикалы являются активными центрами реакции окисления. Начальная температура окисления (tо) зависит от
- 22. Окисление ароматических углеводородов происходит при более высоких температурах, чем предельных и непредельных. Вещества с низкой начальной
- 23. Пероксидная теория позволяет уяснить механизм окислительного действия кислорода на органические соединения в начальной стадии окисления. Однако
- 24. Механизм химической реакции горения необходимо рассматривать с позиций основных законов химической кинетики. Для кинетического описания процесса
- 25. Однако скорость процесса определяется лишь несколькими элементарными реакциями, контролирующими его лимитирующие стадии (протекающие с наименьшей скоростью),
- 26. С точки зрения упрощенной кинетической схемы реакции процессы горения — это радикально-цепные реакции.
- 27. Впервые они были изучены М. Боденштейном в 1913 г. на примере взаимодействия водорода с хлором.
- 28. Согласно закону Эйнштейна при фотохимических процессах каждая вступающая в реакцию молекула поглощает один квант лучистой энергии.
- 29. Например, поглощение смесью водорода с хлором только одного кванта лучистой энергии при длине волны 4000—4360 Å
- 30. Изучая механизм данного химического процесса, М. Боденштейн разработал новую теорию для таких быстропротекающих реакций. Согласно этой
- 31. Цепными называются реакции, протекающие через ряд промежуточных стадий, в которых образуются соединения, обладающие избыточной энергией, необходимой
- 32. Эти частицы, обладающие избыточной энергией, называются радикалами.
- 33. Активный радикал может представлять собой атом, молекулу или группу молекул. Иными словами, цепными называются такие реакции,
- 34. Примером неразветвляющейся цепной реакции является реакция взаимодействия хлора с водородом. С12 + hv = Сl• +
- 35. Неразветвляюшаяся цепная реакция может самоускоряться только при повышенных температурах, а разветвленная — при постоянной температуре.
- 36. Кинетика цепных реакций получила развитие в работах зарубежных и советских ученых и имеет большое значение при
- 37. Радикально-цепные реакции лежат в основе процессов горения. Общие закономерности таких реакций детально изучены. Схема наиболее важных
- 38. (0) Н2 + O2 → 2OН• зарождение цепи; (1) ОН• + Н2 → Н2O + Н•
- 39. Лавинообразное нарастание количества радикалов в реакционной смеси прекратится лишь после израсходования одного из исходных реагентов.
- 40. Самовоспламенение возможно, когда число образующихся радикалов превышает число гибнущих радикалов. Условие цепного самовоспламенения (взрыва): Wроста цепи
- 41. 2. КИНЕТИКА РЕАКЦИЙ, ПРОТЕКАЮЩИХ В ЗОНЕ ГОРЕНИЯ Упрощенная модель возникновения горения на пожаре представляется в виде
- 42. Это качественная сторона явления. Количественный подход требует более глубокого понимания физической сущности процессов горения, физики и
- 43. Химической реакции взаимодействия горючего с окислителем должен предшествовать процесс смешения горючего с окислителем и физический акт
- 44. Расчеты показывают, что для смеси стехиометрического состава водорода с кислородом (2Н2 + O2), находящейся при комнатной
- 45. Это означает, что число эффективных соударений молекул при этих условиях ничтожно мало. Молекулы, которые при соударении
- 46. По своей природе такое возбуждение может быть химическим — наличие у атомов или молекул вещества свободных
- 47. Разность между средним уровнем запаса энергии молекул в возбужденном состоянии и средним уровнем энергии неактивных молекул
- 48. Чем выше численное значение Еакт, тем труднее вступают в реакцию компоненты реакционной смеси. Поэтому величина Еакт
- 49. Энергия расходуется на ослабление или разрыв существующих связей в молекулах горючего и окислителя, чтобы они вступили
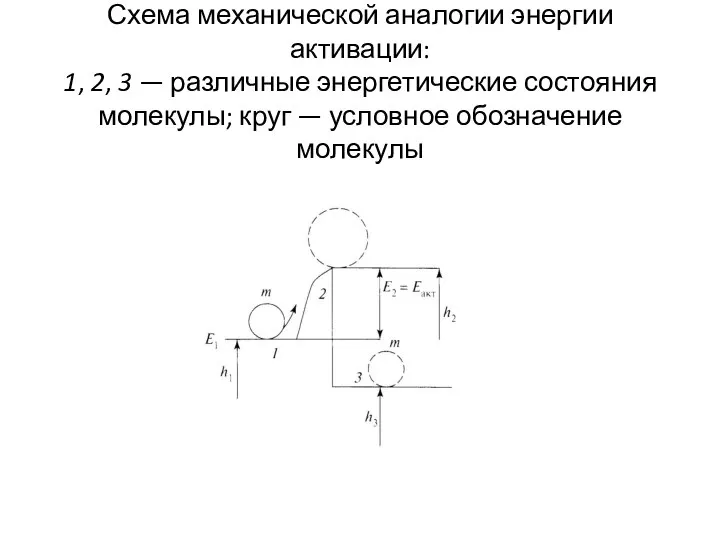
- 50. Схема механической аналогии энергии активации: 1, 2, 3 — различные энергетические состояния молекулы; круг — условное
- 51. Энергетическая модель процесса воспламенения с механической точки зрения может быть представлена в следующем виде. Представим «холодную»
- 52. Чтобы вывести молекулу из состояния 1 в состояние 2 (возбужденное), характеризующееся уровнем энергии h2, необходимо затратить
- 53. Перейдя в состояние 2, молекула активизируется, переходит в неустойчивое состояние и получает возможность перейти на новый,
- 54. Новые связи более прочны, чтобы их разорвать, надо подвести большую дополнительную энергию, чем прежде. При таком
- 55. Чтобы молекулы горючей смеси стали химически активными, необходимо повысить температуру горючей смеси внешним подогревом или вводом
- 56. При этом скорость движения молекул возрастает, увеличивается число и энергия их соударений. Две соударяющиеся молекулы, переходя
- 57. Происходит взаимодействие между молекулами водорода и кислорода — молекулы переходят на более низкий и устойчивый уровень
- 58. Энергия, выделившаяся в результате взаимодействия первых прореагировавших молекул, передается соседним молекулам. Они возбуждаются еще больше, и
- 59. Происходит самоподдерживающийся, самоускоряющийся и самораспространяющийся на всю реакционную смесь процесс химического взаимодействия водорода с кислородом, сопровождающийся
- 60. При исследовании процесса горения скорость химической реакции горения необходимо рассматривать с позиций конечных эффектов химических превращений
- 61. Если горючее и окислитель, условно Г и О, вступают в реакцию, в результате которой образуются два
- 62. Следовательно, перед Q будет знак +. Если концентрация реагентов и продуктов реакции соответственно равны a, b,
- 63. Скорость химических реакций горения можно выразить через скорость превращения исходных компонентов горючей смеси или через скорость
- 64. Так как реакции горения, как правило, идут в сторону образования продуктов горения и количество тепла, выделившегося
- 65. Справедливы те количественные соотношения, которые записаны для числа соударений молекул и для скорости протекания химических реакций
- 66. В этом случае скорость процесса горения зависит от кинетики химических реакций и горение называется кинетическим. Однако
- 68. Скачать презентацию
































































 Ускорение тела
Ускорение тела Дифракция. Дисперсия
Дифракция. Дисперсия Презентация по физике "Альберт Эйнштейн. Биография гениального ученого." - скачать
Презентация по физике "Альберт Эйнштейн. Биография гениального ученого." - скачать  Тепловая разверка
Тепловая разверка Равнодействующие силы в пространстве. (Лекция 3)
Равнодействующие силы в пространстве. (Лекция 3) Презентация по физике "Предмет физики. Физические явления" -
Презентация по физике "Предмет физики. Физические явления" -  Статика
Статика Скачок уплотнения. Возникновение скачка уплотнения
Скачок уплотнения. Возникновение скачка уплотнения Источники звука. Характеристики звука.
Источники звука. Характеристики звука. Магнитное поле. Постоянные магниты и магнитное поле тока. Индукция магнитного поля
Магнитное поле. Постоянные магниты и магнитное поле тока. Индукция магнитного поля Звуковые явления в живой и неживой природе
Звуковые явления в живой и неживой природе Поляризация света. Применение
Поляризация света. Применение Муниципальное Образовательное учреждение «Венёвская средняя общеобразовательная школа №2» «Кипение. Удельная теплота пароо
Муниципальное Образовательное учреждение «Венёвская средняя общеобразовательная школа №2» «Кипение. Удельная теплота пароо Организационно-технологические основы производства изделий микро- и наноэлектроники
Организационно-технологические основы производства изделий микро- и наноэлектроники Молекуляроно-кинетическая теория
Молекуляроно-кинетическая теория Определение волнового процесса. Процесс распространения колебаний
Определение волнового процесса. Процесс распространения колебаний Современные ускорители элементарных частиц
Современные ускорители элементарных частиц Автор презентации: Лебедева Марина Геннадьевна МБОУ СОШ с углубленным изучением отдельных предметов № 1 имени Ф.Г.Логинова Волгог
Автор презентации: Лебедева Марина Геннадьевна МБОУ СОШ с углубленным изучением отдельных предметов № 1 имени Ф.Г.Логинова Волгог Петрофизика. Физико-механические свойства горных пород
Петрофизика. Физико-механические свойства горных пород Закон Снеллиуса (отражения) для монотипных волн
Закон Снеллиуса (отражения) для монотипных волн Принципы полета. Часть 2-2 СВЕРХЗВУК
Принципы полета. Часть 2-2 СВЕРХЗВУК Внутренняя энергия и виды теплопередачи
Внутренняя энергия и виды теплопередачи Волновые процессы
Волновые процессы Теоремы динамики
Теоремы динамики Колебания и волны
Колебания и волны Презентация Реактивное движение
Презентация Реактивное движение  Решение задач по теме «Законы постоянного тока»
Решение задач по теме «Законы постоянного тока» Физика для всех
Физика для всех