Содержание
- 2. Идеальный газ Исторические данные Закон Бойля – Мариотта Закон Шарля Закон Гей – Люссака Сводная таблица
- 3. Газовые законы рассматриваются для идеального газа. Модель идеального газа предполагает следующее: молекулы обладают пренебрежимо малым объемом
- 4. Состояние идеального газа характеризуется тремя макроскопическими параметрами: P – давление (Па) T – температура (ºС) V
- 5. Уравнение состояния идеального газа р = nkT n – концентрация –число молекул газа в единице объема.
- 6. Бенау Клайперон (1799-1864) французский физик получил зависимость, уравнение устанавливающее связь между: P,T, V
- 7. Дмитрий Иванович Менделеев (1834-1907) русский ученый впервые применил соотношение между:P,T, V
- 8. Уравнение Менделеева – Клапейрона: PV=
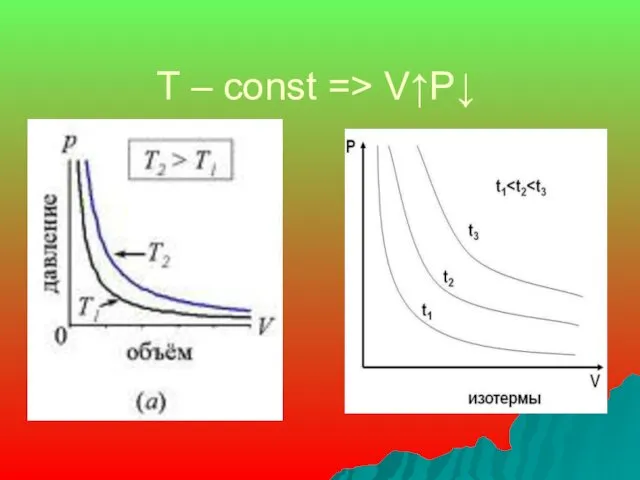
- 9. Закон Бойля – Мариотта: изотермический процесс- процесс изменения состояния газа при постоянной температуре (T-const) => P1V1=P2V2
- 10. T – const => V↑P↓
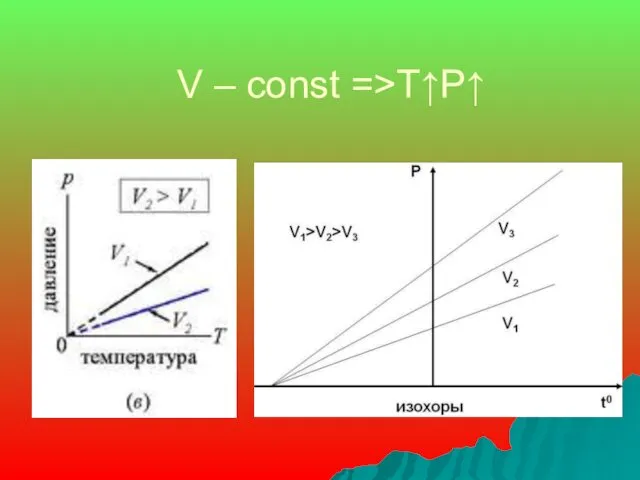
- 11. Закон Шарля: изохорный процесс- процесс изменения состояния газа при постоянном объеме (V-const) =>
- 12. V – const =>T↑P↑
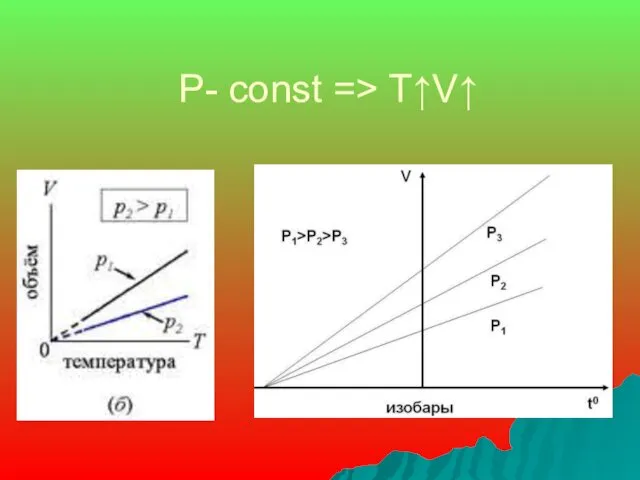
- 13. Закон Гей – Люссака: изобарный процесс - процесс изменения состояния газа при постоянном давлении (P-const) =>
- 14. P- const => T↑V↑
- 17. Скачать презентацию











 Электрические трёхфазные цепи
Электрические трёхфазные цепи Реактивное движение Урок в 9 классе Сидорина Ольга Павловна учитель физики ГБОУ СОШ 371 г.Москва 2013год
Реактивное движение Урок в 9 классе Сидорина Ольга Павловна учитель физики ГБОУ СОШ 371 г.Москва 2013год Оптическая система. Лучевая и волновая оптика
Оптическая система. Лучевая и волновая оптика Пленочные наноматериалы и технологии их получения
Пленочные наноматериалы и технологии их получения Грузовые электромобили
Грузовые электромобили Законы Ома и Кирхгофа
Законы Ома и Кирхгофа Подшипники. Конструкция подшипника скольжения
Подшипники. Конструкция подшипника скольжения Сейсморазведка. Разложение сейсмических колебаний
Сейсморазведка. Разложение сейсмических колебаний Телеграфная связь
Телеграфная связь Будова атома. Закріпити знання про будову атома. Узагальнити знання про стан електронів у атомі
Будова атома. Закріпити знання про будову атома. Узагальнити знання про стан електронів у атомі Бернулли теңдеуі
Бернулли теңдеуі Принцип Гюйгенса в виде формулы Кирхгофа
Принцип Гюйгенса в виде формулы Кирхгофа Электрическое поле в проводниках и дилектриках
Электрическое поле в проводниках и дилектриках Магнетизм. Магнитное поле
Магнетизм. Магнитное поле Коливальний рух у природі і техніці
Коливальний рух у природі і техніці Сложный четырехполюсник (задача)
Сложный четырехполюсник (задача) Лекция 12
Лекция 12 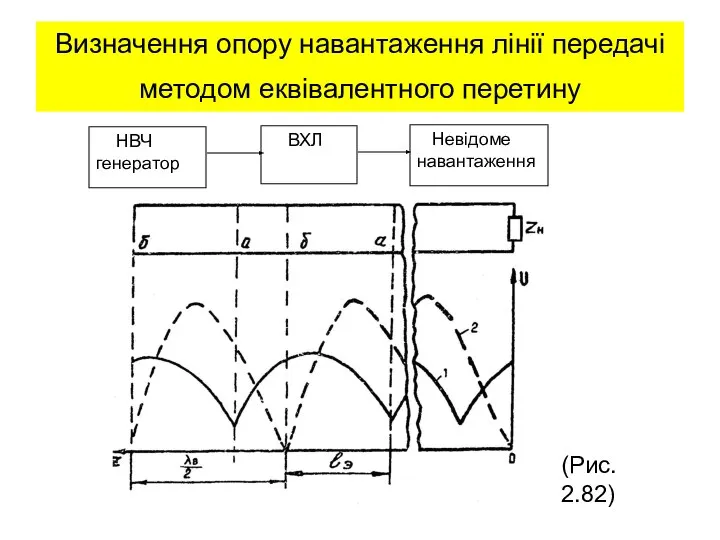 Визначення опору навантаження лінії передачі методом еквівалентного перетину. (Лекция 15)
Визначення опору навантаження лінії передачі методом еквівалентного перетину. (Лекция 15) 25.8. Элементы зонной теории твердого тела
25.8. Элементы зонной теории твердого тела Гипотеза де Бройля. Комптоновская длина волны и длина волны де Бройля
Гипотеза де Бройля. Комптоновская длина волны и длина волны де Бройля Законы термодинамики
Законы термодинамики Ядерный магнитный резонанс
Ядерный магнитный резонанс Силы в природе
Силы в природе Презентация Виды сил 7 класс
Презентация Виды сил 7 класс Расчеты на прочность механических конструкций
Расчеты на прочность механических конструкций Подпрыгивающая вода
Подпрыгивающая вода Примеры решения задач по теме Движение с постоянным ускорением свободного падения
Примеры решения задач по теме Движение с постоянным ускорением свободного падения Датчики давления
Датчики давления