Содержание
- 2. При положительной кривизне дополнительное давление увеличивает внутреннее давление жидкости, а при отрицательной – уменьшает. В первом
- 3. Из уравнения (3) видно влияние кривизны на внутреннее давление тела. В случае сферической поверхности получаем: Уравнение
- 5. Капиллярное поднятие В тонких капиллярных трубках можно наблюдать подъем уровня жидкости, причем чем уже капилляр, тем
- 6. Рис. 4. Капиллярное поднятие жидкости между пластинами Для полного смачивания cos θ = 1, и пренебрегая
- 7. ДИСПЕРСНОСТЬ И РЕАКЦИОННАЯ СПОСОБНОСТЬ ВЕЩЕСТВ Дисперсность или раздробленность вещества D, является самостоятельным термодинамическим параметром состояния системы.
- 8. ПРИМЕРЫ Процессы испарения-конденсации где R – газовая постоянная; T – температура; P – давление насыщенного пара
- 10. 2. Процессы растворения где x – растворимость вещества в дисперсном состоянии; x∞ – растворимость в крупном
- 12. Скачать презентацию
При положительной кривизне дополнительное давление увеличивает внутреннее давление жидкости, а
При положительной кривизне дополнительное давление увеличивает внутреннее давление жидкости, а
Изменение объема жидкости в обоих случаях происходит в результате самопроизвольного уменьшения поверхностной энергии и превращения ее в механическую энергию изменения объема тела δAV = ∆РdV. Процесс превращения поверхностной энергии в механическую можно описать с помощью объединенного уравнения I и II начал термодинамики. Запишем это уравнение относительно изменения энергии Гельмгольца F:
При постоянных T, n, q имеем
В состоянии равновесия:
dF = 0
где Р = ∆Р – дополнительное давление, равное разности между давлением тела с плоской и изогнутой поверхностями; dS/dV – кривизна поверхности
Для сферической поверхности
(1)
(2)
(3)
(4)
Для цилиндрической поверхности
(5)
Из уравнения (3) видно влияние кривизны на внутреннее давление тела. В
Из уравнения (3) видно влияние кривизны на внутреннее давление тела. В
Уравнение (6) называется уравнением Лапласа, являющимся основой теории капиллярных явлений, в котором r – радиус кривизны; 1 / r – кривизна. Для поверхности неправильной формы используют представление о средней кривизне и уравнение Лапласа имеет вид:
(6)
(7)
На законе Лапласа основан один из самых распространенных методов определения поверхностного натяжения – метод наибольшего давления пузырьков, предложенный П. А. Ребиндером. В методе измеряется давление, при котором происходит проскок газового пузырька из капилляра, опущенного в исследуемую жидкость и стандартную.
Метод наибольшего давления пузырьков (метод П.А. Ребиндера):
и для исследуемой жидкости:
разделим (9) на (8):
(8)
(9)
(10)
Запишем уравнение Лапласа
для воды по уравнению (6)
– расчетная формула
метода Ребиндера
Капиллярное поднятие
В тонких капиллярных трубках можно наблюдать подъем уровня жидкости, причем
Капиллярное поднятие
В тонких капиллярных трубках можно наблюдать подъем уровня жидкости, причем
h = 15 км.
Рис. 2. Капиллярное поднятие жидкости в капилляре при смачивании (а) – положительное капиллярное поднятие;
и несмачивании (б) – отрицательное капиллярное поднятие.
а)
б)
Рис. 3. Связь высоты капиллярного
поднятия h с параметрами капилляра и жидкости
(11)
Уравнение (11) – формула Жюрена, где ρ', ρ'' − плотности жидкости и воздуха; σ − поверхностное натяжение жидкости; θ − краевой угол смачивания; R – радиус основания капилляра; r – радиус кривизны.
положительное капиллярное поднятие (h > 0)
Рис. 4. Капиллярное поднятие жидкости
между пластинами
Для полного смачивания cos
Рис. 4. Капиллярное поднятие жидкости
между пластинами
Для полного смачивания cos
(12)
Для поднятия воды в стекле применимо уравнение (12), так как θ = 0–5°, а cos θ = 1.
Капиллярное давление будет наблюдаться и между погруженными параллельными пластинками (рис. 4). Здесь мениск имеет цилиндрическую форму, для него давление Лапласа будет в два раза меньше:
(13)
(14)
Метод определения поверхностного натяжения (по высоте капиллярного поднятия)
Уравнение 12 для исследуемой жидкости
Поделив (16) на (15), имеем расчетное уравнение метода капиллярного поднятия:
(15)
(16)
(17)
Уравнение 12 для стандартной жидкости
ДИСПЕРСНОСТЬ И РЕАКЦИОННАЯ СПОСОБНОСТЬ ВЕЩЕСТВ
Дисперсность или раздробленность вещества D,
ДИСПЕРСНОСТЬ И РЕАКЦИОННАЯ СПОСОБНОСТЬ ВЕЩЕСТВ
Дисперсность или раздробленность вещества D,
С = K – Ф + 3
где С – число степеней свободы; K – число компонентов; Ф – число фаз; 3 – число, включающее в себя, кроме переменных внешних параметров (давления и температуры) еще и дисперсность.
Дисперсность является одним из основных технологических параметров веществ и материалов во многих производственных процессах.
При выборе аппаратов в химической технологии обязательно учитываются дисперсионные характеристики системы, так как меняя дисперсность в системе, можно повлиять на растворимость вещества, на возможность переходить из одной фазы в другую, на температуру фазовых переходов, на способность вступать в химическую реакцию. Иными словами, дисперсность может повлиять на реакционную способность веществ.
В термодинамике, как известно, реакционная способность определяется энергией Гиббса ΔG. Связь между энергией Гиббса и дисперсностью в изотермических условиях можно получить с учетом уравнения Лапласа в следующем виде:
где V – объем системы; ΔP – изменение давления.
(1)
(2)
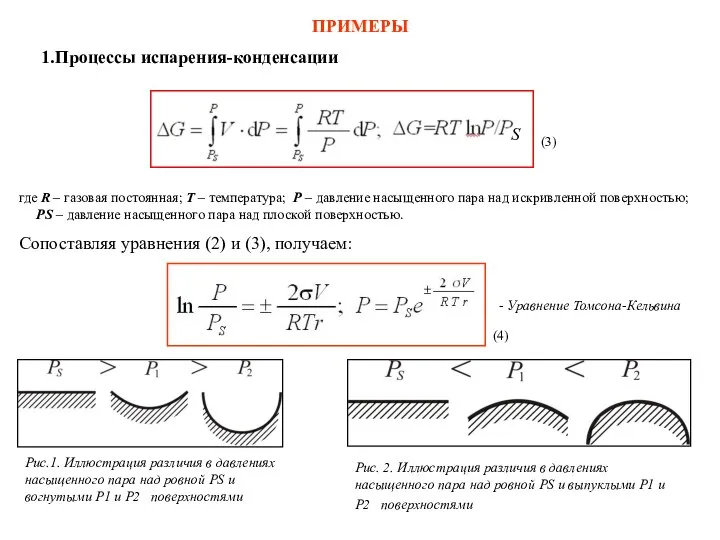
ПРИМЕРЫ
Процессы испарения-конденсации
где R – газовая постоянная; T – температура; P –
ПРИМЕРЫ
Процессы испарения-конденсации
где R – газовая постоянная; T – температура; P –
PS – давление насыщенного пара над плоской поверхностью.
Сопоставляя уравнения (2) и (3), получаем:
(3)
(4)
Рис.1. Иллюстрация различия в давлениях насыщенного пара над ровной PS и вогнутыми Р1 и Р2 поверхностями
Рис. 2. Иллюстрация различия в давлениях насыщенного пара над ровной PS и выпуклыми Р1 и Р2 поверхностями
- Уравнение Томсона-Кельвина
S
2. Процессы растворения
где x – растворимость вещества в дисперсном состоянии; x∞
2. Процессы растворения
где x – растворимость вещества в дисперсном состоянии; x∞
Аналогично процессу испарения, имеем:
(6)
(5)
3. Температуры фазовых переходов
(7)
где ΔТ = Т∞ – ТD; ΔHф.п – теплота фазового перехода; Т∞ − температура плавления недиспергированного вещества; ТD − температура плавления диспергированного вещества.
Полученные из диспергированных веществ материалы обладают повышенными структурно-механическими и прочностными свойствами.








 Применение ядерной энергии
Применение ядерной энергии Общие сведения о системах электросвязи
Общие сведения о системах электросвязи Микроструктура материала
Микроструктура материала Выбор допускаемых напряжений. (Лекция 3)
Выбор допускаемых напряжений. (Лекция 3) Телеграфная связь
Телеграфная связь Реактивное движение. Потенциальная и кинетическая энергия. Закон сохранения энергии. Механика
Реактивное движение. Потенциальная и кинетическая энергия. Закон сохранения энергии. Механика Магнит өрісі
Магнит өрісі Закон всемирного тяготения. Сила тяжести. Вес тела. Невесомость
Закон всемирного тяготения. Сила тяжести. Вес тела. Невесомость Плавание судов
Плавание судов Закон Кулона
Закон Кулона По материалам ФИПИ
По материалам ФИПИ Машины постоянного тока. Устройство, материалы и принцип действия. Карточка 16
Машины постоянного тока. Устройство, материалы и принцип действия. Карточка 16 Электротехника. Электродвижущая сила источников электрической энергии и напряжение. Электромагнитня индукция
Электротехника. Электродвижущая сила источников электрической энергии и напряжение. Электромагнитня индукция Урок решения задач По теме : «Магнитное поле. Применение правил буравчика, правой и левой руки» Выполнила: учитель Удомельской СО
Урок решения задач По теме : «Магнитное поле. Применение правил буравчика, правой и левой руки» Выполнила: учитель Удомельской СО Реальные цепи. Физические состояния и структура полимеров. (Лекция 3-4)
Реальные цепи. Физические состояния и структура полимеров. (Лекция 3-4) Термодинамиканың бірінші заңы
Термодинамиканың бірінші заңы Основные законы электродинамики. Лекция 1
Основные законы электродинамики. Лекция 1 Низкоразмерные структуры и технологии. Структуры с двумерным электронным газом
Низкоразмерные структуры и технологии. Структуры с двумерным электронным газом Основные параметры метода контроля
Основные параметры метода контроля Презентация Майкл Фарадей
Презентация Майкл Фарадей  Анализ характерных ошибок при решении ЕГЭ по физике. Систематизация и тренды
Анализ характерных ошибок при решении ЕГЭ по физике. Систематизация и тренды Явления тяготения. Сила тяжести
Явления тяготения. Сила тяжести Явления переноса в газах. (Лекция 3)
Явления переноса в газах. (Лекция 3) Термоядерная реакция
Термоядерная реакция Системы, элементы, сигналы Составила Антонова Е.П. 2010г.
Системы, элементы, сигналы Составила Антонова Е.П. 2010г. МЕХАНИЧЕСКОЕ ДВИЖЕНИЕ Урок для 9а класс (IIIб.в.) Учитель: Потоцкая С.А.
МЕХАНИЧЕСКОЕ ДВИЖЕНИЕ Урок для 9а класс (IIIб.в.) Учитель: Потоцкая С.А. УРОК ФИЗИКИ В 8 КЛАССЕ ВНУТРЕННЯЯ ЭНЕРГИЯ Учитель Кононов Геннадий Григорьевич СОШ № 29 Славянский район Краснод
УРОК ФИЗИКИ В 8 КЛАССЕ ВНУТРЕННЯЯ ЭНЕРГИЯ Учитель Кононов Геннадий Григорьевич СОШ № 29 Славянский район Краснод Уравнения теории упругости. Геометрические соотношения Коши. Уравнения неразрывности. (Лекция 3)
Уравнения теории упругости. Геометрические соотношения Коши. Уравнения неразрывности. (Лекция 3)