Содержание
- 2. КЛАССИФИКАЦИЯ В основу классификации положена кинетическая теория, согласно которой давление газа определяется количеством ударов молекул в
- 6. По величине создаваемого давления компрессоры делятся на компрессоры низкого давления (р≤10 ати), среднего давления (р=10 –
- 7. Важнейшие показатели компрессоров К числу важнейших показателей компрессоров относят: - степень повышения давления ε=рк/рн ; -
- 8. Основные параметры газов Это физические величины, определяющие состояние газа. К ним относят: плотность газа, удельный объём,
- 10. Скачать презентацию
КЛАССИФИКАЦИЯ
В основу классификации положена кинетическая теория, согласно которой давление газа
КЛАССИФИКАЦИЯ
В основу классификации положена кинетическая теория, согласно которой давление газа
увеличением количества молекул в единице объёма;
увеличением скорости движения молекул.
Сообразно этому компрессоры делятся на две группы: объёмные и лопаточные.
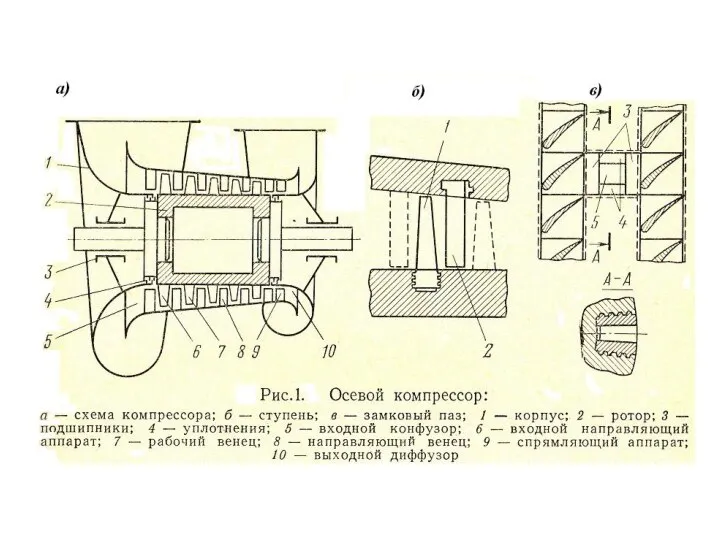
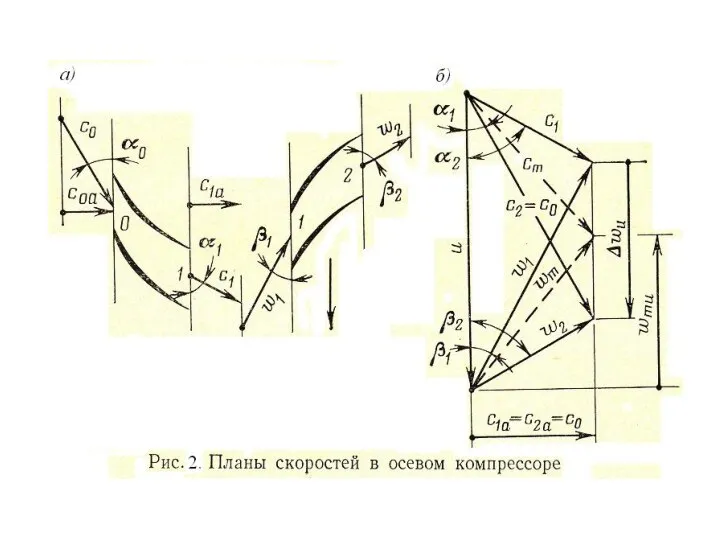
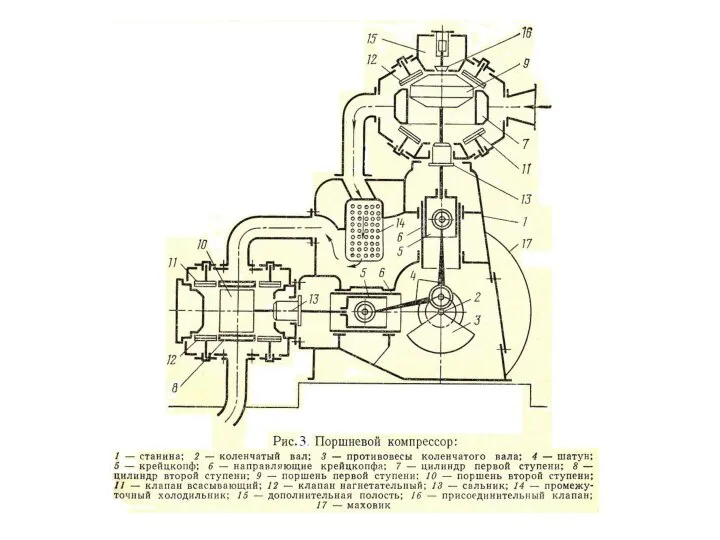
Среди объёмных распространены поршневые, пластинчатые, ротационные и винтовые, а среди лопаточных – радиальные, диагональные, осевые.
Как те, так и другие могут быть одно- и многоступенчатые.
По величине создаваемого давления компрессоры делятся на компрессоры низкого давления (р≤10
По величине создаваемого давления компрессоры делятся на компрессоры низкого давления (р≤10
Компрессоры со степенью повышения давления ε=1,1 – 4,0 относят к газодувным машинам, среди которых вентиляторы (ε=1,0 – 1,15). Машины, в которых понижается давление называют вакуум-насосами (степень ваку-умирования ε=1,0 – 50).
Важнейшие показатели компрессоров
К числу важнейших показателей компрессоров относят:
- степень повышения
Важнейшие показатели компрессоров
К числу важнейших показателей компрессоров относят:
- степень повышения
- производительность, Q м3/с или G кг/с;
- изотермический кпд компрессора ηиз=Аиз/Афакт;
- удельная масса m=M/ Q, кг/м3/час.
Основные параметры газов
Это физические величины, определяющие состояние газа. К ним относят:
Основные параметры газов
Это физические величины, определяющие состояние газа. К ним относят:
Параметры идеального газа связаны уравнением состояния:
где R – газовая постоянная, R=848/М (М – молекулярный вес газа); ν – удельный объём газа; Т=t +273 – температура в градусах Кельвина.
Теплоёмкость
где q – количество тепла, подведенного к 1 кг газа.
Различают изобарную cp и изохорную cv теплоёмкость cp= cv+AR,
А=1/427 какл/кгм.
cp/ cv=к – показатель адиабаты, к=1+2/i i – число степеней свободы молекул газа (для одноатомных i=3, для двухатомных i=5, для трехатомных i=6).




 Реактивное движение. Ракеты
Реактивное движение. Ракеты Магнитное поле Земли. Влияние магнитного поля Земли на человека
Магнитное поле Земли. Влияние магнитного поля Земли на человека Військові засоби зарядки акумуляторних батарей. Генератори постійного струму. (Тема 3.2)
Військові засоби зарядки акумуляторних батарей. Генератори постійного струму. (Тема 3.2) Лекция №6 (6 ). Поле системы элементарных излучателей
Лекция №6 (6 ). Поле системы элементарных излучателей Закон сохранения механической энергии. Механические колебания
Закон сохранения механической энергии. Механические колебания Понятие о радиоволнах. Деление волн на диапазоны. Основные физические свойства радиоволн. Распространение радиоволн
Понятие о радиоволнах. Деление волн на диапазоны. Основные физические свойства радиоволн. Распространение радиоволн Биофизика анализаторов. Модальность
Биофизика анализаторов. Модальность Работа и мощность силы. Консервативные силы, работа консервативных сил. Потенциальная и кинетическая энергия
Работа и мощность силы. Консервативные силы, работа консервативных сил. Потенциальная и кинетическая энергия Открытие радиоактивности. Радиоактивные превращения
Открытие радиоактивности. Радиоактивные превращения  Общие теоремы динамики материальной точки
Общие теоремы динамики материальной точки Аеродинаміка та динаміка польоту літака. Характеристики профілю крила. Центр тиску та фокус профілю. (Лекція 4.2.3)
Аеродинаміка та динаміка польоту літака. Характеристики профілю крила. Центр тиску та фокус профілю. (Лекція 4.2.3) Государственная система обеспечения единства измерений. Единицы величин
Государственная система обеспечения единства измерений. Единицы величин Поверхностное упрочнение деталей. (Лекция 11)
Поверхностное упрочнение деталей. (Лекция 11) Электротехника. Основные понятия и законы. (лекция 2)
Электротехника. Основные понятия и законы. (лекция 2) Аттестационная работа. Методическя разработка по физике: Замена человека на производстве роботизированный манипулятор
Аттестационная работа. Методическя разработка по физике: Замена человека на производстве роботизированный манипулятор История создания лампы накаливания Автор: учитель физики Зыков В.А., МБОУ СОШ №13 г. Балаково Саратовской области
История создания лампы накаливания Автор: учитель физики Зыков В.А., МБОУ СОШ №13 г. Балаково Саратовской области Альтернативные виды энергии
Альтернативные виды энергии Энергия и Момент Импульса (Energy and Angular Momentum)
Энергия и Момент Импульса (Energy and Angular Momentum) Лазерное излучение
Лазерное излучение Параметры антенн. Антенно-фидерные устройства и распространение радиоволн. Основы теории антенн
Параметры антенн. Антенно-фидерные устройства и распространение радиоволн. Основы теории антенн Особливості функціонування лінійних та нелінійних кіл. Зворотні зв'язки в електричних колах
Особливості функціонування лінійних та нелінійних кіл. Зворотні зв'язки в електричних колах Електричний заряд. Електростатичний захист
Електричний заряд. Електростатичний захист Машины постоянного тока. Устройство, материалы и принцип действия. Карточка 16
Машины постоянного тока. Устройство, материалы и принцип действия. Карточка 16 Механические волны
Механические волны Алгоритм решения задач по теме «Динамика»
Алгоритм решения задач по теме «Динамика» Дмитрий Аполлинариевич Рожанский
Дмитрий Аполлинариевич Рожанский Агрегатное состояние вещества Приготовила:Верхозина Анастасия
Агрегатное состояние вещества Приготовила:Верхозина Анастасия  Конвекция. Примеры конвекции
Конвекция. Примеры конвекции