Содержание
- 2. Реальный газ Межмолекулярные взаимодействия. Уравнение состояния реального газа (Уравнение Ван дер Ваальса). Изотермы реального газа. Критические
- 3. Реальный газ Идеальный газ: пренебрегали межмолекулярным взаимодействием собственным объёмом молекул При больших плотностях газа и при
- 4. Межмолекулярные силы действуют на расстояниях Между молекулами действуют как силы притяжения, так и отталкивания: Межмолекулярные взаимодействия
- 5. Межмолекулярные взаимодействия
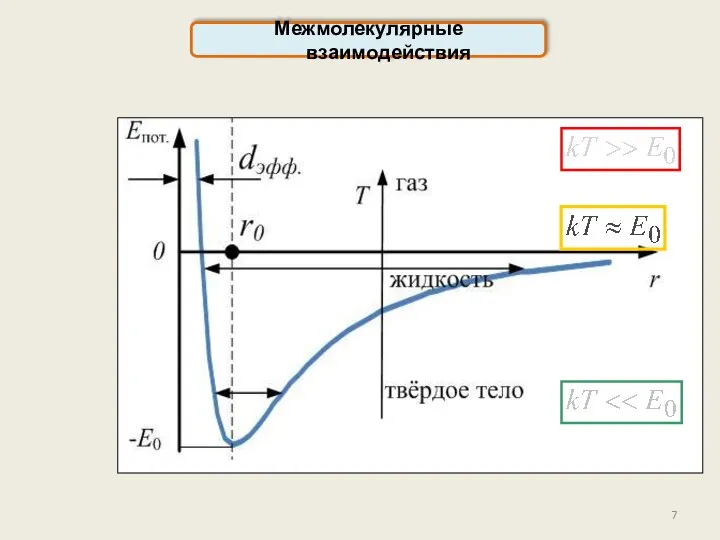
- 6. Равновесное расстояние: минимум потенциальной энергии взаимодействия молекул Межмолекулярные взаимодействия
- 7. Межмолекулярные взаимодействия
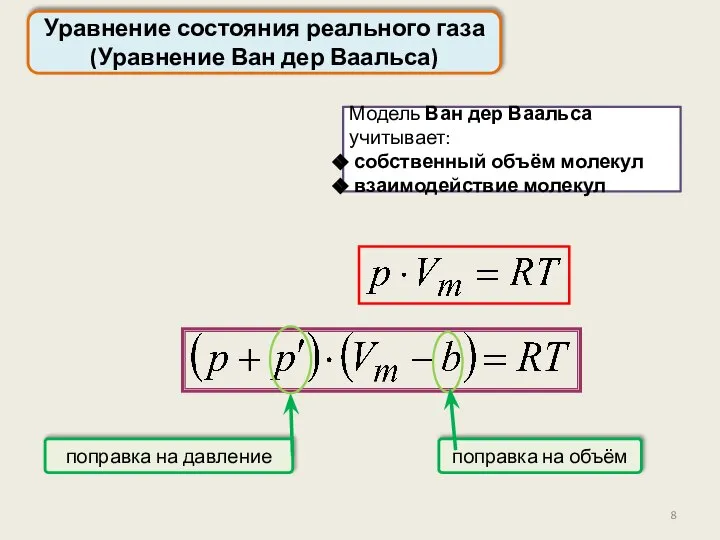
- 8. Уравнение состояния реального газа (Уравнение Ван дер Ваальса) поправка на объём Модель Ван дер Ваальса учитывает:
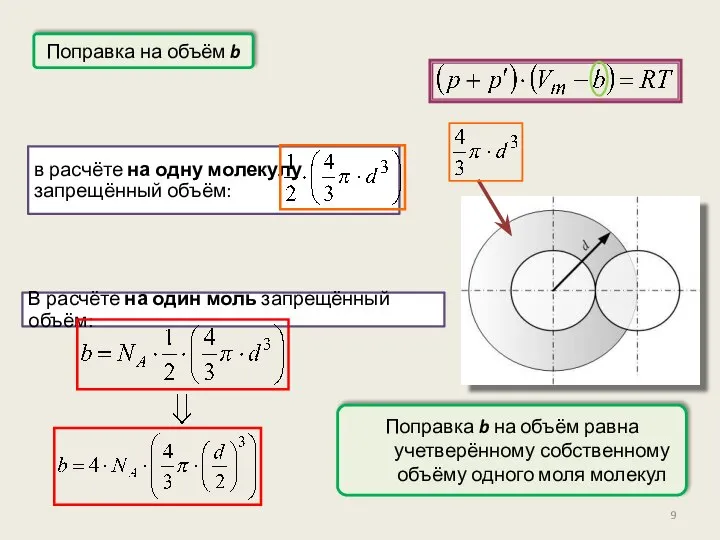
- 9. Поправка на объём b в расчёте на одну молекулу запрещённый объём: В расчёте на один моль
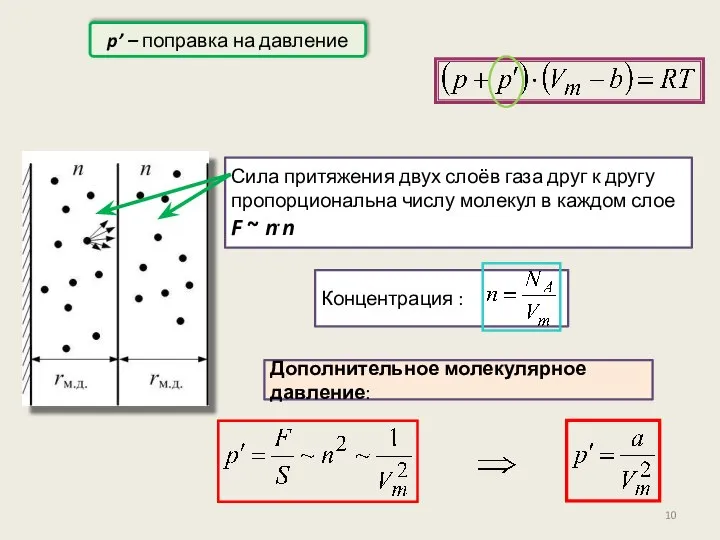
- 10. p’ – поправка на давление Сила притяжения двух слоёв газа друг к другу пропорциональна числу молекул
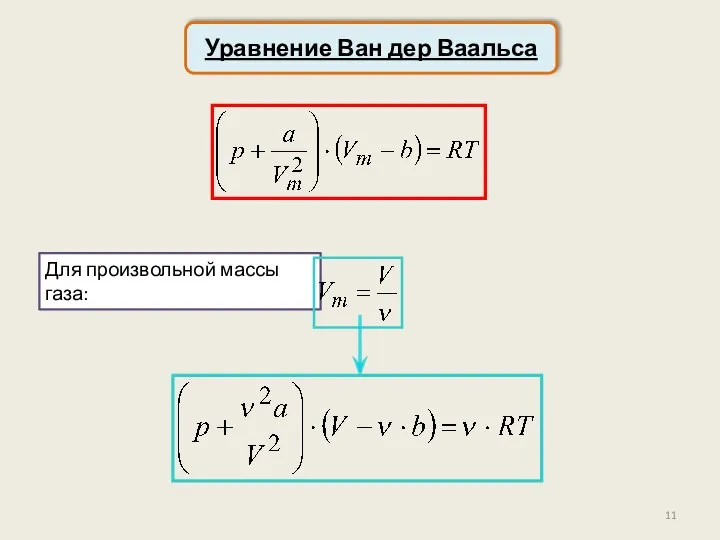
- 11. Уравнение Ван дер Ваальса Для произвольной массы газа:
- 12. Уравнение Ван дер Ваальса Замечание 1: при высоких температурах и низких плотностях (низком давлении) молярный объём
- 13. Уравнение Ван дер Ваальса Замечание 2: уравнение Ван дер Ваальса – одна из возможных моделей. Эта
- 14. Изотермы реального газа. Критические параметры Обозначение:
- 15. Изотермы реального газа. Критические параметры Это уравнение третьей степени относительно объёма В общем случае оно имеет
- 16. Изотермы реального газа. Критические параметры Критическая изотерма Критическая точка По уравнению Ван дер Ваальса Эксперимент
- 17. Изотермы реального газа. Критические параметры Критическая изотерма перегретая жидкость Растянутая жидкость переохлаждённый пар
- 18. Критическое состояние Критическое состояние – особое состояние вещества, пограничное между паром и жидкостью Критическая точка –
- 19. Критическое состояние В критической точке уравнение Ван дер Ваальса имеет три одинаковых корня, поэтому его можно
- 20. Критическое состояние Связь между критическими параметрами pк , Tк и Vк и поправочными коэффициентами a и
- 21. Критическое состояние
- 22. Внутренняя энергия реального газа Внутренняя энергия реального газа равна сумме: кинетической энергии хаотического движения молекул потенциальной
- 23. Внутренняя энергия реального газа Внутренняя энергия произвольного количества газа
- 24. Фазы и фазовые переходы Фаза – термодинамически равновесное однородное по физическим свойствам состояние вещества Графит и
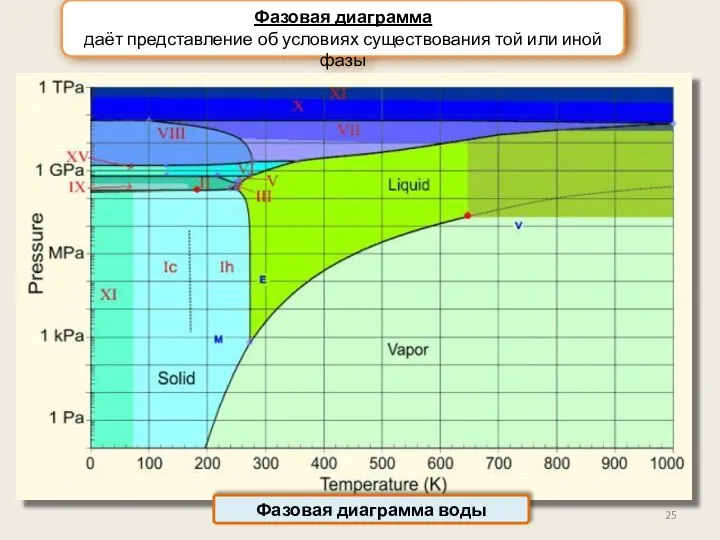
- 25. Фазовая диаграмма даёт представление об условиях существования той или иной фазы Фазовая диаграмма воды
- 26. Фазы и фазовые переходы
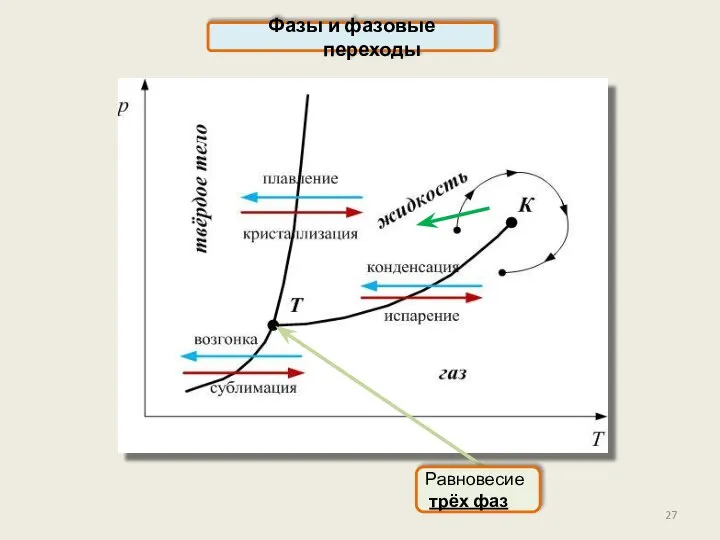
- 27. Фазы и фазовые переходы Равновесие трёх фаз
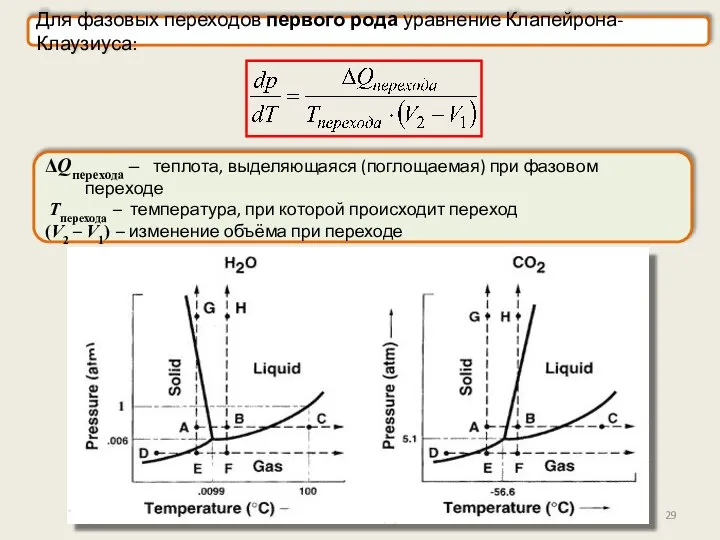
- 28. Фазы и фазовые переходы Все агрегатные превращения – это фазовые переходы первого рода: парообразование, конденсация, сублимация,
- 29. ΔQперехода – теплота, выделяющаяся (поглощаемая) при фазовом переходе Tперехода – температура, при которой происходит переход (V2
- 30. Фазы и фазовые переходы При фазовых переходах второго рода скачкообразно меняются свойства вещества: теплоёмкость, вязкость, ферромагнитные
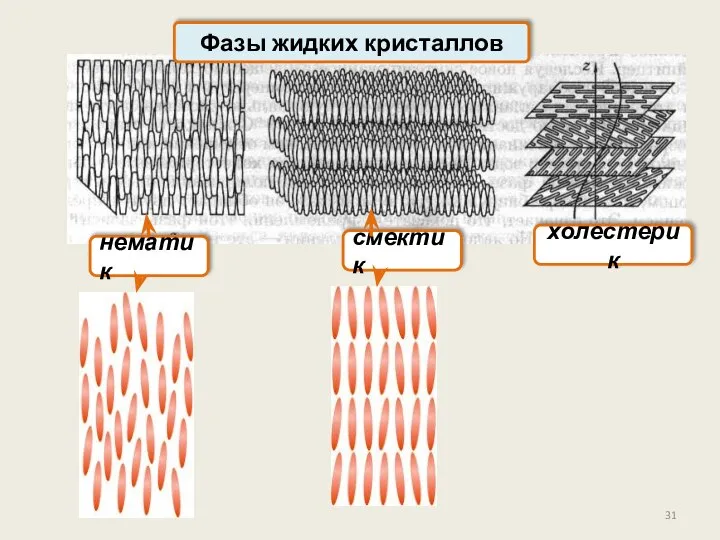
- 31. Фазы жидких кристаллов нематик смектик холестерик
- 32. – промежуточное между газом и твёрдым телом: сочетает свойства того и другого. Жидкое состояние Газ Дальний
- 33. С возрастанием температуры молекулы становятся более подвижными Теории жидкости, объясняющей все её свойства, нет. Некоторые проблемы
- 34. Сохраняют форму, как кристаллические Свойства аморфных тел: Вязкость жидкости при понижении температуры может так сильно увеличиваться,
- 35. Аморфные тела Изотропны Дальний порядок Жидкости Кристаллические тела Ближний порядок Анизотропны
- 36. Жидкие кристаллы В жидких кристаллах в пределах значительного объёма наблюдается одинаковая ориентация молекул (если, например, молекулы
- 37. Поверхностное натяжение Сфера молекулярного действия – сфера с радиусом, равным радиусу молекулярного действия. Любая молекула, находящаяся
- 38. Для перемещения молекулы из глубины жидкости на поверхность молекула должна затратить энергию, следовательно, за счёт своей
- 39. Капли воды на МКС
- 40. α - коэффициент поверхностного натяжения численно равен силе поверхностного натяжения, приходящейся на единицу длины контура
- 41. Давление под искривлённой поверхностью. Формула Лапласа Поверхностная плёнка стремится к сокращению → создаётся дополнительное давление Δp
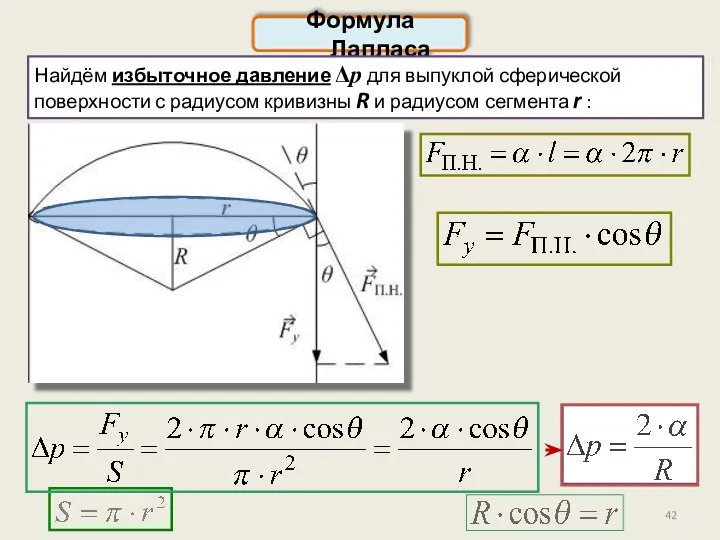
- 42. Формула Лапласа Найдём избыточное давление Δp для выпуклой сферической поверхности с радиусом кривизны R и радиусом
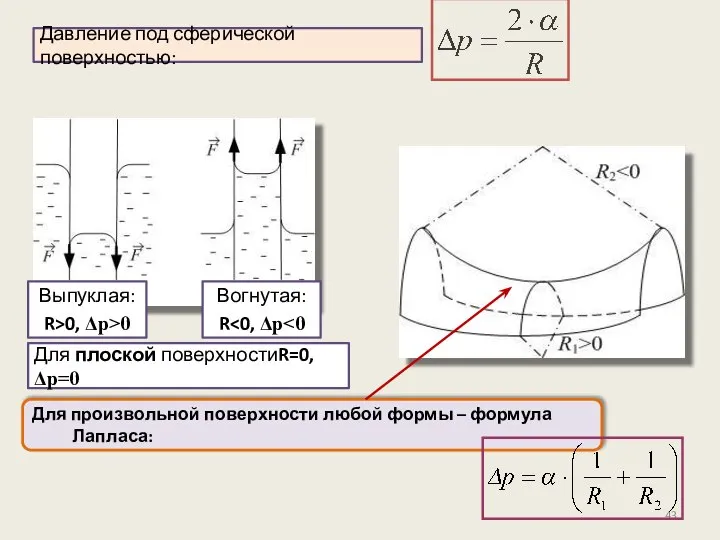
- 43. Для произвольной поверхности любой формы – формула Лапласа: Давление под сферической поверхностью: Для плоской поверхностиR=0, Δp=0
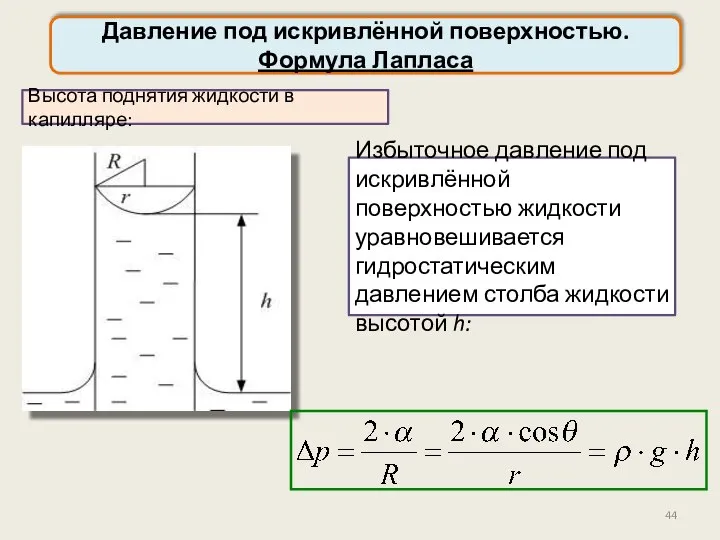
- 44. Давление под искривлённой поверхностью. Формула Лапласа Высота поднятия жидкости в капилляре: Избыточное давление под искривлённой поверхностью
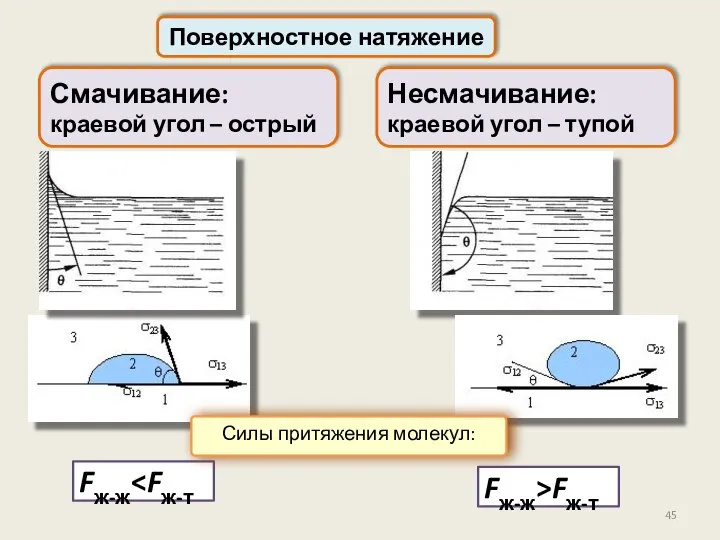
- 45. Поверхностное натяжение Fж-ж Смачивание: краевой угол – острый Несмачивание: краевой угол – тупой Fж-ж>Fж-т Силы притяжения
- 46. кристаллические Твёрдые тела аморфные Примеры: Воск Смолы (битум, янтарь) Стёкла (обсидиан , опал) Клеи Полимеры с
- 47. кристаллические Твёрдые тела аморфные дальний порядок в расположении частиц ближний порядок в расположении частиц
- 48. Кристаллы анизотропны Твёрдые тела Их свойства различны в зависимости от направления внутри кристалла, потому что на
- 49. Кристаллическое состояние Существует 230 видов кристаллических решёток с различным типом симметрии Всякий кристалл может быть получен
- 51. каждый из 8 атомов в вершинах куба принадлежит данной ячейке и семи соседним Простейшая решётка –
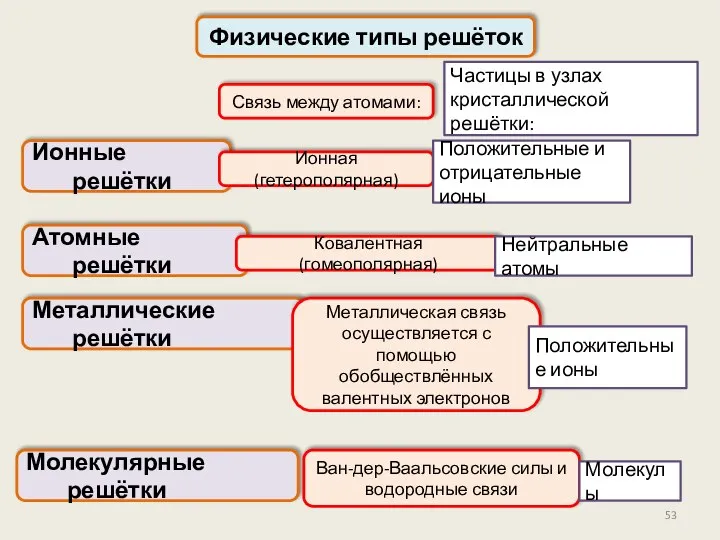
- 52. Физические типы решёток Ионные решётки В зависимости от природы частиц в узлах кристаллической решетки и характера
- 53. Физические типы решёток Ионные решётки Частицы в узлах кристаллической решётки: Ионная (гетерополярная) Атомные решётки Металлические решётки
- 54. Кривая зависимости потенциальной энергии взаимодействия двух частиц от расстояния между ними несимметрична Тепловое расширение твёрдых тел
- 55. Тепловое расширение твёрдых тел Линейные размеры тела при температуре t0 C равны: Коэффициент линейного теплового расширения
- 56. Объём тела при температуре t0 C равен: Коэффициент объёмного теплового расширения β численно равен относительному увеличению
- 57. Число колебательных степени свободы i=3 Теплоёмкость твёрдых тел По теореме о равнораспределении Кинетическая энергия Потенциальная энергия
- 58. Молярная теплоёмкость: Теплоёмкость твёрдых тел. Закон Дюлонга и Пти Молярная теплоёмкость всех химически простых тел одинакова,
- 60. Скачать презентацию










































 Применение законов физики в повседневной жизни
Применение законов физики в повседневной жизни Ядерно-химические свойства
Ядерно-химические свойства Max.Industries. Технология термоядерного реактора
Max.Industries. Технология термоядерного реактора Квантование момента импульса атома. Момент импульса многоэлектронных атомов
Квантование момента импульса атома. Момент импульса многоэлектронных атомов Измерение сопротивления изоляции постоянному току
Измерение сопротивления изоляции постоянному току Тепловое излучение
Тепловое излучение Внутренняя энергия и способы ее изменения
Внутренняя энергия и способы ее изменения Теплові двигуни та охорона навколишнього середовища
Теплові двигуни та охорона навколишнього середовища  Проект Эко-солнце г. Королев 2014 год
Проект Эко-солнце г. Королев 2014 год Открытие нейтрона
Открытие нейтрона Конденсаторы в цепи постоянного тока
Конденсаторы в цепи постоянного тока Резисторы. Основные параметры резисторов
Резисторы. Основные параметры резисторов Презентация по физике "Изопроцессы" - скачать
Презентация по физике "Изопроцессы" - скачать  Презентация по физике "Приручение огня" - скачать бесплатно
Презентация по физике "Приручение огня" - скачать бесплатно Тема урока Приложения определенного интеграла к решению физических задач
Тема урока Приложения определенного интеграла к решению физических задач Елементи режимів різання. Визначення режимів різання. Тема 8
Елементи режимів різання. Визначення режимів різання. Тема 8 Детали машин и основы конструирования. Лекция №4
Детали машин и основы конструирования. Лекция №4 Електричний заряд. Електростатичне поле. Конденсатори
Електричний заряд. Електростатичне поле. Конденсатори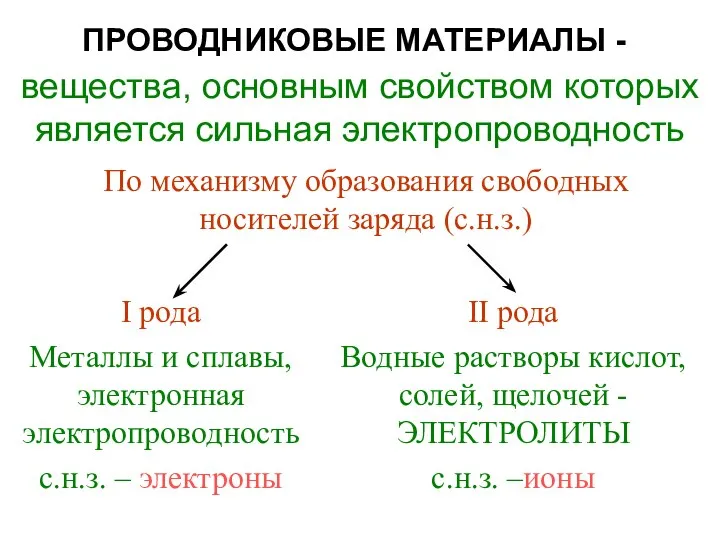 Проводниковые материалы
Проводниковые материалы Обертальний рух твердого тіла
Обертальний рух твердого тіла Класифікація та моделі сигналів та систем. (Лекція 1)
Класифікація та моделі сигналів та систем. (Лекція 1) Избавляемся от статического электричества (Фрагмент урока по теме «Электризация тел») Выполнила Васильева Марина Викторовн
Избавляемся от статического электричества (Фрагмент урока по теме «Электризация тел») Выполнила Васильева Марина Викторовн Газовые законы (10 класс) - Презентация по физике_
Газовые законы (10 класс) - Презентация по физике_ Электрические системы
Электрические системы Электростатическое поле в вакууме
Электростатическое поле в вакууме Элементы квантовой статистики и физики твёрдого тела. Лекция № 6. Часть 1
Элементы квантовой статистики и физики твёрдого тела. Лекция № 6. Часть 1 Своя игра
Своя игра Основы кинематики и динамики
Основы кинематики и динамики