- Главная
- Физика
-
Лекция 16 Тема: Равновесные состояния и процессы, их изображение на термодинамических диаграммах.

Содержание
- 2. Среди равновесных процессов, происходящих с термодинамическими системами, выделяются изопроцессы, при которых один из основных параметров состояния
- 3. Изобарный процесс (p=const). Диаграмма этого процесса (изобара) в координатах р, V изображается прямой, параллельной оси V.
- 4. его внутренняя энергия возрастает на величину (согласно формуле ( ) При этом газ совершит работу, определяемую
- 5. т. е. все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил: (4)
- 8. Графически можно изображать только равновесные процессы-процессы, состоящие из последовательности равновесных состояний. Они протекают так, что изменение
- 9. Изобарный процесс (p=const). Диаграмма этого процесса (изобара) в координатах р, V изображается прямой, параллельной оси V.
- 10. Изотермический процесс (Т= const). Как уже указывалось раньше, изотермический процесс описывается законом Бойля—Мариотта: pV= const. Так
- 12. Скачать презентацию
Среди равновесных процессов, происходящих с термодинамическими системами, выделяются изопроцессы, при которых
Среди равновесных процессов, происходящих с термодинамическими системами, выделяются изопроцессы, при которых
Изохорный процесс (V=const). Диаграмма этого процесса (изохора) в координатах р, V изображается прямой, параллельной оси ординат (рис. 1), где процесс 1—2 есть изохорное нагревание, а 1—3 — изохорное охлаждение. При изохорном процессе газ не совершает работы над внешними телами, т. е.
Рисунок 1
Как уже указывалось в предыдущем лекции, из первого начала термодинамики (δQ=dU+δA) для изохорного процесса следует, что вся теплота, сообщаемая газу, идет на увеличение его внутренней энергии:
Согласно формуле ( ),
Тогда для произвольной массы газа получим
(1)
Изобарный процесс (p=const). Диаграмма этого процесса (изобара) в координатах р, V
Изобарный процесс (p=const). Диаграмма этого процесса (изобара) в координатах р, V
(2)
и определяется площадью заштрихованного прямоугольника (рис. 2). Если использовать уравнение
( ) Клапейрона — Менделеева для выбранных нами двух состояний, то
Рисунок 2
откуда
Тогда выражение ( 2) для работы изобарного расширения примет вид
(3)
Из этого выражения вытекает физический смысл молярной газовой постоянной R: если T2 —T1 =1 К, то для 1 моль газа R=A, т. е. R численно равна работе изобарного расширения 1 моль идеального газа при нагревании его на 1 К.
В изобарном процессе при сообщении газу массой т количества теплоты
его внутренняя энергия возрастает на величину (согласно формуле ( )
При этом
его внутренняя энергия возрастает на величину (согласно формуле ( )
При этом
Изотермический процесс (T=const). Как уже указывалось, изотермический процесс описывается законом Бойля—Мариотта:
Диаграмма этого процесса (изотерма) в координатах р, V представляет собой гиперболу (см. рис. 60), расположенную на диаграмме тем выше, чем выше температура, при которой происходит процесс.
Исходя из выражений ( ) и ( ) найдем работу изотермического расширения газа:
Рисунок 3
Так как при Т=const внутренняя энергия идеального газа не изменяется:
то из первого начала термодинамики (δQ=dU+δA) следует, что для изотермического процесса
т. е. все количество теплоты, сообщаемое газу, расходуется на совершение им
т. е. все количество теплоты, сообщаемое газу, расходуется на совершение им
(4)
Следовательно, для того чтобы при расширении газа температура не понижалась, к газу в течение изотермического процесса необходимо подводить количество теплоты, эквивалентное внешней работе расширения.
Графически можно изображать только равновесные процессы-процессы, состоящие из последовательности равновесных
Графически можно изображать только равновесные процессы-процессы, состоящие из последовательности равновесных
Среди равновесных процессов, происходящих с термодинамическими системами, выделяются изопроцессы, при которых один из основных параметров состояния сохраняется постоянным.
Изохорный процесс (V= const). Диаграмма этого процесса (изохора) в координатах р, V изображается прямой, параллельной оси ординат (рис. 1), где процесс 1—2 есть изохорное нагревание, а 1-3 - изохорное охлаждение. При изохорном процессе газ не совершает работы над внешними телами, т. е.как уже указывалось,из первого начала термодинамики ( ) для изохорного процесса следует, что вся теплота, сообщаемая газу, идет на увеличение его внутренней энергии:
δQ = dU.
δА = pdV = 0.
(
)
Согласно формуле
,отсюда вытекает, что
Тогда для произвольной массы газа получим
(1)
Изобарный процесс (p=const). Диаграмма этого процесса (изобара) в координатах р,
Изобарный процесс (p=const). Диаграмма этого процесса (изобара) в координатах р,
Если использовать уравнение Клапейрона - Менделеева для выбранных нами двух состояний, то
Тогда выражение (7) для работы изобарного расширения примет вид
Из этого выражения вытекает физический смысл молярной газовой постоянной R: если
, то для 1 моль газа R=A, т. е. R численно равна работе изобарного расширения
его внутренняя энергия возрастает на величину (согласно формуле (3)).
При этом газ совершит работу, определяемую выражением (3.
(2)
1 моль идеального газа при нагревании его на 1 К.
В изобарном процессе при сообщении газу массой т количества теплоты
Изотермический процесс (Т= const). Как уже указывалось раньше, изотермический процесс
Изотермический процесс (Т= const). Как уже указывалось раньше, изотермический процесс
pV= const.
Так как при Т= const внутренняя энергия идеального газа не изменяется:
то из первого начала термодинамики (δQ=dU+δA) следует, что для изотермического процесса
δQ = δА.
т. е. все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил:
Следовательно, для того чтобы при расширении газа температура не понижалась, к газу в течение изотермического процесса необходимо подводить количество теплоты, эквивалентное внешней работе расширения.









 Физический диктант по теме: «Магнитное поле»
Физический диктант по теме: «Магнитное поле» Электромагнитная индукция
Электромагнитная индукция Методы измерения токов и напряжений. Метрология, стандартизация и сертификация в телекоммуникациях
Методы измерения токов и напряжений. Метрология, стандартизация и сертификация в телекоммуникациях Механическая работа, мощность. 10 класс
Механическая работа, мощность. 10 класс Плоская и пространственная система сил
Плоская и пространственная система сил Применение лазерных технологий («лазерный пинцет») для исследования динамики наномашин
Применение лазерных технологий («лазерный пинцет») для исследования динамики наномашин Основи спектроскопії. Характеристика і діапазони електромагнітного випромінювання
Основи спектроскопії. Характеристика і діапазони електромагнітного випромінювання Физико-химические методы анализа. Хроматография
Физико-химические методы анализа. Хроматография Сила тяжести. Вес тела. Сила упругости. Решение задач
Сила тяжести. Вес тела. Сила упругости. Решение задач Підготувала учениця 9 класу Нікуліна Єлизавета Вчитель: Підлубна Лілія Миколаївна Володимирівська ЗОШ І-ІІІ ст.
Підготувала учениця 9 класу Нікуліна Єлизавета Вчитель: Підлубна Лілія Миколаївна Володимирівська ЗОШ І-ІІІ ст.  Механика. Основные разделы механики
Механика. Основные разделы механики Движение в поле силы тяжести. Свободное падение
Движение в поле силы тяжести. Свободное падение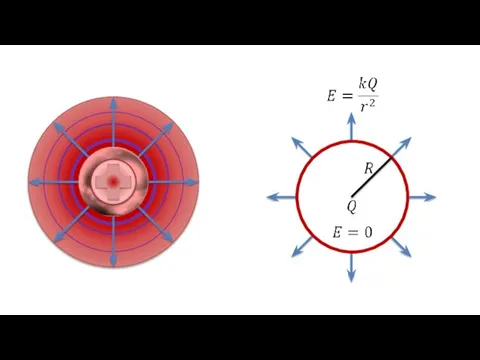 Напряженность заряженного шара
Напряженность заряженного шара Сила Лоренца
Сила Лоренца урок 37. Расчёт давления жидкости на дно и стенки сосуда
урок 37. Расчёт давления жидкости на дно и стенки сосуда Электрические явления
Электрические явления Холодильные процессы
Холодильные процессы История развития электронных двигателей
История развития электронных двигателей Что изучает физика. Некоторые физические термины. Наблюдения и опыты
Что изучает физика. Некоторые физические термины. Наблюдения и опыты Биологическое действие радиации. Закон радиоактивного распада
Биологическое действие радиации. Закон радиоактивного распада Магниты. Магнитное поле, его свойства. Магнитное поле Земли
Магниты. Магнитное поле, его свойства. Магнитное поле Земли Элементы релятивистской механики. (Лекция 10)
Элементы релятивистской механики. (Лекция 10) Тезисы. Естественное освещение. КЕО
Тезисы. Естественное освещение. КЕО Основы гидравлики
Основы гидравлики Створення моделі іонного двигуна та дослідження його характеристик
Створення моделі іонного двигуна та дослідження його характеристик Атом и атомное ядро
Атом и атомное ядро Информационное моделирование заводной сектор мотоцикла Минск
Информационное моделирование заводной сектор мотоцикла Минск Физические основы телевидения.
Физические основы телевидения.