Содержание
- 2. Литература: 1. Кудрявцев Б.Б., Курс физики: Теплота и молекулярная физика. – М.: Учпедгиз, 1960. 210 с.
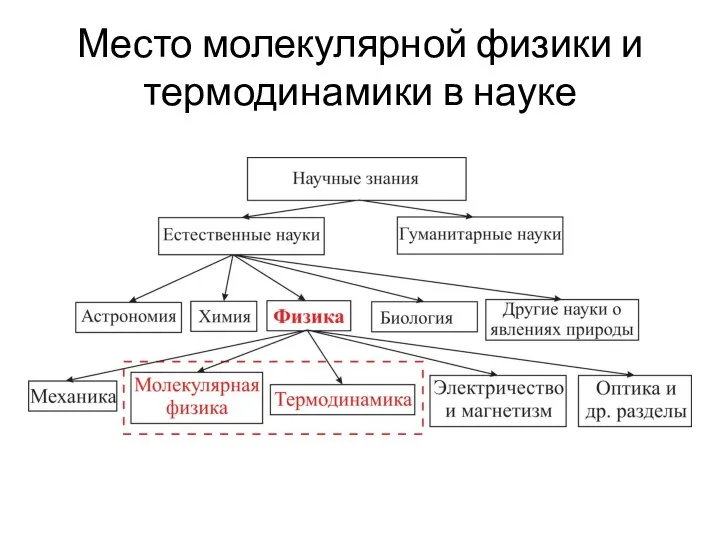
- 3. Место молекулярной физики и термодинамики в науке
- 4. § 1. Молекулярно кинетическая теория газов и термодинамика Молекулярная физика представляет собой раздел физики, изучающий строение
- 5. Броуновское движение Броуновское движение - тепловое движение взвешенных в жидкости или газе частиц.
- 6. Из истории развития МКТ Фундаментом МКТ является атомистическая гипотеза: все тела в природе состоят из мельчайших
- 7. Молекулярно-кинетическая теория ставит себе целью истолковать те свойства тел, которые непосредственно наблюдаются на опыте (Р, Т,
- 8. § 2. Состояние системы. Процесс. Системой тел, или просто системой называется совокупность рассматриваемых тел. Пример системы:
- 9. Всякий процесс, т.е. переход системы из одного состояния в другое, связан с нарушением равновесия системы. Всякий
- 10. Идеальный газ. Основные свойства. 1. Собственный объем идеального газа пренебрежимо мал по сравнению с объемом сосуда,
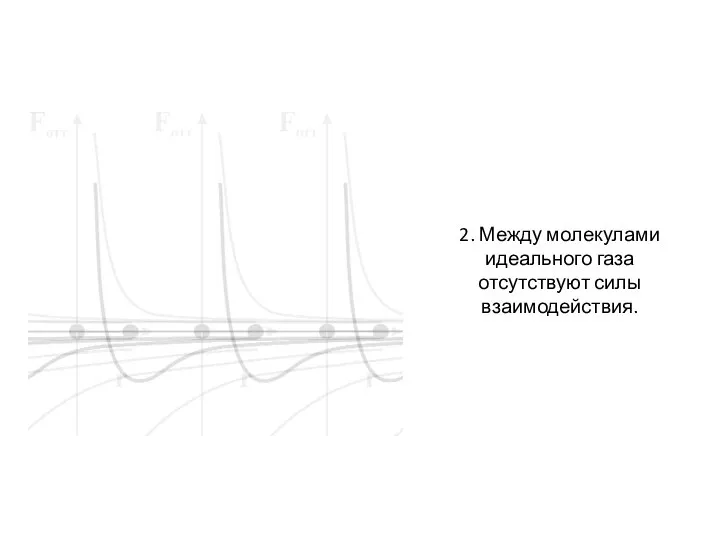
- 11. 2. Между молекулами идеального газа отсутствуют силы взаимодействия.
- 12. 3. Столкновения молекул идеального газа между собой и со стенками сосуда абсолютно упругие.
- 13. § 3. Уравнение состояния идеального газа Состояние некоторой массы газа определяется значением трех параметров: Р, Т,
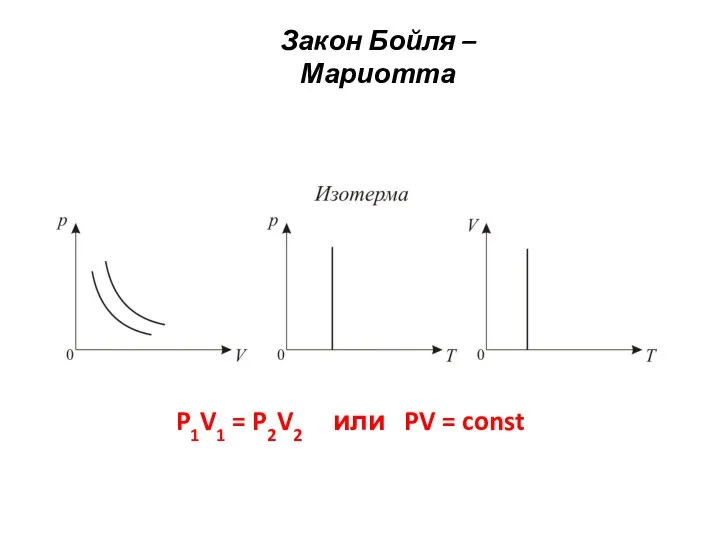
- 14. Закон Бойля – Мариотта Изотермический процесс. Изотермическим процессом называется процесс, протекающий при постоянной температуре T =
- 15. Закон Бойля – Мариотта P1V1 = P2V2 T1 T2 T1 или PV = const
- 16. Закон Гей-Люссака Изобарный процесс – процесс изменения состояния определенной массы газа при постоянном давлении Изобарный процесс
- 17. Закон Гей-Люссака P = const V = V0 + kt При t = - 273 V
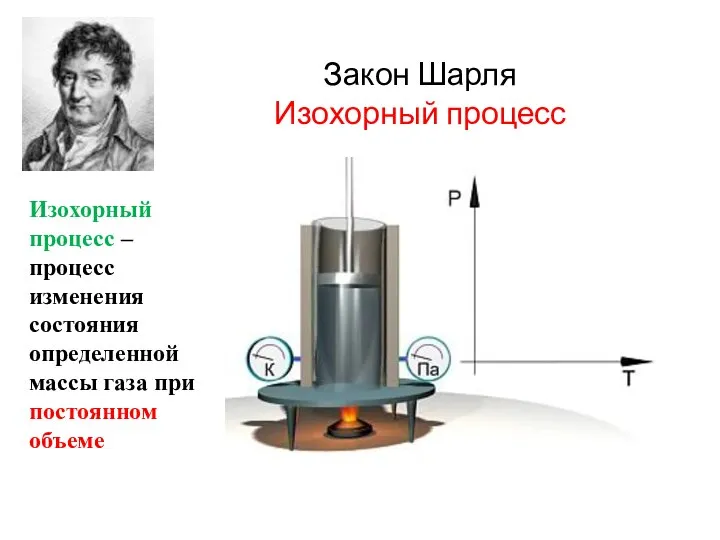
- 18. Закон Шарля Изохорный процесс Изохорный процесс – процесс изменения состояния определенной массы газа при постоянном объеме
- 19. Закон Шарля V = const P = P0 + kt При t = - 273 P
- 20. Переход к температурной шкале Кельвина
- 21. Атомная единица массы. Количество вещества. Число Авогадро. Молярная масса. Атомная единица массы (а.е.м.) – mед –
- 22. Уравнение Клайперона Объединив уравнения Бойля – Мариотта и Шарля, можно найти уравнение идеального газа:
- 23. Универсальная газовая постоянная ; , где В – постоянная для данной массы газа; , где R
- 24. § 4. Основные положения МКТ 1. Вещество состоит из мельчайших частиц атомов или молекул, находящихся в
- 25. § 5. Основное уравнение МКТ У реальных газов молекулы обладают конечными размерами и взаимодействуют друг с
- 26. Отношение Δp1/Δt дает силу, действующую на ΔS, а отношение этой силы к ΔS есть давление P.
- 27. Вычислим импульс, сообщаемый стенке сосуда ударяющейся о нее молекулой. Импульсы молекулы до и после удара о
- 28. Δp/Δt – сила, действующая на площадку, Δp/(Δt ΔS) – давление газа, оказываемое им на стенку сосуда.
- 29. Домножим обе части уравнения на молярный объем. PVмоль = 2/3 (n Vмоль)E (n Vмоль) = NА
- 30. Из полученного выражения следует важный вывод: абсолютная температура есть величина, пропорциональная средней энергии движения молекул. Этот
- 31. § 6. Следствие из основного уравнения Воспользуемся полученной формулой: P = nkT Поскольку k = R/NА,
- 32. Если имеется смесь нескольких газов, разные по массе молекулы будут иметь различную скорость, но средняя энергия
- 33. Давление, обусловленное молекулами какого-либо одного сорта, при условии, что они присутствуют в сосуде в том количестве,
- 34. § 7. Распределение молекул газа в поле земного тяготения Действие силы тяжести приводит не только к
- 35. Давление газа во втором сечении будет на dp меньше чем в первом сечении, т.е. будет равно
- 36. Поскольку P = nkT = nhTR/NA , то Приравняем (1) к (2), получим: -nhmgdh = dnhTR/NA
- 37. При h = 0 nh = n0 следовательно const = ln n0, тогда ……………..(3) Поскольку mnh
- 38. Из (3), домножая на кТ получаем: Данная формула впервые была получена Лапласом и называется барометрической формулой
- 39. § 8. Распределение Больцмана Из уравнения легко получить, что где m – масса одной молекулы, k
- 40. На разной высоте молекула обладает различным запасом потенциальной энергии: En = mgh. Следовательно, распределение молекул по
- 41. как и вытекающая из него формула справедливы не только в случае потенциального поля сил Земного тяготения,
- 42. § 7. Опыты Перрена. Экспериментальное определение числа Авогадро. Работы Перрена, сыгравшие исключительную роль в деле утверждения
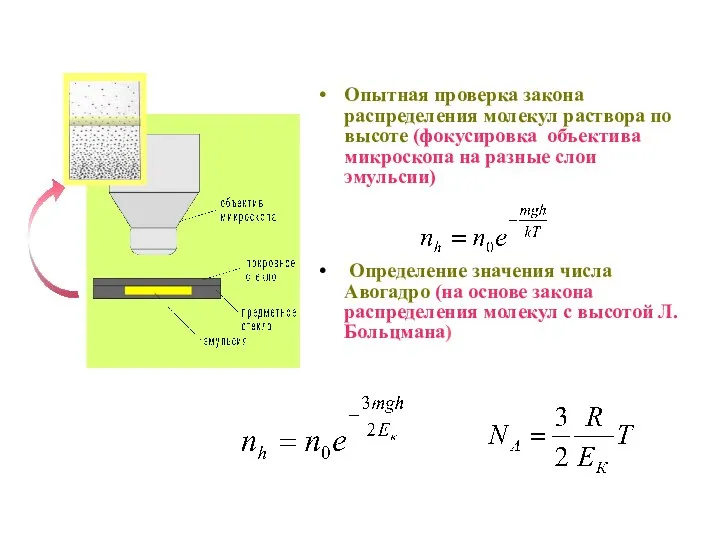
- 43. Опытная проверка закона распределения молекул раствора по высоте (фокусировка объектива микроскопа на разные слои эмульсии) Определение
- 45. Скачать презентацию





































 Мгновенные источники тепла
Мгновенные источники тепла Взаимодействие гамма-излучения с веществом
Взаимодействие гамма-излучения с веществом Оптические приборы
Оптические приборы Радиоактивное загрязнение территории
Радиоактивное загрязнение территории Открытие и применение закона всемирного тяготения
Открытие и применение закона всемирного тяготения Равновесие тел урок физики, 10 класс
Равновесие тел урок физики, 10 класс Структура и спектрально-люминесцентные характеристики керамики Y2O3:Er
Структура и спектрально-люминесцентные характеристики керамики Y2O3:Er Движение по окружности
Движение по окружности Волны Эллиотта
Волны Эллиотта Аттестационная работа. Использование конструктора LEGO. Технология и физика во внеурочной деятельности
Аттестационная работа. Использование конструктора LEGO. Технология и физика во внеурочной деятельности Линзы
Линзы Свойства электромагнитных излучений, спектр излучений, области их применения
Свойства электромагнитных излучений, спектр излучений, области их применения Звук
Звук Использование информационных технологий в школьном лабораторном эксперименте: определение ускорения свободного падения
Использование информационных технологий в школьном лабораторном эксперименте: определение ускорения свободного падения Динаміка матеріальної точки та поступального руху
Динаміка матеріальної точки та поступального руху Транспортные системы ОФ. Расчет пирамидального бункера
Транспортные системы ОФ. Расчет пирамидального бункера Простейшие движения твердых тел
Простейшие движения твердых тел Нейтронно-физические эксперименты в физике ядерных реакторов
Нейтронно-физические эксперименты в физике ядерных реакторов Биофизика и ее место в естествознании. Физическая сущность методов диагностики, применяемых в медицине и ветеринарии
Биофизика и ее место в естествознании. Физическая сущность методов диагностики, применяемых в медицине и ветеринарии Квантовая физика- раздел современной физики, в котором изучаются свойства, строение атомов и молекул, движение и взаимодействи
Квантовая физика- раздел современной физики, в котором изучаются свойства, строение атомов и молекул, движение и взаимодействи Решение задач. Подготовка к контрольной работе №8 по теме «Световые явления»
Решение задач. Подготовка к контрольной работе №8 по теме «Световые явления» Гравиметрия. Гравитационное поле
Гравиметрия. Гравитационное поле Властивості рідин. Поверхневий натяг
Властивості рідин. Поверхневий натяг  Термодинамикалық заң
Термодинамикалық заң Улучшение технико-экономичиских показателей при эксплуатации судовой энергетической установки
Улучшение технико-экономичиских показателей при эксплуатации судовой энергетической установки Принцип действия и КПД тепловых двигателей
Принцип действия и КПД тепловых двигателей Статика. «Дайте мне точку опоры, и я подниму Землю!»
Статика. «Дайте мне точку опоры, и я подниму Землю!» Материя и цвет. Свет
Материя и цвет. Свет