Содержание
- 2. Молекулярно-статистический (молеклярно-кинетический) способ. Поведение большого числа частиц рассматривается, исходя из анализа движения отдельных частиц на основе
- 3. В молекулярно-кинетической теории пользуются моделью идеального газа, удовлетворяющей следующим условиям: 1) собственный объем молекул газа пренебрежимо
- 4. Состояние системы задается термодинамическими параметрами (параметрами состояния) – совокупностью физических величин, характеризующих свойства термодинамической системы. Обычно
- 5. Равновесное состояние – это состояние, к которому система приходит самопроизвольно, если ее изолировать от внешней среды
- 6. В неравновесном состоянии всем или некоторым параметрам системы нельзя приписать определенных значений. Так, газу в цилиндре
- 7. Процесс, состоящий из непрерывной последовательности равновесных состояний, называется равновесным. Процесс, состоящий из последовательности неравновесных состояний, называется
- 9. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ (МКТ). ОСНОВНОЕ УРАВНЕНИЕ МКТ.
- 10. Моль – это стандартизованное количество вещества в любом агрегатном состоянии. Определение моля: 1 моль ≡ количество
- 11. Молекулярная масса соединения представляет собой сумму атомных масс образующих его элементов. Атомная масса изотопа углерода 12С
- 12. Рассмотрим идеальный газ, находящийся в закрытом сосуде. Определим импульс, сообщаемый стенке сосуда, ударяющейся молекулой.
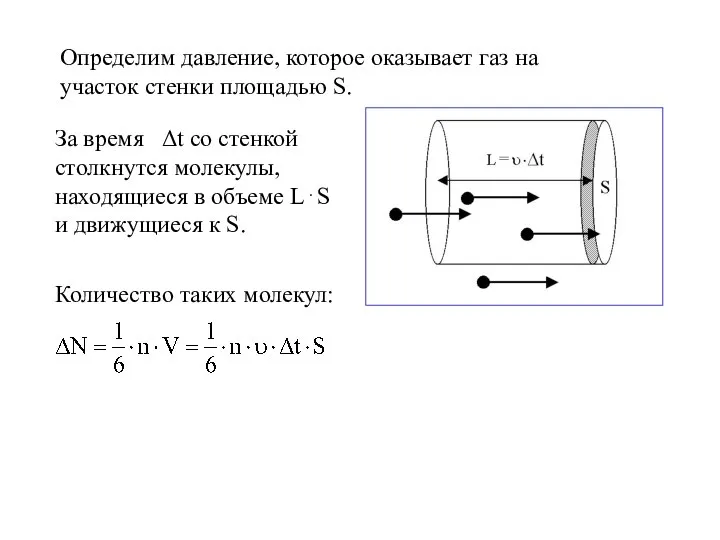
- 13. Определим давление, которое оказывает газ на участок стенки площадью S. За время Δt со стенкой столкнутся
- 14. Импульс, полученный стенкой от этих молекул, равен:
- 15. Так как скорости молекул различны, то: - основное уравнение МКТ или : давление идеального газа численно
- 16. Определение температуры с молекулярно-кинетической точки зрения основывается на среднем значении кинетической энергии теплового движения молекул, так
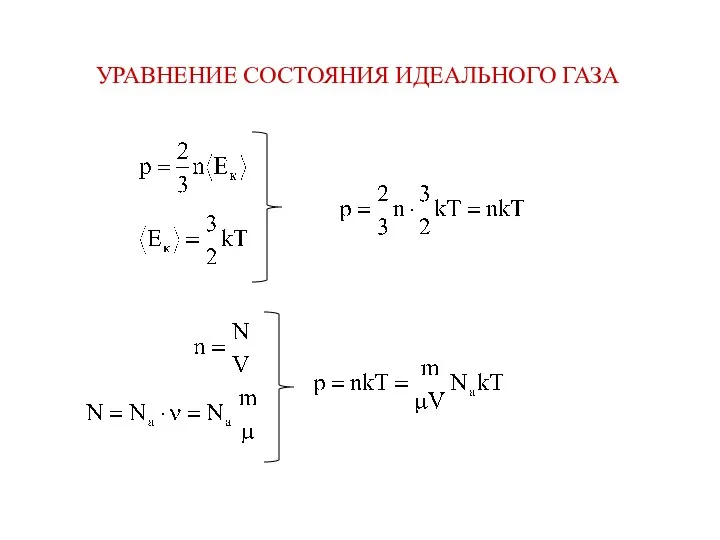
- 17. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- 18. R = k⋅Na = 8,31 Дж/(моль⋅К) - универсальная газовая постоянная Ур. Клапейрона-Менделеева или ур. состояния идеального
- 19. ИЗОПРОЦЕССЫ Изотермическим называется процесс изменения состояния термодинамической системы при постоянной температуре. Для данной массы газа произведение
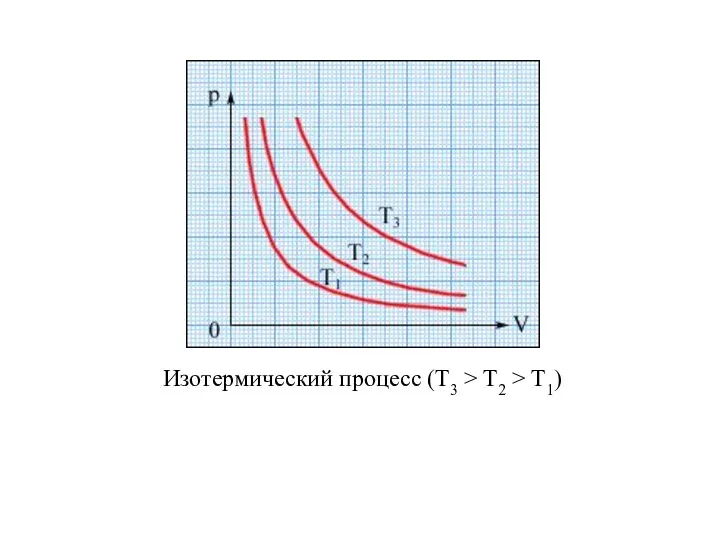
- 20. Изотермический процесс (Т3 > T2 > T1)
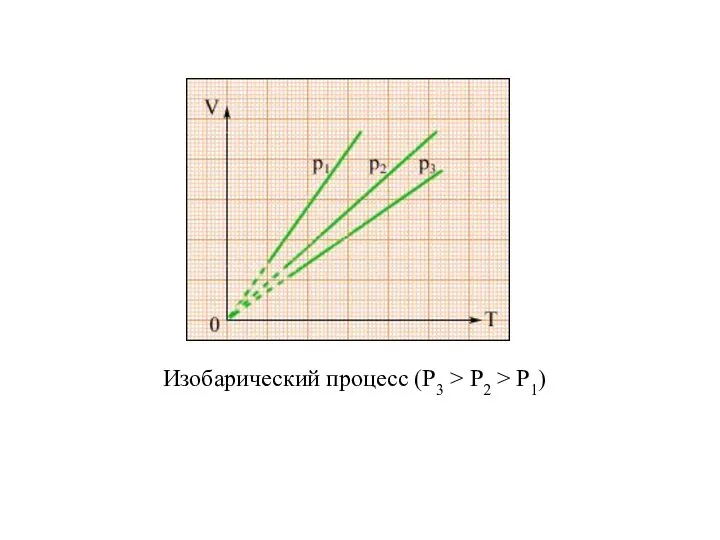
- 22. Изобарический процесс (P3 > P2 > P1)
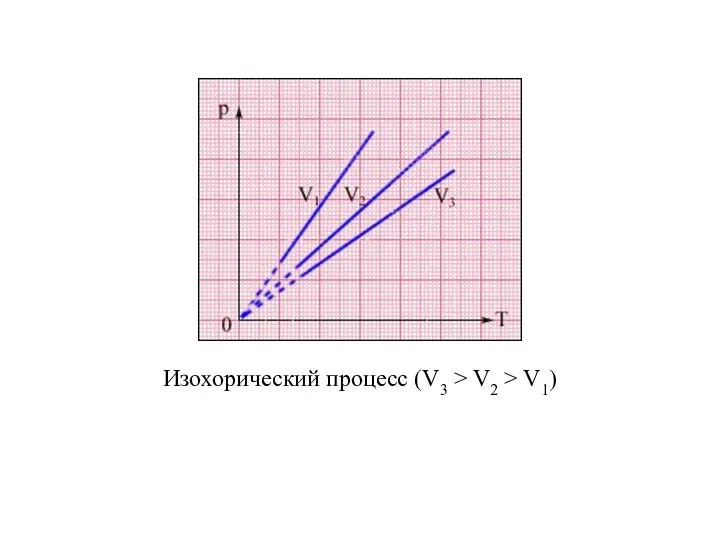
- 24. Изохорический процесс (V3 > V2 > V1)
- 25. Закон Авогадро: моли любых газов при одинаковых температуре и давлении занимают одинаковые объемы. При нормальных условиях
- 26. ЭЛЕМЕНТЫ СТАТИСТИЧЕСКОЙ ФИЗИКИ РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА
- 27. Решим задачу о нахождении вероятности того, что данная (выделенная) молекула имеет скорость, лежащую в определенном интервале
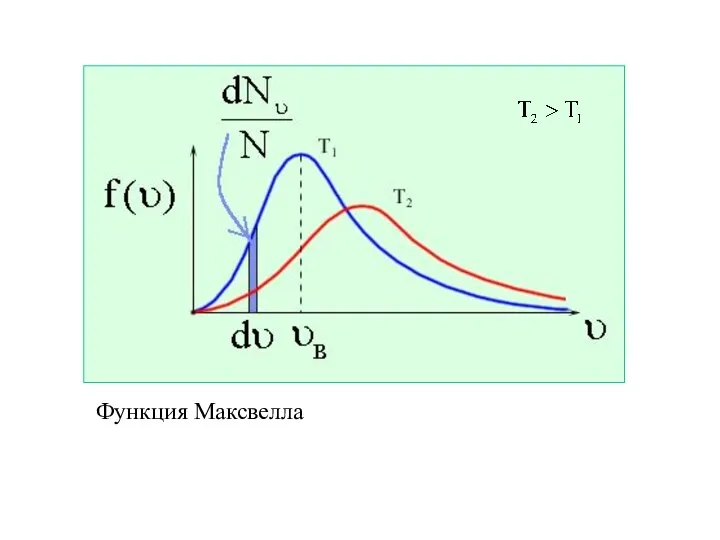
- 28. Получим плотность вероятности (функцию распределения по скоростям): Эта функция - функция распределения Максвелла. Она показывает вероятность
- 29. Функция Максвелла удовлетворяет
- 30. Функция Максвелла
- 31. Скорость υв, соответствующая максимуму функции распределения, называется наиболее вероятной.
- 32. Найдем среднюю скорость (средняя арифметическая скорость):
- 34. Скачать презентацию

























 В поисках нейтрино или Частица-Призрак
В поисках нейтрино или Частица-Призрак Основы молекулярной физики
Основы молекулярной физики Деформационные методы получения наноматериалов. Научные основы метода всесторонней изотермической ковки
Деформационные методы получения наноматериалов. Научные основы метода всесторонней изотермической ковки Химические источники тока
Химические источники тока Определение плотности берёзового сока. Автор: Ковалёв Денис, учащийся 8 класса МОУ «ПССОШ»
Определение плотности берёзового сока. Автор: Ковалёв Денис, учащийся 8 класса МОУ «ПССОШ» Всё живое из яйца. Исследовательская работа
Всё живое из яйца. Исследовательская работа Презентация по физике "Законы сохранения" - скачать бесплатно
Презентация по физике "Законы сохранения" - скачать бесплатно Элементы гидродинамики и теплопереноса в гелии
Элементы гидродинамики и теплопереноса в гелии Переходные процессы
Переходные процессы Курс лекций по теоретической механике. Статика
Курс лекций по теоретической механике. Статика Строения атомов
Строения атомов Презентация по физике "Демонстрация фокуса «Карточка с памятью»" - скачать
Презентация по физике "Демонстрация фокуса «Карточка с памятью»" - скачать  Тракторы МТЗ-82
Тракторы МТЗ-82 Движение с постоянным ускорением
Движение с постоянным ускорением მაგნიტური ლევიტაცია
მაგნიტური ლევიტაცია Масса тела. Измерение массы тела на весах
Масса тела. Измерение массы тела на весах Устойчивое равновесие тела, имеющую одну точку опоры
Устойчивое равновесие тела, имеющую одну точку опоры Явление электромагнитной индукции
Явление электромагнитной индукции Кванттық физика тарихы және тарихи деректерді физика пәнін оқытуда қолдану әдістемесін оқыту
Кванттық физика тарихы және тарихи деректерді физика пәнін оқытуда қолдану әдістемесін оқыту Магнит өрісіндегі тогы бар контур
Магнит өрісіндегі тогы бар контур Гидродинамика
Гидродинамика Реактивное движение и его применение в технике
Реактивное движение и его применение в технике Урок физики в 7 кл. Тема: Сложение двух сил, направленных по одной прямой. Равнодействующая сил.
Урок физики в 7 кл. Тема: Сложение двух сил, направленных по одной прямой. Равнодействующая сил. Молекулярная физика
Молекулярная физика  Импульс. Закон сохранения импульса. Энергия. Закон сохранения механической энергии
Импульс. Закон сохранения импульса. Энергия. Закон сохранения механической энергии Презентация Теплопроводность
Презентация Теплопроводность  Высокочастотный трансформатор Тесла
Высокочастотный трансформатор Тесла Уравнения электромеханической и механической характеристик асинхронного двигателя и их анализ
Уравнения электромеханической и механической характеристик асинхронного двигателя и их анализ