Содержание
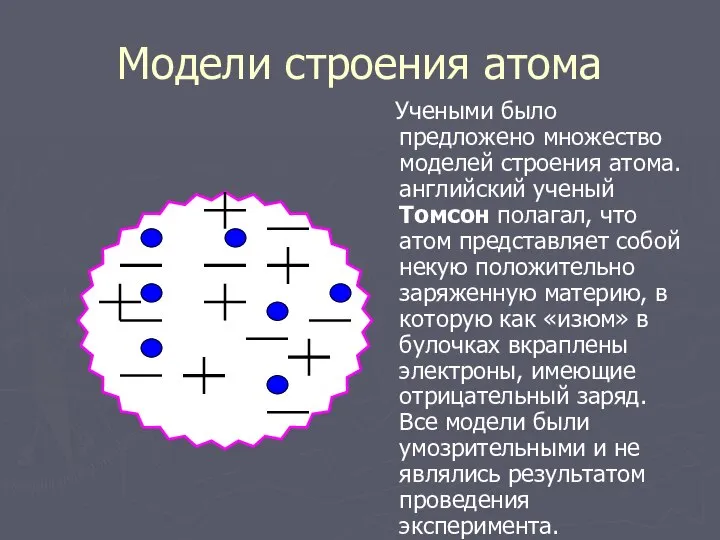
- 2. Модели строения атома Учеными было предложено множество моделей строения атома. английский ученый Томсон полагал, что атом
- 4. Причины рассеивания α-частиц Электрон, входящий в состав атома нет мог рассеивать α-частиц так как масса α-частицы
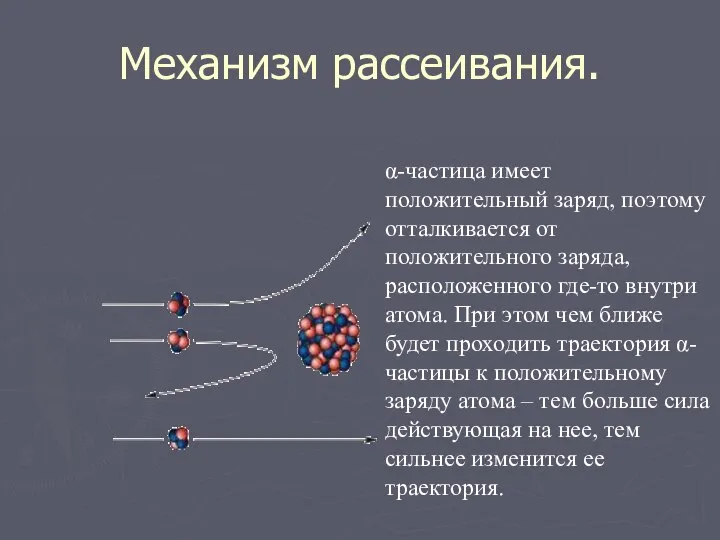
- 5. Механизм рассеивания. α-частица имеет положительный заряд, поэтому отталкивается от положительного заряда, расположенного где-то внутри атома. При
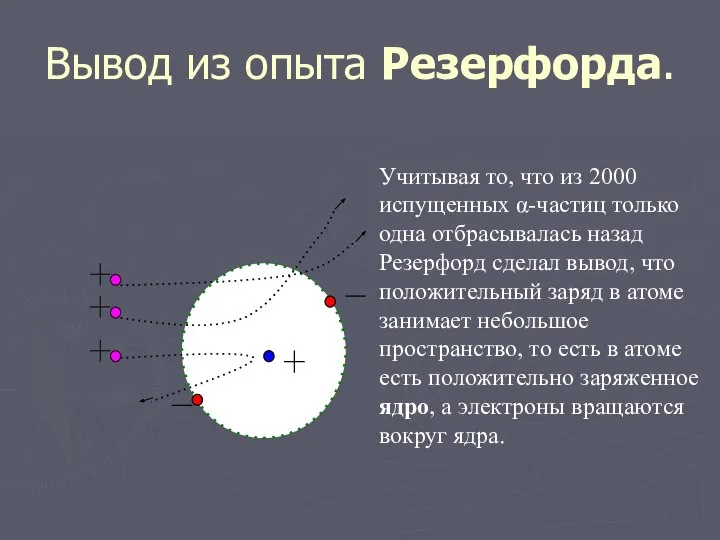
- 6. Вывод из опыта Резерфорда. Учитывая то, что из 2000 испущенных α-частиц только одна отбрасывалась назад Резерфорд
- 8. Скачать презентацию


 Статика
Статика Напівпровідникові прилади та їх застосування
Напівпровідникові прилади та їх застосування Теплообмен в металлургических агрегатах
Теплообмен в металлургических агрегатах Тестовые вопросы по физике 1-35
Тестовые вопросы по физике 1-35 Тема: «Свинец глазами физика и химика». Выполнил ученик 11б класса МОУ «СОШ №27 с углублённым изучением отдельных предметов» Тар
Тема: «Свинец глазами физика и химика». Выполнил ученик 11б класса МОУ «СОШ №27 с углублённым изучением отдельных предметов» Тар Элементы квантовой биофизики
Элементы квантовой биофизики Электромагнитные волны (ЭМВ)
Электромагнитные волны (ЭМВ) «Причину же свойств силы тяготения я до сих пор не мог вывести из явлений, гипотез же я не измышляю». И. Ньютон
«Причину же свойств силы тяготения я до сих пор не мог вывести из явлений, гипотез же я не измышляю». И. Ньютон  Презентация по физике "Отражение и преломление света" - скачать
Презентация по физике "Отражение и преломление света" - скачать  Транзисторы
Транзисторы Магнитные материалы. Магнитные свойства твердых тел
Магнитные материалы. Магнитные свойства твердых тел Геометрическая оптика
Геометрическая оптика Рентгеновские лучи
Рентгеновские лучи Теплопередача. Тепловые процессы
Теплопередача. Тепловые процессы Методи досліджень в біології. Мікроскопічна техника
Методи досліджень в біології. Мікроскопічна техника Дене импульсі. Импульстің сақталу заңы. Реактивті қозғалыс
Дене импульсі. Импульстің сақталу заңы. Реактивті қозғалыс Презентация по физике "Урок-игра по физике" - скачать бесплатно
Презентация по физике "Урок-игра по физике" - скачать бесплатно Ньютон. Спектральный состав света
Ньютон. Спектральный состав света Характеристики основных компонент ГТУ
Характеристики основных компонент ГТУ Задачи с межпредметными связями
Задачи с межпредметными связями Задачи по физике
Задачи по физике Необходимость и методы уравновешивания двс. (лекция 11)
Необходимость и методы уравновешивания двс. (лекция 11) Краткая характеристика вертолета Ми-8МТВ
Краткая характеристика вертолета Ми-8МТВ Лазеры. Принцип действия
Лазеры. Принцип действия Вводная лекция Лекция 1
Вводная лекция Лекция 1  Гармонические колебания. Физика. 9 класс
Гармонические колебания. Физика. 9 класс Презентация по физике "Действие магнитного поля" - скачать
Презентация по физике "Действие магнитного поля" - скачать  Презентация по физике "радиоактивность" - скачать
Презентация по физике "радиоактивность" - скачать