Содержание
- 2. Первое начало термодинамики - представляет собой постулат – оно не может быть доказано логическим путем или
- 3. Первое начало термодинамики устанавливает соотношение между теплотой Q, работой А и изменением внутренней энергии системы ΔU:
- 4. Внутренняя энергия является функцией состояния; это означает, что изменение внутренней энергии ΔU не зависит от пути
- 5. Первое начало термодинамики для определения работы, совершаемой системой при различных термодинамических процессах (мы будем рассматривать простейший
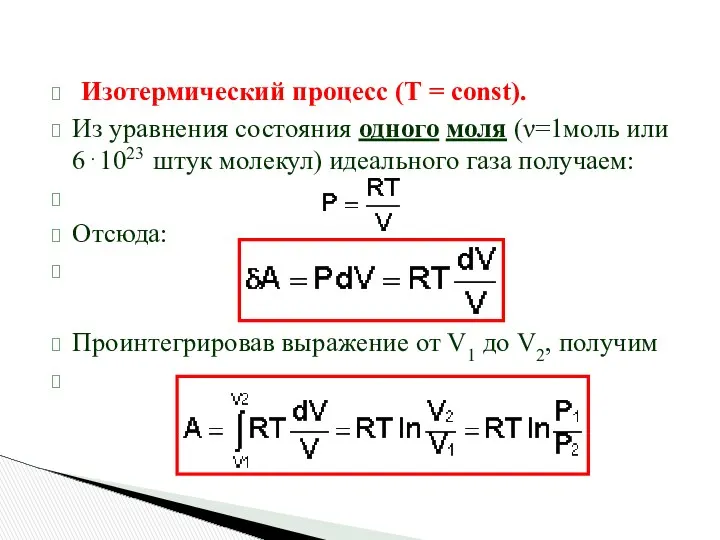
- 6. Изотермический процесс (Т = const). Из уравнения состояния одного моля (ν=1моль или 6⋅1023 штук молекул) идеального
- 7. Изобарный процесс (Р = const). Подставляя полученные выражения для работы различных процессов в уравнение, для тепловых
- 8. Введем новую функцию состояния системы – энтальпию H, тождественно равную сумме внутренней энергии и произведения давления
- 10. Адиабатический процесс (Q = 0). При адиабатическом процессе работа расширения совершается за счёт уменьшения внутренней энергии
- 11. ТЕРМОХИМИЯ Закон Гесса Большинство химических реакций сопровождаются 1. выделением (экзотермические реакции когда ΔrH 2. либо поглощением
- 12. Тепловой эффект (теплота) химической реакции – количество теплоты, выделившейся в окружающую среду ΔrH либо поглотившейся из
- 13. Тепловые эффекты, сопровождающие протекание химических реакций, являются предметом одного из разделов химической термодинамики – термохимии
- 14. 1. Теплота образования вещества – тепловой эффект реакции образования 1 моля сложного вещества из простых. Теплоты
- 15. Теплота растворения – тепловой эффект процесса растворения 1 моля вещества в бесконечно большом количестве растворителя. Теплота
- 16. Основным законом термохимии является закон Гесса, являющийся частным случаем первого начала термодинамики: Тепловой эффект химической реакции,
- 17. Изменение энтальпии ΔН (тепловой эффект изобарного процесса Qp) и изменение внутренней энергии ΔU (тепловой эффект изохорного
- 18. Рассмотрим некоторый обобщенный химический процесс превращения исходных веществ А1, А2, А3... в продукты реакции В1, В2,
- 19. Практическое значение закона Гесса состоит в том, что он позволяет рассчитывать тепловые эффекты химических процессов. В
- 20. 3. Для двух реакций, имеющих одинаковые конечные, но разные исходные состояния, разность тепловых эффектов представляет собой
- 21. Пример: расчет теплового эффекта реакции окисления одного моля глюкозы.: С6Н12О6 + 6 О2 ––> 6 СО2
- 22. Зависимость теплового эффекта реакции от температуры. Закон Кирхгофа В общем случае тепловой эффект химической реакции зависит
- 23. Продифференцируем ΔН и ΔU по температуре при постоянных давлении и температуре соответственно: Производные энтальпии и внутренней
- 24. Для химического процесса изменение теплоемкости задается изменением состава системы и рассчитывается следующим образом:
- 25. Если проинтегрировать выражения от Т = Т1 до Т = Т2, считая ΔСp (ΔСv) не зависящим
- 27. Скачать презентацию























 Электрический ток. Условие существования тока. Уравнение неразрывности
Электрический ток. Условие существования тока. Уравнение неразрывности Моделирование процессов термомодифицирования древесины
Моделирование процессов термомодифицирования древесины Схемы электрических соединений на стороне 6-10 кВ. (Лекция 12)
Схемы электрических соединений на стороне 6-10 кВ. (Лекция 12) Магнитное поле в веществе
Магнитное поле в веществе Информационно- коммуникационные технологии на уроках физики ОБОШИ Суджанская школа-интернат Новикова Л. В. учитель физики Выс
Информационно- коммуникационные технологии на уроках физики ОБОШИ Суджанская школа-интернат Новикова Л. В. учитель физики Выс Презентация по физике "Строение атома" - скачать
Презентация по физике "Строение атома" - скачать  ,,Золоте правило” механіки
,,Золоте правило” механіки Расчет частотных характеристик простейших электрических цепей
Расчет частотных характеристик простейших электрических цепей Уравнение состояния идеального газа
Уравнение состояния идеального газа Уравнение движения системы с переменной массой
Уравнение движения системы с переменной массой Ядерный реактор
Ядерный реактор Предмет и задачи нанохимии и нанотехнологий. (Лекция 1)
Предмет и задачи нанохимии и нанотехнологий. (Лекция 1) Сила трения
Сила трения Волновые свойства света
Волновые свойства света Технология обработки объединенного ремонтного хозяйства. Работа двухмашинного агрегата
Технология обработки объединенного ремонтного хозяйства. Работа двухмашинного агрегата Профессия - ТОРАТ (техническое обслуживание и ремонт автомобильного транспорта)
Профессия - ТОРАТ (техническое обслуживание и ремонт автомобильного транспорта) Презентация по теме: Пьер и Мария Кюри
Презентация по теме: Пьер и Мария Кюри Устранение несоответствия по перетиранию шланга радиатора охлаждения о жгут проводов двигателя а/м LADA XRAY
Устранение несоответствия по перетиранию шланга радиатора охлаждения о жгут проводов двигателя а/м LADA XRAY Изобретение радио А.С. Поповым
Изобретение радио А.С. Поповым Измерение скоростей продольных волн в образцах методом прямого просвечивания
Измерение скоростей продольных волн в образцах методом прямого просвечивания Электролитическая диссоциация
Электролитическая диссоциация Сергеева Л. Ф. Профессиональный лицей № 21 Г. Георгиевск
Сергеева Л. Ф. Профессиональный лицей № 21 Г. Георгиевск Mathematical Modeling of Energy Efficiency
Mathematical Modeling of Energy Efficiency Газовые законы. Основное уравнение состояния газа
Газовые законы. Основное уравнение состояния газа New Technologies Could Make Interstellar Travel Real
New Technologies Could Make Interstellar Travel Real Установочная сессия для специальности «СОДП». Курс физики
Установочная сессия для специальности «СОДП». Курс физики Законы механики
Законы механики Физические основы механики молекулярная физика. Основы термодинамики
Физические основы механики молекулярная физика. Основы термодинамики