Содержание
- 2. 1. Внутренняя энергия. Работа и теплота Наряду с механической энергией любое тело (или система) обладает внутренней
- 3. В термодинамике важно знать не абсолютное значение внутренней энергии, а её изменение. В термодинамических процессах изменяется
- 4. Внутренняя энергия U одного моля идеального газа равна: или Таким образом, внутренняя энергия зависит только от
- 5. Понятно, что в общем случае термодинамическая система может обладать как внутренней, так и механической энергией и
- 6. Количество теплоты, сообщаемой телу, идёт на увеличение внутренней энергии и на совершение телом работы: – это
- 8. Закон сохранения энергии для малого изменения состояния системы будет иметь вид: U – функция состояния системы;
- 9. В каждом состоянии система обладает определенным и только таким значением внутренней энергии, поэтому можно записать Так
- 10. Теплота Q и работа А зависят от того, каким образом совершен переход из состояния 1 в
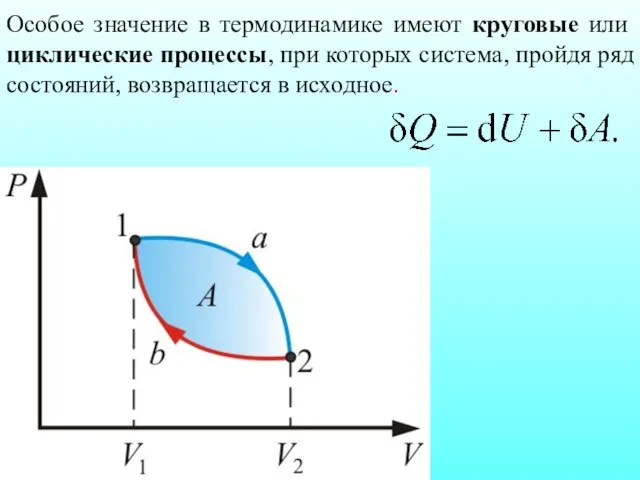
- 11. Особое значение в термодинамике имеют круговые или циклические процессы, при которых система, пройдя ряд состояний, возвращается
- 12. Если то согласно первому началу термодинамики т.е. нельзя построить периодически действующий двигатель, который совершал бы бóльшую
- 13. 2. Теплоёмкость идеального газа Теплоёмкость тела характеризуется количеством теплоты, необходимой для нагревания этого тела на один
- 14. Удельная теплоёмкость Суд – количество теплоты, необходимое для нагревания единицы массы вещества на 1 градус [Cуд]
- 15. Теплоёмкость термодинамической системы зависит от того, как изменяется состояние системы при нагревании. Если газ нагревать при
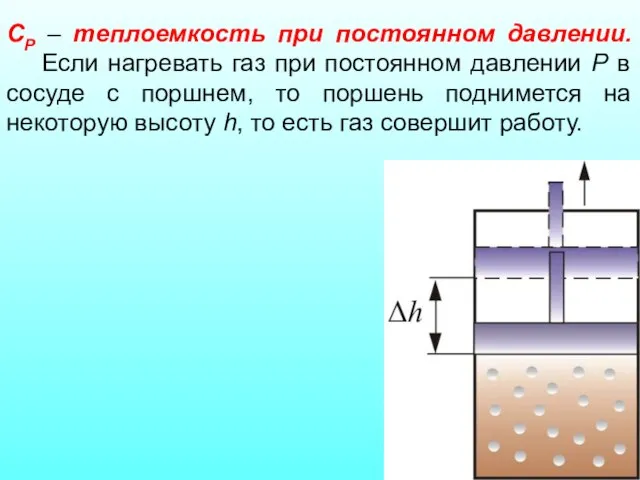
- 16. СР – теплоемкость при постоянном давлении. Если нагревать газ при постоянном давлении Р в сосуде с
- 17. Следовательно, проводимое тепло затрачивается и на нагревание и на совершение работы. Отсюда ясно, что Итак, проводимое
- 18. Пусть мы нагреваем один моль идеального газа при постоянном объёме. Тогда, первое начало термодинамики, запишем в
- 19. В общем случае так как U может зависеть не только от температуры. В случае идеального газа
- 20. Внутренняя энергия идеального газа является только функцией температуры (и не зависит от V, Р и тому
- 21. При изобарическом процессе кроме увеличения внутренней энергии происходит совершение работы газом: Из основного уравнения молекулярно-кинетической теории
- 22. Это уравнение Майера для одного моля газа. Из него следует, что физический смысл универсальной газовой постоянной
- 23. 3. Теплоёмкости одноатомных и многоатомных газов Внутренняя энергия одного моля идеального газа равна
- 24. - постоянная адиабаты (коэффициент Пуассона)
- 25. Так как Тогда Из этого следует, что (4.3.5) Кроме того , где i – число степеней
- 26. Подставив в выражение для внутренней энергии, получим: а так как , то внутреннюю энергию можно найти
- 27. Опыты с двухатомными газами такими как азот, кислород и др. показали, что Для водяного пара и
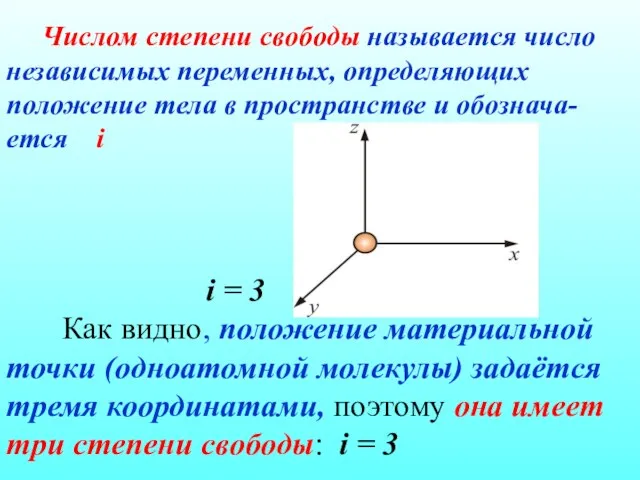
- 28. Числом степени свободы называется число независимых переменных, определяющих положение тела в пространстве и обознача-ется i i
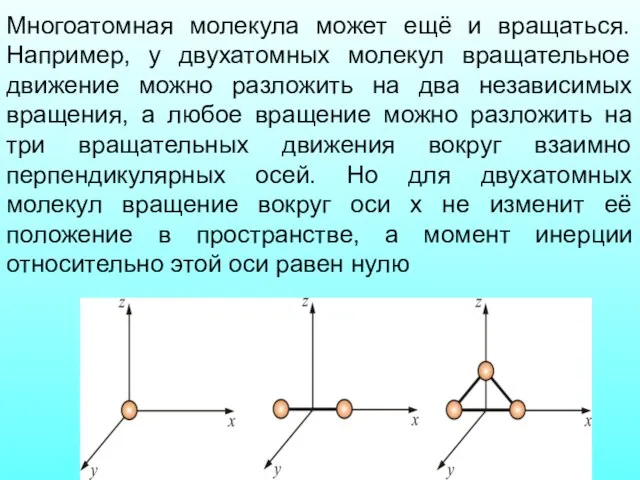
- 29. Многоатомная молекула может ещё и вращаться. Например, у двухатомных молекул вращательное движение можно разложить на два
- 30. i = 6 i = 5 i = 3
- 31. 4. Закон о равномерном распределении энергии по степеням свободы Больцман доказал, что, средняя энергия, приходящаяся на
- 32. Для молярной теплоемкости Для удельной теплоемкости
- 34. Для одноатомных газов это выполняется в очень широких пределах, а для двухатомных газов только в интервале
- 35. Одна колебательная степень свободы несет энергии, так как при этом есть и кинетическая и потенциальная энергия,
- 37. 5. Применение первого начала термодинамики к изопроцессам идеальных газов δQ = 0 Закон Шарля Закон Гей-Люссака
- 41. Политропный процесс – такой процесс, при котором изменяются все основные параметры системы, кроме теплоемкости, т.е. С
- 42. С помощью показателя n можно легко описать любой изопроцесс: 1. Изобарный процесс Р = const, n
- 43. 4. Адиабатический процесс ΔQ = 0, n = γ, Сад = 0. Во всех этих процессах
- 46. Скачать презентацию







































 Методические указания к лабораторным работам по разделу Колебания и волны
Методические указания к лабораторным работам по разделу Колебания и волны Конденсатор
Конденсатор Телеграфный аппарат и азбука Морзе
Телеграфный аппарат и азбука Морзе КСЕ. Современные представления о пространстве и времени. Материя и ее свойства. (Лекция 2)
КСЕ. Современные представления о пространстве и времени. Материя и ее свойства. (Лекция 2) Дисперсия света. Дифракция света
Дисперсия света. Дифракция света Аттестационная работа. Проектно – исследовательская деятельность на уроках физики Научное общество школьников
Аттестационная работа. Проектно – исследовательская деятельность на уроках физики Научное общество школьников Сложный теплообмен
Сложный теплообмен Гидродинамика. Полная диаграмма циркуляции воды в трубе
Гидродинамика. Полная диаграмма циркуляции воды в трубе Строение тел. Агрегатные состояния вещества и фазовые переходы. Законы термодинамики
Строение тел. Агрегатные состояния вещества и фазовые переходы. Законы термодинамики Лекция 3. Работа pn-перехода. pn-переход в состоянии термодинамического равновесия
Лекция 3. Работа pn-перехода. pn-переход в состоянии термодинамического равновесия Физические свойства воды в разных агрегатных состояниях
Физические свойства воды в разных агрегатных состояниях Устройство, принцип работы, виды пресса и домкрата
Устройство, принцип работы, виды пресса и домкрата Космическая динамика. Законы Кеплера
Космическая динамика. Законы Кеплера Масс-спектрометрия (МС)
Масс-спектрометрия (МС) Авторский урок физики в 10 профильном классе. Учитель физики высшей категории Рыженко Александра Федоровна. ЧСШ №1. г. Саяногор
Авторский урок физики в 10 профильном классе. Учитель физики высшей категории Рыженко Александра Федоровна. ЧСШ №1. г. Саяногор Изучение кристаллической структуры материалов
Изучение кристаллической структуры материалов Сұйықтың тұтқырлығын зерттеу әдістері
Сұйықтың тұтқырлығын зерттеу әдістері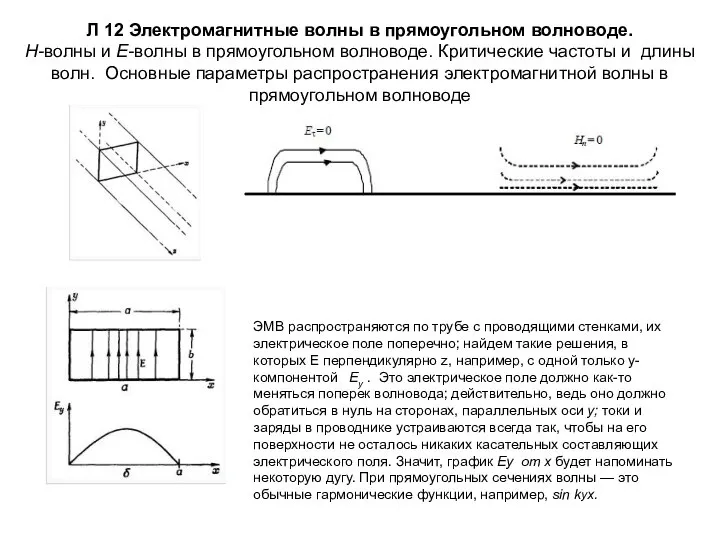 Электромагнитные волны в прямоугольном волноводе
Электромагнитные волны в прямоугольном волноводе Диффузия. Движение молекул
Диффузия. Движение молекул Сравнительная характеристика методов нейтронного каротажа для определения водонасыщенной пористости
Сравнительная характеристика методов нейтронного каротажа для определения водонасыщенной пористости Световые явления. Обобщающий урок
Световые явления. Обобщающий урок Полупроводниковые теплоэлектрогенераторы
Полупроводниковые теплоэлектрогенераторы Школьное учебно-методическое объединение учителей физики
Школьное учебно-методическое объединение учителей физики Презентация по физике. Тема: Цепная реакция деления ядер урана . Класс: 9 «б»
Презентация по физике. Тема: Цепная реакция деления ядер урана . Класс: 9 «б» Освещение жилого дома. Типы освещения
Освещение жилого дома. Типы освещения Історія виникнення радіо підготували: Учні 11-м класу Бережна Тамара, Пуха Катерина, Веретенніков Олександр, Ковтун Ярослав
Історія виникнення радіо підготували: Учні 11-м класу Бережна Тамара, Пуха Катерина, Веретенніков Олександр, Ковтун Ярослав  Оптика полупроводников
Оптика полупроводников Хроматографические методы анализа и их применение для контроля качества лекарственных средств
Хроматографические методы анализа и их применение для контроля качества лекарственных средств