Содержание
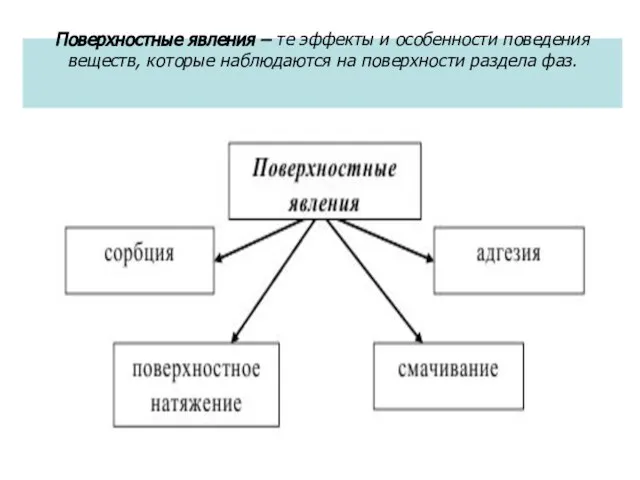
- 2. Поверхностные явления – те эффекты и особенности поведения веществ, которые наблюдаются на поверхности раздела фаз.
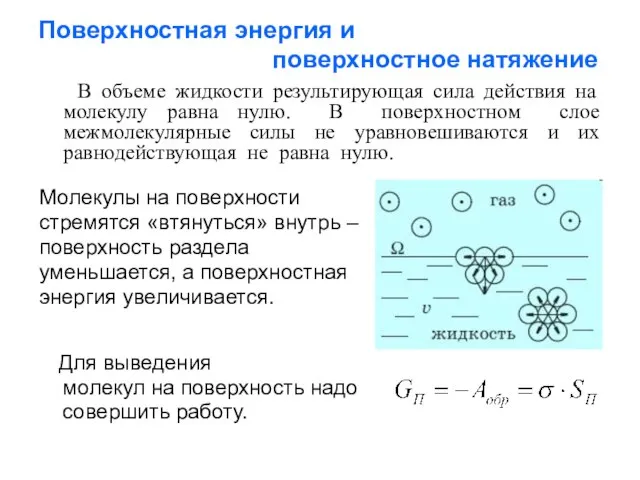
- 3. Поверхностная энергия и поверхностное натяжение В объеме жидкости результирующая сила действия на молекулу равна нулю. В
- 4. Физический смысл поверхностного натяжения Энергетическая трактовка: поверхностное натяжение равно работе, затраченной на образование единицы поверхности: ,
- 5. Благодаря поверхностному натяжению капля жидкости в свободном падении принимает сферическую форму.
- 6. Факторы, влияющие на поверхностное натяжение 1) Температура С увеличением температуры σ уменьшается. Температура, при которой поверхностное
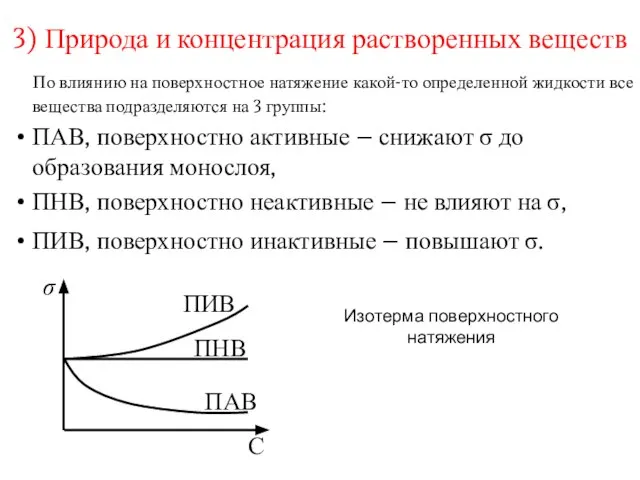
- 7. 3) Природа и концентрация растворенных веществ По влиянию на поверхностное натяжение какой-то определенной жидкости все вещества
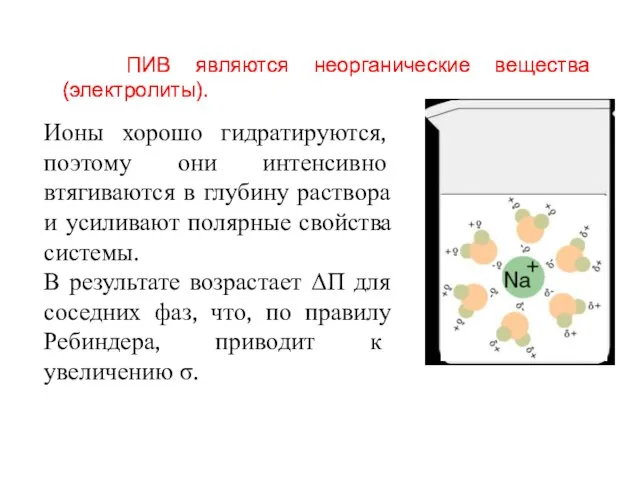
- 8. ПИВ являются неорганические вещества (электролиты). Ионы хорошо гидратируются, поэтому они интенсивно втягиваются в глубину раствора и
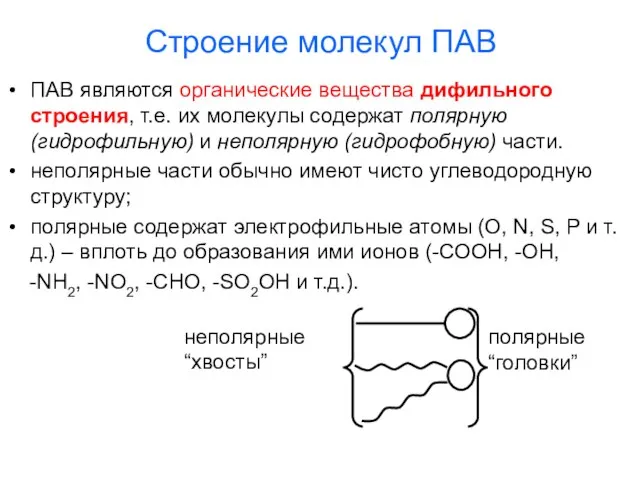
- 9. Строение молекул ПАВ ПАВ являются органические вещества дифильного строения, т.е. их молекулы содержат полярную (гидрофильную) и
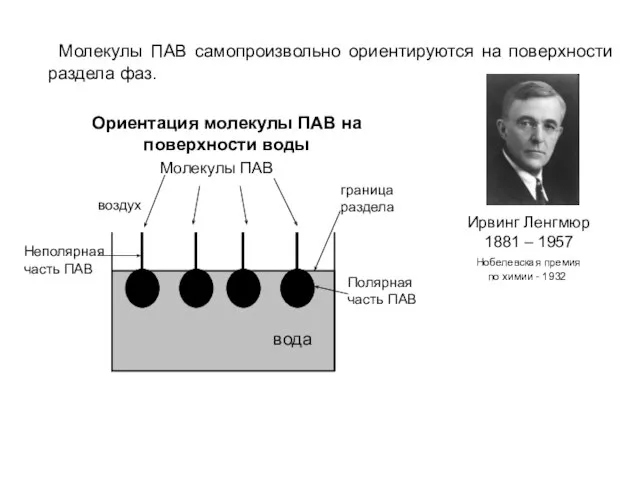
- 10. Молекулы ПАВ самопроизвольно ориентируются на поверхности раздела фаз. Ирвинг Ленгмюр 1881 – 1957 Нобелевская премия по
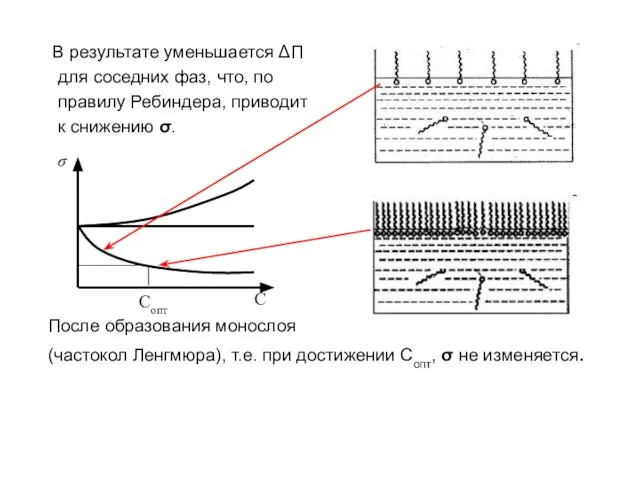
- 11. В результате уменьшается ΔП для соседних фаз, что, по правилу Ребиндера, приводит к снижению σ. После
- 13. Поверхностная активность Количественной мерой способности ПАВ понижать поверхностное натяжение на границе раздела фаз служит поверхностная активность
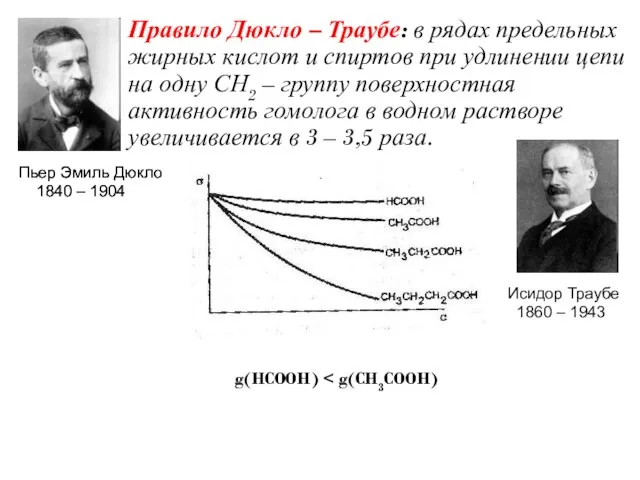
- 14. Правило Дюкло – Траубе: в рядах предельных жирных кислот и спиртов при удлинении цепи на одну
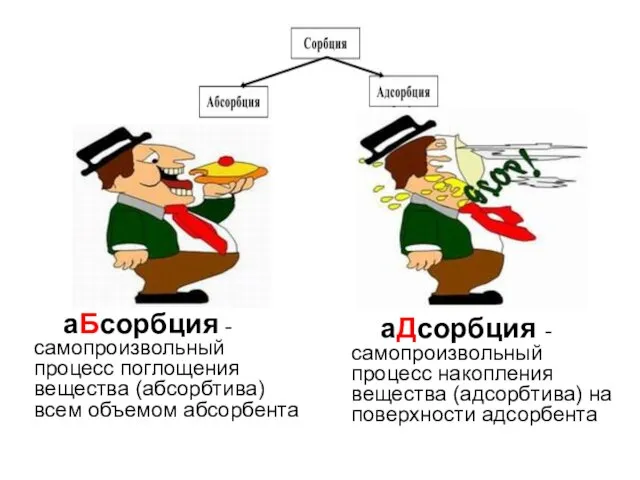
- 15. аБсорбция - самопроизвольный процесс поглощения вещества (абсорбтива) всем объемом абсорбента аДсорбция - самопроизвольный процесс накопления вещества
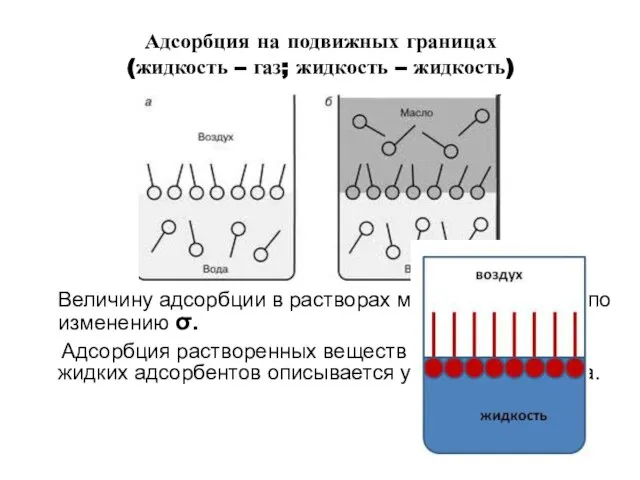
- 16. Адсорбция на подвижных границах (жидкость – газ; жидкость – жидкость) Величину адсорбции в растворах можно определить
- 17. Изотерма адсорбции Гиббса Уравнение, описывающее зависимость между адсорбцией и концентрацией вещества называется изотермой адсорбции. Уравнение адсорбции
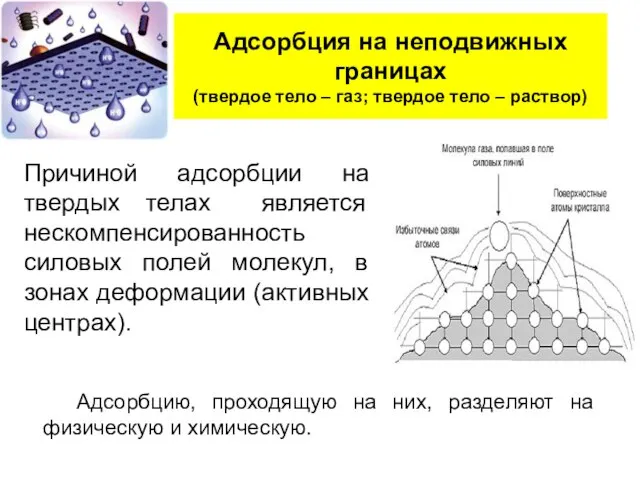
- 18. Адсорбция на неподвижных границах (твердое тело – газ; твердое тело – раствор) Причиной адсорбции на твердых
- 19. Физическая адсорбция (ФАд) возникает за счет ван-дер-ваальсовых взаимодействий и происходит на активных центрах (во впадинах поверхности).
- 20. Количественно адсорбция (Г) на подвижной и неподвижной границах раздела описывается уравнением Ленгмюра. где Г∞ – предельная
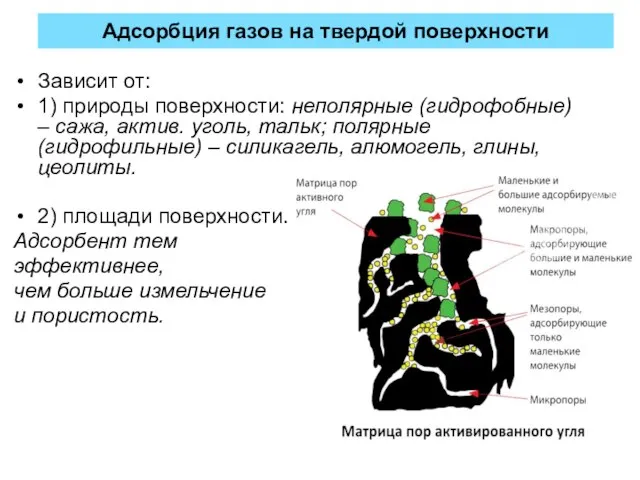
- 21. Адсорбция газов на твердой поверхности Зависит от: 1) природы поверхности: неполярные (гидрофобные) – сажа, актив. уголь,
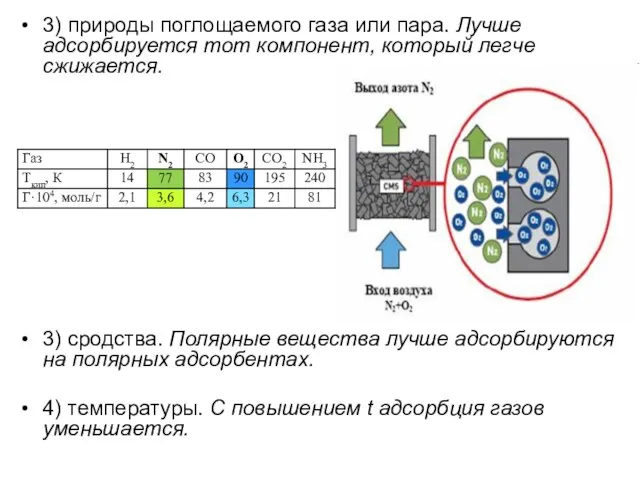
- 22. 3) природы поглощаемого газа или пара. Лучше адсорбируется тот компонент, который легче сжижается. 3) сродства. Полярные
- 23. Отличие от адсорбции газов – это конкуренции между растворителем и растворенным веществом за возможность адсорбироваться на
- 24. Молекулярная (неэлектролитов) адсорбция Зависит от: 1) природы адсорбента. Полярные адсорбенты поглощают полярные вещества. 2) природы растворителя.
- 25. 4) природы поглощаемого вещества (адсорбтива): а) Правило Шилова: чем больше растворимость вещества в растворителе, тем хуже
- 26. Адсорбция ионов из растворов в зависимости от природы адсорбента подразделяется на ионную адсорбцию и ионнообменную адсорбцию
- 27. Ионная адсорбция По сравнению с молекулярной адсорбцией более сложный процесс, т.к. в растворе присутствует уже 3
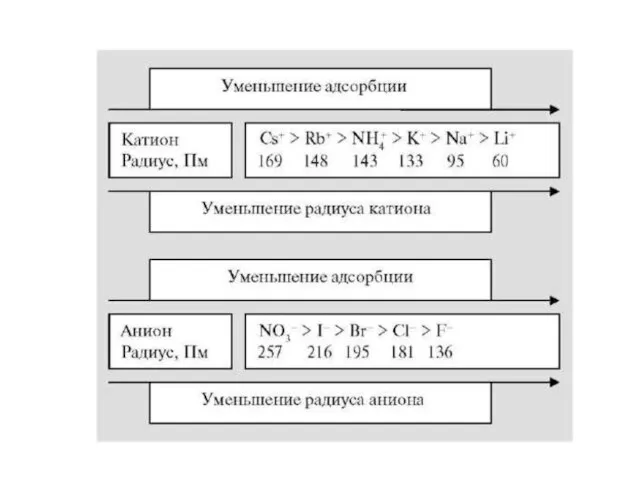
- 28. Зависит от: 1) природы адсорбента. Чем более полярный адсорбент, тем лучше адсорбция ионов. 2) природы иона:
- 30. Избирательная адсорбция ионов подчиняется правилу Панета – Фаянса Например: на AgI могут адсорбироваться Ag+ и I-,
- 31. Ионообменная адсорбция Ионообменная адсорбция – это процесс, при котором твердый адсорбент обменивает свои ионы на ионы
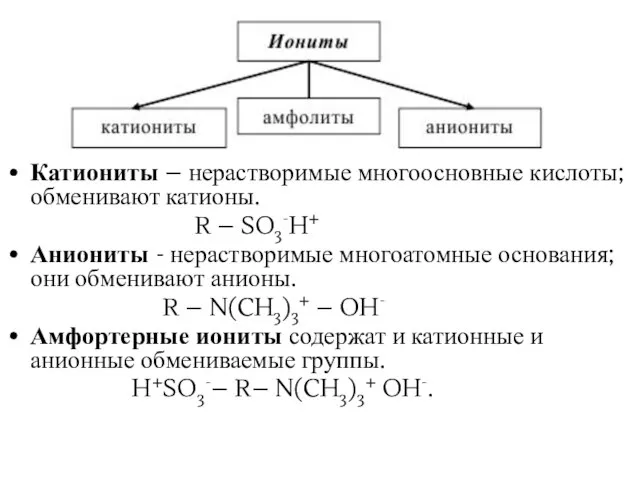
- 32. Катиониты – нерастворимые многоосновные кислоты; обменивают катионы. R – SO3-H+ Аниониты - нерастворимые многоатомные основания; они
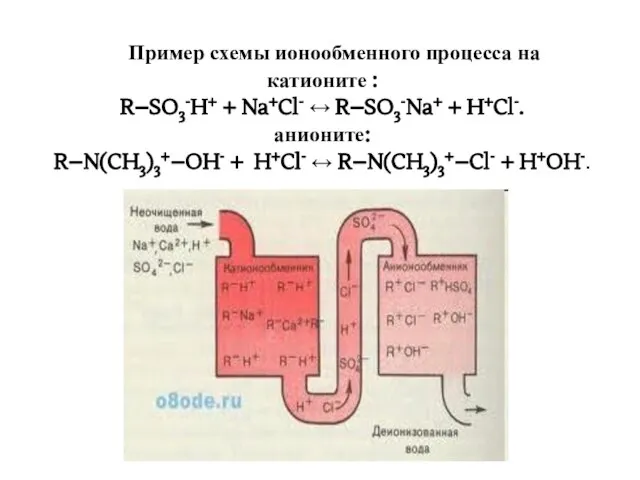
- 33. Пример схемы ионообменного процесса на катионите : R–SO3-H+ + Na+Cl- ↔ R–SO3-Na+ + H+Cl-. анионите: R–N(CH3)3+–OH-
- 34. Адсорбционные процессы, используемые в медицине Адсорбционная терапия применяется для удаления токсинов и вредных веществ из ЖКТ
- 36. Скачать презентацию

















 Анализ вибрации: диагноз и лечение
Анализ вибрации: диагноз и лечение Тепловые двигатели
Тепловые двигатели Гравиметрия, или гравиразведка. (Лекция 5)
Гравиметрия, или гравиразведка. (Лекция 5) Выпускная система дизеля
Выпускная система дизеля Ионизирующее излучение
Ионизирующее излучение Нанотехнологии и науки о материалах
Нанотехнологии и науки о материалах Биполярный транзистор. Проверка исправности
Биполярный транзистор. Проверка исправности Встроенные гидроусилители рулевого управления
Встроенные гидроусилители рулевого управления Конденсаторы. Электроёмкость конденсатора. Энергия заряжённого конденсатора. Применение конденсаторов
Конденсаторы. Электроёмкость конденсатора. Энергия заряжённого конденсатора. Применение конденсаторов Тепловые явления (8 класс)
Тепловые явления (8 класс) Первоначальные сведения об электрическом токе
Первоначальные сведения об электрическом токе Лауреат Нобелевской премии Артур Эшкин
Лауреат Нобелевской премии Артур Эшкин Вынужденные колебания
Вынужденные колебания Плотность вещества
Плотность вещества Магнитное поле
Магнитное поле Ом зањы
Ом зањы Гидропривод и пневмопривод
Гидропривод и пневмопривод Методы уменьшения потерь мощности в питающих сетях
Методы уменьшения потерь мощности в питающих сетях Плавание тел
Плавание тел  Сила Лоренца
Сила Лоренца Elektron hukumat & tijorat
Elektron hukumat & tijorat Электричество и магнетизм
Электричество и магнетизм Тема урока: «Влажность воздуха. Насыщенный пар» Тип урока: закрепление и совершенствование знаний
Тема урока: «Влажность воздуха. Насыщенный пар» Тип урока: закрепление и совершенствование знаний Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразовательная школа № 19 г. Белово» Влияние атмосферног
Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразовательная школа № 19 г. Белово» Влияние атмосферног Механическая работа и мощность
Механическая работа и мощность Конденсатор. Емкость конденсатора. Энергия электрического поля конденсатора
Конденсатор. Емкость конденсатора. Энергия электрического поля конденсатора Манометры
Манометры Применение векторов при решении физических задач
Применение векторов при решении физических задач