Содержание
- 2. Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном.
- 3. Изотермы реального газа Область I – жидкость, область II – двухфазная система «жидкость + насыщенный пар»,
- 4. В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул,
- 5. Если конденсация и испарение уравновешивают друг друга, то наступает динамическое равновесие между жидкостью и ее паром
- 6. Изотермы реального газа При температуре выше критической исчезает физическое различие между жидкостью и ее паром, и
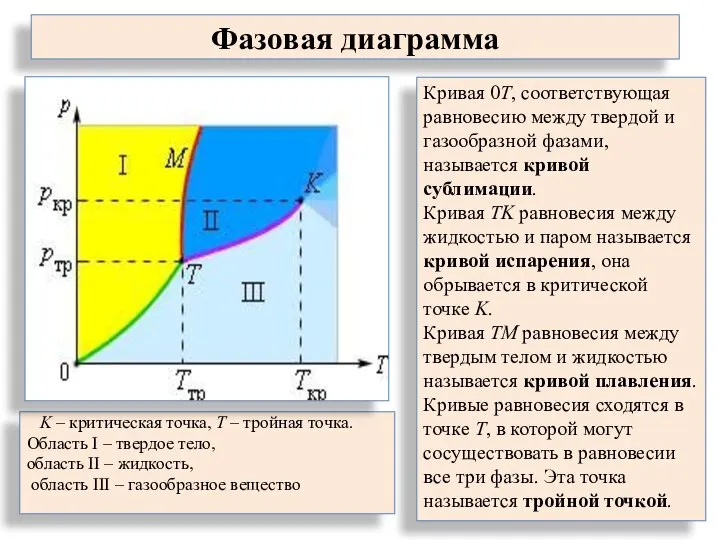
- 7. Фазовая диаграмма K – критическая точка, T – тройная точка. Область I – твердое тело, область
- 9. Для многих веществ давление pтр в тройной точке меньше 1 атм ? 105 Па. Такие вещества
- 10. Тест по теме «Молекулярная физика» Следствиями теории «Термодинамика» являются: Описание фазовых переходов Описание цикла Карно Объяснение
- 11. 3.Какой из участков изотермы соответствует процессу конденсации пара: 1 -2 2 -3 1- 3 2 -4
- 12. 5 .Объектом описания тепловых явлений статистическим методом является : Газ – макроскопическая система Газ – микроскопическая
- 13. 7.Формулировки II закона термодинамики предложили: Р.Клаузиус Д.Джоуль У. Томсон (Кельвин) Л. Больцман 8. Следствием какого закона
- 14. 9.Что не входит в ядро молекулярно-кинетической теории: Законы изопроцессов Объяснение свойств тел в различных агрегатных состояниях
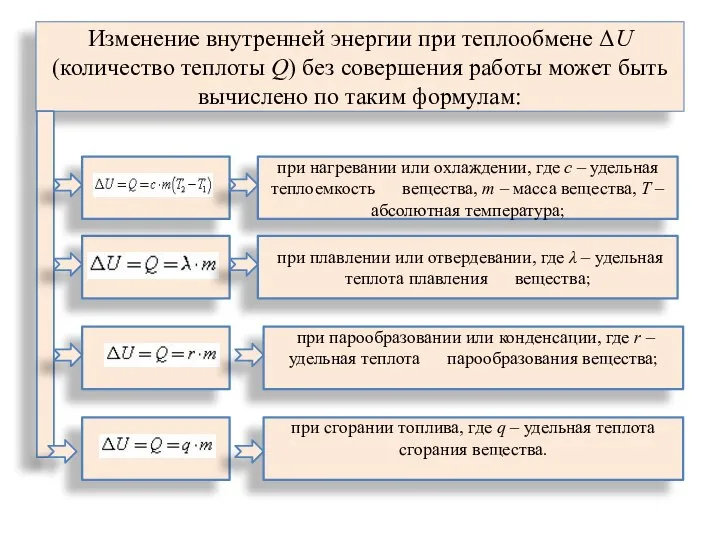
- 15. Изменение внутренней энергии при теплообмене ΔU (количество теплоты Q) без совершения работы может быть вычислено по
- 16. Задача ЕГЭ
- 17. Задача ЕГЭ
- 18. Задача ЕГЭ
- 19. Задача ЕГЭ
- 20. Использованные ресурсы: http://tvsh2004.narod.ru/phis.htm http://www.ido.rudn.ru/nfpk/fizika/mkt/3.html
- 22. Скачать презентацию
















 Гидравлика машин
Гидравлика машин Световые явления
Световые явления Давление твердых тел, жидкостей и газов
Давление твердых тел, жидкостей и газов Постулаты теории относительности
Постулаты теории относительности Вес тела и сила тяжести
Вес тела и сила тяжести Индукционные нагреватели. Перспективы и области применения
Индукционные нагреватели. Перспективы и области применения Теоретическая (техническая) механика. Статика
Теоретическая (техническая) механика. Статика Характеристики движения
Характеристики движения Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц
Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц Плоская система сил
Плоская система сил Магнитные подшипники
Магнитные подшипники Аморфні та склоподібні матеріали. (Лекція 2)
Аморфні та склоподібні матеріали. (Лекція 2) Реальные газы, жидкости и твердые тела
Реальные газы, жидкости и твердые тела Давление. Единицы давления
Давление. Единицы давления Закон всемирного тяготения
Закон всемирного тяготения Интеллектуальная игра «Физбой»
Интеллектуальная игра «Физбой» Тепловозы. Устройство тепловоза
Тепловозы. Устройство тепловоза Кристаллические тела (10 класс)
Кристаллические тела (10 класс) Квантовые методы в медицине. Ядерный магнитный резонанс. Электронный парамагнитный резонанс. (Лекция 14)
Квантовые методы в медицине. Ядерный магнитный резонанс. Электронный парамагнитный резонанс. (Лекция 14) Теоретическая механика как наука и ее место среди естественных наук
Теоретическая механика как наука и ее место среди естественных наук Сила упругости. Закон Гука
Сила упругости. Закон Гука Електричний струм у газах
Електричний струм у газах  Подготовила учитель физики МОУ СОШ №1 р.п. Степное Бейбулатова Е.А.
Подготовила учитель физики МОУ СОШ №1 р.п. Степное Бейбулатова Е.А. Механика. Наука о движении тел
Механика. Наука о движении тел Энергия движущейся воды и ветра
Энергия движущейся воды и ветра Работа силы тяжести
Работа силы тяжести Оценка угла места в системах локации метрового диапазона
Оценка угла места в системах локации метрового диапазона «Интерференция света»
«Интерференция света»