Содержание
- 2. 1. Скорости газовых молекул. Опыт Штерна. Поставьте себя на место исследователей 60-х годов позапрошлого столетия. Сформулирована
- 3. (17.2) Получена хорошая формула, но масса молекулы неизвестна! Тогда можно записать: (17.3) А мы знаем, что
- 4. Например: плотность азота (N2) равна 1,25 кг/м3 при Т=0°С и р=1 атм, υN2=500 м/c. Для водорода:
- 5. Экспериментально впервые скорости молекул были измерены в 1920 г. Штерном. За этот опыт и за большой
- 6. 2. Вероятность события. Понятие о распределении молекул газа по скоростям Математическое определение вероятности: вероятность какого-либо события
- 7. Отсюда следует, что Р может быть от нуля до единицы (Р=0÷1). Или по определению Лапласа: вероятность
- 8. Например: на переписи населения, когда указывается возраст (20 лет) – это не значит, что 20 лет,
- 9. Мы будем искать число частиц (∆n), скорости которых лежат в определённом интервале значения скорости ∆υ (от
- 10. Итак: ∆n=nf(υ)∆υ (17.6) или перейдя к пределу dn=nf(υ)dυ, (17.7) где f(υ) – функция распределения. Трудность вычисления
- 11. 3. Функция распределения Максвелла Распределение молекул идеального газа по скоростям было получено Максвеллом в 1860 году
- 12. Пусть имеется n тождественных молекул, находящихся в состоянии беспорядочного теплового движения при определенной температуре. После каждого
- 13. В результате каждого столкновения проекции скорости молекулы испытывают случайное изменение на Δυx, Δυy, Δυz, причем изменения
- 14. При этом, мы не можем ничего определенного сказать о точном значении скорости той или иной частицы
- 15. Если скорость частицы попадает в интервал от υ до , то такая частица изобразится точкой между
- 16. Мы воспользуемся результатами этого вывода. Скорость – векторная величина. Для x-ой составляющей скорости dnx = nf(υx)dυx,
- 17. А1 – постоянная равная Графическое изображение функции показано на рис 17.1. Видно, что доля молекул со
- 18. Очевидно, что и Вероятность того, что скорость молекулы одновременно удовлетворяет трём условиям: x – компонента скорости
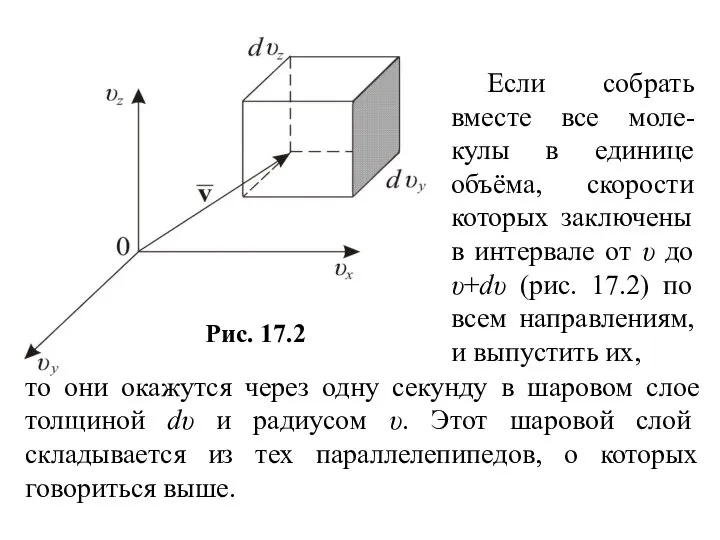
- 19. То есть (17.9) Этой формуле можно дать геометрическое истолкование: dnxyz – это число молекул в паралле-лепипеде
- 20. Если собрать вместе все моле-кулы в единице объёма, скорости которых заключены в интервале от υ до
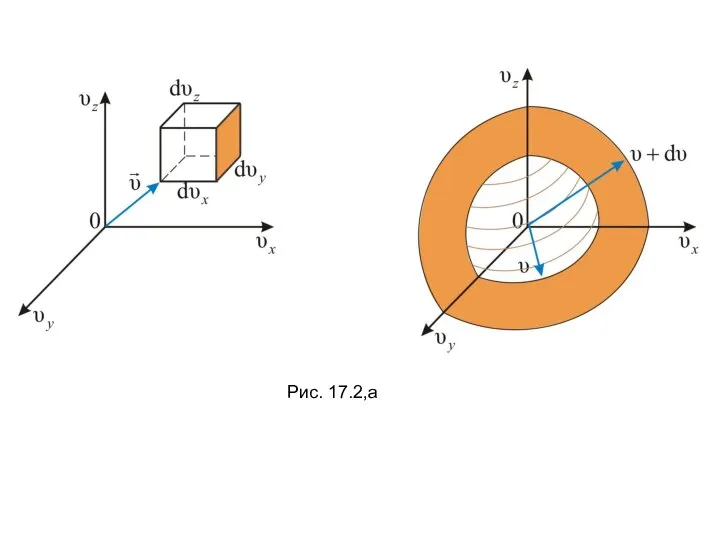
- 21. Рис. 17.2,а
- 22. Рис. 17.2,б
- 23. Объём этого шарового слоя dΩ=4πυ2dυ, (17.10) тогда общее число молекул в слое (17.11) Отсюда следует закон
- 24. При dυ=1 получаем плотность вероятности, или функцию распределения молекул по скоростям: (17.14) Эта функция обозначает долю
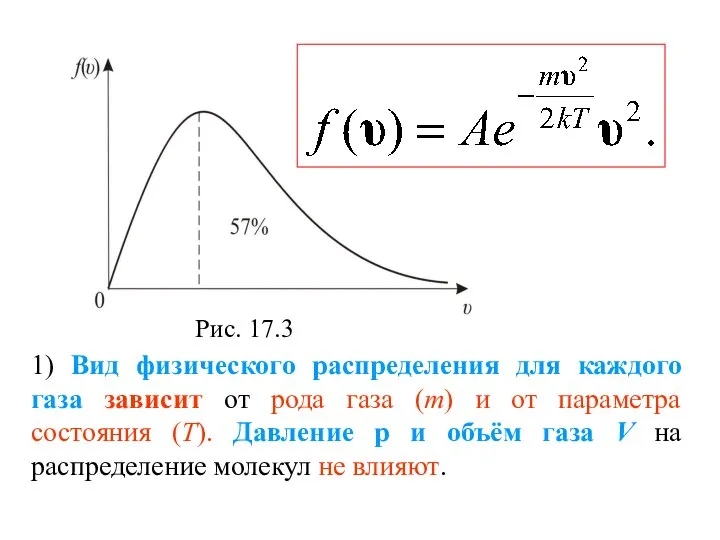
- 25. 1) Вид физического распределения для каждого газа зависит от рода газа (m) и от параметра состояния
- 26. 2) В показателе степени стоит отношение кинетической энергии, соответствующей данной скорости υ к (kТ) – средней
- 28. Рассмотрим пределы применимости классического описания распределения частиц по скоростям. Для этого воспользуемся соотношением неопределенностей Гейзенберга. Согласно
- 29. Здесь – фундаментальная константа (постоянная Планка), определяющая масштаб квантовых (микроскопических процессов). Таким образом, если частица находится
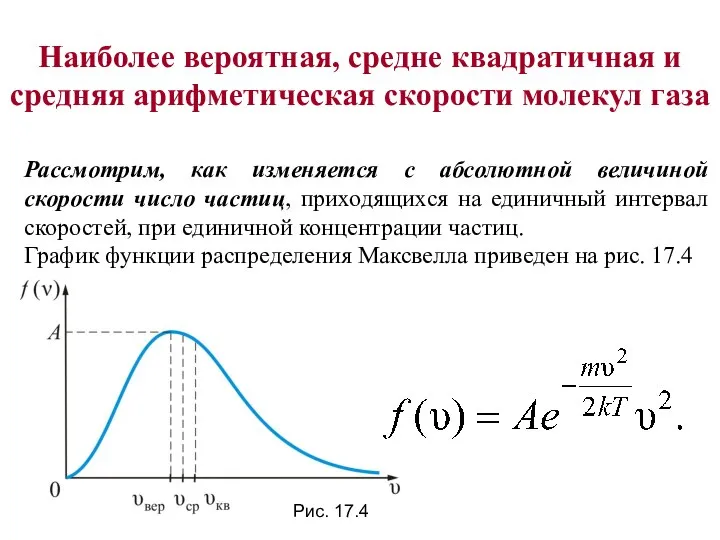
- 30. Наиболее вероятная, средне квадратичная и средняя арифметическая скорости молекул газа Рассмотрим, как изменяется с абсолютной величиной
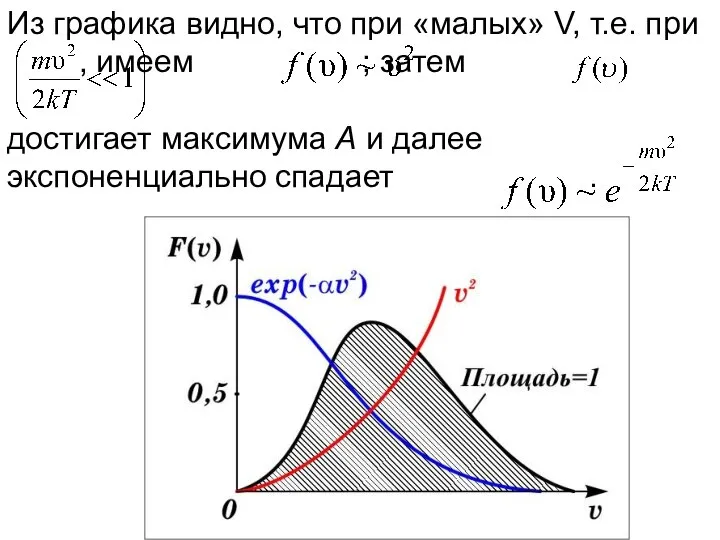
- 31. Из графика видно, что при «малых» V, т.е. при , имеем ; затем достигает максимума А
- 32. Величина скорости, на которую приходится максимум зависимости называют наиболее вероятной скоростью. Величину этой скорости найдем из
- 33. Среднюю квадратичную скорость найдем используя соотношение Тогда
- 34. Средняя арифметическая скорость − υср (17.20) где nf(υ)dυ=dn – число молекул со скоростью от υ до
- 35. Формула Максвелла для относительных скоростей Для решения многих задач удобно использовать формулу Максвелла, где скорость выражена
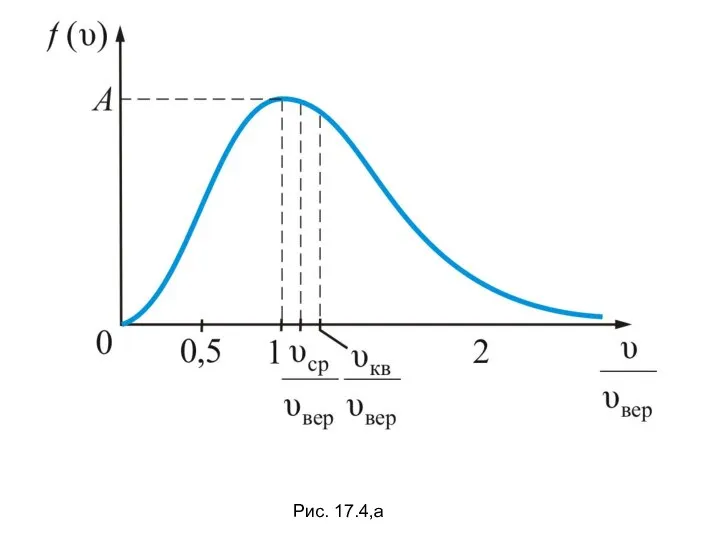
- 36. Рис. 17.4,а
- 37. На рисунке 17.4,а показано максвелловское распределение частиц f(υ) имеющих скорости от υ до За единицу скорости
- 38. Зависимость функции распределения Максвелла от массы и температуры газа Если у нас смесь газов, то в
- 39. Максвелловский закон распределения по скоростям и все вытекающие следствия справедливы только для газа в равновесной системе.
- 41. Скачать презентацию
































 Задачи на сопротивление
Задачи на сопротивление Методы машинного обучения для краткосрочного прогноза стока почвенных вод
Методы машинного обучения для краткосрочного прогноза стока почвенных вод Трение. (Тема 1.6)
Трение. (Тема 1.6) Архимедова сила 7 класс учитель физики МОУ СОШ с. Волово Антипов Владимир Васильевич
Архимедова сила 7 класс учитель физики МОУ СОШ с. Волово Антипов Владимир Васильевич Основные виды повреждений подшипников скольжения и причины их появления. Комплекс для нанесения плазменного покрытия
Основные виды повреждений подшипников скольжения и причины их появления. Комплекс для нанесения плазменного покрытия Системы наддува. Мощность двигателя внутреннего сгорания
Системы наддува. Мощность двигателя внутреннего сгорания Кинетика биологических процессов
Кинетика биологических процессов Лекция 24 (7). Квантовые статистики
Лекция 24 (7). Квантовые статистики Влияние колебаний напряжения на работу силовых элементов и автоматических устройств, технологических установок
Влияние колебаний напряжения на работу силовых элементов и автоматических устройств, технологических установок Плавление и кристаллизация Выполнил ученик 10 А класса Морозов Алексей
Плавление и кристаллизация Выполнил ученик 10 А класса Морозов Алексей Преобразование энергии в электрической цепи. (Лекция 5)
Преобразование энергии в электрической цепи. (Лекция 5)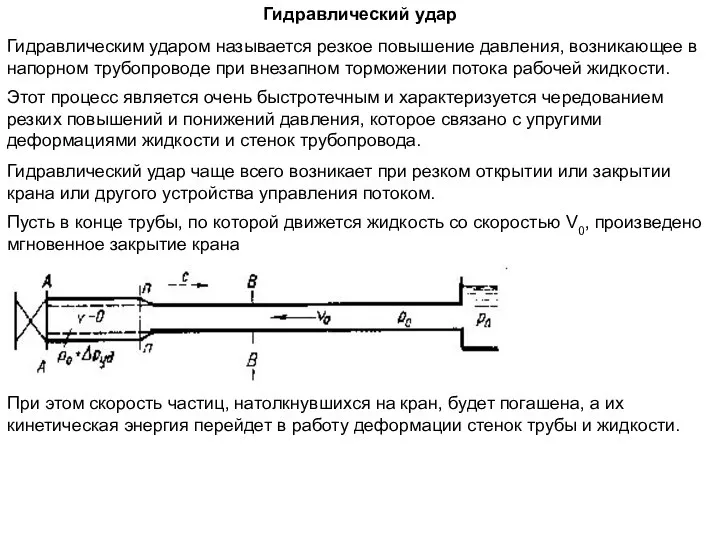 Гидравлический удар. Гидравлический таран
Гидравлический удар. Гидравлический таран Презентация по физике "Использование атома" - скачать
Презентация по физике "Использование атома" - скачать  Оборудование и технология наноматериалов механическим измельчением и механохимическим воздействием
Оборудование и технология наноматериалов механическим измельчением и механохимическим воздействием Разбор выполнения заданий
Разбор выполнения заданий Обертальний рух в нашому житті
Обертальний рух в нашому житті Изгиб. Основные понятия. Классификация видов изгибов
Изгиб. Основные понятия. Классификация видов изгибов Измерительные приборы Измери́тельный прибо́р — средство измерений, предназначенное для получения значений измеряемой физической величины в установленном диапазоне. Часто измерительным прибором называют средство измерений для выработки сигнала измерительн
Измерительные приборы Измери́тельный прибо́р — средство измерений, предназначенное для получения значений измеряемой физической величины в установленном диапазоне. Часто измерительным прибором называют средство измерений для выработки сигнала измерительн Валы и подшипники
Валы и подшипники *Физический брейн-ринг. Ребусы
*Физический брейн-ринг. Ребусы Электрический диполь
Электрический диполь Детерминированность и хаос. Характеристики хаотического движения. Определение странных аттракторов
Детерминированность и хаос. Характеристики хаотического движения. Определение странных аттракторов Излучение звука. Источники звука. Излучатели и приемники. Сферические и цилиндрические волны. Гидродинамическое звукообразование
Излучение звука. Источники звука. Излучатели и приемники. Сферические и цилиндрические волны. Гидродинамическое звукообразование Ось, балка, втулка
Ось, балка, втулка Магнитный поток. Решение задач
Магнитный поток. Решение задач Топки. Пылеприготовление. Котельные установки
Топки. Пылеприготовление. Котельные установки Гальванометр. Виды и применение
Гальванометр. Виды и применение Тема урока: Повторение темы «Термодинамика». Цель урока: повторить основные понятия темы «Термодинамика», продолжить формиро
Тема урока: Повторение темы «Термодинамика». Цель урока: повторить основные понятия темы «Термодинамика», продолжить формиро